Recubrimientos que liberan fármacos para dispositivos médicos.
Dispositivo médico para administrar un agente terapéutico a un tejido,
comprendiendo el dispositivo una capa que se superpone a una superficie exterior del dispositivo médico, comprendiendo la capa un agente terapéutico y un aditivo, en el que el aditivo incluye una combinación o mezcla tanto de un tensioactivo como de un compuesto químico,
en el que el agente terapéutico se selecciona de paclitaxel, rapamicina, daunorubicina, doxorubicina, lapachona, vitamina D2 y vitamina D3;
en el que el tensioactivo se selecciona de PEG-ésteres grasos, PEG-ésteres y alcoholes grasos omega-3, PEG-ésteres grasos de glicerilo, PEG-ésteres grasos de sorbitano y PEG-ésteres de azúcar; y
en el que el compuesto químico se selecciona de N-octanoil-N-metilglucamina, meglumina, sorbitol, ácido lactobiónico, xilitol, 2-etoxietanol, galactosa, glucosa, ribosa, manosa, xilosa, sacarosa, lactosa, maltosa, dietilenglicol, trietilenglicol y tetraetilenglicol
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2008/006348.
Solicitante: LUTONIX, INC.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 7351 KIRKWOOD LANE SUITE 138 MAPLE GROVE, MN 55369 ESTADOS UNIDOS DE AMERICA.
Inventor/es: WANG,LIXIANO.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61L29/16 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61L PROCEDIMIENTOS O APARATOS PARA ESTERILIZAR MATERIALES U OBJECTOS EN GENERAL; DESINFECCION, ESTERILIZACION O DESODORIZACION DEL AIRE; ASPECTOS QUIMICOS DE VENDAS, APOSITOS, COMPRESAS ABSORBENTES O ARTICULOS QUIRURGICOS; MATERIALES PARA VENDAS, APOSITOS, COMPRESAS ABSORBENTES O ARTICULOS QUIRURGICOS (conservación de cuerpos o desinfección caracterizada por los agentes empleados A01N; conservación, p. ej. esterilización de alimentos o productos alimenticios A23; preparaciones de uso medico, dental o para el aseo A61K). › A61L 29/00 Materiales para catéteres o para su revestimiento (forma o estructura de los catéteres A61M 25/00). › Materiales biológicamente activos, p. ej. sustancias terapéuticas.
- A61L31/16 A61L […] › A61L 31/00 Materiales para otros artículos quirúrgicos. › Materiales biológicamente activos, p. ej. sustancias terapéuticas.
PDF original: ES-2504541_T3.pdf
Fragmento de la descripción:
Recubrimientos que liberan fármacos para dispositivos médicos Campo de la invención
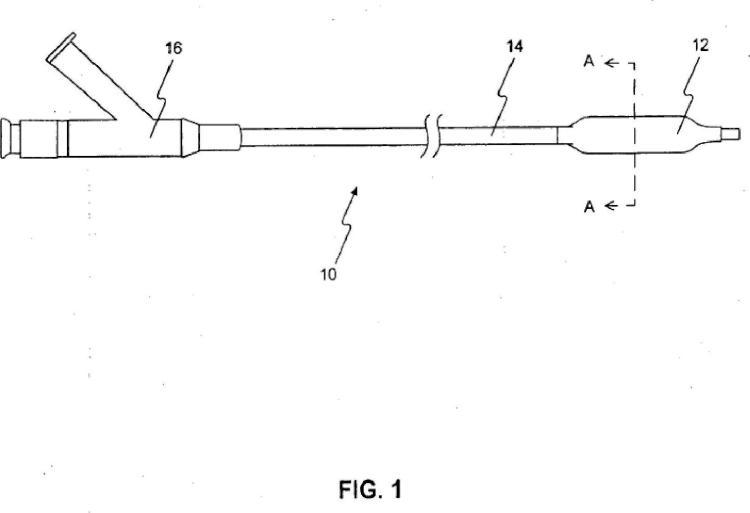
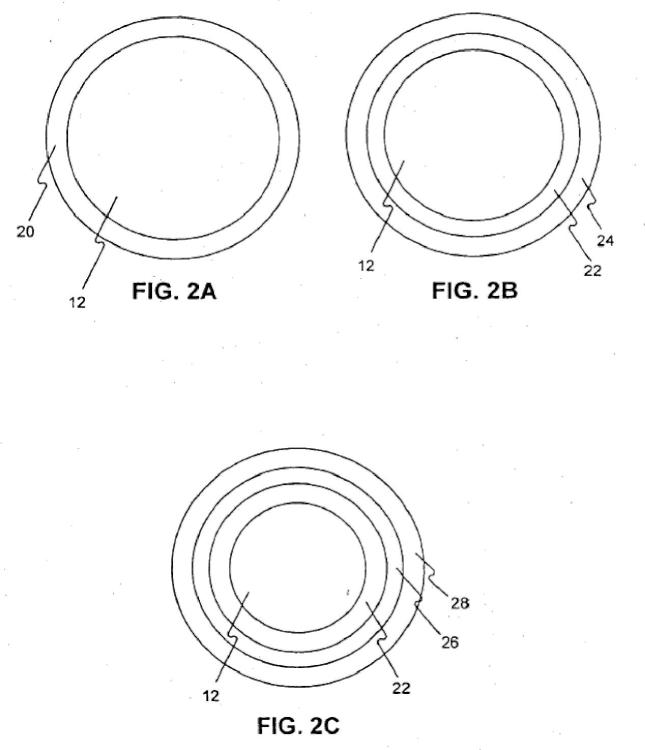
Las realizaciones de la presente invención se refieren a dispositivos médicos recubiertos, y particularmente a catéteres de balón recubiertos, y a su uso para administrar rápidamente un agente terapéutico a un tejido o una luz corporal particular, para el tratamiento de enfermedad y particularmente para reducir la estenosis y la pérdida luminal tardía de una luz corporal. Las realizaciones de la presente invención también se refieren a métodos de fabricación de estos dispositivos médicos, a los recubrimientos proporcionados sobre estos dispositivos médicos, a las disoluciones para preparar esos recubrimientos, y a métodos para tratar una luz corporal tal como la vasculatura, incluyendo particularmente vasculatura arterial, por ejemplo, usando estos dispositivos médicos recubiertos.
Antecedentes de la invención
Se ha vuelto cada vez más común tratar una variedad de estados médicos introduciendo un dispositivo médico en el sistema vascular u otra luz dentro de un paciente humano o veterinario tal como el esófago, la tráquea, el colon, el tracto biliar o el tracto urinario. Por ejemplo, los dispositivos médicos usados para el tratamiento de enfermedad vascular incluyen endoprótesis, catéteres, catéteres de balón, hilos guia, cánulas y similares. Aunque estos dispositivos médicos parecen ser inicialmente satisfactorios, los beneficios se ven a menudo comprometidos por la aparición de complicaciones, tales como trombosis tardía, o reaparición de la enfermedad, tal como estenosis (reestenosis), tras tal tratamiento.
La reestenosis, por ejemplo, implica una respuesta fisiológica a la lesión vascular provocada por angioplastia. Con el tiempo, la desendotelización y lesión en células de músculo liso da como resultado deposición de trombos, infiltración de leucocitos y macrófagos, proliferación/migración de células de músculo liso, fibrosis y deposición de matriz extracelular. La inflamación desempeña un papel fundamental vinculando la lesión vascular temprana con la consecuencia final de crecimiento de la neoíntima y que se vea comprometida la luz. En arterias lesionadas con balón, el reclutamiento de leucocitos está restringido a infiltración de neutrófilos tempranos, mientras que en arterias con endoprótesis, al reclutamiento de neutrófilos tempranos le sigue una acumulación de macrófagos prolongada. El uso extendido de endoprótesis coronarias ha alterado la respuesta vascular a la lesión provocando un estado inflamatorio más intenso y prolongado, debido a irritación crónica del cuerpo foráneo implantado, y en el caso de una endoprótesis de elución de fármaco (drug eluting stent, DES), por la biocompatibilidad insuficiente del recubrimiento de polímero.
A lo largo de los últimos varios años, se han desarrollado numerosos sistemas de administración de fármacos locales para el tratamiento y/o la prevención de la reestenosis tras angioplastia de balón o implantación de endoprótesis. Los ejemplos incluyen catéteres de administración de fármacos locales, catéteres de balón de administración y endoprótesis recubiertas con fármacos poliméricos. Dado que muchas enfermedades afectan a un órgano o sitio local específico dentro del cuerpo, es ventajoso tratar preferentemente sólo la zona afectada. Esto evita altos niveles sistémicos de fármaco, que pueden dar como resultado efectos secundarios adversos, y concentra los agentes terapéuticos en la zona local donde se necesitan. Tratando tan sólo el tejido enfermo, la cantidad total de fármaco usado puede reducirse significativamente. Además, la administración de fármaco local puede permitir el uso de determinados agentes terapéuticos eficaces, que se han considerado anteriormente demasiado tóxicos o no específicos para usarlos de manera sistémica.
Un ejemplo de un sistema de administración local es una endoprótesis de elución de fármaco (DES). La endoprótesis se recubre con un polímero en el que está impregnado el fármaco. Cuando se inserta la endoprótesis en un vaso sanguíneo, el polímero se degrada y el fármaco se libera lentamente. La lenta liberación del fármaco, que tiene lugar a lo largo de un periodo de semanas a meses, se ha notificado como una de las principales ventajas del uso de DES. Sin embargo, aunque la liberación lenta puede ser ventajosa en el caso en el que se despliega un cuerpo foráneo, tal como una endoprótesis, que es una fuente de irritación e inflamación crónicas, si no se implanta un cuerpo foráneo es ventajoso en su lugar administrar rápidamente el fármaco al tejido vascular en el momento del tratamiento para inhibir la inflamación y proliferación celular tras la lesión aguda. Por tanto, una desventaja considerable de una DES, o cualquier otro dispositivo médico implantado diseñado para la liberación sostenida de un fármaco, es que el fármaco no puede liberarse rápidamente al vaso.
El documento WO 24/26357 describe un dispositivo que contiene una pluralidad de orificios conteniendo cada orificio un agente terapéutico incluido en una capa de agente terapéutico y una capa protectora que impide que el agente terapéutico se libere hasta que la capa protectora se ha erosionado sustancialmente. Las capas de agente terapéutico pueden estar hechas de polímeros farmacéuticamente aceptables, y el copolímero preferido para la capa de agente terapéutico son polímeros de poli(lactida-co-glicolida) (PLGA).
El documento US 25/123582 describe una endoprótesis que tiene una sustancia biológica cargada con fármaco adherida sobre la misma. Aunque no está claro con qué rapidez eluye el fármaco, D2 describe que la sustancia
biológica está configurada y adaptada para una liberación de fármaco lenta.
El documento US 23/23562 describe dispositivos médicos recubiertos que proporcionan una liberación controlada de un agente terapéutico. La capa de liberación comprende un copolímero de estireno y un polímero adicional y regula la velocidad de liberación del agente terapéutico desde el dispositivo médico tras la implantación o inserción del dispositivo en un paciente.
El documento US 25/29664 describe composiciones para recubrir implantes médicos o dispositivos médicos eléctricos implantables de modo que puedan administrarse agentes terapéuticos seleccionados. Se describen varios polímeros preferidos usados en el sistema de liberación de fármacos y el periodo de liberación preferido oscila entre 1-18 días o hasta 6 meses.
Los documentos EP 1586 338 y US 25/222191 describen el uso de antioxidantes para impedir la oxidación y reducir la degradación de fármacos en dispositivos médicos de elución de fármacos. La composición para recubrir la superficie de un dispositivo médico implantable usa una combinación de dos polímeros químicamente diferentes para lograr un recubrimiento que proporciona una barrera química y física a la liberación de fármacos. Se usan copolímeros de polifluoro, lo que conduce a una administración prolongada (de 1 a 2. horas) del fármaco.
El documento WO 27/149161 propone separar una capa de recubrimiento en una capa de liberación rápida y lenta. Aunque esto permite controlar la liberación en estallido inicial y la posterior elución a largo plazo, el recubrimiento descrito en ese documento continúa eluyendo el fármaco a lo largo de muchos días.
El documento US 24/22712 describe una emulsión de alfa-tocoferol, estabilizada mediante tensloactlvos compatibles, como vehículo o portador para fármacos terapéuticos, que está sustanclalmente libre de etanol y que puede administrarse a animales o seres humanos mediante diversas vías se da a conocer.
El documento US 24/127551 describe composiciones a base de taxano y métodos de uso de las mismas para lograr niveles en sangre objetivo de un taxano en un mamífero, por ejemplo, para tratar enfermedades malignas y no malignas sensibles a taxano.
Adicionalmente, aunque inicialmente se mostró que las endoprótesis de elución de fármaco constituían una técnica eficaz para reducir y evitar la reestenosls, recientemente se han cuestionado su eficacia y su seguridad. Ha surgido una complicación potenclalmente mortal de la tecnología, la trombosis tardía, como preocupación principal. Las endoprótesis de elución de fármaco producen una alteración sustancial de la cicatrización arterial, caracterizada por una falta de reendotelizaclón completa y una persistencia de fibrina cuando se comparan con las endoprótesis de metal desnudo (BMS), que se entiende que es la causa subyacente de la trombosis tardía por DES. También han surgido preocupaciones en relación con que la matriz pollmérlca en la endoprótesis en la que está... [Seguir leyendo]
Reivindicaciones:
1. Dispositivo médico para administrar un agente terapéutico a un tejido, comprendiendo el dispositivo una capa que se superpone a una superficie exterior del dispositivo médico, comprendiendo la capa un agente
terapéutico y un aditivo, en el que el aditivo incluye una combinación o mezcla tanto de un tensioactivo
como de un compuesto químico,
en el que el agente terapéutico se selecciona de paclitaxel, rapamicina, daunorubicina, doxorubicina, lapachona, vitamina D2 y vitamina D3;
en el que el tensioactivo se selecciona de PEG-ésteres grasos, PEG-ésteres y alcoholes grasos omega-3, PEG-ésteres grasos de glicerilo, PEG-ésteres grasos de sorbitano y PEG-ésteres de azúcar; y
en el que el compuesto químico se selecciona de N-octanoil-N-metilglucamina, meglumina, sorbitol, ácido 15 lactobiónico, xilitol, 2-etoxietanol, galactosa, glucosa, ribosa, mañosa, xilosa, sacarosa, lactosa, maltosa,
dletllenglicol, trietilengllcol y tetraetllengllcol.
2. Dispositivo médico según la reivindicación 1, en el que el tejido incluye tejido de uno de vasculatura coronaria, vasculatura periférica, vasculatura cerebral, esófago, vías respiratorias, seno, tráquea, colon,
tracto billar, tracto urinario, próstata y vías cerebrales.
3. Dispositivo médico según la reivindicación 1, en el que el dispositivo incluye uno de un catéter de balón, un catéter de balón de perfusión, un catéter de infusión, un catéter de balón de corte, un catéter de balón de ranurado, un catéter láser, un dispositivo de aterectomía, un catéter de aterorreducción, una endoprótesls,
un filtro, un injerto de endoprótesis, una endoprótesls cubierta, un parche, un hilo y una válvula.
4. Dispositivo médico según la reivindicación 1, en el que el agente terapéutico es paclitaxel o rapamicina.
5. Dispositivo médico según la reivindicación 1 en el que el PEG-éster graso de sorbitano se selecciona de
Tween® 2, Tween® 4, Tween® 6 o Tween® 8.
6. Dispositivo médico según la reivindicación 1, en el que el tensioactivo es Tween 2 y el compuesto químico se selecciona de sorbitol o ácido lactobiónico.
7. Dispositivo médico según la reivindicación 1, que puede obtenerse pulverizando una disolución de
recubrimiento sobre un catéter de balón y luego sometiendo el balón recubierto a una etapa de secado en la que se evapora el disolvente en la disolución de recubrimiento, en el que la disolución de recubrimiento se prepara mezclando 35-7 mg de paclitaxel, ,4-1, mi de acetona, ,4-1, mi de etanol, ,2-,4 mi de agua, 35-7 mg de Tween 2 y 35-7 mg de sorbitol.
Patentes similares o relacionadas:
Endoprótesis híbrida helicoidal, del 22 de Julio de 2020, de MEDINOL LTD.: Componente de endoprótesis principal para formar una endoprótesis, que comprende: una sola tira que tiene una pluralidad de arrollamientos […]
Dispositivo médico que tiene un revestimiento que comprende ACCS, del 15 de Julio de 2020, de Noveome Biotherapeutics, Inc: Un dispositivo médico implantable que tiene un revestimiento en su superficie, útil para la implantación quirúrgica en el cuerpo de un sujeto, […]
Composición de fármaco y revestimiento asociado, del 1 de Julio de 2020, de W.L. GORE & ASSOCIATES, INC.: Un producto sanitario para administrar un agente terapéutico a un tejido, y el producto tiene una capa de revestimiento aplicada en una superficie del producto, y la capa […]
Método de preparación de un artículo elastomérico antimicrobiano, del 20 de Mayo de 2020, de ALLEGIANCE CORPORATION: Un método de preparación de un artículo elastomérico antimicrobiano, que comprende: recubrir un artículo elastomérico con una composición de recubrimiento antimicrobiano […]
Formulación de Mesna y su uso, del 29 de Abril de 2020, de AuXin Surgery SA: Un dispositivo para administrar una formulación de Mesna a tejidos y/u órganos, que comprende una primera cámara que comprende el Mesna en forma sólida, una segunda cámara […]
Nuevos dispositivo médico y composición para ingeniería tisular basados en A-PRP, máquinas y procesos de fabricación, del 18 de Marzo de 2020, de Regen Lab SA: Una composición que comprende al menos un ácido hialurónico de bajo peso molecular y al menos un ácido hialurónico de alto peso molecular caracterizada por que: […]
Emulsiones de copolímero de politetrafluoroetileno, del 12 de Febrero de 2020, de W.L. GORE & ASSOCIATES, INC.: Un método de preparación de una emulsión de agua en disolvente que comprende un copolímero de tetrafluoroetileno disuelto en un disolvente orgánico miscible […]
Método de fabricación de dispositivos médicos antitrombogénicos, del 12 de Febrero de 2020, de Covidien LP (100.0%): Un metodo para proporcionar un dispositivo medico, en donde el dispositivo medico comprende: un cuerpo tubular expandible que comprende una pluralidad de […]