Procedimiento para preparar 3,3'',5,5'',6,6''-hexaalquil-2,2''-bifenoles, 3,3''-4,4'',5,5''-hexaalquil-2,2''-bifenoles y 3,3'',4,4'',5,5'',6,6''-octaalquil-2,2''-bifenoles.
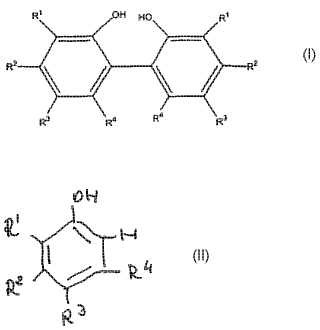
Un procedimiento para preparar un compuesto de la fórmula**Fórmula**
que comprende:
el acoplamiento oxidativo de un compuesto de la fórmula**Fórmula**
a una temperatura entre 5ºC y 100ºC, en un disolvente aprótico inerte que tiene un punto de inflamación más altoque la temperatura de reacción, en presencia de un gas que contiene oxígeno molecular y un catalizador quecontiene cobre, catalizador que contiene cobre producido por un procedimiento que comprende poner en contactouna sal haluro de cobre con un compuesto diamina orgánica, en la que
R1 es alquilo C1-6 primario, secundario o cicloalquilo;
R2 es H, alquilo C1-6 primario, secundario, terciario o cicloalquilo;
R3 es alquilo C1-6 primario, secundario, terciario o cicloalquilio;
R4 es H, alquilo C1-6 primario, secundario o cicloalquilo,
con la condición de que R2 y R4 15 no sean ambos H.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2002/037306.
Solicitante: INVISTA TECHNOLOGIES S.A.R.L..
Nacionalidad solicitante: Suiza.
Dirección: Zweigniederlassung St. Gallen, Kreuzackerstrasse 9 9000 St. Gallen SUIZA.
Inventor/es: SHAPIRO, RAFAEL.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C07B61/00 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07B PROCESOS GENERALES DE QUIMICA ORGANICA; SUS APARATOS (preparación de ésteres de ácidos carboxílicos por telomerización C07C 67/47; procesos para la preparación de compuestos macromoleculares, p.ej. telomerzación C08F, C08G). › Otros procesos generales.
- C07C37/11 C07 […] › C07C COMPUESTOS ACICLICOS O CARBOCICLICOS (compuestos macromoleculares C08; producción de compuestos orgánicos por electrolisiso electroforesis C25B 3/00, C25B 7/00). › C07C 37/00 Preparación de compuestos que tienen grupos hidroxilo o grupos O-metal unidos a un átomo de carbono de un ciclo aromático de seis miembros. › por reacciones que aumentan el número de átomos de carbono.
- C07C39/12 C07C […] › C07C 39/00 Compuestos que tienen al menos un grupo hidroxilo u O-metal unido a un átomo de carbono de un ciclo aromático de seis miembros. › policíclicos sin otra insaturación que la de los ciclos aromáticos.
- C07C39/15 C07C 39/00 […] › estando todos los grupos hidroxilo unidos a ciclos no condensados.
PDF original: ES-2449040_T3.pdf
Fragmento de la descripción:
Procedimiento para preparar 3, 3’, 5, 5’, 6, 6’-hexaalquil-2, 2’-bifenoles, 3, 3’- 4, 4’, 5, 5’-hexaalquil-2, 2’-bifenoles y 3, 3’, 4, 4’, 5, 5’, 6, 6’-octaalquil-2, 2’-bifenoles Campo de la invención La invención se refiere a un procedimiento para preparar 3, 3’, 4, 4’, 5, 5’, 6, 6’-octaalquil-2, 2’-bifenoles. 3, 3’, 4, 4’, 5, 5’hexaalquil 2, 2’-bifenoles y 3, 3’, 5, 5’, 6, 6’-hexaalquil-2, 2’-bifenoles.
Antecedentes de la invención Los bifenoles sustituidos tales como 3, 3’, 6, 6’-tetraalquil-2, 2’bifenol; 3, 3’, 4, 4’, 5, 5’-hexaalquil-2, 2’-bifenoles; 3, 3’, 4, 4’, 5, 5’, 6, 6’-octaalquil-2, 2’-bifenoles; 3, 3’, 5, 5’, 6, 6’-hexaalquil-2, 2’-bifenoles; 3, 3’, 5, 5’-tetraalquil-2, 2’-bifenol; 3-alquil5, 5’, 6, 6’, 7, 7’, 8, 8’-octahidro-2, 2’-binaftol; 3, 3’-dialquil-5, 5’, 6, 6’, 7, 7’, 8, 8’-octahidro-2, 2’-binaftol y 3, 3’, 6, 6’-tetraalquil5, 5’-dihalo-2, 2’-bifenol son compuestos que se pueden usar para preparar ligandos de catalizadores basados en fósforo. Tales ligandos incluyen fosfinas, fosfinitos, fosfonitos y fosfitos. Los ligandos monofosforosos son compuestos que contienen un único átomo de fósforo que actúa como dador a un metal de transición, mientras que los ligandos bifosforosos en general contienen dos átomos de fósforo dadores y típicamente forman estructuras cíclicas de quelato con metales de transición.
En general, los bifenoles se pueden preparar por acoplamiento oxidativo de monofenoles, pero con frecuencia se obtienen otros tipos de productos tales como cetonas, y/o por otras razones los rendimientos globales son malos.
Los fenoles se pueden acoplar oxidativamente para producir los correspondientes bifenoles usando una variedad de agentes oxidantes tales como ácido nítrico, cloruro férrico, ferricianuro potásico, ácido crómico, 2, 3-dicloro-5, 6dicianobenzoquinona y peróxido de dibutilo. Se puede preparar 2, 2’-dihidroxi-3, 3’-di-isopropil-6, 6’-dimetilbifenilo a partir de 2-isopropil-5-metilfenol con 2, 3-dicloro-5, 6-dicianobenzoquinona o di-t-butilperóxido. Véase Tetrahedron, 1875, 1971 y J. Chem. Soc., Perkin Trans. II, 587, 1983. Algunos de los oxidantes y/o cocatalizadores implican el uso de compuestos relativamente caros y/o explosivos (peróxidos) , que tienen inconvenientes para uso comercial a gran escala.
Los fenoles también se pueden acoplar oxidativamente usando una combinación de un catalizador de metal de transición y un agente oxidante tal como un anión persulfato u oxígeno. Véanse patentes U.S. nos. 6.077.979, 4.139.544, 4.132.722, 4.354.048 y 4.108.908, J. Org. Chem. 1984, 49, 4456 y J. Org. Chem. 1983, 48, 4948. Las patentes citadas describen el uso de oxígeno como agente oxidante con diversos catalizadores complejos de cobre tales como cromito de cobre, acetato de cobre con mercaptoacetato sódico, acetato de cobre con dietilentriaminapentaacetato pentasódico y acetato de cobre con ácido 1, 3-diamino-2-hidroxipropano-tetraacético. Los ejemplos de las patentes describen el uso de fenol 2, 6-disustituido o 2, 4-di-t-butilfenol.
El uso de catalizadores de cobre-amina con oxígeno como agente oxidante se ha descrito en conexión con el acoplamiento oxidante de 2, 4-di-t-butilfenol, 2-metil-4-t-butilfenol, 2-cloro-4-t-butilfenol y 4-t-butilfenol. Véase J. Org. Chem. 1984, 49, 4456 y J. Org. Chem. 1983, 48, 4948.
Hay una necesidad continua en la técnica de procedimientos para producir con rendimientos decentes bifenoles sustituidos adecuados para preparar ligandos de catalizador basado en fósforo.
El documento US-B-4085124 da cuenta del acoplamiento oxidativo acuoso de alquilfenoles, alcoxifenoles y 1naftofenoles.
J. Chem. Soc. 1951, págs. 1726-1730 describe la oxidación acuosa con peróxido de hidrógeno de p-cresol, m-4xilenol, m-2-xilenol y mesitol.
El Bulletin de la Societé chimique de France, 1957, págs. 304-310 discute la síntesis y reactividad de 4-metiltimol.
Sumario de la invención En un primer aspecto, la presente invención es un procedimiento para preparar un compuesto de la fórmula
que comprende: el acoplamiento oxidativo de un compuesto de la fórmula
contiene cobre, catalizador que contiene cobre producido por un procedimiento que comprende poner en contacto una sal haluro de cobre con un compuesto diamina orgánica, en la que R1 es alquilo C1-6 primario, secundario o cicloalquilo; R2 es H, alquilo C1-6 primario, secundario, terciario o cicloalquilo; R3 es alquilo C1-6 primario, secundario, terciario o cicloalquilio; R4 es H, alquilo C1-6 primario, secundario o cicloalquilo, con tal que R2 y R4 no sean ambos H. En un segundo aspecto, la presente invención es un compuesto de la fórmula
en la que R1 es etilo, n-propilo o isopropilo; R2 es H o metilo; R3 es metilo, etilo, n-propilo, isopropilo o t-butilo, y R4 es metilo; con la condición de que si R1 es isopropilo y R2 es hidrógeno, R3 no sea metilo. Los compuestos preferidos son los descritos antes en los que R1 es isopropilo, R2 es H o metilo, R3 es metilo, isopropilo o t-butilo, y R4 es metilo. Son compuestos muy preferidos de los del párrafo inmediatamente precedente aquellos en los que R2 es H, R3 es isopropilo y R4 es metilo.
Descripción detallada de la invención La presente invención proporciona un procedimiento para preparar 3, 3’, 5, 5’, 6, 6’-hexaalquil-2, 2’-bifenol, 3, 3’, 4, 4’, 5, 5’-hexaalquil-2, 2’-bifenol o 3, 3’, 4, 4’, 5, 5’, 6, 6’-octaalquil-2, 2’-bifenol por acoplamiento oxidativo de 2, 4, 5trialquilfenol, 2, 3, 4-trialquilfenol o 2, 3, 4, 5-tetraalquilfenol, respectivamente, con un catalizador cobre-amina y
oxígeno como agente oxidante. Los fenoles adecuados están representados por la fórmula en la que R1 es alquilo C1-6 primario, secundario o cicloalquilo;
R2 es H, alquilo C1-6 primario, secundario, terciario o cicloalquilo; R3 es alquilo C1-6 primario, secundario, terciario o cicloalquilio; R4 es H, alquilo C1-6 primario, secundario o cicloalquilo, con tal que R2 y R4 no sean ambos H. Los grupos alquilo pueden estar unidosentre sí o desunidos. Por ejemplo, los grupos alquilo R1 y R2 pueden estar
conectados formando grupos alquilo cíclicos condensados. Análogamente, los grupos alquilo R2 y R3, o R3 y R4 10 pueden estar conectados formando grupos alquilo cíclicos condensados. Algunos 2, 4, 5-trialquilfenoles, 2, 3, 4trialquilfenoles y 2, 3, 4, 5-tetraalquilfenoles representativos son los que se muestran en las fórmulas siguientes
La dimerización de 2, 4, 5-trialquilfenoles, 2, 3, 4-trialquilfenoles, 2, 3, 4, 5-tetraalquilfenoles o 2.4-dialquilfenoles por
acoplamiento oxidativo conduce a los correspondientes bifenoles. El acoplamiento oxidativo se realiza con una o varias gamas de disolventes apróticos, entre los que están incluidos diclorometano, clorobenceno, tolueno, xilenos, nitrometano, parafinas, etc. Como oxidante se usa un gas que contiene oxígeno molecular. Por ejemplo, en el acoplamiento oxidativo se puede usar aire estático, una corriente de aire, u oxígeno. Típicamente la reacción se realiza poniendo en contacto el fenol con un complejo de cobre de una diamina en un disolvente inerte,
preferiblemente aprótico, tal como diclorometano, tolueno, clorobenceno, o un hidrocarburo saturado, preferiblemente uno que tenga un punto de inflamación más alto que la temperatura de reacción, a una temperatura entre 5 y 100ºC, preferiblemente en torno a 30ºC. Generalmente el producto se aísla por dilución con un disolvente hidrocarburo saturado, filtración y opcionalmente purificación por lavado con un ácido mineral acuoso o un reactivo secuestrador de cobre tal como EDTA sódico. Opcionalmente el bifenol se puede purificar por recristalización.
El catalizador de cobre-diamina se puede preparar usando el procedimiento descrito en Tetrahedron Letters, 1994, 35, 7983. Se añade un haluro de cobre tal como CuCl, CuBr, CuI, CuCl2 a una mezcla de un alcohol tal como
metanol, y agua y se añade lentamente la diamina. Después de la adición de la diamina, se hace pasar por la mezcla aire con una agitación vigorosa. Se filtra el catalizador. Se puede obtener catalizador adicional concentrando el filtrado y filtrando el catalizador deseado. También se puede preparar el catalizador in situ poniendo en contacto el haluro de cobre y la diamina en el disolvente para la reacción... [Seguir leyendo]
Reivindicaciones:
1. Un procedimiento para preparar un compuesto de la fórmula
que comprende: el acoplamiento oxidativo de un compuesto de la fórmula
a una temperatura entre 5ºC y 100ºC, en un disolvente aprótico inerte que tiene un punto de inflamación más alto que la temperatura de reacción, en presencia de un gas que contiene oxígeno molecular y un catalizador que contiene cobre, catalizador que contiene cobre producido por un procedimiento que comprende poner en contacto una sal haluro de cobre con un compuesto diamina orgánica, en la que R1 es alquilo C1-6 primario, secundario o cicloalquilo; R2 es H, alquilo C1-6 primario, secundario, terciario o cicloalquilo; R3 es alquilo C1-6 primario, secundario, terciario o cicloalquilio; R4 es H, alquilo C1-6 primario, secundario o cicloalquilo,
con la condición de que R2 y R4 no sean ambos H.
2. El procedimiento de la reivindicación 1, en el que la sal haluro de cobre es CuCl, CuBr, CuI o CuCl2.
3. El procedimiento de la reivindicación 2, en el que el compuesto diamina orgánica es N, N, N’, N’-tetraetilendiamina, N, N, N’, N’-tetraetil-1, 3-propanodiamina, N, N, N’, N’-tetraetilmetanodiamina, N, N, N’, N’-tetrametil-1, 6-hexanodiamina, N, N, N’, N’-tetrametil-1, 3-propanodiamina, dipiperidinometano, N, N, N’, N’-tetrametiletilendiamina o 1, 4-diazabiciclo
(2, 2, 2) octano.
4. El procedimiento de la reivindicación 3, en el que cada uno de R2, R3 y R4 es metilo o etilo.
5. Un compuesto de la fórmula
en la que R1 es etilo, n-propilo o isopropilo; R2 es H o metilo; R3 es metilo, etilo, n-propilo isopropilo o t-butilo, y
R4 es metilo, con la condición de que si R1 es isopropilo y R2 es hidrógeno, R3 no sea metilo.
6. Un compuesto de la reivindicación 5, en el que R2 es H o metilo,
R3 es metilo, isopropilo o t-butilo, y R4 es metilo.
7. Un compuesto de la reivindicación 6, en el que R2 es H y R3 es isopropilo.
Patentes similares o relacionadas:
Procedimiento para la preparación de orto-fenilfenol (OPP), del 13 de Mayo de 2020, de LANXESS DEUTSCHLAND GMBH: Procedimiento para la preparación de orto-fenilfenol (OPP) mediante deshidrogenación catalítica de al menos un compuesto del componente A, que […]
Composiciones para el tratamiento de la fibrosis y de las afecciones relacionadas con la fibrosis, del 23 de Octubre de 2019, de VECTUS BIOSYSTEMS LIMITED: Un compuesto de la fórmula:**Fórmula** en donde: A se selecciona de un heterociclo de 5 o 6 miembros opcionalmente substituido saturado, parcialmente saturado […]
Compuestos de 1-fenil(3,4-disustituido)-2-feniletano(3,4-disustituido) y uso de los mismos, del 11 de Septiembre de 2019, de L'OREAL: Uso cosmético, en una composición con un medio fisiológicamente aceptable, de al menos un compuesto de fórmula (I):**Fórmula** donde: […]
Serie de compuestos para blanquear (aclarar) la piel, del 10 de Julio de 2019, de Unigen, Inc: Un compuesto de fórmula I:**Fórmula** o una sal farmacéuticamente aceptable del mismo, en donde R es un fenilo sustituido, un bifenilo sustituido, […]
MONÓMEROS DE RESINA Y AGENTES DE CURADO DE BASE BIOLÓGICA DERIVADOS DE EUGENOL Y USO DE LOS MISMOS, del 17 de Enero de 2019, de FUNDACION IMDEA MATERIALES: Monómeros de resina y agentes de curado de base biológica derivados de eugenol y uso de los mismos. La presente invención se refiere a monómeros de resina […]
Procedimiento mejorado para producir (S)-equol, del 30 de Noviembre de 2016, de DR. REDDY'S LABORATORIES LTD.: Un procedimiento para la preparación de (S)-equol **Fórmula** que comprende: (a) hacer reaccionar ácido 4-hidroxi fenil acético y 2,4-dihidroxi benzaldehído en presencia […]
INHIBIDORES DE LA HISTIDINA QUINASA CON ACTIVIDAD ANTIBACTERIANA, del 12 de Mayo de 2016, de CONSEJO SUPERIOR DE INVESTIGACIONES CIENTIFICAS (CSIC): La presente invención se refiere a un grupo de compuestos con actividad inhibidorade la autofosforilación y actividad antibacteriana frente a diferentes […]
Inhibidores de la histidina quinasa con actividad antibacteriana, del 10 de Mayo de 2016, de CONSEJO SUPERIOR DE INVESTIGACIONES CIENTIFICAS (CSIC): Inhibidores de la histidina guinasa con actividad antibacteriana. La presente invención se refiere a un grupo de compuestos con actividad inhibidora de la autofosforilación […]