Material compuesto de estilbita-nanohidroxiapatita, procedimiento de preparación y utilización para la eliminación de fluoruro del agua.
La presente invención se refiere a un material compuesto basado en una zeolita natural rica en Calcio,
estilbita, en cuya superficie se hace crecer de manera controlada hidroxiapatita de tamaño nanométrico, al procedimiento mediante el cual se obtiene dicho material compuesto, así como a su aplicación en la eliminación de fluoruro del agua con fines de potabilización.
Como consecuencia de las citadas características particulares de los cristales de hidroxiapatita, ésta posee una capacidad intrínseca (en base a peso de hidroxiapatita) de eliminación de fluoruro extremadamente elevada lo cual, unido al bajo coste y fácil accesibilidad de los materiales empleados en su preparación, así como a la facilidad del procedimiento, convierte estos materiales en candidatos idóneos para su empleo en la eliminación de fluoruro de aguas ricas en este contaminante.
Tipo: Patente de Invención. Resumen de patente/invención. Número de Solicitud: P201330262.
Solicitante: CONSEJO SUPERIOR DE INVESTIGACIONES CIENTIFICAS (CSIC).
Nacionalidad solicitante: España.
Inventor/es: DIAZ CARRETERO,ISABEL, GOMEZ - HORTIGUELA SAINZ,LUIS, CHEBUDE,Yonas, PÉREZ PARIENTE,Jaquín.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- B01J20/16 TECNICAS INDUSTRIALES DIVERSAS; TRANSPORTES. › B01 PROCEDIMIENTOS O APARATOS FISICOS O QUIMICOS EN GENERAL. › B01J PROCEDIMIENTOS QUÍMICOS O FÍSICOS, p. ej. CATÁLISIS O QUÍMICA DE LOS COLOIDES; APARATOS ADECUADOS. › B01J 20/00 Composiciones absorbentes o adsorbentes sólidas o composiciones que facilitan la filtración; Absorbentes o adsorbentes para cromatografía; Procedimientos para su preparación, regeneración o reactivación. › Alumino-silicatos (B01J 20/12 tiene prioridad).
- B01J20/30 B01J 20/00 […] › Procedimientos de preparación, de regeneración o de reactivación.
- C02F1/28 QUIMICA; METALURGIA. › C02 TRATAMIENTO DEL AGUA, AGUA RESIDUAL, DE ALCANTARILLA O FANGOS. › C02F TRATAMIENTO DEL AGUA, AGUA RESIDUAL, DE ALCANTARILLA O FANGOS (procedimientos para transformar las sustancias químicas nocivas en inocuas o menos perjudiciales, efectuando un cambio químico en las sustancias A62D 3/00; separación, tanques de sedimentación o dispositivos de filtro B01D; disposiciones relativas a las instalaciones para el tratamiento del agua, agua residual o de alcantarilla en los buques, p. ej. para producir agua dulce, B63J; adición al agua de sustancias para impedir la corrosión C23F; tratamiento de líquidos contaminados por radiactividad G21F 9/04). › C02F 1/00 Tratamiento del agua, agua residual o de alcantarilla (C02F 3/00 - C02F 9/00 tienen prioridad). › por absorción o adsorción (utilizando cambiadores de iones C02F 1/42; composiciones absorbentes o adsorbentes B01J).
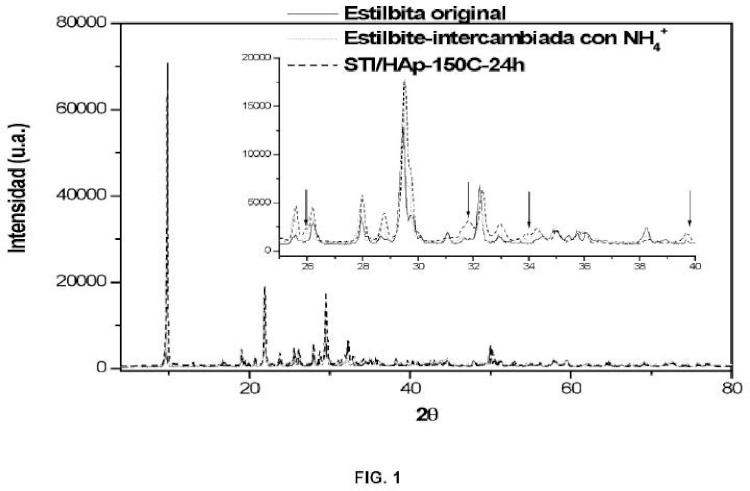
Fragmento de la descripción:
Material compuesto de estilbita-nanohidroxiapatita, procedimiento de preparación y utilización para la eliminación de fluoruro del agua SECTOR DE LA TÉCNICA
La presente invención se sitúa principalmente en el sector de los productos minerales no metálicos y en el sector de la quimica, ya que se refiere a un material compuesto formado por cristales de nanohidroxiapatita crecidos sobre la superficie de la zeolita natural estilbita, que presenta una alta capacidad de eliminación de fluoruro, y a su procedimiento de obtención.
Adicionalmente, se sitúa también en el sector del tratamiento de aguas, dentro de un marco medioambiental benigno al emplear materiales naturales y no perjudiciales para el medio ambiente, ya que las características del material compuesto y su preparación, lo convierten en una alternativa idónea para el tratamiento de eliminación de fluoruro en aguas.
ESTADO DE LA TÉCNICA
El agua representa una materia prima esencial para el desarrollo de la vida. La composición química del agua procedente de diversas fuentes naturales constituye el principal factor que determina su finalidad: en industria, en agricultura, o para uso doméstico (incluyendo agua para beber) . A pesar de que el agua procedente del subsuelo implica únicamente un 0, 6%
del total de agua disponible en la corteza terrestre, ésta supone el principal suministro de agua para beber.
El ión fluoruro (F") constituye uno de los aniones más abundantes en aguas del subsuelo de todo el mundo. El f1uoruro está presente en rocas y suelos de la corteza terrestre. En este contexto, la presencia de fluoruro en aguas del subsuelo procede fundamentalmente de la disolución parcial de minerales que contienen fluoruro, principalmente fluorita (CaF2) , criolita (Na, AIFPO, ) y fluoroapatita (Ca5 (P04hF) , presentes en las rocas del subsuelo.
La presencia de fluoruro en agua para beber puede ser beneficiosa o perjudicial para la salud en función de su concentración. En concentraciones en agua entre 0, 4 y 1, 0 mg/L, el fluoruro es beneficioso, especialmente en niños de menos de 8 años, para la calcificación del esmalte dental. Por el contrario, una ingesta elevada de fluoruro puede dar lugar a Iluorosis dental y/o esqueleta!. Asi pues, la Organización Mundial de la Salud (OMS) estableció el valor límite máximo de concentración de fluoruro en aguas para consumo humano en 1, 5 mg/L (WHO, Guidelines for drinking water quality, 1985, Vol. 3, 1-2, World
Health Organization, Geneva) .
Elevadas concentraciones de fluoruro están frecuentemente presentes en aguas del subsuelo donde el tiempo de contacto entre el agua y los minerales ricos en F es mayor, especialmente en Norteamérica, Ã?frica, sobre todo en la zona del Valle del Rift, y Asia. En España, en concreto en la zona norte de Tenerife, también se han observado elevadas concentraciones de fluoruro en aguas y casos asociados de fluorosis. Por tanto, el desarrollo de tecnologías, preferiblemente de bajo coste y no perjudiciales para el medio ambiente, para la eliminación de fluoruro de agua por debajo del límite establecido por la OMS representa hoy en día un objetivo vital a nivel mundial.
En la actualidad existen diversas tecnologías para la eliminación de fluoruro de agua; sin embargo, no existe un acuerdo ampliamente aceptado sobre la más conveniente. Las tecnologías existentes incluyen precipitación-coagulación , procesos basados en membranas, métodos de intercambio iónico, y métodos de adsorción (S. Jagtap, M. K.
Yenkie, N. Labhsetwar, S. Rayalu, Chem. Rev. 112 (2012) 2454-2466) .
En los métodos de adsorción el fluoruro se elimina por adsorción en diversos tipos de materiales (adsorbentes) . Estos métodos son los más prometedores debido a su bajo coste y facilidad de operación, elevada eficacia, fácil accesibilidad, respeto al medioambiente, y
reciclado de los adsorbentes.
La principal cuestión en la implantación de los métodos de adsorción es la selección del material adsorbente adecuado. La evaluación de un adsorbente implica la consideración de su capacidad de adsorción en disoluciones diluidas, pH, tiempo de eliminación, estabilidad 30 del adsorbente, capacidad de regeneración, posibles interferencias con otros iones, y por supuesto, su coste y accesibilidad . Se ha estudiado una gran variedad de materiales sintéticos y naturales, incluyendo alúminas activadas e impregnadas, óxidos de tierras raras, arcillas y otros materiales derivados de suelos, sílices impregnadas, materiales carbonosos, materiales basados en Calcio, materiales de desechos industriales, zeolitas o biopolímeros 35 naturales. Sin embargo, al disminuir la concentración de fluoruro en el agua (a concentraciones reales presentes en aguas del subsuelo, en general menor de 10 mg/L) ,
muchos de estos materiales pierden parcialmente su capacidad de eliminar fluoruro, y frecuentemente no son capaces de reducir la concentración de f1uoruro por debajo del límite de 1, 5 mg/L. Además, en ocasiones, liberan especies al agua que pueden resultar perjudiciales.
Uno de los adsorbentes más ampliamente usados es la hidroxiapatita (HAp, Cas (P04hOH) , debido a su capacidad para intercambiar iones hidróxido por f1uoruro, que ha sido ampliamente discutido en la bibliografía, especialmente debido a su bajo coste y elevada eficacia. Estudios iniciales demostraron la capacidad de la HAp de reducir la concentración de fluoruro por debajo de 1, 5 mg/L. Se observó además que la capacidad de eliminación de fluoruro de la HAp depende del tamaño de partícula: la capacidad de eliminación aumentaba con la reducción del tamaño de partícula. El principal mecanismo de eliminación de fluoruro por parte de la HAp transcurre a través de la sustitución isomórfica del hidróxido por f1uoruro en la red cristalina debido a su misma carga eléctrica y similar radio iónico, unido a la mayor estabilidad de la f1uoroapatita. Asumiendo este mecanismo, la capacidad teórica máxima de eliminación de fluoruro sería de 37, 8 mg de F-/g de HAp. No obstante, en la red cristalina de la HAp, los iones hidróxido se encuentran en el centro de canales de 6 miembros, y por tanto la difusión a través de estos canales y la consiguiente sustitución isomórfica por fluoruro está parcialmente restringida, lo que explica la mayor capacidad intrínseca de eliminación observada a menores tamaños de partícula. En este sentido, la disminución del tamaño de partícula de la HAp a la escala nanométrica debería conllevar una notable mejora de la capacidad de eliminación . De hecho, se han observado elevadas capacidades de eliminación para nanohidroxiapatitas (nHAp) , con capacidades en general entre 1 y 2 mg de F /g de HAp. En todo caso, estos valores de capacidad son sensiblemente inferiores al máximo teórico de 37, 8 mg (F-) /g, suponiendo menos de un 10% de sustitución del hidróxido presente en la HAp, poniendo de manifiesto de nuevo los problemas difusionales.
No obstante, el tamaño nanométrico de estas HAps implica que su empleo en aplicaciones reales puede dar lugar a caídas de presión significativas durante los procesos de filtración, lo cual resulta un inconveniente importante. Para evitar esto, Sundaram y colaboradores prepararon materiales compuestos de HAp y biopolímeros como quitosano o quitina (C. Sundaram, N. Viswanathan, S. Meenakshi, BioresourceTechn. 99 (2008) 8226-8230. 2. C. Sundaram, N. Viswanathan, S. Meenakshi, J. Haz. Mater. 172 (2009) 147-151) , los cuales pueden ser preparados en cualquier forma deseada, dando lugar a razonables capacidades de eliminación.
Todos estos estudios demuestran que la nHAp es capaz de eliminar f1uoruro por debajo del límite establecido por la OMS, si bien la capacidad es baja comparada con la máxima teórica, debido a las restricciones difusionales. Una reducción del tamaño de particula supondrá una mejora de la capacidad intrínseca de eliminación de la HAp. En este contexto se centra la presente invención, que supone un método de preparación de nanohidroxiapatita de muy elevada capacidad de eliminación , empleando una zeolita natural, estilbita, como fuente de Calcio y agente modulante del crecimiento de la HAp, dando lugar así a un material compuesto zeolita-HAp.
Las zeolitas son aluminosilicatos microporosos cristalinos con una estructura tridimensional definida formada por tetraedros de Si y Al. El ordenamiento tridimensional de estas unidades da lugar a la formación de muy diversas estructuras microporosas. La incorporación de AI+3 en la red inorgánica zeolitica genera una carga negativa en la red que es compensada por la presencia de cationes en los poros y/o cavidades. Estas especies (cationes extrarreticulares) no forman enlace con la red, y por...
Reivindicaciones:
1. Material compuesto de estilbita-nanohidroxiapatita, caracterizado por que comprende: -una zeolita estilbita con una topología formada por canales de pequeño tamaño con diámetros de 0, 50 x 0, 47 nm y 0, 27 x 0, 56 nm, y -cristales de HAp con un porcentaje de hidróxidos intercambiables de al menos un 10%.
2. Material compuesto según la reivindicación 2, caracterizado por que la zeolita estilbita es 10 una zeolita natural estilbita que procede de minas de Etiopía y por que posee un contenido en Ca2 <-de 5, 23% en peso, y una composición molar de la celda unidad de la zeolita (Na094
KO_ (6) (Ca3_5 Mg018) Als_6 Si27A On 3. Procedimiento de obtención del material compuesto según las reivindicaciones 1 y 2, 15 caracterizado por que el crecimiento de cristales de hidroxiapatita sobre la zeolita estilbita se consigue mediante un intercambio catiónico controlado del Ca2 + de la zeolita, y posterior
precipitación de HAp en presencia de una fuente de fósforo sobre la superficie de la zeolita, según ecuaciones 1 a 3 (ac. se refiere a en disolución acuosa) :
(NH4 ) , HP0 4 (dis) ~2NH; (ac) + HPO.'~ (ac) [ec~ 1] 20 STI-Ca'· + 2NH; (ac) ~STI- (NH; ) , + Ca'· (ac) (ec. 2] STI- (NH; ) , + 5Ca'· (ac) + 3HPO/' (ac) + 4N H, (ac) + H, O ~STI- (NH; h "Ca, (P04 ) , OH + 4NH; (ac) (ec. 3]
4. Procedimiento de obtención del material compuesto según la reivindicación 3,
caracterizada por que comprende los siguiente pasos: a) molido de la zeolita estilbita, tamizado a través de tamices con mallas de 200 y 120, Y selección de la fracción con tamaño de partícula menor de 0, 125 mm, b) mezclado de la zeolita estilbita con una fuente de fósforo en una relación comprendida entre 10 9 (zeolita) /30 mi (disolución) y 1 9 (zeolita) /30 mi (disolución) y
agitado durante un período de tiempo comprendido entre 5 y 15 minutos, e) ajuste del pH de la mezcla hasta valores comprendidos entre 8, 5 y 10, 0, incluidos ambos límites, empleando una disolución acuosa de NH3 al 25%,
d) aplicación de un tratamiento térmico que comprende temperaturas desde 15 hasta 170º C, incluidos ambos límites, y durante tiempos que abarcan desde 0, 5 hasta 120 35 horas, incluidos ambos límites,
e) separación del sólido de la disolución por filtración y lavado con agua destilada empleando una relación 1 litro de agua/2 g de sólido, y f) secado del sólido.
5. Procedimiento de obtención del material compuesto según la reivindicación 4, caracterizado por que en la aplicación del paso d) del tratamiento térmico se utilizan temperaturas iguales o superiores a 60º C.
6. Procedimiento de obtención del material compuesto según la reivindicación 4, 10 caracterizado por que en la aplicación del paso d) del tratamiento térmico se utilizan temperaturas inferiores a 60º C e iguales o superiores a 40º C.
7. Procedimiento de obtención del material compuesto según la reivindicación 4, caracterizado por que en la aplicación del tratamiento térmico del paso d) se utilizan 15 temperaturas inferiores a 40º C e iguales o superiores a 15º C.
B. Procedimiento de obtención del material compuesto según las reivindicaciones 4 y 7 caracterizado por que: a) la zeolita estilbita es una zeolita natural estilbita procedente de minas de Etiopia que se muele utilizando un molino de discos, y se tamiza hasta alcanzar partículas comprendidas en el rango entre 0, 074 y 0, 125 mm, b) el mezclado de la zeolita natural estilbita, con una fuente de fósforo que es fosfato amónico dibásico [ (NH4 hHP0 4] con una concentración 1 M, en una relación 2 g (zeolita) /30 mL (disolución) , se realiza en un bote de polipropileno y se agita durante un período de 10 minutos, c) el ajuste del pH del medio de preparación del material compuesto, se realiza a un valor de 9, 0, utilizando una disolución acuosa de NH3 al 25%, d) la aplicación del tratamiento térmico se realiza durante 19 horas y a una temperatura de 23'C.
e) la separación del sólido de la disolución se realiza por filtración a vacío, y lavado con agua destilada en una relación de 1 L por cada 2 g de sólido obtenido, y f) el secado del sólido se realiza al aire.
9. Procedimiento de obtención del material compuesto según las reivindicaciones 4 y 7, 35 caracterizada porque: a) la zeolita estilbita es una zeolita natural estilbita procedente de minas de Etiopía que se muele utilizando un molino de discos, y se tamiza hasta alcanzar partículas comprendidas en el rango entre 0, 074 y 0, 125 mm, b) el mezclado de la zeolita natural estilbita, con una fuente de fósforo que es fosfato amónico dibásico [ (NH4hHP04] con una concentración 1M, en una relación 2 g (zeolita) /30 mL (disolución) , se realiza en un bote de polipropileno y se agita durante un período de 10 minutos, c) el ajuste del pH del medio de preparación del material compuesto, se realiza a un valor de 9, 02, utilizando una disolución acuosa de NHJ al 25%,
d) la aplicación del tratamiento térmico se realiza durante 6 horas y a una temperatura de 23'C. e) la separación del sólido de la disolución se realiza por filtración a vacío, y lavado con agua destilada en una relación de 1 L por cada 2 g de sólido obtenido, y f) el secado del sólido se realiza al aire.
1.
10. Uso del material compuesto segun las reivindicaciones 1 y 2, para la eliminación de fluoruro en agua.
. Uso del material compuesto segun la reivindicación 10, caracterizada por que comprende las siguientes etapas: i) preparación del material compuesto segun una cualquiera de las reivindicaciones 3 a 9, ii) contacto en agitación del material compuesto con aguas que tienen una concentración inicial de fluoruro comprendida entre 4 y 20 mg/L y pH entre 6 y 8, 5 a una relación comprendida entre 2 y 50 g de material por litro de agua a tratar durante un periodo de tiempo comprendido entre 0, 5 y 20 horas, y iii) regeneración del material compuesto mediante tratamiento con una disolución de NaOH a pH=11 en agitación durante un período de tiempo comprendido entre 0, 5 y 24 horas.
3.
12. Uso del material compuesto segun la reivindicación 11, caracterizado por que: i) la preparación del material compuesto se realiza segun una cualquiera de las reivindicaciones 3 a 9, ii) el contacto en agitación del material de la invención se realiza con aguas que comprenden una concentración inicial de fluoruro de 10, 8 mg/L, y valor de pH de 8, a una relación de 10 g de material por litro de agua a tratar, y durante un periodo de tiempo de 19 horas, y iii) la regeneración del material compuesto, se realiza con una disolución de NaOH a pH=11 en agitación, durante un periodo de tiempo de 3 horas.
Patentes similares o relacionadas:
Composición a base de hidroxiapatita en polvo para el tratamiento del linfoma B o T, del 1 de Julio de 2020, de URODELIA: Composición para uso como autovacuna antitumoral para el tratamiento de linfomas B o T en un sujeto, que comprende un polvo de hidroxiapatita y/o de […]
Arena para animales autoaglomerante extruida y método de fabricación de arena para animales autoaglomerante extruida, del 17 de Junio de 2020, de Pioneer Pet Products, LLC: Una arena para gatos autoaglomerante formada por gránulos de arena compuestos de pellas extruidas que contienen almidón y que tienen, cada una, una pluralidad de […]
Desulfuración y procedimientos novedosos para la misma, del 17 de Junio de 2020, de CHINA PETROLEUM & CHEMICAL CORPORATION: Procedimiento para la producción de una composición que comprende: (a) mezclar: 1) un líquido, 2) un compuesto que contiene cinc, 3) un material […]
Membranas para cromatografía formadas por reacciones de polimerización clic de tiol-eno o tiol-ino, del 10 de Junio de 2020, de Merck Millipore Ltd: Un material compuesto, que comprende: un miembro de soporte, que comprende una pluralidad de poros que se extienden a través del miembro de […]
RED HÍBRIDA METAL-ORGÁNICA MULTIVARIANTE CONSTITUIDA POR DOS METALES Y LIGANDOS OXAMIDATO DIFERENTES Y SU UTILIZACIÓN COMO ADSORBENTE SIMULTÁNEO DE CONTAMINANTES INORGÁNICOS Y ORGÁNICOS, del 4 de Junio de 2020, de UNIVERSITAT DE VALENCIA: La presente invención se refiere a una red híbrida metal-orgánica multivariante constituida por dos metales diferentes (M1 y M2) con al menos dos ligandos oxamidato diferentes […]
RED HÍBRIDA METAL-ORGÁNICA MULTIVARIANTE CONSTITUIDA POR DOS METALES Y LIGANDOS OXAMIDATO DIFERENTES Y SU UTILIZACIÓN COMO ADSORBENTE SIMULTÁNEO DE CONTAMINANTES INORGÁNICOS Y ORGÁNICOS, del 2 de Junio de 2020, de UNIVERSITAT DE VALENCIA: La presente invención se refiere a una red híbrida metal-orgánica multivariante constituida por dos metales diferentes (M1 y M2) con al menos dos […]
MATERIAL METAL-ORGÁNICO CRISTALINO BASADO EN MAGNESIO, PROCEDIMIENTO DE SÍNTESIS Y USOS, del 28 de Mayo de 2020, de UNIVERSIDAD REY JUAN CARLOS: La presente invención se refiere a un material metal-orgánico cristalino que está formado por iones Mg2+ que están coordinados con […]
MATERIAL METAL-ORGÁNICO CRISTALINO BASADO EN MAGNESIO, PROCEDIMIENTO DE SÍNTESIS Y USOS, del 25 de Mayo de 2020, de UNIVERSIDAD REY JUAN CARLOS: La presente invención se refiere a un material metal-orgánico cristalino que está formado por iones Mg2+ que están coordinados con iones de ácido 3,3',5,5'-azobenzeno […]