Aparato, sistemas y métodos para lograr la neuromodulación renal intravascular térmicamente inducida.
Un aparato de catéter (12) para la inserción en una arteria femoral,
arteria ilíaca y la aorta abdominal deun paciente, que comprende:
un vástago alargado (16) que se extiende por un eje, comprendiendo el vástago alargadouna región extrema proximal (18) que incluye una sección (30) de transmisión de fuerza yuna región extrema distal (20),
un mango (22) acoplado a la región extrema proximal (18);
con lo cual
la región extrema distal (18) incluye una primera zona de flexión (32) distal de la sección (30) de transmisión defuerza, una segunda zona de flexión (34) que se extiende en sentido distal desde la primera zona de flexión (32) yuna tercera zona de flexión (44) junto a, y que se extiende en sentido distal más allá de, la segunda zona de flexión(34); y el aparato de catéter (12) comprende además:
un elemento de calentamiento térmico (21) llevado por, y que se extiende en sentido distal más allá de, la tercerazona de flexión (44) en el que el elemento de calentamiento térmico (24) se configura para someter a ablacióntérmica los nervios renales adyacentes a la arteria renal;
un elemento de control de flexión (40) acoplado a la segunda zona de flexión (34) y configurado para aplicar unaprimera fuerza a la segunda zona de flexión (34) para mover la segunda zona de flexión (34) de la región distal delvástago alargado en una dirección radial lejos del eje y hacia una pared de la arteria renal;
una estructura flexible dentro de la tercera zona de flexión (44) que está acoplada al elemento de calentamientotérmico (24) y configurada para permitir la flexión pasiva alrededor del eje en respuesta a una segunda fuerzaaplicada al elemento de calentamiento térmico (24) a través del contacto con la pared de la arteria renal;
un controlador de flexión (42) llevado por el mango y acoplado al elemento de control de flexión (40), en el que elcontrolador de flexión (42) se configura para hacer que el elemento de control de flexión (40) aplique la primerafuerza para mover la segunda zona de flexión (34); y
un conector (28) llevado por el mango (22) y configurado para conectar el elemento de calentamiento térmico (24) auna fuente de energía térmica,
caracterizado porque dichas zonas de flexión se adaptan además para facilitar la navegación del elemento térmicoen una arteria renal y la neuromodulación renal térmicamente inducida desde dentro de dicha arteria renal de dichopaciente.
Tipo: Patente Europea. Resumen de patente/invención. Número de Solicitud: E09167937.
Solicitante: Medtronic Ardian Luxembourg S.à.r.l.
Nacionalidad solicitante: Luxemburgo.
Dirección: 102 rue des Maraîchers 2124 Luxembourg LUXEMBURGO.
Inventor/es: THAI,Erik, Clark,Benjamin,J, Wu,Andrew, Zarins,Denise.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61B18/14 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61B DIAGNOSTICO; CIRUGIA; IDENTIFICACION (análisis de material biológico G01N, p.ej. G01N 33/48). › A61B 18/00 Instrumentos, dispositivos o procedimientos quirúrgicos para transferir formas de energía no mecánica hacia o desde el cuerpo (cirugía ocular A61F 9/007; cirugía otorrina A61F 11/00). › Sondas o electrodos a tal efecto.
PDF original: ES-2386829_T3.pdf
Fragmento de la descripción:
Aparato, sistemas y métodos para lograr la neuromodulación renal intravascular térmicamente inducida
Ámbito técnico
Las tecnologías descritas en la presente solicitud están relacionadas generalmente con aparatos, sistemas y métodos para la neuromodulación intravascular. Más particularmente, las tecnologías descritas en esta memoria están relacionadas con aparatos, sistemas y métodos para lograr la neuromodulación renal intravascular mediante calentamiento térmico.
Antecedentes
La hipertensión, el fallo del corazón y la enfermedad renal crónica representan un asunto mundial de la salud significativo y creciente. Las terapias actuales para estas situaciones incluyen enfoques no farmacológicos, farmacológicos y basados en dispositivos. A pesar de esta variedad de opciones de tratamiento, las tasas de control de la tensión arterial y los esfuerzos terapéuticos para prevenir la progresión del fallo del corazón y la enfermedad renal crónica y sus secuelas siguen siendo insatisfactorias. Aunque las razones de esta situación sean múltiples e incluyan asuntos de incumplimiento con la terapia prescrita, la heterogeneidad de las respuestas en función de la eficacia y el perfil de acontecimientos adversos y otros, es evidente que se necesitan opciones alternativas para complementar los regímenes actuales de tratamiento terapéutico para estas condiciones.
La reducción de la actividad del nervio simpático renal (por ejemplo, mediante denervación) , puede invertir estos procesos. Ardian, Inc. ha descubierto que un campo de energía, incluyendo y comprendiendo un campo eléctrico, puede iniciar la neuromodulación renal mediante denervación causada por electroevaporación irreversible, electrofusión, apoptosis, necrosis, ablación, alteración térmica, alteración de expresión genética u otra modalidad adecuada.
Un dispositivo según el preámbulo de la reivindicación 1 se conoce a partir del documento WO2006121883.
Sumario
El siguiente sumario se proporciona solo en beneficio del lector y no está pensado para limitar de ninguna manera la descripción. La invención se define en la reivindicación 1.
Un aspecto de la presente solicitud proporciona aparatos, sistemas y métodos que incorporan un dispositivo de tratamiento que comprende un vástago alargado. El vástago alargado se dimensiona y se configura para administrar un elemento de calentamiento térmico a una arteria renal a través de un recorrido intravascular que incluye una arteria femoral, una arteria ilíaca y la aorta. Las diferentes secciones del vástago alargado sirven como diferentes funciones mecánicas cuando está en uso. Las secciones se diferencian en función de su tamaño, configuración y propiedades mecánicas para (i) introducción percutánea en una arteria femoral por un lugar de acceso de diámetro pequeño; (ii) paso atraumático a través del recorrido sinuoso intravascular a través de una arteria ilíaca, a la aorta y a una respectiva arteria renal izquierda/derecha, incluyendo (iii) dar cabida a una flexión significativa en la unión de las arterias renales izquierda/derecha y la aorta para obtener una entrada a la respectiva arteria renal izquierda o derecha; (iv) dar cabida a una traslación controlada, desviación y/o rotación dentro de la respectiva arteria renal para alcanzar las proximidades y una alineación deseada con una pared interior de la respectiva arteria renal; y (v) permitir la colocación de un elemento de calentamiento térmico en contacto con tejido en la pared interior con una orientación que optimice el área superficial activa del elemento de calentamiento térmico.
Breve descripción de los dibujos
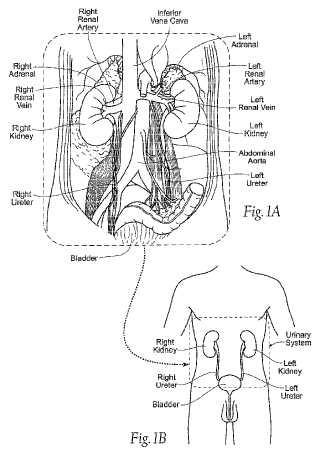
La Fig. 1A es una vista interior anatómica de una cavidad torácica de un humano, con los intestinos quitados, que muestra los riñones y estructuras circundantes.
La Fig. 1B en una vista anatómica del sistema urinario de un humano, del que forman parte los riñones mostrados en la Fig. 1A.
Las Figs. 2A, 2B, y 2C son una serie de vistas anatómicas ampliadas que muestran varias regiones interiores de un riñón humano.
La Fig. 3A es una ilustración conceptual del sistema nervioso simpático (SNS) y cómo se comunica el cerebro con el cuerpo a través del SNS.
La Fig. 3B es una vista anatómica ampliada de los nervios que inervan a un riñón izquierdo para formar el plexo renal que rodea la arteria renal izquierda.
Las Figs. 3C y 3D proporcionan unas vistas anatómicas y conceptuales de un cuerpo humano, respectivamente, que representa la comunicación neural eferente y aferente entre el cerebro y los riñones
Las Figs. 4A y 4B son, respectivamente, unas vistas anatómicas de los sistemas vasculares arterial y venoso de un humano.
La Fig. 5 es una vista en perspectiva de un sistema para lograr la neuromodulación renal intravascular, térmicamente inducida, que comprende un dispositivo de tratamiento y un generador.
Las Figs. 6A y 6B son unas vistas anatómicas de la administración intravascular, la desviación y la colocación del dispositivo de tratamiento mostrado en la Fig. 5 a través de la arteria femoral y a una arteria renal.
Las Figs. 7A a 7D son una serie de vistas del vástago alargado del dispositivo de tratamiento mostrado en la Fig. 5, que muestran las diferentes regiones mecánicas y funcionales que incorpora el vástago alargado.
La Fig. 7E muestra una vista anatómica de la colocación del dispositivo de tratamiento mostrado en la Fig. 5 dentro de las dimensiones de la arteria renal.
Las Figs. 8A a 8C muestran la colocación de un elemento de calentamiento térmico, que es llevado en el extremo distal del vástago alargado del dispositivo de tratamiento mostrado en la Fig. 5, hasta el contacto con tejido por una arteria renal.
Las Figs. 9A y 9B muestran la colocación del elemento de calentamiento térmico mostrado en las Figs. 8A a 8C hasta el contacto con tejido a lo largo de una arteria renal y la administración del tratamiento térmico al plexo renal.
Las Figs. 10A y 10B muestran una realización representativa de la sección de transmisión de fuerza del vástago alargado del dispositivo de tratamiento mostrado en la Fig. 5.
Las Figs. 11A a 11C muestran una realización representativa de la zona proximal de flexión del vástago alargado del dispositivo de tratamiento mostrado en la Fig. 5.
Las Figs. 12A a 12D muestran una realización representativa de la zona intermedia de flexión del vástago alargado del dispositivo de tratamiento mostrado en la Fig. 5.
Las Figs. 13A a 13C muestran unas realizaciones alternativas de la zona intermedia de flexión del vástago alargado del dispositivo de tratamiento mostrado en la Fig. 5.
Las Figs. 14A a 14C muestran unas realizaciones alternativas de la zona intermedia de flexión del vástago alargado del dispositivo de tratamiento mostrado en la Fig. 5.
Las Figs. 15A a 15C muestran una realización representativa de la zona distal de flexión del vástago alargado del dispositivo de tratamiento mostrado en la Fig. 5.
Las Figs. 15D a 15F muestran múltiples vistas planas de la capacidad de doblado de la zona distal de flexión del vástago alargado del dispositivo de tratamiento mostrado en la Fig. 5.
Las Figs. 15G a 15H muestran unas realizaciones alternativas de la zona distal de flexión correspondiente al vástago alargado del dispositivo de tratamiento mostrado en la Fig. 5.
Las Figs. 151 y 15J muestran una realización alternativa de catéter del dispositivo de tratamiento mostrado en la Fig. 5 que comprende una sección intermedia que comprende un alambre de arco.
Las Figs. 16A y 16B muestran una realización representativa de un mecanismo de control rotatorio acoplado al mango del dispositivo de tratamiento mostrado en la Fig. 5.
Las Figs. 16C y 16D muestran un mango del dispositivo de tratamiento mostrado en la Fig. 5 con un mecanismo de control rotatorio que tiene un elemento de limitación de rotación y una palanca de accionamiento.
Las Figs. 17A y 17B son unas realizaciones representativas alternativas de un vástago alargado para un dispositivo de tratamiento como el mostrado en la Fig. 5, que muestran unos ejemplos de las diferentes regiones mecánicas... [Seguir leyendo]
Reivindicaciones:
1. Un aparato de catéter (12) para la inserción en una arteria femoral, arteria ilíaca y la aorta abdominal de un paciente, que comprende:
un vástago alargado (16) que se extiende por un eje, comprendiendo el vástago alargado
una región extrema proximal (18) que incluye una sección (30) de transmisión de fuerza y
una región extrema distal (20) ,
un mango (22) acoplado a la región extrema proximal (18) ;
con lo cual
la región extrema distal (18) incluye una primera zona de flexión (32) distal de la sección (30) de transmisión de fuerza, una segunda zona de flexión (34) que se extiende en sentido distal desde la primera zona de flexión (32) y una tercera zona de flexión (44) junto a, y que se extiende en sentido distal más allá de, la segunda zona de flexión (34) ; y el aparato de catéter (12) comprende además:
un elemento de calentamiento térmico (21) llevado por, y que se extiende en sentido distal más allá de, la tercera zona de flexión (44) en el que el elemento de calentamiento térmico (24) se configura para someter a ablación térmica los nervios renales adyacentes a la arteria renal;
un elemento de control de flexión (40) acoplado a la segunda zona de flexión (34) y configurado para aplicar una primera fuerza a la segunda zona de flexión (34) para mover la segunda zona de flexión (34) de la región distal del vástago alargado en una dirección radial lejos del eje y hacia una pared de la arteria renal;
una estructura flexible dentro de la tercera zona de flexión (44) que está acoplada al elemento de calentamiento térmico (24) y configurada para permitir la flexión pasiva alrededor del eje en respuesta a una segunda fuerza aplicada al elemento de calentamiento térmico (24) a través del contacto con la pared de la arteria renal;
un controlador de flexión (42) llevado por el mango y acoplado al elemento de control de flexión (40) , en el que el controlador de flexión (42) se configura para hacer que el elemento de control de flexión (40) aplique la primera fuerza para mover la segunda zona de flexión (34) ; y
un conector (28) llevado por el mango (22) y configurado para conectar el elemento de calentamiento térmico (24) a una fuente de energía térmica,
caracterizado porque dichas zonas de flexión se adaptan además para facilitar la navegación del elemento térmico en una arteria renal y la neuromodulación renal térmicamente inducida desde dentro de dicha arteria renal de dicho paciente.
2. El aparato de catéter (12) de la reivindicación 1 en el que la segunda zona de flexión (34) se configura para moverse en una dirección radial predeterminada en respuesta a la primera fuerza aplicada por el elemento de control de flexión (40) .
3. El aparato de catéter de cualquiera de las reivindicaciones 1 a 2 en el que el elemento de control de flexión comprende un alambre (40) acoplado a una parte distal de la segunda zona de flexión (34) , y en el que la primera fuerza aplicada a la segunda zona de flexión (34) es una fuerza de doblado o de compresión que resulta del accionamiento del controlador de flexión (42) .
4. El aparato de catéter de una cualquiera de las reivindicaciones 1 a 3, que comprende además un sensor adyacente a, sobre, o dentro del elemento de calentamiento térmico (24) , y en el que el sensor se configura para monitorizar un parámetro de por lo menos el aparato y la superficie del tejido.
5. El aparato de catéter de la reivindicación 4 en el que el sensor es por lo menos uno de un sensor de temperatura, sensor de impedancia, sensor óptico o micro sensor.
6. El aparato de catéter de una cualquiera de las reivindicaciones 4 a 5, que comprende además un sistema de control de reacción configurado para alterar el tratamiento administrado a la pared renal de la arteria en respuesta al parámetro monitorizado.
7. El aparato de catéter de la reivindicación 6 en el que el sistema de control de reacción comprende un algoritmo (102) para controlar la producción de la fuente de energía térmica (26) .
8. El aparato de catéter de una cualquiera de las reivindicaciones 1 a 7 en el que el elemento de control de flexión (40) y la estructura flexible se configuran para crear mutuamente, a través de la segunda zona de
flexión (34) y la tercera zona de flexión (44) , una fuerza estabilizadora entre el elemento de calentamiento térmico (24) y la pared de la arteria renal.
9. El aparato de catéter de la reivindicación 8 en el que la fuerza estabilizadora hace que por lo menos un veinticinco por ciento del área superficial total del elemento de calentamiento térmico (24) haga contacto con la pared de la arteria renal.
10. El aparato de catéter de una cualquiera de las reivindicaciones 1 a 9 en el que el elemento de calentamiento térmico (24) se configura para aplicar tratamiento a la pared de la arteria renal utilizando energía de radiofrecuencia.
11. El aparato de catéter de una cualquiera de las reivindicaciones 1 a 10 en el que la tercera zona de flexión
(44) tiene una longitud de aproximadamente 2 mm a aproximadamente 5 mm.
12. El aparato de catéter de una cualquiera de las reivindicaciones 1 a 11, que comprende además un marcador radiopaco configurado para facilitar la visualización angiográfica del aparato de catéter.
13. El aparato de catéter de una cualquiera de las reivindicaciones 1 a 12 en el que el mango (22) comprende un accesorio rotatorio acoplado al vástago alargado (16) y configurado para rotar el vástago alargado (16) alrededor del eje sin rotar el mango (22) , y en el que el accesorio rotatorio comprende un elemento de limitación de rotación configurado para impedir la rotación del vástago alargado más allá de un número predeterminado de vueltas.
14. El aparato de catéter de una cualquiera de las reivindicaciones 1 a 13 en el que el aparato de catéter es un componente de un kit de tratamiento médico, y en el que el kit de tratamiento médico comprende además un cable configurado para conectar eléctricamente el aparato de catéter a la fuente de energía térmica y un electrodo dispersivo configurado para proporcionar un recorrido de regreso para un campo de energía del aparato de catéter.
15. El aparato de catéter de una cualquiera de las reivindicaciones 1 a 14 en el que la segunda zona de flexión (34) tiene una longitud de aproximadamente 5 mm a aproximadamente 15 mm.
16. El aparato de catéter de una cualquiera de las reivindicaciones 1 a 15 en el que la primera zona de flexión (32) es más flexible que la sección (30) de transmisión de fuerza del vástago alargado (16) .
17. El aparato de catéter de una cualquiera de las reivindicaciones 1 a 16 en el que el elemento de calentamiento térmico se adapta para aplicar tratamiento térmico utilizando por lo menos una de energía de RF, luz, microondas, ultrasonidos, fluido calentado.
18. El aparato de catéter de una cualquiera de las reivindicaciones 1 a 17 en el que el elemento de calentamiento térmico comprende un electrodo.
Patentes similares o relacionadas:
Dispositivos médicos inflables, del 29 de Julio de 2020, de Loma Vista Medical, Inc: Balón inflable, que comprende: un balón de base que tiene una sección cilíndrica y una sección cónica; al menos una fibra (86a) circunferencial […]
Aparato electroquirúrgico para el suministro de energía de radiofrecuencia y energía de microondas, del 8 de Julio de 2020, de Creo Medical Limited: Aparato electroquirúrgico que comprende: un generador electroquirúrgico dispuesto para generar energía electromagnética de radiofrecuencia […]
Estructura de aguja para realizar biopsias por punción, del 8 de Julio de 2020, de Creo Medical Limited: Aparato quirúrgico para introducir material a través de una aguja en un tejido biológico, comprendiendo el aparato: una fuente de alimentación para suministrar […]
Electrodo bipolar para ablación por radiofrecuencia, del 1 de Julio de 2020, de STARmed Co., Ltd: Un electrodo bipolar para ablación por radiofrecuencia, comprendiendo el electrodo: un cuerpo cilíndrico provisto de una primera y […]
Catéter con ramas transversales, del 24 de Junio de 2020, de Biosense Webster (Israel), Ltd: Un aparato, que comprende: un tubo de inserción flexible , que tiene un segmento distal que está configurado para insertarse en un órgano del cuerpo; […]
Aparato para tratar un tumor mediante un campo eléctrico, del 10 de Junio de 2020, de Novocure GmbH: Una prenda de vestir que incorpora un aparato para destruir selectivamente células en división en un área diana de un tejido, teniendo las células […]
Aparato para tratar un tumor mediante un campo eléctrico, del 10 de Junio de 2020, de Novocure GmbH: Un aparato para destruir selectivamente células en división en un área diana de tejido, teniendo las células en división componentes intracelulares […]
Aparato para tratar un tumor mediante un campo eléctrico, del 10 de Junio de 2020, de Novocure GmbH: Un aparato para destruir selectivamente células en división en tejido que se va a tratar por debajo de la piel, teniendo las células en división componentes intracelulares […]