UN KIT PARA DETECCIÓN INMUNOLOGICA DE NUROGLOBULINA LIGADA A ENZIMA Y USO DEL MISMO.
Un kit NGB-ELISA que comprende un anticuerpo monoclonal anti-NGB,
un anticuerpo policlonal anti-NGB, un anticuerpo marcado con enzimas y un patrón de proteína NGB, en el que el anticuerpo monoclonal anti- NGB se obtiene inmunizando ratones con el antígeno de NGB seguido por la fusión celular para producir una célula de hibridoma y posteriormente cultivando la célula de hibridoma, en el que el anticuerpo policlonal anti- NGB se obtiene inmunizando un animal con el antígeno de NGB y recogiendo a continuación del suero del animal, y en el que la proteína NGB patrón es el antígeno de NGB obtenido por medio de las siguientes etapas: (1) construir un vector de expresión procariota que contenga una secuencia de ADNc de NGB de longitud integral de origen humano; (2) transformar el vector de expresión procariota construido en la cepa HB101 de E. coli, y a continuación seleccionar los clones positivos; (3) inducir la expresión de NGB por estimulación térmica para obtener un producto de expresión; y (4) purificar el producto de expresión en primer lugar por filtración en gel y a continuación por cromatografía de intercambio aniónico para obtener el antígeno de NGB
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/CN2005/000613.
Solicitante: INSTITUTE OF RADIATION MEDICINE, ACADEMY OF MILITARY MEDICAL SCIENCES; PEOPLE'S LIBERATION ARMY OF
BEIJING THREEMAN MEDICINE SCIENCE AND TECHNOLOGY LIMITED COMPANY.
Nacionalidad solicitante: China.
Dirección: 27 TAIPING ROAD HAIDAN DISTRICT BEIJING 100850 CHINA.
Inventor/es: WANG,Lihong , CHEN,Tingfang , SHANG,Aijia , GAO,Yan , ZHANG,Chennang.
Fecha de Publicación: .
Fecha Solicitud PCT: 30 de Abril de 2005.
Clasificación Internacional de Patentes:
- G01N33/68V2
Clasificación PCT:
- G01N33/53 FISICA. › G01 METROLOGIA; ENSAYOS. › G01N INVESTIGACION O ANALISIS DE MATERIALES POR DETERMINACION DE SUS PROPIEDADES QUIMICAS O FISICAS (procedimientos de medida, de investigación o de análisis diferentes de los ensayos inmunológicos, en los que intervienen enzimas o microorganismos C12M, C12Q). › G01N 33/00 Investigación o análisis de materiales por métodos específicos no cubiertos por los grupos G01N 1/00 - G01N 31/00. › Ensayos inmunológicos; Ensayos en los que interviene la formación de uniones bioespecíficas; Materiales a este efecto.
- G01N33/535 G01N 33/00 […] › con un marcador enzimático.
- G01N33/577 G01N 33/00 […] › en los que interviene anticuerpos monoclonados.
- G01N33/68 G01N 33/00 […] › en los que intervienen proteínas, péptidos o aminoácidos.
- G01N33/72 G01N 33/00 […] › en los que intervienen pigmentos de la sangre, p. ej. la hemoglobina, la bilirrubina.
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Eslovenia, Finlandia, Rumania, Chipre, Lituania.
Fragmento de la descripción:
Campo de la invención
La presente invención se refiere a un kit de inmunoensayo, en especial a un kit de ensayo de inmunoabsorción de neuroglobina ligado a enzima (kit NGB-ELISA) para detectar la neuroglobina y a un uso del mismo. 5
Antecedentes de la invención
La neuroglobina (NGB) es el tercer tipo de proteína transportadora de oxígeno aparte de la hemoglobina y la mioglobina. La proteína NGB se expresa especialmente en el sistema nervioso y se distribuye extensamente en el cerebro. Al igual que la mioglobina, la proteína NGB puede fijar el oxígeno de manera reversible con una afinidad de fijación muy alta. Es bien sabido que la concentración de mioglobina en el suero es muy baja 10 para su detección en el individuo normal, por lo que cuando se producen heridas en los músculos cardiacos y en los músculos esqueléticos, la mioglobina se liberará a la sangre desde las células lesionadas, dando como resultado un aumento significativo de la proteína mioglobina en el suero. Por consiguiente, se ha considerado a la concentración de mioglobina en el suero (mioglobina sérica) un marcador biológico específico y sensible para algunas enfermedades importantes tales como el infarto de miocardio y la insuficiencia renal, etc. Es 15 interesante destacar que las características de la NGB y la MGB son muy similares entre sí. Por ejemplo, hay 151 aminoácidos (aa) en la proteína NGB, y 154 aa en la proteína MGB. El peso molecular tanto para la MGB como para la NGB es de 17 kD. Puesto que las funciones de la NGB y la MGB son tan similares (es decir, la MGB es responsable del suministro de oxígeno del músculo cardíaco y del músculo esquelético, mientras que la NGB es responsable del suministro de oxígeno del cerebro), y ambas pueden ser liberadas en el suero 20 desde las células lesionadas, es razonable deducir que la concentración de la proteína NGB en el suero tiene valor potencial para el diagnóstico clínico de las enfermedades del sistema nervioso tales como la enfermedad de Alzheimer, el ictus y otros daños cerebrales. De manera análoga, la detección de la proteína NGB en la sangre tiene también un valor significativo para revelar el estadio de la enfermedad cuando nos referimos a las anteriores enfermedades del sistema nervioso. 25
Actualmente, el principal procedimiento para detectar la proteína NGB es el análisis de inmunotransferencia. En detalle, los usuarios deben someter la muestra de prueba en primer lugar a SDS-PAGE y a continuación deben detectar la proteína NGB con un anticuerpo anti-NGB, seguido por la reacción usando un segundo anticuerpo específico marcado con enzimas para posteriormente exponer la señal de la banda en la película de rayos X. Finalmente, los usuarios deben realizar la exploración de la película en un ordenador para 30 realizar otro análisis de imágenes para estimar aproximadamente el nivel de la proteína NGB en la muestra de prueba. La mayor desventaja de este procedimiento es que no puede obtenerse la concentración exacta de la proteína NGB.
Resumen de la invención
El objeto de la presente invención es proporcionar un kit NGB-ELISA para medir la concentración de la 35 proteína NGB en diversas muestras.
El kit NGB-ELISA de la presente invención comprende un anticuerpo monoclonal anti-NGB, un anticuerpo policlonal anti-NGB, un anticuerpo marcado con enzimas y un patrón de NGB, en el que el anticuerpo monoclonal anti-NGB se obtiene inmunizando ratones con el antígeno de NGB seguido por la fusión celular para producir una célula de hibridoma y posteriormente cultivando la célula de hibridoma; en el que el 40 anticuerpo policlonal anti-NGB se obtiene inmunizando un animal con el antígeno de NGB y recogiendo a continuación del suero del animal, y en el que la proteína NGB patrón es el antígeno de NGB obtenido por medio de las siguientes etapas:
(1) construir un vector de expresión procariota que contenga una secuencia de ADNc de NGB de longitud integral de origen humano; 45
(2) transformar el vector de expresión procariota construido en la cepa HB101 de E. coli, y a continuación seleccionar los clones positivos;
(3) inducir la expresión de NGB por estimulación térmica para obtener un producto de expresión; y
(4) purificar el producto de expresión en primer lugar por filtración en gel y a continuación por cromatografía de intercambio aniónico para obtener el antígeno de NGB. 50
Más específicamente, el vector de expresión procariota es pBV220-rhNGB.
Las condiciones para cultivar los clones positivos son: inocular la cepa de E. coli en medio de cultivo LB que contiene ampicilina 80-120 μg/ml y cultivar durante 2-3 horas a 28-32 ºC, seguido por el cultivo con agitación a 40-44 ºC para inducir la expresión de rhNGB.
En el kit según la invención, el anticuerpo marcado con enzimas es típicamente inmunoglobulina de cabra anti-conejo marcada con HRP. 5
Por lo general, el kit NGB-ELISA comprende además la placa de marcado con enzimas, la proteína NGB patrón y reactivo para el desarrollar color. En la presente invención, el reactivo para desarrollar el color es TMB (3,3‟,5.5‟-tetrametilbencidina).
Otro objeto de la presente invención es proporcionar un uso del kit NGB-ELISA.
El kit de la presente invención tiene especificidad alta y sensibilidad alta. Por consiguiente, el kit puede 10 utilizarse para ayudar en el diagnóstico clínico de la demencia senil, el infarto cerebral o la lesión traumática del cerebro.
Breve descripción de los dibujos
La Figura 1 es un diagrama que muestra el dibujo de la electroforesis del producto amplificado de rhNGB obtenido por la técnica de PCR; 15
La Figura 2 son diagramas que muestran el mapa de restricción de los clones positivos para rhNGB después de identificar por medio de PCR y el procedimiento de enzimas de restricción, respectivamente;
La Figura 3 es un diagrama que muestra el análisis de inmunotransferencia del anticuerpo monoclonal obtenido;
La Figura 4 son diagramas que muestran la identificación de la subclase de los anticuerpos monoclonales 20 obtenidos;
La Figura 5 son diagramas que muestran el análisis de inmunotransferencia del anticuerpo policlonal obtenido;
La Figura 6 es un diagrama que muestra la distribución de las proteínas NGB en el cerebro de un jerbo adulto detectadas por medio del anticuerpo policlonal obtenido; 25
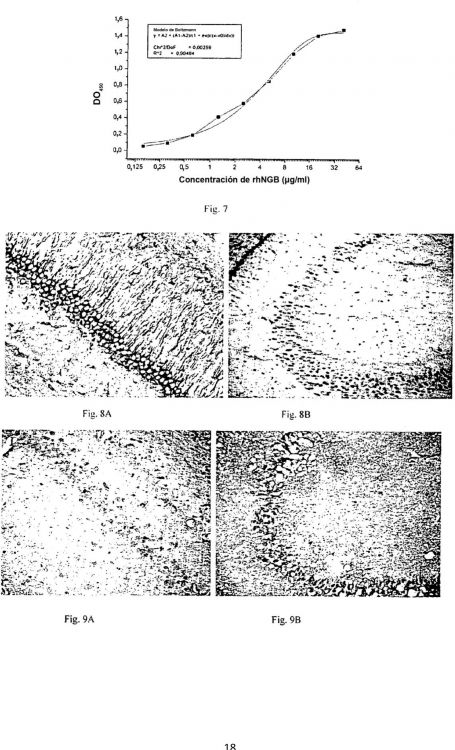
La Figura 7 es un diagrama que muestra la curva patrón para la proteína NGB detectada por el kit de la presente invención;
La Figura 8 son diagramas que muestran la distribución de las neuronas positivas para NGB en el hipocampo del jerbo;
La Figura 9 son diagramas que muestran la distribución de las neuronas positivas para NGB en el cerebro 72 30 horas después de la lesión por reperfusión tras la isquemia;
La Figura 10 es un diagrama que muestra el cambio serológico de la NGB en el cerebro del jerbo de 2 a 72 horas después de la lesión por reperfusión tras la isquemia.
Descripción detallada de la invención
Ejemplo 1. La preparación del kit NGB-ELISA 35
I. Preparación del antígeno de NGB
1. Construcción de la cepa de E. coli de pBV220-rhNGB/HB101 1
1) Síntesis de los cebadores: los cebadores específicos de NGB pU y pD se diseñaron y sintetizaron según la secuencia conocida de un gen humano de NGB (hNGB), en el que se incorpora al extremo 5‟ del cebador “pU” un sitio de restricción de EcoRI y un codón de inicio ATG, y se incorpora al extremo 5' 40 del cebador “pD” un sitio de restricción de BamHI. Los cebadores fueron sintetizados por Shangai Boya Biotechnique Inc. Las secuencias de los cebadores son:
pU: 5‟-CCggAATTCATggAgCgCCCggAg-3‟
pD: 5‟-ggTggATCCTTACTCgCCATCCCAgCCTCg-3‟.
2) Amplificación por PCR: se utilizó el fragmento de ADNc del gen humano de la neuroglobina (a saber, Neurosurvivin (NSV)), que fue obtenido en nuestro laboratorio previamente de la biblioteca de ADNc de cerebro fetal humano por la técnica de PCR) como molde para realizar la amplificación por PCR con los cebadores sintetizados en la etapa 1) (Referencia: Burmester T, Weich B, Reinhardt S, Hankeln T. A vertebrate globin expressed in the brain. Nature. 2000;...
Reivindicaciones:
1. Un kit NGB-ELISA que comprende un anticuerpo monoclonal anti-NGB, un anticuerpo policlonal anti-NGB, un anticuerpo marcado con enzimas y un patrón de proteína NGB, en el que el anticuerpo monoclonal anti-NGB se obtiene inmunizando ratones con el antígeno de NGB seguido por la fusión celular para producir una célula de hibridoma y posteriormente cultivando la célula de hibridoma, en el que el anticuerpo policlonal anti-5 NGB se obtiene inmunizando un animal con el antígeno de NGB y recogiendo a continuación del suero del animal, y en el que la proteína NGB patrón es el antígeno de NGB obtenido por medio de las siguientes etapas:
(1) construir un vector de expresión procariota que contenga una secuencia de ADNc de NGB de longitud integral de origen humano; 10
(2) transformar el vector de expresión procariota construido en la cepa HB101 de E. coli, y a continuación seleccionar los clones positivos;
(3) inducir la expresión de NGB por estimulación térmica para obtener un producto de expresión; y
(4) purificar el producto de expresión en primer lugar por filtración en gel y a continuación por cromatografía de intercambio aniónico para obtener el antígeno de NGB. 15
2. El kit NGB-ELISA según la reivindicación 1, en el que el vector de expresión procariota es pBV220-rhNGB.
3. El kit NGB-ELISA según la reivindicación 1, en el que las condiciones para el cultivo de los clones positivos son: inocular la cepa de E. coli en medio de cultivo LB que contiene 80-120 μg/ml de ampicilina y cultivar durante 2-3 horas a 28-32 ºC, seguido por el cultivo con agitación a 40-44 ºC para inducir la expresión de rhNGB. 20
4. El kit NGB-ELISA según cualquiera de las reivindicaciones 1-3, en el que el anticuerpo marcado con enzimas es inmunoglobulina de cabra anti-conejo marcada con HRP.
5. El kit NGB-ELISA según cualquiera de las reivindicaciones 1-3, en el que el kit NGB-ELISA comprende además una placa de marcación enzimática y un reactivo de desarrollo de color.
6. El kit NGB-ELISA según la reivindicación 5, en el que el reactivo de desarrollo de color es 3,3‟,5,5‟-25 tetrametilbencidina (TMB).
7. Un uso del kit NGB-ELISA según la reivindicación 1 para ayudar en el diagnóstico clínico de la demencia senil, el infarto cerebral o la lesión traumática del cerebro.
Patentes similares o relacionadas:
ENSAYO DE PRIONES, del 8 de Febrero de 2012, de NOVARTIS AG: Un procedimiento de ensayo, que comprende las etapas de: (a) obtener una muestra que se sospecha que contiene una forma patógena de proteína priónica (PrP Sc ) que […]
COMPOSICIONES Y USOS PARA ESTABILIZAR LA TRANSTIRETINA E INHIBIR EL PLEGAMIENTO ANÓMALO DE LA TRANSTIRETINA, del 7 de Febrero de 2012, de THE SCRIPPS RESEARCH INSTITUTE: Diflunisal para uso en el tratamiento de una enfermedad amiloide por transtiretina, en donde el diflunisal se prepara para ser administrado en una cantidad de 250 mg […]
EMPLEO DE INHIBIDORES DE ADAM-17 EN REGENERACIÓN NEURONAL, del 5 de Diciembre de 2011, de UNIVERSIDAD DE CADIZ: La presente invención se refiere al uso de un agente inhibidor de la actividad y/o expresión de ADAM-17 en la preparación de un medicamento, o composición farmacéutica, para […]
PROCEDIMIENTO IN VITRO PARA LA DIAGNOSIS DE ENFERMEDADES NEURODEGENERATIVAS, del 1 de Diciembre de 2011, de B.R.A.H.M.S GMBH: Procedimiento in vitro para la detección, para determinación del grado de severidad y para la valoración evolutiva y la prognosis de enfermedades neurodegenerativas, caracterizado […]
MÉTODO DE DIAGNÓSTICO IN VITRO DE LA ENFERMEDAD DE ALZHEIMER MEDIANTE UN ANTICUERPO MONOCLONAL, del 8 de Noviembre de 2011, de CONSEJO SUPERIOR DE INVESTIGACIONES CIENTIFICAS: Método de diagnóstico in vitro de la enfermedad de Alzheimer medante un anticuerpo monoclonal. Dicho anticuerpo es capaz de unire al menos a los aminoácidos 12-16 del […]
PRODUCTOS DE DEGRADACIÓN PROTEOLÍTICA DE MAP-2 COMO BIOMARCADORES DE DIAGNÓSTICO PARA LAS LESIONES NEURALES, del 2 de Noviembre de 2011, de UNIVERSITY OF FLORIDA RESEARCH FOUNDATION, INC. BANYAN BIOMARKERS: Método in vitro para determinar la presencia de una lesión neural en un sujeto, que comprende detectar por lo menos uno o más productos de degradación proteolítica de una […]
PROCEDIMIENTO DE COMPROBACIÓN Y CONTROL DEL PROCESO DE FERMENTACIÓN DEL ÁCIDO LÁCTICO EN MAMÍFEROS/RUTA METABÓLICA DE FERMENTACIÓN AEROBIA DE LA GLUCOSA EN EL ORGANISMO DE MAMÍFEROS, del 5 de Septiembre de 2011, de COY, JOHANNES, DR.: El uso de la enzima TKTL1 como molécula indicadora y diana para la detección cualitativa y cuantitativa del grado de uso y del flujo correcto del proceso de la ruta […]
MÉTODOS DE TRATAMIENTO DE PSICOSIS Y ESQUIZOFRENIA BASADOS EN POLIMORFISMOS DEL GEN DEL CNTF, del 23 de Agosto de 2011, de NOVARTIS AG: Un método para determinar la capacidad de respuesta de un individuo con un trastorno psicótico al tratamiento con Iloperidona, que comprende; […]