Vector retroviral seudotipo que contiene proteína de membrana que tiene actividad hemaglutinina.
Un método para producir un vector retroviral seudotipo, comprendiendo el método la etapa de transcribir un ADN vector de transferencia génica derivado de retrovirus a una célula de empaquetamiento que comprende ADN que codifica las proteínas HN y F del virus Sendai de una manera expresable,
en donde una porción de un dominio citoplásmico de la proteína F ha sido suprimida para conservar de 0 a 4 aminoácidos del dominio citoplásmico para producir un vector retroviral seudotipo que tiene dichas proteínas HN y F.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/JP2001/004659.
Solicitante: DNAVEC RESEARCH INC..
Nacionalidad solicitante: Japón.
Dirección: 25-11 Kannondai 1-chome Tsukuba-shi Ibaraki 305-0856 JAPON.
Inventor/es: IIDA, AKIHIRO, KOBAYASHI, MASANORI, HASEGAWA, MAMORU, YONEMITSU,YOSHIKAZU, UEDA,YASUJI, NAKAJIMA,TOSHIHIRO, NAKAMARU,KENJI, SAKAKIBARA,HIROYUKI.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K35/76 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 35/00 Preparaciones medicinales que contienen sustancias de constitución indeterminada o sus productos de reacción. › Virus; Partículas subvirales; Bacteriófagos.
- A61K48/00 A61K […] › Preparaciones medicinales que contienen material genético que se introduce en las células del cuerpo vivo para tratar enfermedades genéticas; Terapia génica.
- C12N15/09 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 15/00 Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K). › Tecnología del ADN recombinante.
- C12N15/867 C12N 15/00 […] › Vectores retrovirales.
- C12N5/10 C12N […] › C12N 5/00 Células no diferenciadas humanas, animales o vegetales, p. ej. líneas celulares; Tejidos; Su cultivo o conservación; Medios de cultivo para este fin (reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00). › Células modificadas por introducción de material genético extraño, p. ej. células transformadas por virus.
- C12R1/91 C12 […] › C12R SISTEMA DE INDEXACION ASOCIADO A LAS SUBCLASES C12C - C12Q, RELATIVO A LOS MICROORGANISMOS. › C12R 1/00 Microorganismos. › Líneas celulares.
- C12R1/92 C12R 1/00 […] › Virus.
PDF original: ES-2430991_T3.pdf
Fragmento de la descripción:
Vector retroviral seudotipo que contiene proteína de membrana que tiene actividad hemaglutinina
Campo técnico
La presente invención se refiere a vectores virales seudotipo que contienen la proteína HN de paramixovirus.
Técnica anterior
Los vectores retrovirales se han utilizado para expresar genes foráneos en células diana para investigación, terapia génica, etc. Los vectores retrovirales se pueden producir con un método relativamente simple, y también tienen algunas ventajas, como por ejemplo, para introducir genes foráneos en los cromosomas del anfitrión. Normalmente, las proteínas virales localizadas en la envoltura viral juegan un papel crucial en la infección por el vector retroviral. Se ha invertido mucho esfuerzo para ampliar la gama de células anfitrionas a las que los vectores pueden infectar o para desarrollar vectores virales que infectan solamente células específicas mediante la modificación de las proteínas de la envoltura del vector retroviral.
Por ejemplo, se ha desarrollado un sistema en el que se integra la proteína VSV-G en la envoltura del vector retroviral para asegurar la infectividad de una gama más amplia de células anfitrionas (H. Yu et al, 1999, Gene Therapy, 6, 1876 -1883) . La VSV-G es una proteína expresada en la superficie de la envoltura del virus de la estomatitis vesicular, que es infeccioso para una gama considerablemente amplia de células anfitrionas. Además, por ejemplo, proteína F del virus Sendai se ha utilizado como una proteína de envoltura a modo de experimento. Se encontró que un retrovirus seudotipado con la proteína F mostraba una infectividad específica para las células positivas para el receptor asialoglicoproteínas (M. Spiegel et al, 1998, Hepatology, 28, 1429-1429; M. Spiegel et al, 1998, J. Virology, 72, 5296 a 5302) .
Sin embargo, estos retrovirus seudotipo convencionales tienen solo infectividad insuficiente para diversos tejidos y células. Por ejemplo, una variedad de células pluripotenciales, incluyendo células pluripotenciales hematopoyéticas pueden ser células diana importantes en la terapia génica o similar (Y. Hanazono, Molecular Medicine, vol. 36, Núm. 7, 1999) , pero la mayoría de las células pluripotenciales se encuentran en estado de no división (Abkowitz, J. L. et al., Nat. Med., 2 (2) , 190-7, 1996) . En general, resulta difícil introducir genes utilizando el vector retroviral que muestra una baja infectividad contra tales células que no están en división. Además, el sistema vector que utiliza técnicas convencionales ha fracasado al introducir genes en células con abundante matriz extracelular tales como células epiteliales de la mucosa de las vías respiratorias pulmonares. Un método para introducir genes en estos tipos de células requiere la eliminación física de la matriz extracelular, por ejemplo el moco, mediante lavado. Sin embargo, este método es complicado y los tejidos se pueden dañar.
Descripción de la invención Un objetivo de la presente invención es proporcionar vectores retrovirales seudotipo que contienen proteínas de membrana que tienen actividad hemaglutinina.
Los autores de la presente invención seleccionaron proteínas que tenían actividad hemaglutinina como proteínas para retrovirus seudotipo. La hemaglutinina (HAin) es una proteína que induce la hemaglutinación (HA; aglutinación de eritrocitos) , y se sabe que diversos virus tienen esta actividad. Los autores de la presente invención consideraron que se podría construir un vector retroviral susceptible de transferencia génica de alta eficacia para diferentes tipos de células y tejidos basado en un retrovirus con una envoltura que contuviera proteínas de membrana con actividad hemaglutinina. Con el fin de construir tal retrovirus, los autores de la presente invención utilizaron proteínas de la envoltura de paramixovirus que tenían una amplia gama de anfitriones. En primer lugar, basándose en un vector que expresaba la proteína de la envoltura del virus Sendai (SeV) , se seudotipó un vector viral derivado de un retrovirus de ratón con proteína F y/o HN de SeV. Específicamente, utilizando virus de células pluripotenciales murinas (MSCV) como material de partida, se construyó un retrovirus para que tuviera las proteínas F y/o HN de SeV además de la proteína de la envoltura ecotrópica o la proteína de la envoltura anfotrópica; el vector resultante se sometió a ensayo para determinar la eficacia de la transferencia génica a células humanas (Ejemplos 1 y 2) .
Cuando se llevó a cabo el empaquetamiento utilizando la proteína de la envoltura ecotrópica que no mostraba la infectividad para las células humanas, no se consiguió la transferencia génica a las células humanas con el virus seudotipado para la proteína F o la proteína HN solas. Sin embargo, después de haber sido seudotipado mediante la co-expresión de la proteína F y la proteína HN, el virus, que originalmente no tuvo infectividad en células humanas, pudo introducir genes en las células humanas (Eco en la Fig. 1) . Este resultado demostró que la gama de anfitriónes para la infección del vector viral podría ampliarse mediante seudotipado de un vector derivado de virus distintos del virus Sendai utilizando proteína F y proteína HN del virus Sendai.
Se encontró que, cuando el empaquetamiento se llevó a cabo utilizando la proteína de la envoltura anfotrópica que tenía infectividad para las células humanas, mejoró notablemente la eficacia de la transferencia génica mediante el seudotipado del virus o bien mediante la expresión de la proteína HN sola o bien mediante la co-expresión de la proteína F y la proteína HN (Ampho en la Fig. 1) . El resultado demostró que el vector retroviral podría ser por seudotipado por la proteína HN del virus Sendai sola, y que la eficacia de la transferencia génica del vector retroviral se podía mejorar, o bien mediante seudotipado utilizando la proteína HN del virus Sendai sola o bien mediante seudotipado utilizando la proteína F y proteína HN del virus Sendai.
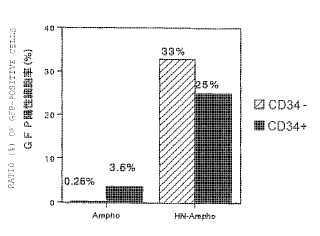
Los autores de la presente invención también prepararon un vector retroviral anfotrópico mediante seudotipado con la proteína HN y determinaron la eficacia de la transferencia génica en células de médula ósea humanas, incluyendo células pluripotenciales hematopoyéticas (Ejemplo 3) . Se infectaron células de médula ósea humana positivas para CD34 con el vector seudotipado con la proteína HN, y las células que contenían el gen introducido se fraccionaron mediante citometría de flujo utilizando CD34 como marcador. El resultado demostró que el seudotipado utilizando la proteína HN mejoró notablemente la eficacia de transferencia génica en células tanto positivas para CD34 como en células negativas para CD34 (Fig. 3) . Se cree que la fracción de células positivas para CD34 contiene células pluripotenciales hematopoyéticas. Por lo tanto, el seudotipado basado en proteína HN también es útil para la transferencia génica a hemocitos y células hematopoyéticas, incluyendo células pluripotenciales hematopoyéticas.
A continuación, utilizando lentivirus que se espera que sea más adecuado como vector para la terapia génica en comparación con otros diversos tipos de retrovirus, los autores de la presente invención construyeron un vector seudotipado con proteína F y/o proteína HN de paramixovirus. El lentivirus usado es el virus de la inmunodeficiencia de simios (SIV) (Ejemplo 5) , que ofrece varias ventajas, incluyendo un mayor grado de seguridad cuando se compara con el virus de la inmunodeficiencia humana (VIH) , comúnmente utilizado en la terapia génica. Las partículas del virus SIV que comprendían la proteína de la envoltura del virus Sendai (SeV) se produjeron preparando virosoma que contenía la envoltura reconstituida a partir de SeV o virus Sendai inactivado y fusionándolos con SIV seudotipado con la proteína VSV-G. Las partículas de virus se incubaron con células humanas para evaluar la eficacia de la infección del vector (Ejemplos 6 y 7) . Los resultados demostraron que el SIV que contenía la envoltura resultante de la fusión con la envoltura de SeV mostraba una mayor infectividad en comparación con SIV seudotipado con la proteína VSV-G (Fig. 8) . El incremento de infectividad fue atribuible a la proteína HN del virus Sendai.
Para estimar de modo preciso la contribución de la proteína de la envoltura de SeV, los autores de la presente invención prepararon virosoma de FHN, virosoma de F y virosoma de HN, y prepararon vectores mediante fusión de SIV seudotipado con VSV-G con cada virosoma. A continuación, se evaluaron los vectores resultantes basándose en experimentos de infección (Ejemplo 7) . El vector que se fusiona con el virosoma de FHN mostró una eficacia de... [Seguir leyendo]
Reivindicaciones:
1. Un método para producir un vector retroviral seudotipo, comprendiendo el método la etapa de transcribir un ADN vector de transferencia génica derivado de retrovirus a una célula de empaquetamiento que comprende ADN que codifica las proteínas HN y F del virus Sendai de una manera expresable, en donde una porción de un dominio citoplásmico de la proteína F ha sido suprimida para conservar de 0 a 4 aminoácidos del dominio citoplásmico para producir un vector retroviral seudotipo que tiene dichas proteínas HN y F.
2. El método de acuerdo con la reivindicación 1, en donde una porción de un dominio citoplásmico de la proteína F ha sido suprimida para conservar 4 aminoácidos del dominio citoplásmico.
3. El método de acuerdo con la reivindicación 1, en donde el dominio citoplásmico de la proteína HN ha sido modificado mediante la adición de o el remplazo por un dominio citoplásmico de una proteína de la envoltura retroviral.
4. El método de acuerdo con la reivindicación 1, en donde la célula de empaquetamiento comprende adicionalmente ADN que codifica la proteína HA de ortomixovirus.
5. El método de acuerdo con la reivindicación 1, en donde la célula de empaquetamiento comprende adicionalmente ADN que codifica una proteína de la envoltura derivada de un virus que es infeccioso para células humanas.
6. El método de acuerdo con la reivindicación 5, en donde la proteína de la envoltura derivada de un virus que es infeccioso para células humanas es
(a) una proteína de la envoltura anfotrópica derivada de un retrovirus; o
(b) la proteína VSV-G derivada de un virus de la estomatitis vesicular.
7. El método de acuerdo con la reivindicación 1, en donde el vector retroviral deriva de
(a) oncovirus; o
(b) lentivirus.
8. El método de acuerdo con la reivindicación 7, en donde el lentivirus deriva del virus de la inmunodeficiencia de simios.
9. El método de acuerdo con la reivindicación 1, en donde el dominio citoplásmico de la proteína HN ha sido modificado para que comprenda un dominio citoplásmico de una proteína de la envoltura del virus de la inmunodeficiencia de simios.
10. El método de acuerdo con la reivindicación 1, en donde la proteína HN del virus Sendai ha sido modificada para que comprenda la secuencia del SEQ ID NO: 40 o 41.
11. El método de acuerdo con la reivindicación 1, en donde la proteína F comprende la secuencia de aminoácidos del SEQ ID NO: 42.
12. El método de acuerdo con la reivindicación 1, en donde la proteína F ha sido modificada adicionalmente para que comprenda un dominio citoplásmico de una proteína de la envoltura del virus de la inmunodeficiencia de simios.
13. El método de acuerdo con la reivindicación 12, en donde la proteína F del virus Sendai comprende la secuencia del SEQ ID NO: 45.
14. El método de acuerdo con una cualquiera de las reivindicaciones 1 a 13, en donde el vector comprende un gen foráneo de una manera expresable.
15. Un vector retroviral seudotipo que tiene las proteínas HN y F del virus Sendai, en donde una porción de un dominio citoplásmico de la proteína F ha sido suprimida para conservar de 0 a 4 aminoácidos del dominio citoplásmico.
16. El vector retroviral seudotipo de acuerdo con la reivindicación 15, en donde una porción de un dominio citoplásmico de la proteína F ha sido suprimida para conservar de 4 aminoácidos del dominio citoplásmico.
17. El vector retroviral seudotipo de acuerdo con la reivindicación 15, en donde el dominio citoplásmico de la proteína HN ha sido modificado mediante la adición de o el remplazo por un dominio citoplásmico de una proteína de la envoltura retroviral.
18. El vector retroviral seudotipo de acuerdo con la reivindicación 15, comprende adicionalmente la proteína HA de ortomixovirus.
19. El vector retroviral seudotipo de acuerdo con la reivindicación 15, comprende adicionalmente una proteína de la envoltura derivada de un virus que es infeccioso para células humanas.
20. El vector retroviral seudotipo de acuerdo con la reivindicación 19, en donde la proteína de la envoltura derivada de un virus que es infeccioso para células humanas es
(a) una proteína de la envoltura anfotrópica derivada de un retrovirus; o
(b) la proteína VSV-G derivada de un virus de la estomatitis vesicular.
21. El vector retroviral seudotipo de acuerdo con la reivindicación 15, en donde el vector retroviral deriva de
(a) oncovirus; o
(b) lentivirus.
22. El vector retroviral seudotipo de acuerdo con la reivindicación 21, en donde el lentivirus deriva del virus de la inmunodeficiencia de simios.
23. El vector retroviral seudotipo de acuerdo con la reivindicación 15, en donde el dominio citoplásmico de la proteína HN del virus Sendai ha sido modificado para que comprenda un dominio citoplásmico de una proteína de la envoltura del virus de la inmunodeficiencia de simios.
24. El vector retroviral seudotipo de acuerdo con la reivindicación 15, en donde la proteína HN del virus Sendai ha sido modificada para que comprenda la secuencia del SEQ ID NO: 40 o 41.
25. El vector retroviral seudotipo de acuerdo con la reivindicación 15, en donde la proteína F comprende la secuencia de aminoácidos del SEQ ID NO: 42.
26. El vector retroviral seudotipo de acuerdo con la reivindicación 15, en donde la proteína F ha sido modificada adicionalmente para que comprenda un dominio citoplásmico de una proteína de la envoltura del virus de la inmunodeficiencia de simios.
27. El vector retroviral seudotipo de acuerdo con la reivindicación 26, en donde la proteína F del virus Sendai comprende la secuencia del SEQ ID NO: 45.
28. El vector retroviral seudotipo de acuerdo con una cualquiera de las reivindicaciones 15 a 27, en donde el vector comprende un gen foráneo de una manera expresable.
29. El uso del vector retroviral seudotipo de acuerdo con una cualquiera de las reivindicaciones 15 a 28, para la preparación de una composición farmacéutica para transferir un gen foráneo a una célula en terapia génica.
30. El uso de acuerdo con la reivindicación 29, en donde la célula es una célula que tiene moco.
31. El uso de acuerdo con la reivindicación 30, en donde la célula que tiene moco es una célula epitelial de la mucosa.
32. El uso de acuerdo con la reivindicación 31, en donde la célula epitelial de la mucosa es una célula epitelial de la mucosa de la cavidad nasal o del tubo bronquial pulmonar.
33. El uso de acuerdo con la reivindicación 29, en donde la célula es un hemocito o una célula hematopoyética.
34. El uso de acuerdo con la reivindicación 33, en donde el hemocito o la célula hematopoyética es una célula pluripotencial hematopoyética.
35. Una composición para la transferencia génica, comprendiendo la composición el vector retroviral seudotipo de acuerdo con una cualquiera de las reivindicaciones 15 a 28 para la transferencia génica.
36. La composición de acuerdo con la reivindicación 35, en donde la composición es una composición farmacéutica.
37. Un método in vitro para introducir un gen foráneo en células, comprendiendo el método la etapa de poner en contacto las células con el vector retroviral seudotipo de acuerdo con una cualquiera de las reivindicaciones 15 a 28.
38. Una célula de empaquetamiento para producir el vector retroviral seudotipo, comprendiendo la célula, de una manera expresable, ADN que codifica las proteínas HN y F del virus Sendai, en donde una porción de un dominio citoplásmico de la proteína F ha sido suprimida para conservar de 0 a 4 aminoácidos del dominio citoplásmico.
39. La célula de empaquetamiento de acuerdo con la reivindicación 38, en donde una porción de un dominio citoplásmico de la proteína F ha sido suprimida para conservar 4 aminoácidos del dominio citoplásmico.
40. La célula de empaquetamiento de acuerdo con la reivindicación 38, en donde el dominio citoplásmico de la proteína HN ha sido modificado mediante la adición de o el remplazo por un dominio citoplásmico de una proteína de la envoltura retroviral.
Patentes similares o relacionadas:
Composiciones útiles en el tratamiento de la deficiencia de ornitina transcarbamilasa (OTC), del 8 de Julio de 2020, de THE TRUSTEES OF THE UNIVERSITY OF PENNSYLVANIA: Un vector vírico recombinante que comprende una secuencia de ácido nucleico que codifica la proteína ornitina transcarbamilasa humana (hOTC) y secuencias […]
Terapia génica para la diabetes, del 8 de Julio de 2020, de UCL Business Ltd: Una molécula de ácido nucleico que comprende una secuencia de nucleótidos que codifica una proteína preproinsulina funcional en donde la secuencia de nucleótidos tiene al menos […]
Vacuna de ADN que contiene un epítopo específico de VEGF y/o un epítopo específico de angiopoyetina-2, del 1 de Julio de 2020, de OSAKA UNIVERSITY: Un vector de expresión que codifica un polipéptido del antígeno del núcleo del virus de la hepatitis B quimérico con una inserción para uso en el tratamiento o la profilaxis […]
Composiciones para modular la expresión de SOD-1, del 24 de Junio de 2020, de Biogen MA Inc: Un compuesto antisentido según la siguiente fórmula: mCes Aeo Ges Geo Aes Tds Ads mCds Ads Tds Tds Tds mCds Tds Ads mCeo Aes Geo mCes Te (secuencia […]
Ácido nucleico antisentido, del 24 de Junio de 2020, de NIPPON SHINYAKU CO., LTD.: Un oligómero antisentido de 14 a 32 bases de longitud, que comprende dos unidades de oligómeros conectadas seleccionadas del grupo que consiste […]
Plekhg5 como diana farmacéutica para trastornos neurológicos, del 15 de Junio de 2020, de CONSEJO SUPERIOR DE INVESTIGACIONES CIENTIFICAS (CSIC): Plekhg5 como diana farmacéutica para trastornos neurológicos. La invención hace referencia al uso del gen Plekhg5 como diana farmacológica para el cribado, […]
Vectores de AAV dirigidos a oligodendrocitos, del 10 de Junio de 2020, de THE UNIVERSITY OF NORTH CAROLINA AT CHAPEL HILL: Un ácido nucleico que codifica una cápside de AAV, comprendiendo el ácido nucleico una secuencia codificante de la cápside de AAV que es al menos el 96 % idéntica […]
Método para activar células T auxiliares, del 10 de Junio de 2020, de OTSUKA PHARMACEUTICAL CO., LTD.: Una composición para su uso en el tratamiento o prevención del cáncer mediante la activación de células T auxiliares en un sujeto, en donde dicha composición […]