VARIANTE GENETICA DEL GEN DE ANEXINA A5.
Molécula de ácido nucleico que comprende un promotor de anexina A5 (ANXA5) humana,
promotor que comprende las siguientes mutaciones (sustituciones) puntuales (i) una mutación puntual de G por A en una posición que corresponde al nucleótido 186 de la SEQ ID NO: 2; (ii) una mutación puntual de A por C en una posición que corresponde al nucleótido 203 de la SEQ ID NO: 2; (iii)una mutación puntual de T por C en una posición que corresponde al nucleótido 229 de la SEQ ID NO: 2; y (iv) una mutación puntual de G por A en una posición que corresponde al nucleótido 276 de la SEQ ID NO:
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2005/012259.
Solicitante: UNIVERSITATSKLINIKUM MUNSTER.
Nacionalidad solicitante: Alemania.
Dirección: DOMAGKSTRASSE 5 48149 MUNSTER.
Inventor/es: MARKOFF,NADJA, HORST,JURGEN, GERKE,VOLKER, MARKOFF,ARSENI.
Fecha de Publicación: .
Fecha Solicitud PCT: 15 de Noviembre de 2005.
Fecha Concesión Europea: 30 de Junio de 2010.
Clasificación Internacional de Patentes:
- C07K14/47A12
- C12Q1/68M6
- C12Q1/68P
Clasificación PCT:
- C12N15/11 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 15/00 Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K). › Fragmentos de ADN o de ARN; sus formas modificadas (ADN o ARN no empleado en tecnología de recombinación C07H 21/00).
- C12Q1/68 C12 […] › C12Q PROCESOS DE MEDIDA, INVESTIGACION O ANALISIS EN LOS QUE INTERVIENEN ENZIMAS, ÁCIDOS NUCLEICOS O MICROORGANISMOS (ensayos inmunológicos G01N 33/53 ); COMPOSICIONES O PAPELES REACTIVOS PARA ESTE FIN; PROCESOS PARA PREPARAR ESTAS COMPOSICIONES; PROCESOS DE CONTROL SENSIBLES A LAS CONDICIONES DEL MEDIO EN LOS PROCESOS MICROBIOLOGICOS O ENZIMOLOGICOS. › C12Q 1/00 Procesos de medida, investigación o análisis en los que intervienen enzimas, ácidos nucleicos o microorganismos (aparatos de medida, investigación o análisis con medios de medida o detección de las condiciones del medio, p. ej. contadores de colonias, C12M 1/34 ); Composiciones para este fin; Procesos para preparar estas composiciones. › en los que intervienen ácidos nucleicos.
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Eslovenia, Finlandia, Rumania, Chipre, Lituania, Letonia.
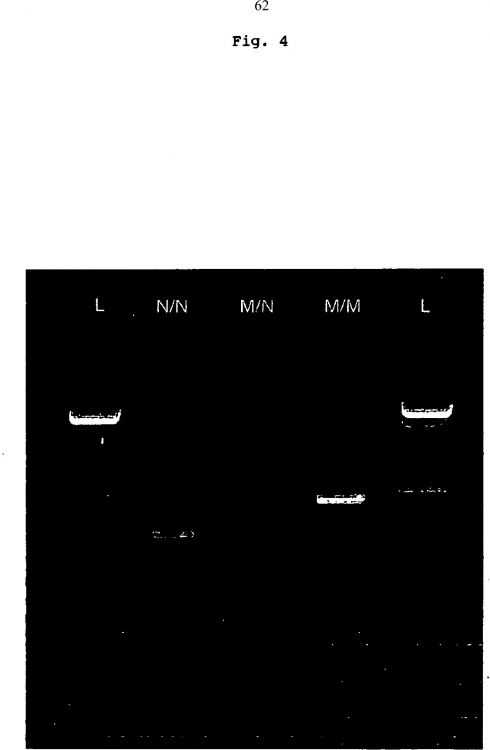
Fragmento de la descripción:
La memoria descriptiva da a conocer una molécula de ácido nucleico que comprende un elemento de regulación del gen de anexina A5 (ANXA5) que comprende al menos una mutación puntual, mediante lo cual dicha al menos una mutación (sustitución) puntual se selecciona del grupo que consiste en (i) una mutación puntual de G por A en una posición que corresponde al nucleótido 186 de la SEQ ID NO: 2; (ii) una mutación puntual de A por C en una posición que corresponde al nucleótido 203 de la SEQ ID NO: 2; (iii) una mutación puntual de T por C en una posición que corresponde al nucleótido 229 de la SEQ ID NO: 2; y (iv) una mutación puntual de G por A en una posición que corresponde al nucleótido 276 de la SEQ ID NO: 2.
La presente invención se refiere a una molécula de ácido nucleico que comprende un promotor de anexina A5 (ANXA5) humana, promotor que comprende las siguientes mutaciones (sustituciones) puntuales: (i) una mutación puntual de G por A en una posición que corresponde al nucleótido 186 de la SEQ ID NO: 2; (ii) una mutación puntual de A por C en una posición que corresponde al nucleótido 203 de la SEQ ID NO: 2; (iii) una mutación puntual de T por C en una posición que corresponde al nucleótido 229 de la SEQ ID NO: 2; y (iv) una mutación puntual de G por A en una posición que corresponde al nucleótido 276 de la SEQ ID NO: 2. La presente invención se refiere además a una molécula de ácido nucleico que comprende un promotor de anexina A5 (ANXA5) humana, promotor que comprende las siguientes mutaciones (sustituciones) puntuales: (ii) una mutación puntual de A por C en una posición que corresponde al nucleótido 203 de la SEQ ID NO: 2; y (iii) una mutación puntual de T por C en una posición que corresponde al nucleótido 229 de la SEQ ID NO: 2.
Además, la presente invención proporciona un vector que comprende la molécula de ácido nucleico de la invención y un huésped transformado con el vector. La invención también se refiere a usos específicos, en particular usos de diagnóstico de las moléculas de ácido nucleico descritas en el presente
documento. Además, la memoria descriptiva da a conocer un método para determinar el haplotipo de un elemento de regulación del gen ANXA5 en un individuo que comprende las etapas de: (a) aislar un ácido nucleico a partir de una muestra que se ha extraído del individuo; (b) determinar la presencia de los nucleótidos presentes en las posiciones 186, 203, 229 y 276 de la copia del individuo del elemento de regulación del gen ANXA5, en el que los números de posición se determinan mediante comparación con la SEQ ID NO: 2; (c) asignar a los individuos a un haplotipo particular mediante comparación de los nucleótidos presentes en dichas posiciones con los nucleótidos referidos en los haplotipos tal como se define en el presente documento.
El aborto es un fenómeno frecuente con origen heterogéneo. El estado genético más prevalente, especialmente para casos de pérdida en los primeros meses de embarazo, son las aberraciones cromosómicas. Los trastornos de hipercoagulabilidad que promueven trombosis, denominados colectivamente trombofilia son aún otro factor genético significativo. Los defectos más significativos (riesgo de 3 a 6 veces mayor de aborto) incluyen la mutación del factor V de Leiden, variantes genéticas de metilentetrahidrofolatorreductasa (MTHFR), y mutación 20210G→A del factor II (protrombina). Entre estos, se han demostrado las asociaciones del factor V de Leiden y la 20210G→A de protrombina (PTm) con el aborto recurrente mediante meta-análisis estadístico [Rey, 2003]. La asociación entre algunas de las variantes genéticas de MTHFR y la trombosis es controvertida [Rey, 2003, Key, 2002, Seligsohn, 2001]. Otro factor principal para las pérdidas repetidas del embarazo es la presencia de anticuerpos antifosfolípidos maternos circulantes (aPL). El aumento de los riesgos de aborto se ha documentado en embarazos de bajo riesgo y de alto riesgo (más de 3 muertes fetales), cuando están presentes aPL [Empson, 2002 y bibliografía en el mismo].
La anexina A5 (proteína anticoagulante placentaria) se encuentra en vellosidades placentarias normales y parece reducirse en presencia de aPL [Rand, 1994]. Otros estudios confirman la expresión de anexina A5 reducida en trofoblastos
placentarios de pacientes con preeclampsia mediante inmunohistoquímica.
La anexina A5 es un miembro típico de la familia de genes de anexina de cordados. Ésta proyecta la estructura de tétrada esencial y la unión a fosfolípidos dependiente de calcio, que se han convertido en un modelo clave para estudiar la función de la anexina [Gerke y Moss, 2002]. Es una proteína expresada de manera abundante y ubicua presente mayormente en el riñón, el hígado y la placenta [Morgan, 1998]. La anexina A5 puede funcionar de manera extracelular como un inhibidor de la coagulación sanguínea y se propone que esta proteína puede formar un escudo anticoagulante protector en la superficie de los trofoblastos placentarios [Rand y Wu, 1999; Rand, 2003].
Hayes trata el posible papel de la expresión de anexina 5 en algunos estados patológicos, tales como el aborto. Sin embargo no se sugiere que estos estados puedan estar relacionados con un promotor de ANXA5 mutado.
El gen de anexina A5 se ha caracterizado hace una década [Cookson, 1994] y el gen y la proteína codificada se estudian y caracterizan de manera extensa. Sin embargo, hasta hace poco, se conocía poco sobre la regulación de la expresión de anexina A5. El gen de anexina A5 (ANXA5) humana produce varios transcritos y tiene un promotor complejo con regulación intrincada [Carcedo, 2001].
No se han asociado mutaciones de anexina A5 con un fenotipo de enfermedad, a excepción de la variante genética “-1 CT”, que se propone que protege frente al infarto de miocardio en pacientes jóvenes [Gonzalez-Conejero, 2002]. Sin embargo existen otros datos y consideraciones, que refutan la validez de este hallazgo [Kozak, 2003; van Heerde, 2003].
El problema técnico de la presente invención es la provisión de medios y métodos para determinar el riesgo de aborto. La solución a este problema técnico se proporciona en la presente invención tal como se caracteriza en las reivindicaciones y tal como se ilustra y ejemplifica en el presente documento.
La presente invención se refiere a una molécula de ácido nucleico que comprende un promotor de anexina A5 (ANXA5) humana, promotor que comprende las siguientes mutaciones (sustituciones) puntuales: (i) una mutación puntual de G por A en una posición que corresponde al nucleótido 186 de la SEQ ID NO: 2; (ii) una mutación puntual de A por C en una posición que corresponde al nucleótido 203 de la SEQ ID NO: 2; (iii) una mutación puntual de T por C en una posición que corresponde al nucleótido 229 de la SEQ ID NO: 2; y (iv) una mutación puntual de G por A en una posición que corresponde al nucleótido 276 de la SEQ ID NO: 2. La presente invención se refiere además a una molécula de ácido nucleico que comprende un promotor de anexina A5 (ANXA5) humana, promotor que comprende las siguientes mutaciones (sustituciones) puntuales: (ii) una mutación puntual de A por C en una posición que corresponde al nucleótido 203 de la SEQ ID NO: 2; y (iii) una mutación puntual de T por C en una posición que corresponde al nucleótido 229 de la SEQ ID NO: 2.
La presente invención se refiere a una molécula de ácido nucleico que comprende un elemento de regulación del gen de anexina A5 (ANXA5) que comprende las siguientes mutaciones (sustituciones) puntuales
(i) una mutación puntual de G por A en una posición que corresponde al nucleótido 186 de la SEQ ID NO: 2; (ii)una mutación puntual de A por C en una posición que corresponde al nucleótido 203 de la SEQ ID NO: 2; (iii)una mutación puntual de T por C en una posición que corresponde al nucleótido 229 de la SEQ ID NO: 2; y (iv)una mutación puntual de G por A en una posición que corresponde al nucleótido 276 de la SEQ ID NO: 2.
Tal como se documentó en los ejemplos adjuntos, se encontró de manera sorprendente una variante genética en la región promotora de ANXA5 (BamHI) en el gen de anexina A5 (ANXA5) entre mujeres que se examinaron para determinar diferentes defectos genéticos de trombosis hereditarios debido a aborto repetido. Esta variante consiste en sustituciones de cuatro nucleótidos, que se heredan como un haplotipo. Sin restringirse a la teoría, estos cuatro cambios son importantes para la actividad del
promotor de anexina A5...
Reivindicaciones:
1. Molécula de ácido nucleico que comprende un promotor de anexina A5 (ANXA5) humana, promotor que comprende las siguientes mutaciones (sustituciones) puntuales
(i) una mutación puntual de G por A en una posición que corresponde al nucleótido 186 de la SEQ ID NO: 2;
(ii) una mutación puntual de A por C en una posición que corresponde al nucleótido 203 de la SEQ ID NO: 2;
(iii)una mutación puntual de T por C en una posición que corresponde al nucleótido 229 de la SEQ ID NO: 2; y
(iv) una mutación puntual de G por A en una posición que corresponde al nucleótido 276 de la SEQ ID NO: 2.
2. Molécula de ácido nucleico que comprende un promotor de anexina A5 (ANXA5) humana, promotor que comprende las siguientes mutaciones (sustituciones) puntuales
(ii) una mutación puntual de A por C en una posición que corresponde al nucleótido 203 de la SEQ ID NO: 2; y
(iii)una mutación puntual de T por C en una posición que corresponde al nucleótido 229 de la SEQ ID NO: 2.
3. Fragmento de ácido nucleico de las moléculas de ácido nucleico definidas en una cualquiera de las reivindicaciones 1 ó 2, que comprende las sustituciones como se definen en una cualquiera de las reivindicaciones 1 ó 2.
4. Oligómero que tiene una longitud de al menos 20 nucleótidos, que hibrida específicamente con las moléculas/fragmentos de ácido nucleico como se define en una cualquiera de la reivindicación 1 a 3.
5. Molécula de ácido nucleico según la reivindicación 1 ó 2 que se une operativamente a un gen que codifica una proteína marcadora, una proteína señal, un gen reportero, o una etiqueta.
6. Molécula de ácido nucleico según una cualquiera de las reivindicaciones de 1 a 5 que es ADN, ARN o APN.
7. Vector que comprende la molécula de ácido nucleico según una cualquiera de las reivindicaciones 1 a 3 ó 5.
8. Método in vitro para diagnosticar o detectar una predisposición para una tendencia al aborto (pérdida del embarazo) y/o un mayor riesgo para desarrollar anticuerpos antifosfolípidos, comprendiendo dicho método las etapas de
(a) examinar un promotor de ANXA5 para detectar al menos una sustitución según una cualquiera de las reivindicaciones 1 ó 2; y
(b) determinar si está presente alguna de las al menos una de dichas sustituciones.
9. Método in vitro según la reivindicación 8, en el que la detección de dicha al menos una sustitución en dicho promotor de ANXA5 se lleva a cabo o se determina mediante técnicas de ácidos nucleicos basadas en el tamaño o la secuencia.
10. Método in vitro según la reivindicación 9, en el que dicha técnica basada en el tamaño o la secuencia se selecciona del grupo que consiste en técnicas de hibridación, secuenciación de ácidos nucleicos, PCR, determinación de fragmentos de restricción, determinación de polimorfismos de un solo nucleótido (SNP), LCR (reacción en cadena de ligamiento) o determinación de polimorfismos de la longitud de los fragmentos de restricción (RFLP).
11. Método in vitro según una cualquiera de las reivindicaciones 8 a 10, que comprende la etapa de amplificar un tramo de ADN del promotor de ANXA5 a partir del ADN genómico mediante PCR.
12. Método in vitro según la reivindicación 10, en el que dicha determinación de fragmentos de restricción o dicho RFLP comprende la determinación de un sitio de restricción BamHI.
13. Método según una cualquiera de las reivindicaciones 8 a 12, en el que se determina la ausencia o la presencia de una sustitución correspondiente a la posición 276 de un promotor del gen ANXA5 tal como se muestra en la SEQ ID NO:
2.
14. Método según una cualquiera de las reivindicaciones 8 a 13, que se lleva a cabo en ADN genómico.
15. Uso de la molécula de ácido nucleico definida en la reivindicación 1 ó 2, el fragmento de ácido nucleico definido en la reivindicación 3, el oligómero de la reivindicación 4, o de un par de cebadores capaces de amplificar tramos relevantes de la molécula de ácido nucleico definida según la reivindicación 1 ó 2, para la preparación de una composición de diagnóstico para diagnosticar o detectar una predisposición para o una tendencia al aborto y/o para diagnosticar o detectar una predisposición o una tendencia para el desarrollo de anticuerpos antifosfolípidos.
16. Método de selección de moléculas capaces de interaccionar con un promotor mutado de ANXA5 como se define en una cualquiera de las reivindicaciones 1 ó 2, que comprende las etapas de
(a) poner en contacto una molécula de ácido nucleico según una cualquiera de las reivindicaciones 1 ó 2, un vector según la reivindicación 7 ó un huésped que comprende dicha molécula de ácido nucleico con una molécula candidata;
(b) medir y/o detectar una respuesta;
(c) comparar dicha respuesta con una respuesta patrón tal como se mide en ausencia de dicha molécula candidata, y
(d) comparar dicha respuesta con una respuesta obtenida con dicha molécula candidata y el promotor no mutado (de tipo natural) de ANXA5.
Patentes similares o relacionadas:
MODULADORES DEL PESO CORPORAL, ÁCIDOS NUCLEICOS Y PROTEÍNAS CORRESPONDIENTES, Y USOS DIAGNÓSTICOS Y TERAPÉUTICOS DE LOS MISMOS, del 17 de Febrero de 2012, de THE ROCKEFELLER UNIVERSITY: LA PRESENTE INVENCION SE REFIERE GENERALMENTE AL CONTROL DEL PESO CORPORAL DE ANIMALES INCLUIDOS MAMIFEROS Y HUMANOS, Y EN CONCRETO A MATERIALES […]
POLIMORFISMOS DE VEGF Y TERAPIA ANTI-ANGIOGÉNESIS, del 17 de Enero de 2012, de GENENTECH, INC.: Método para predecir si un paciente se encuentra con un mayor riesgo de hipertensión asociada con el tratamiento con un antagonista de VEGF, que comprende cribar […]
MÉTODO DE DIAGNÓSTICO Y DE SEGUIMIENTO DE UNA VAGINOSIS BACTERIANA MEDIANTE CUANTIFICACIÓN MOLECULAR, del 28 de Diciembre de 2011, de UNIVERSITE DE LA MEDITERRANEE, AIX-MARSEILLE II: Método de diagnóstico y de seguimiento in vitro del estado de la flora bacteriana vaginal frente a la presencia de una vaginosis bacteriana […]
DETECCIÓN DE GÉRMENES ASOCIADOS A PERIODONTITIS, del 9 de Diciembre de 2011, de GREINER BIO-ONE GMBH: Procedimiento para la detección y/o para la determinación de bacterias asociadas a periodontitis de una muestra biológica, que comprende las etapas i) obtención […]
CONFORMACIÓN DE ADN (ESTRUCTURAS DE BUCLE) EN EXPRESIÓN GÉNICA NORMAL Y ANORMAL, del 22 de Noviembre de 2011, de ISIS INNOVATION LIMITED: Procedimiento de diagnóstico de un cancer por detección de expresión genica anormal en un individuo que comprende determinar en una muestra del individuo […]
USO DE POLIMORFISMOS GENÉTICOS QUE SE ASOCIAN CON LA EFICACIA DEL TRATAMIENTO DE UNA ENFERMEDAD INFLAMATORIA, del 4 de Noviembre de 2011, de NOVARTIS AG NOVARTIS PHARMA GMBH: Uso de pimecrolimus en la fabricación de un medicamento para el tratamiento de dermatitis atópica pediátrica en una población seleccionada de pacientes, en donde la población […]
MÉTODOS PARA EVALUAR ESTADOS PATOLÓGICOS USANDO ARN EXTRACELULAR, del 2 de Noviembre de 2011, de ONCOMEDX INC: Método para detectar, diagnosticar o monitorizar una lesión de un órgano en un ser humano, comprendiendo el método la etapa de detectar cualitativa o cuantitativamente […]
MÉTODOS DE TRATAMIENTO DE PSICOSIS Y ESQUIZOFRENIA BASADOS EN POLIMORFISMOS DEL GEN DEL CNTF, del 23 de Agosto de 2011, de NOVARTIS AG: Un método para determinar la capacidad de respuesta de un individuo con un trastorno psicótico al tratamiento con Iloperidona, que comprende; […]