VACUNAS CONTRA LA MALARIA.
Un polipéptido que comprende una secuencia antigénica derivada de regiones de repetición de alelos de bloque 2 de MSP1 de tipo K1 de Plasmodium falciparum,
en el que dicha secuencia antigénica se selecciona de la secuencia de SEC. ID no.1 (denominada secuencia de repetición sintética 1 de tipo K1; KISR):
y análogos funcionales de la misma de la misma longitud y sustancialmente la misma inmunogenicidad tal como se determina en forma de una proteína de fusión unida en el extremo N-terminal a una secuencia de glutatión-S-transferasa (GST) N-terminal
Tipo: Resumen de patente/invención. Número de Solicitud: W06050126GB.
Solicitante: LONDON SCHOOL OF HYGIENE AND TROPICAL MEDICINE.
Nacionalidad solicitante: Reino Unido.
Dirección: KEPPEL STREET,LONDON WC1E 7HT.
Inventor/es: TETTEH,KEVIN K. A.,THE LONDON SCHOOL OF HYGIENE, CONWAY,DAVID J.
Fecha de Publicación: .
Fecha Concesión Europea: 28 de Octubre de 2009.
Clasificación Internacional de Patentes:
- C07K14/445 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 14/00 Péptidos con más de 20 aminoácidos; Gastrinas; Somatostatinas; Melanotropinas; Sus derivados. › Plasmodium.
Clasificación PCT:
- A61K39/002 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 39/00 Preparaciones medicinales que contienen antígenos o anticuerpos (materiales para ensayos inmunológicos G01N 33/53). › Antígenos de protozoos.
- C07K14/445 C07K 14/00 […] › Plasmodium.
- C07K19/00 C07K […] › Péptidos híbridos (Inmoglobulinas híbridas compuestas solamente de inmoglobulinas C07K 16/46).
- C12N15/30 C […] › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 15/00 Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K). › Genes que codifican proteínas de protozoos, p. ej. Plasmodium, Trypanosoma, Eimeria.
- C12N15/62 C12N 15/00 […] › Secuencias de ADN que codifican proteínas de fusión.
- G01N33/569 FISICA. › G01 METROLOGIA; ENSAYOS. › G01N INVESTIGACION O ANALISIS DE MATERIALES POR DETERMINACION DE SUS PROPIEDADES QUIMICAS O FISICAS (procedimientos de medida, de investigación o de análisis diferentes de los ensayos inmunológicos, en los que intervienen enzimas o microorganismos C12M, C12Q). › G01N 33/00 Investigación o análisis de materiales por métodos específicos no cubiertos por los grupos G01N 1/00 - G01N 31/00. › para microorganismos, p. ej. protozoarios, bacterias, virus.
Fragmento de la descripción:
Vacunas contra la malaria.
La presente invención se refiere a vacunas contra la malaria que incluyen como componente antigénico una secuencia sintética que representa una combinación de fragmentos de la región de repetición de bloque 2 de tipo K1 de la proteína de superficie del merozoíto 1 (MSP1) de Plasmodium falciparum. El tipo K1 de la región de bloque 2 de MSP1 es sumamente polimórfico y se ha encontrado que el tipo K1 es el más común de los tipos de región de bloque 2 de MSP 1 en poblaciones africanas. La presente invención se refiere entre otras cosas a aprovechar la amplia diversidad de secuencia de la región de bloque 2 de tipo K1 de MSP1 para su uso en vacunas en una secuencia denominada secuencia de repetición sintética de tipo K1 (K1SR). Esta secuencia puede inducir respuestas de anticuerpos que tienen amplia capacidad para seleccionar como diana alelos de la región de bloque 2 de tipo K1 de MSP1. Para mejorar la amplitud de la eficacia como inmunógeno frente a P. falciparum, además puede incorporarse en constructos de fusión con otros epítopos de MSP1 de P. falciparum.
Antecedentes de la invención
El polimorfismo en antígenos de patógenos representa un desafío complejo para el diseño de vacunas, particularmente cuando la diversidad es extensa. La región de bloque 2 N-terminal de MSP1 de Plasmodium falciparum ejemplifica una alta diversidad en un antígeno de patógenos. Se conoce que esta región es la diana de anticuerpos humanos adquiridos de manera natural que están asociados con un riesgo reducido de malaria clínica (Conway et al., (2000) Nature Med. 6, 689-692; Polley et al., (2003) Infect. & Immun. 71, 1833-1842; Cavanagh et al., (2004) Infect. & Immun.72, 6492-6502). Por tanto, ha habido un interés en respuestas de sensibilización frente a la región de bloque 2 de MSP 1 mediante vacunación, particularmente en niños pequeños. Sin embargo, hay tres tipos alélicos principales de la región de bloque 2 de MSP1 (el tipo K1, el tipo MAD20 y el tipo R033) y existe mucho polimorfismo de subtipo dentro de dos de éstos (K1 y MAD20).
Los tipos de bloque 2 tanto K1 como MAD20 presentan una extensa diversidad de secuencia dentro de las secuencias de repetición de tri- y hexa-péptido central de cada tipo. Los tipos K1 y MAD20 contienen secuencias de repetición de tri- y hexa-péptido diferentes con serina en la primera posición y las variaciones en la secuencia y el número de repeticiones producen diferencias alélicas de subtipo dentro de cada uno de los tipos (Conway et al., (2000) Nature Med. 6, 689-692; Miller et al., (1993) Mol. Biochem. Parasitol. 59,1-14). A pesar de esta diversidad de secuencia, la mayoría de los sueros humanos de individuos en regiones endémicas de malaria reconocen múltiples variantes alélicas del bloque 2 dentro de un tipo, y aunque algunos individuos tienen respuestas de anticuerpos específicos de un único alelo frente al bloque 2 de MSP1, esto es menos común (Cavanagh et al. (1998) J. Immunol. 161, 347-359; Cavanagh & McBride (1997) Mol. & Biochem. Parasitol. 85,197-211). Esto puede explicarse de dos modos. En primer lugar, hay secuencias flanqueantes específicas del tipo compartidas asociadas con los tipos de bloque 2 tanto K1 como MAD20, que son la diana de algunas respuestas de anticuerpos, y en segundo lugar, las características específicas de la diversidad de secuencia dentro de los tipos K1 y MAD20. Se usan cuatro tripéptidos diferentes en el tipo K1 y se usan 5 tripéptidos (diferentes) en el tipo MAD20. Por tanto, todos los alelos de bloque 2 de tipo K1 contienen combinaciones de los tripéptidos SAQ, SGA, SGP y SGT, flanqueadas por secuencias comunes únicas para el tipo K1 del bloque 2. Todos los alelos de bloque 2 de tipo MAD20 contienen combinaciones de los tripéptidos SGG y SVA (con variaciones menores en el extremo N-terminal de las repeticiones usando los tripéptidos SVT, SKG y SSG), flanqueadas por secuencias comunes del tipo MAD20. La variación dentro de los tipos de bloque 2 K1 y MAD20 parece estar restringida a estas diferencias, más alguna restricción de tamaño en la longitud de la secuencia repetitiva permitida por la molécula MSP1 (Jiang et al. (2000) Acta Tropica 74, 51-61).
Tal como ya se indicó anteriormente, el tipo K1 es el más común de los tipos de región de bloque 2 de MSP1 en poblaciones africanas. Por ejemplo, los inventores encontraron en una población de Zambia que 49 de 91 alelos de la región de bloque 2 de MSP1 de P. falciparum eran del tipo K1 y que la mayoría de éstos tenían secuencias únicas debido a la variación en motivos repetitivos de tri- y hexa-péptido. Tal como se indica en Polley et al. (2003) ibídem, hay por tanto un interés particular en respuestas inmunitarias de sensibilización que seleccionen como diana ampliamente la diversidad alélica asociada con las repeticiones de las regiones de bloque 2 de tipo K1 de MSP1 incluyendo motivos de repetición a partir de tales regiones en vacunas contra la malaria.
Sumario de la invención
Como enfoque para abordar la necesidad indicada anteriormente, se ha diseñado una secuencia polipeptídica novedosa de longitud mínima de 78 residuos de aminoácido que contiene una gran proporción de todos los epítopos de anticuerpo dentro de las secuencias de repetición de la región de bloque 2 de tipo K1 de MSP1 (la secuencia de repetición sintética de tipo K1 denominada K1SR y presentada como SEC. ID. No.1). Esto se logró usando sueros de regiones endémicas de malaria y 23 péptidos sintéticos que representan todas las secuencias de aminoácidos de 12-meros (con la serina de los tri-péptidos en la posición 1) derivados de una colección de secuencias de repetición del bloque 2 de tipo K1 de MSP 1 presentes en la base de datos GenBank. La secuencia sintética resultante se ha expresado como una proteína de fusión recombinante que tiene en el extremo N-terminal una secuencia de glutatión-S-transferasa (GST) y de esta forma se ha mostrado que presenta una reactividad específica de tipo más amplio con el suero humano que alelos individuales conocidos de la región de bloque 2 de tipo K1 de MSP1.
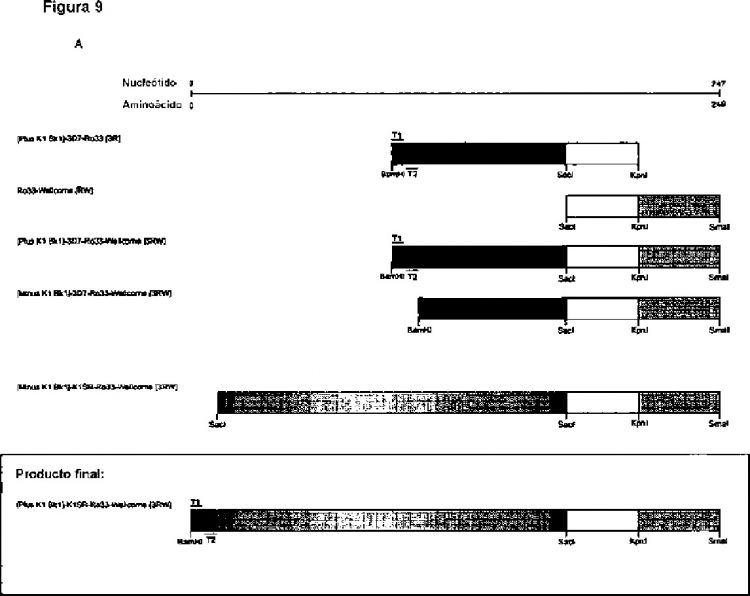
En un aspecto, la presente invención proporciona por tanto un polipéptido que comprende la siguiente secuencia de aminoácidos como secuencia antigénica (SEC ID no.1; véase también la figura 4):

La invención también se extiende a polipéptidos antigénicos que comprenden un análogo funcional de la secuencia de K1SR que es de la misma longitud y que conserva sustancialmente la misma inmunogenicidad que la secuencia de K1SR cuando está en forma de una proteína de fusión con GST, es decir, unida en el extremo N-terminal a una secuencia de GST. Una secuencia de este tipo puede ser cualquier secuencia de GST convencional tal como se emplea comúnmente para la expresión y purificación de proteínas recombinantes como proteínas de fusión, por ejemplo, una secuencia de GST codificada por un vector de expresión pGEX (Smith et al., Single-step purification of polypeptides expressed in Escherichia coli as fusions with glutathione S-transferase (1988) Gene 67, 31-40). Se ha encontrado que las regiones de repetición de bloque 2 de MSP1 son poco inmunógenas a menos que se conjuguen con una proteína portadora. Puede considerarse "sustancialmente la misma inmunogenicidad" usando un panel de diferentes sueros o anticuerpos monoclonales que se unen a fragmentos que presentan epítopos que abarcan toda la secuencia de K1SR. Una variante con "sustancialmente la misma inmunogenicidad" se unirá deseablemente con todos los mismos anticuerpos o al menos aproximadamente del 90 al 99% de los mismos, preferiblemente al menos aproximadamente el 99% de los mismos. Un análogo funcional de este tipo puede tener una o más sustituciones, por ejemplo, una o más sustituciones conservadoras, que conservan la inmunogenicidad deseada.
Tal como se trató anteriormente, puede esperarse que un análogo funcional comparta con la secuencia de SEC. ID. NO.1 la capacidad de unirse con anticuerpos monoclonales a cada una de las siguientes secuencias: (i) SGASAQSG (ii) SAQSGTSGTS y (iii) SAQSGTSGT. Tales anticuerpos monoclonales se ejemplifican mediante los anticuerpos monoclonales Mab 12.2, Mab 123D3 y Mab CE2, respectivamente, tal como se denominan en los ejemplos más adelante. Tales anticuerpos monoclonales pueden usarse en la selección inicial para buscar análogos funcionales de SEC. ID. No. 1.
Los polipéptidos preferidos de la invención son proteínas de fusión...
Reivindicaciones:
1. Un polipéptido que comprende una secuencia antigénica derivada de regiones de repetición de alelos de bloque 2 de MSP1 de tipo K1 de Plasmodium falciparum, en el que dicha secuencia antigénica se selecciona de la secuencia de SEC. ID no.1 (denominada secuencia de repetición sintética 1 de tipo K1; KISR):

y análogos funcionales de la misma de la misma longitud y sustancialmente la misma inmunogenicidad tal como se determina en forma de una proteína de fusión unida en el extremo N-terminal a una secuencia de glutatión-S-transferasa (GST) N-terminal.
2. Una proteína de fusión que comprende un polipéptido según la reivindicación 1, en la que dicha secuencia antigénica está unida en el extremo N-terminal y/o el extremo C-terminal a una secuencia de aminoácidos adicional.
3. Una proteína de fusión según la reivindicación 2, en la que dicha secuencia antigénica está unida directa o indirectamente en el extremo N-terminal a una secuencia de GST o una secuencia de cola de His.
4. Una proteína de fusión según la reivindicación 2 o la reivindicación 3, en la que dicha secuencia antigénica está unida a una o más secuencias que contienen epítopos adicionales que pueden producir una respuesta de anticuerpos o una respuesta inmunitaria celular en seres humanos frente a un antígeno de P. falciparum.
5. Una proteína de fusión según la reivindicación 4, en la que dichas secuencias que contienen epítopos adicionales son secuencias derivadas de MSP 1 de P. falciparum seleccionadas de (i) secuencias que contienen epítopos de células T humanas que pueden inducir una respuesta inmunitaria celular frente a P. falciparum; (ii) una secuencia que proporciona una región de repetición de bloque 2 de MSP1 del tipo MAD 20 y (iii) una secuencia que proporciona una región de repetición de bloque 2 de MSP 1 del tipo RO33.
6. Una proteína de fusión según la reivindicación 5, que comprende un constructo híbrido en el que una secuencia antigénica según la reivindicación 1 está unida en el extremo N-terminal a una secuencia que proporciona uno o más epítopos de células T humanas derivados de un alelo de MSP1.
7. Una proteína de fusión según la reivindicación 6, que comprende un constructo híbrido constituido por (i) un alelo de bloque 1-bloque 2 de MSP1 de tipo K1 y (ii) una secuencia antigénica según la reivindicación 1.
8. Una proteína de fusión según la reivindicación 6 o la reivindicación 7, en la que dicho constructo híbrido se extiende adicionalmente mediante la adición de una secuencia que proporciona una región de bloque 2 de MSP1 del tipo RO33 y una región de bloque 2 de MSP 1 del tipo MAD 20.
9. Una proteína de fusión según la reivindicación 8, en la que dicho constructo híbrido está constituido por los siguientes componentes en la dirección de N- a C-terminal: (i) un alelo de bloque 1-bloque 2 de MSP1 de tipo K1; (ii) una secuencia antigénica según la reivindicación 1; y (iii) una secuencia que proporciona una región de bloque 2 de MSP1 del tipo RO33 y una región de bloque 2 de MSP1 del tipo MAD 20.
10. Una proteína de fusión según la reivindicación 8, en la que dicho constructo híbrido está constituido por los siguientes componentes en la dirección de N- a C-terminal: (i) una secuencia que proporciona uno o más epítopos de células T humanas derivados de un alelo de MSP1 de tipo K1; (ii) una secuencia antigénica según la reivindicación 1 y (iii) una secuencia que proporciona una región de bloque 2 de MSP1 del tipo RO33 y una región de bloque 2 de MSP1 del tipo MAD 20.
11. Una proteína de fusión según una cualquiera de las reivindicaciones 6 a 10, en la que dicho constructo híbrido está unido además en el extremo N-terminal a una secuencia de cola de His o secuencia de GST N-terminal.
12. Un polinucleótido que codifica un polipéptido o una proteína según una cualquiera de las reivindicaciones anteriores.
13. Un polinucleótido según la reivindicación 12, que es un ADN.
14. Un vector que comprende un polinucleótido según la reivindicación 13.
15. Un polinucleótido según la reivindicación 13, en el que la secuencia codificante para dicho polipéptido o dicha proteína está operativamente unida a una secuencia promotora.
16. Un vector de expresión que comprende un polinucleótido según la reivindicación 15.
17. Un procedimiento de producción de un polipéptido o una proteína según una cualquiera de las reivindicaciones 1 a 11, que comprende cultivar células huésped que contienen un vector de expresión según la reivindicación 16 en condiciones por las cuales se expresa dicho polipéptido o dicha proteína y aislar dicho polipéptido o dicha proteína.
18. Una célula huésped in vitro que contiene un vector de expresión según la reivindicación 16.
19. Una composición para inducir una respuesta inmunitaria frente a P. falciparum que comprende un polipéptido o una proteína según cualquiera de las reivindicaciones 1 a 11 junto con un adyuvante o diluyente farmacéuticamente aceptable.
20. Una composición para inducir una respuesta inmunitaria frente a P. falciparum que comprende un polinucleótido según la reivindicación 15 o un vector de expresión según la reivindicación 16 junto con un vehículo.
21. Uso de un polipéptido o una proteína según una cualquiera de las reivindicaciones 1 a 11, un polinucleótido según la reivindicación 15 o un vector de expresión según la reivindicación 16, en la fabricación de una composición para su uso en la inducción de una respuesta inmunitaria frente a P. falciparum.
22. Un procedimiento de tipificación de la región de bloque 2 de MSP 1 en un suero de un individuo infectado con P. falciparum que comprende poner en contacto dicho suero con un polipéptido que comprende una secuencia antigénica según la reivindicación 1 y determinar si se unen anticuerpos en dicho suero a dicha secuencia.
23. Un procedimiento de tipificación de la región de bloque 2 de MSP 1 en esquizontes de P. falciparum cultivados que comprende poner en contacto los esquizontes con un suero que contiene anticuerpos producidos frente a una secuencia antigénica según la reivindicación 1 y determinar la unión de dichos anticuerpos a dichos esquizontes.
Patentes similares o relacionadas:
Partículas de tipo virus que comprenden proteínas diana fusionadas a proteínas de revestimiento de virus vegetales, del 4 de Septiembre de 2019, de FRAUNHOFER, USA, INC.: Una partícula de tipo virus que consiste en una proteína de fusión, en la que la proteína de fusión comprende (a) una proteína que tiene una secuencia […]
Procedimiento novedoso y composiciones, del 12 de Junio de 2019, de GLAXOSMITHKLINE BIOLOGICALS S.A.: Uno o más primeros polipéptidos inmunógenos para su uso en un procedimiento de generación de una respuesta inmunológica frente a Mycobacterium spp., en los […]
Direccionamiento de glicanos de sulfato de condroitina, del 11 de Abril de 2018, de Var2 Pharmaceuticals ApS: Un conjugado que comprende un polipéptido VAR2CSA y una fracción efectora terapéutica o de diagnóstico seleccionada de un agente anticanceroso o un soporte sólido; […]
Vectores adenovirales que codifican un patógeno o antígeno tumoral, del 16 de Agosto de 2017, de Oxford University Innovation Limited: Un vector adenoviral que comprende un promotor y una secuencia de ácido nucleico que codifica un patógeno o antígeno tumoral bajo el control de dicho promotor, donde […]
Vector adenoviral que codifica un antígeno de malaria, del 12 de Julio de 2017, de Oxford University Innovation Limited: Un vector de adenovirus de simio recombinante deficiente en replicación que comprende un genoma del adenovirus de simio en el que se ha integrado de forma estable un transgén, […]
Secuencias de nucleótidos y aminoácidos que codifican una proteína exportada 1 derivada de Plasmodium vivax y usos de las mismas, del 9 de Noviembre de 2016, de ABBOTT LABORATORIES: Un ácido nucleico aislado que consiste en una secuencia de ácido nucleico que tiene una identidad de al menos un 98 % con la secuencia de nucleótidos de SEQ […]
Procedimiento novedoso y composiciones, del 19 de Octubre de 2016, de GLAXOSMITHKLINE BIOLOGICALS SA: Una composición de vacuna que comprende (i) uno o más primeros polipéptidos inmunógenos que comprenden uno o más antígenos del VIH seleccionados […]
Vector adenoviral que codifica un antígeno de malaria, del 21 de Septiembre de 2016, de Oxford University Innovation Limited: Una combinación de productos o kit que comprende: i) una composición de sensibilización que comprende un vector de adenovirus de simio, deficiente […]