REACTIVOS DE MARCAJE DE LANTÁNIDO LUMINISCENTES Y SU USO.
Molécula detectable que comprende un reactante de unión bioespecífico unido a un quelato de lantánido luminiscente que comprende un ión lantánido y un ligando quelante de fórmula (I) en la que,
a) R1A y R1B se seleccionan independientemente entre sí del grupo que consiste en hidrógeno, metilo, etilo, -COOH, -COO-, -CH2COOH, -CH2COO-, hidroxilo u OR2; b) R2 se selecciona del grupo que consiste en -CH3, -C(CH3)3, -C(CR4)3, en el que R4 es un alquilo con de 1 a 6 átomos de carbono, -CH2COOH, -CH2COO - , c) R3 es un conector para el acoplamiento a un reactante de unión bioespecífico seleccionado del grupo que consiste en tiourea (-NH-CS-NH-), aminoacetamida (-NH-CO-CH2-NH-), amida (-NH-CO- y -CO-NH-), tioéter alifático (-S-), disulfuro (-S-S-) y 6-sustituido-1,3,5- triazin-2,4-diamina; y d) el ión lantánido se selecciona del grupo que consiste en europio (III), terbio (III), disprosio (III) y samario (III)
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/FI2007/000202.
Solicitante: ABACUS DIAGNOSTICA OY.
Nacionalidad solicitante: Finlandia.
Dirección: TYKISTÖKATU 4 D 20520 TURKU FINLANDIA.
Inventor/es: TAKALO, HARRI, KANKARE,JOUKO, TIENARI,Elina.
Fecha de Publicación: .
Fecha Solicitud PCT: 17 de Agosto de 2007.
Clasificación Internacional de Patentes:
- G01N33/533 FISICA. › G01 METROLOGIA; ENSAYOS. › G01N INVESTIGACION O ANALISIS DE MATERIALES POR DETERMINACION DE SUS PROPIEDADES QUIMICAS O FISICAS (procedimientos de medida, de investigación o de análisis diferentes de los ensayos inmunológicos, en los que intervienen enzimas o microorganismos C12M, C12Q). › G01N 33/00 Investigación o análisis de materiales por métodos específicos no cubiertos por los grupos G01N 1/00 - G01N 31/00. › con un marcador fluorescente.
- G01N33/58D
Clasificación PCT:
- C07D213/00 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07D COMPUESTOS HETEROCICLICOS (Compuestos macromoleculares C08). › Compuestos heterocíclicos que contienen ciclos de seis miembros, no condensados con otros ciclos, con un átomo de nitrógeno como el único heteroátomo del ciclo y tres o más enlaces dobles entre miembros cíclicos o entre miembros cíclicos y miembros no cíclicos.
- G01N33/533 G01N 33/00 […] › con un marcador fluorescente.
- G01N33/58 G01N 33/00 […] › en los que intervienen sustancias marcadas (G01N 33/53 tiene prioridad).
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Eslovenia, Finlandia, Rumania, Chipre, Lituania, Letonia, Ex República Yugoslava de Macedonia, Albania.
PDF original: ES-2356021_T3.pdf
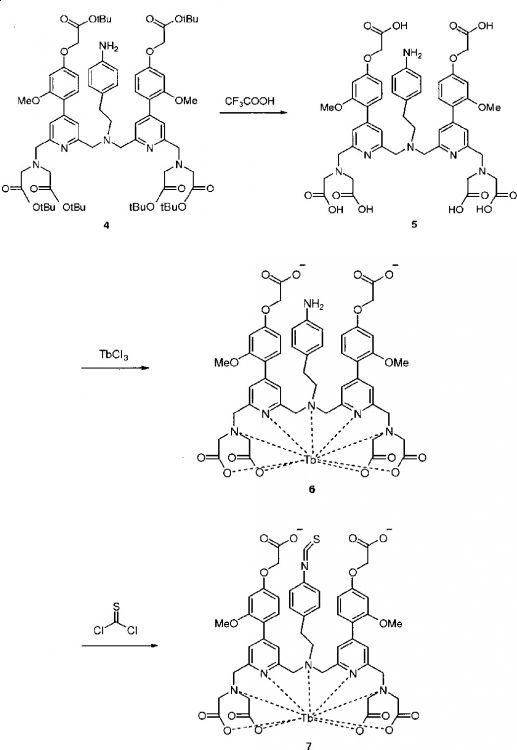
Fragmento de la descripción:
CAMPO DE LA INVENCIÓN
La presente invención se refiere a quelatos de lantánido detectables que van a unirse a un reactante de unión 5 bioespecífico para formar moléculas detectables y al uso de las moléculas detectables en ensayos de unión basados en bioafinidad.
ANTECEDENTES DE LA INVENCIÓN 10
En ensayos de unión bioespecíficos, tales como, por ejemplo inmunoensayos, ensayos de hibridación de ácidos nucleicos, ensayos de unión a receptores, y ensayos de unión celular, los analitos que van a medirse generalmente están presentes a concentraciones muy bajas. Se han desarrollado 15 diversos compuestos de marcaje que permiten que se detecten y se cuantifiquen reactantes de marcaje con alta sensibilidad. La espectroscopía de luminiscencia con resolución temporal que usa quelatos de lantánido se ha aplicado durante varios años en inmunoensayos y ensayos de hibridación de ácidos nucleicos 20 [por ejemplo, I. Hemmilä, T. Stålberg y P. Mottram (eds.), “Bioanalytical Applications of Labelling Technologies”, Wallac, Turku, 1994 y D. Wild (eds), “The Immunoassay Handbook”, Nature Publishing Group, 2001]. Los quelatos de lantánido fotoluminiscentes estables (denominados en el 25 contexto de esta memoria descriptiva simplemente luminiscentes) también tienen otras aplicaciones, por ejemplo citometría y microscopía de fluorescencia. Por tanto, se han realizado varios intentos de desarrollar nuevos quelatos altamente luminiscentes adecuados para esos tipos de 30 aplicaciones fluorométricas con resolución temporal. Éstos incluyen por ejemplo quelatos estables que se componen de derivados de piridina (documentos US 4.920.195; US 4.801.77; US 4.761.481; Bush. C.E. et al. 1992, Anal. Biochem., 202,146; documento WO 92/14841; Hemmilä, et al., 1993, J. Biochem. 35
Biophys. Methods, 26, 283; documentos US 5.571.897; US 5.859.215, Latva, M. et al., 1997, J. Luminescence, 75, 149; Takalo, H. et al., 1996, Helv. Chim. Acta, 79, 789; von Lode, P. et al., 2003, Anal. Chem. 75, 3193; documentos US 7.018.851; WO 2005/021538; US 2005/0181393); bipiridinas 5 (documento US 5.216.134), terpiridinas (documentos US 4.859.777; US 5.202.423; US 5.324.825) o diversos compuestos fenólicos (documentos US 4.670.572; US 4.794.191; IT 1235668) como los grupos de mediación de energía y ácidos policarboxílicos como las partes quelantes. Además, se han 10 dado a conocer diversos derivados de dicarboxilato (documentos US 5.032.677; US 5.055.578; US 4.772.563), criptatos macrocíclicos (documentos US 4.927.923; WO 93/5049; EP 0 493 745), calixarenos (Sato, N. et al., 1993, J. Chem. Soc. Perkin Trans. 2, 621; Steemers, F.J. et al., 1995, J. Am. Chem. Soc., 15 117, 9408), conjugado de DTPA-carboestirilo 124 (Selvin, P.R., et al., 1994, J. Am. Chem. Soc., 116, 6029) y bases de Schiff macrocíclicas (documento EP 0 369 000) en solicitudes de patentes y/o patentes.
Desde la publicación de quelatos, que contienen dos y 20 tres restos de 4-(feniletinil)piridina separados (Takalo, H. et al., Helv. Chim. Acta, 79, 789), se han aplicado las estructuras quelantes diseñadas en solicitudes de patentes y publicaciones en las que se han reemplazado los sustituyentes feniletinilo por 2-furilos y trialcoxifenilos (documentos WO 25 2005/021538; US 2005/0181393, Jaakkola, L. et al. 2005, Bioconjugate Chem., 16, 700). Además, combinando dos grupos funcionales reactivos para el acoplamiento del marcador a un reactante de unión bioespecífico, se han obtenido quelatos altamente luminiscentes (documento US 7.018.851). Los quelatos 30 con cromóforos de 2,4,6-trimetoxipiridina han mostrado alta luminiscencia especialmente con iones Tb (III) y Dy (III) (documento US 4.761.481; Hemmilä, et al, 1993, J. Biochem. Biophys. Methods, 26, 283; Latva, M. et al., 1997, J. Luminescence, 75, 149, documento US 2005/0181393; Jaakkola, L. 35
et al. 2005, Bioconjugate Chem., 16, 700). El nivel de energía del estado triplete del ligando, la naturaleza del cromóforo y el grupo de unión a la biomolécula tienen efectos significativos sobre las propiedades luminiscentes de los marcadores de Tb (III) (véase, por ejemplo, Sabbatini, N. et 5 al., 1991, J. Luminescence 48 y 49: 463; Hemmilä, et al., 1997, J. of Alloys and Compounds 249, 158). Por tanto, incluso pequeños cambios en la estructura del quelato pueden reducir significativamente la luminiscencia de los marcadores de Tb (III). 10
Se conoce que la adición de cromóforos disminuye la solubilidad de los ligandos y quelatos en agua, aumenta la formación de agregados de reactante de unión bioespecífico durante el proceso de marcaje y las propiedades de unión no específica de las biomoléculas marcadas. Los agregados 15 producirán problemas de purificación y una reducción del rendimiento del material marcado. Además, el aumento de la unión no específica de la biomolécula marcada intensificará la luminiscencia de fondo de los ensayos bioespecíficos y por tanto reduce la sensibilidad del ensayo. 20
OBJETOS Y SUMARIO DE LA PRESENTE INVENCIÓN
Un objeto de la presente invención es proporcionar una molécula detectable que comprende un reactante de unión bioespecífico unido a un quelato de lantánido luminiscente. 25
Otro objeto de la presente invención es proporcionar un quelato de lantánido luminiscente.
Un objeto adicional de la presente invención es proporcionar el uso de la molécula detectable de la invención en un ensayo de unión bioespecífico. 30
Por tanto, esta invención proporciona una molécula detectable que comprende un reactante de unión bioespecífico unido a un quelato de lantánido luminiscente que comprende un ión lantánido y un ligando quelante de fórmula (I)
en la que,
a) R1A y R1B se seleccionan independientemente entre sí del grupo que consiste en hidrógeno, metilo, etilo, -COOH, -COO-, -CH2COOH, -CH2COO-, hidroxilo u OR2; 5
b) R2 se selecciona del grupo que consiste en -CH3, -C(CH3)3, -C(CR4)3, en el que R4 es un alquilo con de 1 a 6 átomos de carbono, -CH2COOH, -CH2COO-,
c) R3 es un conector para el acoplamiento a un reactante de 10 unión bioespecífico seleccionado del grupo que consiste en tiourea (-NH-CS-NH-), aminoacetamida (-NH-CO-CH2-NH-), amida (-NH-CO- y -CO-NH-), tioéter alifático (-S-), disulfuro (-S-S-) y 6-sustituido-1,3,5-triazin-2,4-diamina; y
d) el ión lantánido se selecciona del grupo que consiste en europio (III), terbio (III), disprosio (III) y samario (III).
La invención también proporciona un quelato de lantánido luminiscente que comprende un ión lantánido y un ligando quelante de fórmula (I) 5
en la que,
a) R1A y R1B se seleccionan independientemente entre sí del grupo que consiste en hidrógeno, metilo, etilo, -COOH, -COO-, -CH2COOH, -CH2COO-, hidroxilo u OR2; 10
b) R2 se selecciona del grupo que consiste en -CH3, -C(CH3)3, -C(CR4)3, en el que R4 es un alquilo con de 1 a 6 átomos de carbono, -CH2COOH, -CH2COO-,
c) R3 es un conector para el acoplamiento a un reactante de 15 unión bioespecífico seleccionado del grupo que consiste en
grupos amino, aminooxilo, carboxilo, aldehído o mercapto y derivados activados de los mismos; y
d) el ión lantánido se selecciona del grupo que consiste en europio (III), terbio (III), disprosio (III) y samario (III).
La invención proporciona además el uso de la molécula 5 detectable según la invención en un ensayo de unión bioespecífico.
DESCRIPCIÓN DETALLADA DE LA INVENCIÓN Y REALIZACIONES PREFERIDAS
El objetivo de la presente invención es proporcionar 10 medios para obtener marcadores de quelato de lantánido mejorados que van a usarse en ensayos de unión basados en bioafinidad específicos, tales como inmunoensayos (ensayos tanto heterogéneos como homogéneos), ensayos de hibridación de ácidos nucleicos, ensayos de unión a receptores, ensayos 15 inmunocitoquímicos o inmunohistoquímicos que utilizan determinación fluorométrica o fluorométrica con resolución temporal de la luminiscencia específica.
Los quelatos de esta invención tienen como objetivo combinar varias características importantes en un solo 20 marcador, tales como
1. alta absorción a una longitud de onda adecuada, preferible mayor que 300 nm,
2. varias partes de absorción de UV separadas (cromóforos) en la misma estructura de ligando, preferible dos cromóforos,... [Seguir leyendo]
Reivindicaciones:
1. Molécula detectable que comprende un reactante de unión bioespecífico unido a un quelato de lantánido luminiscente que comprende un ión lantánido y un ligando quelante de fórmula (I) 5
en la que,
a) R1A y R1B se seleccionan independientemente entre sí del grupo que consiste en hidrógeno, metilo, etilo, -COOH, -COO-, -CH2COOH, -CH2COO-, hidroxilo u OR2; 10
b) R2 se selecciona del grupo que consiste en -CH3, -C(CH3)3, -C(CR4)3, en el que R4 es un alquilo con de 1 a 6 átomos de carbono, -CH2COOH, -CH2COO-,
c) R3 es un conector para el acoplamiento a un reactante de unión bioespecífico seleccionado del grupo que consiste en tiourea (-NH-CS-NH-), aminoacetamida (-NH-CO-CH2-NH-), amida (-NH-CO- y -CO-NH-), tioéter alifático (-S-), disulfuro (-S-S-) y 6-sustituido-1,3,5-5 triazin-2,4-diamina; y
d) el ión lantánido se selecciona del grupo que consiste en europio (III), terbio (III), disprosio (III) y samario (III).
2. Molécula detectable según la reivindicación 1, 10 caracterizada porque el reactante de unión bioespecífico se selecciona del grupo que consiste en un anticuerpo, antígeno, un ligando receptor, un péptido o una proteína de unión específica, una molécula de ácido nucleico, una sonda de ARN o ADN, derivados de ácido nucleico y 15 moléculas quiméricas que comprenden ácidos nucleicos y/o derivados de ácido nucleico.
3. Molécula detectable según la reivindicación 1, caracterizada porque el quelato de lantánido unido al reactante de unión bioespecífico es {2,2',2”,2”'-{[2-(4-20 isotiocianatofenil)-etilimino]bis(metilen)bis{4-[2-metoxi-4-(carboxi-metoxi)fenil]piridin-6,2-diil}-bis(metilen-nitrilo)}tetrakis(acetato)}terbio (III).
4. Molécula detectable según la reivindicación 1, caracterizada porque el conector R3 es 6-sustituido-25 1,3,5-triazin-2,4-diamina y la sustitución en 6 se selecciona del grupo que consiste en hidrógeno, halógeno, alcoxilo, ariloxilo, amino, alquilo con de 1 a 6 átomos de carbono, amino o tioéteres sustituidos, y preferiblemente se selecciona del grupo que consiste en 30 cloro, fluoro, etoxilo, 2-metoxietoxilo, 2-cianoetoxilo, 2,2,2-trifluoroetoxilo, tiofenoxilo y etoxicarboniltiometoxilo.
5. Quelato de lantánido luminiscente que comprende un ión lantánido y un ligando quelante de fórmula (I) 35
en la que,
a) R1A y R1B se seleccionan independientemente entre sí del grupo que consiste en hidrógeno, metilo, etilo, -COOH, -COO-, -CH2COOH, -CH2COO-, hidroxilo u OR2; 5
b) R2 se selecciona del grupo que consiste en -CH3, -C(CH3)3; -C(CR4)3, en el que R4 es un alquilo con de 1 a 6 átomos de carbono, -CH2COOH, -CH2COO-,
c) R3 es un conector para el acoplamiento a un 10 reactante de unión bioespecífico seleccionado del grupo que consiste en grupos amino, aminooxilo, carboxilo, aldehído o mercapto y derivados activados de los mismos; y
d) el ión lantánido se selecciona del grupo que consiste en europio (III), terbio (III), disprosio (III) y samario (III).
6. Quelato de lantánido luminiscente según la reivindicación 5, caracterizado porque el conector R3 es 5 un derivado activado seleccionado del grupo que consiste en isocianato, isotiocianato, diazonio, bromoacetamido, yodoacetamido, ésteres reactivos, piridil-2-ditio y 6-sustituido-4-cloro-1,3,5-triazin-2-ilamino.
7. Quelato de lantánido luminiscente según la 10 reivindicación 5, caracterizado porque el conector R3 es un 6-sustituido-4-cloro-1,3,5-triazin-2-ilamino y la sustitución en 6 se selecciona del grupo que consiste en hidrógeno, halógeno, alcoxilo, ariloxilo, amino, alquilo con de 1 a 6 átomos de carbono, amino o tioéteres 15 sustituidos, y preferiblemente se selecciona del grupo que consiste en cloro, fluoro, etoxilo, 2-metoxietoxilo, 2-cianoetoxilo, 2,2,2-trifluoroetoxilo, tiofenoxilo y etoxicarboniltiometoxilo.
8. Uso de la molécula detectable según cualquiera de las 20 reivindicaciones 1 a 4, en un ensayo de unión bioespecífico.
Patentes similares o relacionadas:
Método y kit para preparar un par de anticuerpos y uso del kit, y sistema para preparar un par de anticuerpos, del 13 de Mayo de 2020, de Shenzhen New Industries Biomedical Engineering Co., Ltd: Método para preparar un par de anticuerpos, que comprende: usar un fragmento de unión a antígeno de un anticuerpo existente como anticuerpo de captura y usar un anticuerpo […]
Novedosos conjugados de anticuerpos adecuados para su uso en inmunoensayos aislados de desplazamiento de la inactivación de la fluorescencia, del 11 de Marzo de 2020, de Life Science Inkubator Sachsen GmbH & Co. KG: Un conjugado para inmunoensayos de inactivación de la fluorescencia que comprende un anticuerpo unido a un conector, caracterizado por que en su extremo […]
Compuestos de polimetina y su uso como marcadores fluorescentes, del 19 de Febrero de 2020, de ILLUMINA CAMBRIDGE LIMITED: Un compuesto de la fórmula (I) o formas mesoméricas del mismo: **(Ver fórmula)** en donde mCat+ o mAn- es un contraión cargado positivamente/negativamente […]
Haptenos, conjugados de haptenos, composiciones de los mismos y método para su preparación y uso, del 7 de Agosto de 2019, de VENTANA MEDICAL SYSTEMS, INC.: Un conjugado que tiene una fórmula (hapteno)m-(conector),,-(grupo reactivo)0-(vehículo)p donde: el hapteno es una tiazol sulfonamida, donde el hapteno tiene la fórmula […]
Usos de vesículas extracelulares recombinantes, del 15 de Mayo de 2019, de UNIVERSITEIT GENT: Un método para determinar la tasa de recuperación de vesículas extracelulares de muestra, comprendiendo el método: - mezclar una muestra de […]
Desarrollo y utilización de sondas fluorescentes de bilirubina no enlazada, del 1 de Mayo de 2019, de Kleinfeld, Alan M: Una composición que comprende: (a) una sonda que se une a la bilirrubina pero que no se une significativamente al ácido graso, comprendiendo dicha sonda una […]
Transportadores poliméricos para inmunohistoquímica e hibridación in situ, del 17 de Abril de 2019, de VENTANA MEDICAL SYSTEMS, INC.: Un conjugado, que comprende un anticuerpo, que tiene una porción Fc oxidada para crear un grupo funcional reactivo hidracida, unido covalentemente a un […]
Marcadores de diagnóstico para el tratamiento de los trastornos proliferativos celulares con inhibidores de la telomerasa, del 13 de Marzo de 2019, de GERON CORPORATION: Un método de selección de un individuo diagnosticado o sospechoso de tener cáncer que se beneficiará del tratamiento con un inhibidor de la telomerasa, […]