Proteína quimérica inhibidora de la angiogénesis y el uso.
Una proteína quimérica que comprende diferentes fragmentos de los receptores de VEGF,
FLT-1 y KDR, caracterizada porque la proteína quimérica consiste en el 2º dominio de tipo Ig de FLT-1, los dominios 3º y 4º de tipo Ig de KDR y Fc de inmunoglobulina humana, designándose la proteína quimérica como FLTd2KDRd3, 4-Fc.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/CN2005/000802.
Solicitante: CHENGDU KANGHONG BIOTECHNOLOGIES CO., LTD.
Nacionalidad solicitante: China.
Dirección: NO. 36 SHUXI RD JINNIU DISTRICT CHENGDU CITY 610036, SICHUAN CHINA.
Inventor/es: LIU,Zheng.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K38/00 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00).
- A61K38/18 A61K […] › A61K 38/00 Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00). › Factores de crecimiento; Reguladores de crecimiento.
- A61P35/00 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › Agentes antineoplásicos.
- C07K14/47 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 14/00 Péptidos con más de 20 aminoácidos; Gastrinas; Somatostatinas; Melanotropinas; Sus derivados. › de mamíferos.
- C07K14/705 C07K 14/00 […] › Receptores; Antígenos celulares de superficie; Determinantes celulares de superficie.
- C07K14/71 C07K 14/00 […] › para factores de crecimiento; para reguladores de crecimiento.
- C12N15/09 C […] › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 15/00 Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K). › Tecnología del ADN recombinante.
- C12N15/11 C12N 15/00 […] › Fragmentos de ADN o de ARN; sus formas modificadas (ADN o ARN no empleado en tecnología de recombinación C07H 21/00).
- C12N5/10 C12N […] › C12N 5/00 Células no diferenciadas humanas, animales o vegetales, p. ej. líneas celulares; Tejidos; Su cultivo o conservación; Medios de cultivo para este fin (reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00). › Células modificadas por introducción de material genético extraño, p. ej. células transformadas por virus.
PDF original: ES-2381014_T3.pdf
Fragmento de la descripción:
Proteína quimérica inhibidora de la angiogénesis y el uso Campo de la invención La presente invención se refiere a la tecnología de ingeniería genética, más específicamente a secuencias de ADN que codifican para proteínas quiméricas recombinantes inhibidoras de la angiogénesis, a las proteínas quiméricas codificadas del presente documento, a aplicaciones terapéuticas de las mismas y a composiciones farmacéuticas que contienen las proteínas quiméricas.
Antecedentes de la invención
La angiogénesis es un proceso de crecimiento de nuevos vasos sanguíneos a partir de vasos sanguíneos existentes. La mayor parte del sistema vascular adulto es quiescente, sólo se produce angiogénesis en algunos mecanismos fisiológicos y patológicos, tales como tumor, retinopatías diabéticas, artritis, órganos anémicos, hiperplasia del endometrio, etc. La angiogénesis desempeña papeles clave en el crecimiento rápido de células tumorales durante el desarrollo tumoral (Hanahan y Folkman: Patterns and emerging mechanisms of the angiogenic switch during tumorigenesis, Cell, 1996, 86:353-364) . Estudios de modelos de cáncer con animales y ensayos clínicos con seres humanos ya han demostrado que la inhibición de la angiogénesis tumoral pudo inhibir de manera eficaz el crecimiento y el desarrollo tumorales, por tanto prolongar la vida del paciente. La angiogénesis está mediada y regulada por muchos factores biológicos. Las células principales que median la angiogénesis son células endoteliales vasculares que forman la pared interna de los vasos sanguíneos. Diversos factores de crecimiento pueden unirse a receptores relevantes en la superficie de las células endoteliales vasculares, regular procesos celulares a través de la transducción de señales intracelulares, y por tanto mediar la angiogénesis.
Entre diversos factores de crecimiento, VEGF (factor de crecimiento de células endoteliales vasculares) es el factor angiogénico más importante (Ferrara: VEGF and the quest for tumor angiogenesis factor, Nat. Rev. Cancer, 2002, 10: 795-803; Ferrara: Role of vascular endothelial growth factor in physiologic and pathologic angiogenesis: therapeutic implications, Semin. Oncol., 2002, 29 (6 supl.) : 10-14) . VEGF podría secretarse por muchos tipos de células, pero a menudo se sobreexpresa en células tumorales. VEGF funciona mediante la unión a a receptores apropiados. Existen principalmente dos tipos de receptores de VEGF: FLT-1 (tirosina cinasa de tipo fms) y KDR. En cuanto a las estructuras moleculares, estos dos receptores consisten ambos en tres regiones funcionales diferentes: la primera región es la región extracelular, que consiste en siete dominios de tipo inmunoglobulina (de tipo Ig) (d1d7) , que tiene afinidad específica por VEGF, y es la región clave para la unión a VEGF; la segunda región es la región transmembrana que contiene residuos de aminoácidos hidrófobos; la tercera región es el dominio intracelular que contiene un grupo con funcionamiento de tirosina quinasa, que se fosforila después de que se activa el receptor por VEGF, desencadenando la transducción de señales intracelulares, que conduce a efectos funcionales de células endoteliales y angiogénesis.
FLT-1 y KDR se distribuyen principalmente en las células endoteliales vasculares. Por tanto, la actividad mediadora de VEGF en células endoteliales vasculares es altamente específica. VEGF promueve diferenciaciones de células endoteliales, guía las migraciones de células endoteliales, inhibe la apoptosis, induce cambios morfológicos vasculares, y es un factor proangiogénico altamente eficaz.
El nivel de expresión de VEGF en tejidos tumorales es superior a aquél en los tejidos normales. Además, el crecimiento rápido de células tumorales conduce a menudo a hipoxia dentro del tumor, y la hipoxia induce además la expresión de VEGF. Por tanto, VEGF es el factor clave que promueve la angiogénesis tumoral. Muchos estudios con animales han mostrado que inhibiendo la unión a VEGF a sus receptores pudo inhibirse de manera eficaz la angiogénesis tumoral, y por tanto inhibir el crecimiento tumoral. En otras enfermedades relacionadas con la angiogénesis, tales como retinopatías diabéticas y artritis, etc., VEGF también está implicado estrechamente en el desarrollo de estas enfermedades (Ferrara: Role of vascular endothelial growth factor in physiologic and pathologic angiogenesis: therapeutic implications. Semin. Oncol. 2002, 29 (6 supl.) : 10-14) .
Debido a los papeles críticos de VEGF en cánceres y otras enfermedades, las proteínas o químicos que inhiben específicamente VEGF tienen potenciales terapéuticos. Por ejemplo, estudios han mostrado que el anticuerpo neutralizante contra VEGF pudo inhibir de manera eficaz el crecimiento tumoral (Jain: Tumor angiogenesis and accessibility: role of vascular endothelial growth factor, Semin. Oncol., 2002, 29 (6 supl.) : 3-9) . Por tanto, el desarrollo de inhibidores de VEGF eficaces novedosos es importante en investigación clínica. Puesto que FLT-1 y KDR son elementos de unión naturales de VEGF, hubo estudios que investigaron los papeles antiangiogénicos del FLT-1 soluble (el dominio extracelular de FLT-1) y el KDR soluble (el dominio extracelular de KDR) (Yoko Hasumi: Soluble FLT-1 Expression Suppresses Carcinomatous Ascites in Nude Mice Bearing Ovarian Cancer. Cancer Research 62, 2002: 2019-2023) . El FLT-1 soluble pudo inhibir de manera eficaz el crecimiento de células endoteliales vasculares in vitro, pero tiene una corta semivida sérica y no puede alcanzar una concentración sérica eficaz. De manera similar, el KDR soluble también pudo inhibir el crecimiento de células endoteliales vasculares in vitro, pero su actividad antitumoral en modelos con animales no fue satisfactoria (Yoko Hasumi: Soluble FLT-1 Expression Suppresses Carcinomatous Ascites in Nude Mice Bearing Ovarian Cancer. Cancer Research 62, 2002: 2019-2023) .
La patente estadounidense n.º 6.100.071 da a conocer proteínas receptoras de VEGF quiméricas que comprenden secuencias derivadas de los receptores flt-1 y KDR. La publicación de patente internacional n.º WO 00/75319 da a conocer polipéptidos quiméricos modificados del receptor Flt-1. Shinkai et al. (J. Biol. Chem. (1998) 273 (47) , págs. 31283-31288) dan a conocer mutantes de deleción del receptor KDR y examinan las afinidades de unión de estos mutantes para VEGF. Ninguno de estos documentos da a conocer proteínas quiméricas tal como se reivindica actualmente.
Para superar las deficiencias de la técnica anterior, la presente invención proporciona proteínas quiméricas novedosas que contienen diferentes fragmentos de FLT-1 y KDR para bloquear de manera eficaz la actividad biológica de VEGF e inhibir la angiogénesis.
Sumario de invención
La invención proporciona proteínas quiméricas recombinantes novedosas que bloquean la actividad biológica de VEGF e inhiben la angiogénesis, secuencias de ADN que codifican para las proteínas quiméricas mencionadas anteriormente, y vectores que contienen las secuencias de ADN codificantes de las proteínas quiméricas y huéspedes recombinantes de los mismos, tal como se reivindica en el presente documento.
La invención también proporciona el uso de las proteínas quiméricas en la preparación de medicamentos que bloquean la actividad de VEGF e inhiben la angiogénesis, y composiciones farmacéuticas que contienen las proteínas quiméricas y vehículos médicos apropiados, así como aplicaciones terapéuticas de la composición médica, tal como se reivindica en el presente documento.
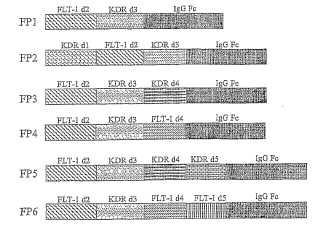
Los puntos clave de la invención son diseñar y construir una serie de proteínas quiméricas con diferentes fragmentos de FLT-1 o KDR, que contienen Fc de inmunoglobulina humana (en la figura 1 se muestra el método de construcción preferido) , y entonces seleccionar la proteína quimérica con alta afinidad para VEGF usando ensayos incluyendo el ensayo de unión a VEGF, y finalmente obtener el inhibidor de VEGF apropiado. La construcción de la proteína quimérica se basa preferiblemente en las tecnologías de clonación molecular convencionales. Podría encontrarse la metodología experimental detallada en manuales de laboratorio tales como Molecular Cloning, la 2ª o la 3ª edición (Joseph Sambrook) .
Las proteínas quiméricas que pueden prepararse a través de tecnología de ADN recombinante para contener diferentes fragmentos de los receptores de VEGF, FLT-1 y KDR, incluyen los siguientes grupos:
a. Que consiste en el 1er dominio de tipo Ig de KDR, el 2º dominio de tipo Ig de FLT-1 y el 3er dominio de tipo Ig de KDR, designado como KDRd1-FLTd2-KDRd3;... [Seguir leyendo]
Reivindicaciones:
1. Una proteína quimérica que comprende diferentes fragmentos de los receptores de VEGF, FLT-1 y KDR, caracterizada porque la proteína quimérica consiste en el 2º dominio de tipo Ig de FLT-1, los dominios 3º y 4º de tipo Ig de KDR y Fc de inmunoglobulina humana, designándose la proteína quimérica como FLTd2KDRd3, 4-Fc.
2. La proteína quimérica según la reivindicación 1, en donde la secuencia de aminoácidos es como se muestra en SEQ ID NO: 7.
3. ADN recombinante que codifica para la proteína quimérica según la reivindicación 1 o la reivindicación 2.
4. El ADN recombinante según la reivindicación 3 que codifica para la proteína quimérica según la reivindicación 2, en donde la secuencia de ADN es como se muestra en SEQ ID NO: 6.
5. Un vector que comprende las secuencias de ADN recombinante según las reivindicaciones 3 ó 4, donde el vector es seleccionado de un plásmido, un virus o un fragmento de ADN.
6. Un huésped recombinante que contiene el vector recombinante según la reivindicación 5, en donde las células huésped son células eucariotas o células procariotas.
7. Una composición farmacéutica la cual comprende una proteína quimérica según la reivindicación 1 o la reivindicación 2 y un vehículo farmacéuticamente aceptable.
8. Una composición farmacéutica según la reivindicación 7, en la que la composición farmacéutica es una disolución inyectable.
9. Una composición farmacéutica como se reivindica en la reivindicación 7 o la reivindicación 8 para su uso en el tratamiento de enfermedades relacionadas con la angiogénesis incluyendo tumor, retinopatías diabéticas, artritis, anemia o hiperplasia del endometrio.
10. El uso de una proteína quimérica según la reivindicación 1 o la reivindicación 2 en la fabricación de un medicamento para el tratamiento antiangiogénico.
11. El uso según la reivindicación 10 en el tratamiento de enfermedades relacionadas con la angiogénesis incluyendo tumor, retinopatías diabéticas, artritis, anemia o hiperplasia del endometrio.
12. La proteína quimérica según la reivindicación 1 o la reivindicación 2 para su uso en el tratamiento antiangiogénico.
13. La proteína quimérica según la reivindicación 12, para su uso en el tratamiento de enfermedades relacionadas con la angiogénesis incluyendo tumor, retinopatías diabéticas, artritis, anemia o hiperplasia del endometrio.
Patentes similares o relacionadas:
Neuregulina para tratar la insuficiencia cardíaca, del 29 de Julio de 2020, de Zensun (Shanghai) Science & Technology, Co., Ltd: Neuregulina para usar en un método para tratar la insuficiencia cardíaca crónica en un paciente, donde el paciente tiene un nivel plasmático de NT-proBNP […]
Dispositivo médico que tiene un revestimiento que comprende ACCS, del 15 de Julio de 2020, de Noveome Biotherapeutics, Inc: Un dispositivo médico implantable que tiene un revestimiento en su superficie, útil para la implantación quirúrgica en el cuerpo de un sujeto, […]
Composiciones que comprenden cócteles de fagos antibacterianos y usos de las mismas para el tratamiento de infecciones bacterianas, del 24 de Junio de 2020, de Tecnifar-Indústria Técnica Farmacêutica, S.A: Una composicion que comprende: una primera y una segunda cepa purificada de bacteriofago, cada una de dichas cepas que tiene un genoma que comprende […]
Combinacion de peptidos tolerogenos con TFG-â para inducir y mantener la tolerancia oral en mamiferos jovenes, del 3 de Junio de 2020, de SOCIETE DES PRODUITS NESTLE S.A.: Una composición nutricional - que contiene al menos un péptido de cinco hasta doce aminoácidos de longitud e incluye una secuencia elegida entre […]
Formulaciones con oxidación reducida, del 3 de Junio de 2020, de F. HOFFMANN-LA ROCHE AG: Una formulación líquida que comprende un anticuerpo y un compuesto que previene la oxidación del anticuerpo en la formulación líquida, en la que el compuesto es […]
Trampas de GDF, del 3 de Junio de 2020, de ACCELERON PHARMA, INC: Un polipéptido aislado que comprende la secuencia de aminoácidos de SEQ ID NO: 28.
Modulación de la actividad del factor de crecimiento epidérmico de unión a heparina para la curación de la membrana timpánica, del 6 de Mayo de 2020, de THE BOARD OF TRUSTEES OF THE LELAND STANFORD JUNIOR UNIVERSITY: Un agente que proporciona actividad de factor de crecimiento epidérmico de unión a heparina (HB-EGF) para su uso en el tratamiento de una perforación crónica de la membrana […]
Composiciones para lograr niveles plasmáticos deseados del factor 2 de crecimiento glial, del 6 de Mayo de 2020, de ACORDA THERAPEUTICS, INC: Factor de crecimiento glial 2 (GGF2) para su uso en la promocion de la remielinizacion celular en un paciente, donde el GGF2 se administra al paciente en una cantidad de […]