Proceso para la preparación de cristales.
Un proceso para la preparación de partículas cristalinas de al menos un principio activo que comprende la puestaen contacto de una solución saturada de al menos un soluto en un disolvente en una primera corriente fluida con unno disolvente en una segunda corriente fluida en el que la relación de caudales de la segunda corrientefluida:
primera corriente fluida es de al menos 20:1, y el no disolvente y el disolvente no son inmiscibles entre sí y elno disolvente contiene un tensioactivo o dispersante, que forma una emulsión o una dispersión de gotitas, en el quedicho soluto se vuelve supersaturado dentro de las gotitas de la emulsión o dispersión así formadas, y someter laemulsión o dispersión a irradiación ultrasónica, en la que al menos un soluto es un principio activo o uno de susprecursores, los ultrasonidos que inducen la nucleación y por tanto la cristalización del al menos un soluto; larecirculación del no disolvente y el soluto en una corriente en continua recirculación; y posteriormente el aislamientode las partículas cristalinas resultantes.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/GB2008/050452.
Solicitante: PROSONIX LIMITED.
Nacionalidad solicitante: Reino Unido.
Dirección: Magdalen Centre Robinson Avenue Oxford Science Park Oxford Oxfordshire OX4 4GA REINO UNIDO.
Inventor/es: RUECROFT, GRAHAM, ROBINSON,JAMES, PARIKH,DIPESH.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K9/16 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 9/00 Preparaciones medicinales caracterizadas por un aspecto particular. › Aglomerados; Granulados; Microbolitas.
- B01D9/00 TECNICAS INDUSTRIALES DIVERSAS; TRANSPORTES. › B01 PROCEDIMIENTOS O APARATOS FISICOS O QUIMICOS EN GENERAL. › B01D SEPARACION (separación de sólidos por vía húmeda B03B, B03D, mesas o cribas neumáticas B03B, por vía seca B07; separación magnética o electrostática de materiales sólidos a partir de materiales sólidos o de fluidos, separación mediante campos eléctricos de alta tensión B03C; aparatos centrifugadores B04B; aparato de vórtice B04C; prensas en sí para exprimir los líquidos de las sustancias que los contienen B30B 9/02). › Cristalización (directamente a partir de la fase de vapor B01D 7/02; producción de monocristales C30B).
- B01J2/02 B01 […] › B01J PROCEDIMIENTOS QUÍMICOS O FÍSICOS, p. ej. CATÁLISIS O QUÍMICA DE LOS COLOIDES; APARATOS ADECUADOS. › B01J 2/00 Procedimientos o dispositivos para la granulación de sustancias, en general; Tratamiento de materiales particulados para hacer que fluyan libremente, en general, p. ej. haciéndolos hidrófobos. › por división del producto líquido en gotitas, p. ej. por pulverización, y solidificación de las gotitas.
- B01J2/18 B01J 2/00 […] › mediante la utilización de un vibrador.
PDF original: ES-2429295_T3.pdf
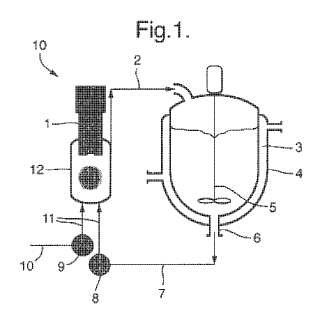
Fragmento de la descripción:
Proceso para la preparación de cristales Campo de la invención Esta invención se refiere a un proceso para la preparación de cristales pequeños en presencia de radiación ultrasónica en el que se emplean al menos dos líquidos diferentes.
Antecedentes de la invención En algunas circunstancias es muy importante el control del tamaño de los cristales y partículas precipitadas, en particular en las industrias farmacéutica y agroquímica en las que la forma del producto final del principio activo de interés se encuentra en forma de polvo fino. La manera en que se comporta un principio activo en un sistema biológico depende de muchos factores, entre otros, del tamaño de partícula y la forma del cristal. Las partículas pequeñas se pueden preparar mediante procesos tales como molienda, pero esos procesos pueden tener un efecto perjudicial sobre las propiedades del material y también pueden producir una fracción significativa de partículas que no son adecuadas para el uso deseado, por ejemplo, pueden tener una forma inadecuada. Estas partículas pueden experimentar alteraciones morfológicas, produciendo transformaciones polimorfológicas superficiales poco deseables que a su vez pueden dar lugar a la formación de estructuras amorías. Las partículas pueden quedar altamente cargadas, lo que puede contribuir a mermar los caudales. Además, las partículas destinadas a su utilización en aerosoles se pueden ver comprometidas en caso de quedar altamente cargadas. Sería deseable la cristalización de cristales en el intervalo de tamaños deseado directamente en una solución.
Durante muchos años se ha sabido cómo provocar la cristalización al mezclar un disolvente que contiene un principio activo a cristalizar con un anti-disolvente, de manera que después de la mezcla la solución está supersaturada y se produce la cristalización. La mezcla se puede producir en presencia de radiación ultrasónica o de una forma diferente en la que no se utiliza radiación ultrasónica, por ejemplo, mezcla con un vórtice de fluido. El término "anti-disolvente" significa un fluido que promueve la precipitación del principio activo de interés (o de un precursor del principio activo) en el disolvente. El anti-disolvente puede comprender un gas frío, o un fluido que promueve la precipitación mediante una reacción química, o que reduce la solubilidad del principio activo de interés en el disolvente; puede ser el mismo líquido que el disolvente pero a una temperatura diferente, o puede ser un líquido diferente al disolvente.
El documento EP 1144065 describe un sistema en el que se consigue la mezcla de un anti-disolvente con un disolvente que comprende un principio activo a cristalizar mediante la utilización de una relación de caudales de antidisolvente:disolvente de hasta 10:1 en presencia de radiación ultrasónica en una celda de flujo continuo. Se describe la mezcla de un disolvente caliente con un anti-disolvente miscible frío, aunque no se revela la temperatura real del anti-disolvente frío.
El documento EP 1469938 describe un sistema en el que el caudal de mezcla del anti-disolvente con el disolvente que comprende un principio activo a cristalizar supera al del disolvente, a una relación de caudales de hasta 10:1, por lo general desde 2:1 hasta 5:1. La mezcla se lleva a cabo en presencia de radiación ultrasónica.
El documento EP 1688169 A1 desvela un método para producir partículas orgánicas finas en las que un compuesto orgánico disuelto en un disolvente orgánico se pone en contacto con un anti-disolvente en presencia de radiación ultrasónica y el anti-disolvente se hace recircular después de separar los sólidos de él.
Los procesos de la técnica anterior permiten la producción de cristales utilizando relaciones de caudales de antidisolvente:disolvente que por lo general son inferiores a 20:1 (es decir, a una relación de caudales de 10:1 hasta un mínimo de 1:1) .
Sumario de la invención De acuerdo con la presente invención se proporciona un proceso como se especifica en la reivindicación 1.
La corriente no disolvente se debe recircular, por ejemplo, en una corriente de recirculación que fluye de forma continua, es decir, una segunda corriente fluida. La relación de caudales de dicha segunda corriente fluida (es decir, que es o que comprende el no disolvente) :primera corriente fluida (es decir, que es o que comprende el disolvente) puede ser cualquier relación de caudales de al menos 20:1 dependiendo del diseño y del fin último de los cristales obtenidos utilizando el proceso de la invención. La relación de caudales empleada en el proceso de la invención se puede decidir teniendo en cuenta la sustancia de interés, el tamaño deseado de los cristales necesarios para un fin determinado, y cómo se deben administrar los cristales a un sujeto, tal como un mamífero (por ejemplo, un ser humano; un caballo; un animal bovino; un cerdo; o una oveja) en forma de medicamento adecuado, o a una planta en forma de compuesto agroquímico adecuado, por ejemplo, un pesticida, un herbicida, un fungicida, un bactericida,
o un viricida. Las relaciones de caudales adecuadas para su utilización en el proceso de la invención pueden ser cualquier relación de caudales de la segunda corriente fluida:primera corriente fluida de hasta 1000:1, por ejemplo, 900:1, 800:1, 700:1, 600:1, 500:1, 400:1, 300:1, 200:1, 100:1, 50:1, 40:1, 30:1 o 20:1, o 1:1 o cualquier relación de caudales entre medias, tal como 380:1, 330:1, 333:1, 165:1, 80:1, 60:1, 40:1, 30:1, 20:1 y similares. Las relaciones de caudales preferidas incluyen desde al menos 20:1 hasta 1000:1; desde al menos 20:1 hasta 800:1; desde al menos 20:1 hasta 600:1. La relación de caudales estará determinada por el tamaño de los cristales necesarios para un fin último determinado y el vehículo de administración propuesto para su utilización en un organismo.
En la técnica son muy conocidas las emulsiones y dispersiones y su formación. Las emulsiones son, por definición, gotitas estabilizadas en una fase continua, por ejemplo, mediante la utilización de tensioactivos conocidos en la técnica. Las dispersiones se pueden considerar como gotitas dispersas en una fase continua en las que las gotitas no están estabilizadas, es decir, no permanecen en forma de gotitas sino que después de un corto periodo de tiempo se unen formando un sistema bifásico con la fase continua. Con el fin de estabilizar las dispersiones, en la técnica se conoce la adición de tensioactivos u otros agentes estabilizantes a ellas, permitiendo la formación de gotitas estabilizadas y de, esta forma, una emulsión estable.
Las gotitas pueden ser de un líquido orgánico o inorgánico, y la fase continua puede ser acuosa o no acuosa dependiendo del fin último y del diseño. Por lo general, las emulsiones de la presente invención comprenden gotitas de un líquido orgánico que comprende un soluto (es decir, formado de al menos un principio activo) , y la fase continua es una fase acuosa, que juntos forman una dispersión o emulsión acuosa.
La emulsión contiene tensioactivos o dispersantes, conocidos en la técnica, para ayudar a la formación y estabilización de la emulsión. Dichos tensioactivos y dispersantes se pueden seleccionar de acuerdo con la naturaleza de la emulsión, y pueden ser no iónicos, aniónicos y/o catiónicos dependiendo del diseño. Los aditivos estarán presentes por lo general en una cantidad del 0, 01-30% en peso/peso, preferentemente del 0, 1-20% en peso/peso.
Por lo general las gotitas pueden variar su diámetro entre 0, 05 y 80 μm aproximadamente. Las gotitas con un diámetro en el intervalo de 0, 3 a 80 μm son conocidas como "macro-gotitas", y las emulsiones como "macroemulsiones". Las gotitas con un diámetro en el intervalo de 0, 05 a 0, 3 μm son conocidas como "micro-gotitas", y las emulsiones como "micro-emulsiones". Para los fines de la presente invención, los términos "gotitas" y "emulsiones" se utilizan en este documento para englobar tanto macro- y micro-gotitas como macro- y micro-emulsiones.
La fase líquida orgánica de las gotitas será insoluble en agua. En algunas situaciones, la fase líquida orgánica por lo general se disolverá en agua en una cantidad no superior al 10% en peso/peso a una temperatura a la que puede tener lugar la cristalización.
En la técnica es sabido que la emulsión además puede contener un agente tamponante, tal como acetato de sodio y ácido acético, para mantener el pH de la emulsión a un nivel deseado, agentes anticongelantes y agentes para ajustar la solubilidad; y también puede contener un solubilizante para un principio o principios activos, tal como acetona o diclorometano o una mezcla de alcohol etílico y diclorometano, que se pueden retirar fácilmente... [Seguir leyendo]
Reivindicaciones:
1. Un proceso para la preparación de partículas cristalinas de al menos un principio activo que comprende la puesta en contacto de una solución saturada de al menos un soluto en un disolvente en una primera corriente fluida con un no disolvente en una segunda corriente fluida en el que la relación de caudales de la segunda corriente fluida:primera corriente fluida es de al menos 20:1, y el no disolvente y el disolvente no son inmiscibles entre sí y el no disolvente contiene un tensioactivo o dispersante, que forma una emulsión o una dispersión de gotitas, en el que dicho soluto se vuelve supersaturado dentro de las gotitas de la emulsión o dispersión así formadas, y someter la emulsión o dispersión a irradiación ultrasónica, en la que al menos un soluto es un principio activo o uno de sus precursores, los ultrasonidos que inducen la nucleación y por tanto la cristalización del al menos un soluto; la recirculación del no disolvente y el soluto en una corriente en continua recirculación; y posteriormente el aislamiento de las partículas cristalinas resultantes.
2. Un proceso de acuerdo con la reivindicación 1 en el que la relación de caudales de la segunda corriente fluida:primera corriente fluida es de al menos 20:1 hasta 1000:1.
3. Un proceso de acuerdo con la reivindicación 2 en el que la relación de caudales de la segunda corriente fluida:primera corriente fluida es de al menos 20:1 hasta 600:1.
4. Un proceso de acuerdo con una cualquiera de las reivindicaciones 1 a 3, en el que la emulsión o dispersión comprende al menos un principio activo o uno de sus precursores, y una sustancia vehículo.
5. Un proceso de acuerdo con una cualquiera de las reivindicaciones anteriores, en el que la emulsión o dispersión comprende una mezcla de dos principios activos.
6. Un proceso de acuerdo con la reivindicación 4 o la reivindicación 5 en el que el principio activo se selecciona entre propionato de fluticasona, ibuprofeno y budesonida.
7. Un proceso de acuerdo con una cualquiera de las reivindicaciones 1 a 6, en el que la temperatura del no disolvente y disolvente líquidos oscila entre -10 °C y 120 °C y las temperaturas del disolvente y del no disolvente están separadas por una diferencia de temperatura de al menos 5 °C.
8. Un proceso de acuerdo con la reivindicación 7 en el que dicha diferencia de temperaturas es de hasta 60 °C.
9. Un proceso de acuerdo con la reivindicación 7 o la reivindicación 8, en el que dicha diferencia de temperaturas es de hasta 50 °C.
10. Un proceso de acuerdo con la reivindicación 9 en el que dicha diferencia de temperaturas es de hasta 30 °C.
11. Un proceso de acuerdo con la reivindicación 10 en el que la diferencia de temperaturas es de hasta 20 °C.
12. Un proceso de acuerdo con la reivindicación 11 en el que la diferencia de temperaturas es de hasta 10 °C.
13. Un proceso de acuerdo con una cualquiera de las reivindicaciones 1 a 12, en el que la emulsión o dispersión comprende un principio activo o sustancia vehículo adecuados para la terapia de inhalación.
Patentes similares o relacionadas:
Unidad de dosificación farmacéutica sólida desintegrante por vía oral que contiene una sustancia de control de partos, del 22 de Julio de 2020, de Oxytone Bioscience B.V: Unidad de dosificacion farmaceutica solida desintegrante por via oral que tiene un peso de entre 50 y 1.000 mg, donde dicha unidad de dosificacion consiste en: • 5-100 […]
Granulados secos de polvos de sílice mesoporosa, del 1 de Julio de 2020, de FORMAC PHARMACEUTICALS N.V: Un granulado seco que comprende desde el 50% al 100% p/p de sílice mesoporosa ordenada que tiene una organización bidimensional hexagonalmente […]
COMPOSICIONES DE ALPRAZOLAM AMORFO CON ACTIVIDAD ANSIOLÍTICA, CON ETILCELULOSA Y CROSPOVIDONA, Y PROCEDIMIENTOS CORRESPONDIENTES, del 18 de Junio de 2020, de LABORATORIOS BAGO S.A.: Composición de alprazolam amorfo con actividad ansiolítica que comprende: a) una premezcla que contiene: - entre 0,33 y 0,66% p/p de alprazolam; - entre […]
Sales de butirato para uso en enfermedades inflamatorias, del 17 de Junio de 2020, de Birrbeheer B.V: Una preparación que comprende una sal de butirato para uso en el tratamiento de un sujeto que padece una enfermedad que está asociada con inflamación sistémica, […]
Métodos para el tratamiento de la enfermedad ocular en sujetos humanos, del 10 de Junio de 2020, de Clearside Biomedical, Inc: Una formulación farmacéutica que comprende un fármaco para su uso en un método de tratamiento de un trastorno ocular posterior en un sujeto humano que […]
Formulaciones de inulina y de acetato de inulina, del 5 de Junio de 2020, de SOUTH DAKOTA STATE UNIVERSITY (100.0%): Una composición que comprende micropartículas o nanopartículas de acetato de inulina (InAc) y una molécula de carga, en la que la molécula de carga está encapsulada […]
Gránulos de dispersión rápida, comprimidos de desintegración oral y métodos, del 3 de Junio de 2020, de Adare Pharmaceuticals, Inc: Microgránulos de dispersión rápida, farmacéuticamente aceptables, que tienen una mediana del tamaño de partícula en el rango de 100 μm a 300 […]
Composiciones de polifenol, del 3 de Junio de 2020, de Nugerontix Limited: Enoteína B para uso en terapia para tratar, prevenir o retrasar la aparición de disfunción endotelial donde el tratamiento, prevención o retraso comprende […]