PROCEDIMIENTOS PARA TRATAR DOLOR POSTQUIRÚRGICO MEDIANTE LA ADMINISTRACIÓN DE UN ANTICUERPO FRENTE AL FACTOR DE CRECIMIENTO NERVIOSO Y COMPOSICIONES QUE CONTIENEN EL MISMO.
Un anticuerpo anti-NGF para su uso en el tratamiento de dolor postquirúrgico
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2003/032089.
Solicitante: RINAT NEUROSCIENCE CORP..
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 230 EAST GRAND AVENUE SOUTH SAN FRANCISCO, CA 94080 ESTADOS UNIDOS DE AMERICA.
Inventor/es: SHELTON,DAVID,L, VERGARA,GERMAN,J.
Fecha de Publicación: .
Fecha Solicitud PCT: 8 de Octubre de 2003.
Clasificación Internacional de Patentes:
- C07K16/22 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 16/00 Inmunoglobulinas, p. ej. anticuerpos mono o policlonales. › contra factores de crecimiento.
Clasificación PCT:
- A61K39/395 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 39/00 Preparaciones medicinales que contienen antígenos o anticuerpos (materiales para ensayos inmunológicos G01N 33/53). › Anticuerpos (aglutininas A61K 38/36 ); Inmunoglobulinas; Inmunosuero, p. ej. suero antilinfocitario.
- G01N33/53 FISICA. › G01 METROLOGIA; ENSAYOS. › G01N INVESTIGACION O ANALISIS DE MATERIALES POR DETERMINACION DE SUS PROPIEDADES QUIMICAS O FISICAS (procedimientos de medida, de investigación o de análisis diferentes de los ensayos inmunológicos, en los que intervienen enzimas o microorganismos C12M, C12Q). › G01N 33/00 Investigación o análisis de materiales por métodos específicos no cubiertos por los grupos G01N 1/00 - G01N 31/00. › Ensayos inmunológicos; Ensayos en los que interviene la formación de uniones bioespecíficas; Materiales a este efecto.
Clasificación antigua:
- A61K39/395 A61K 39/00 […] › Anticuerpos (aglutininas A61K 38/36 ); Inmunoglobulinas; Inmunosuero, p. ej. suero antilinfocitario.
- G01N33/53 G01N 33/00 […] › Ensayos inmunológicos; Ensayos en los que interviene la formación de uniones bioespecíficas; Materiales a este efecto.
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Eslovenia, Finlandia, Rumania, Chipre, Lituania, Letonia, Ex República Yugoslava de Macedonia, Albania.
PDF original: ES-2357948_T3.pdf




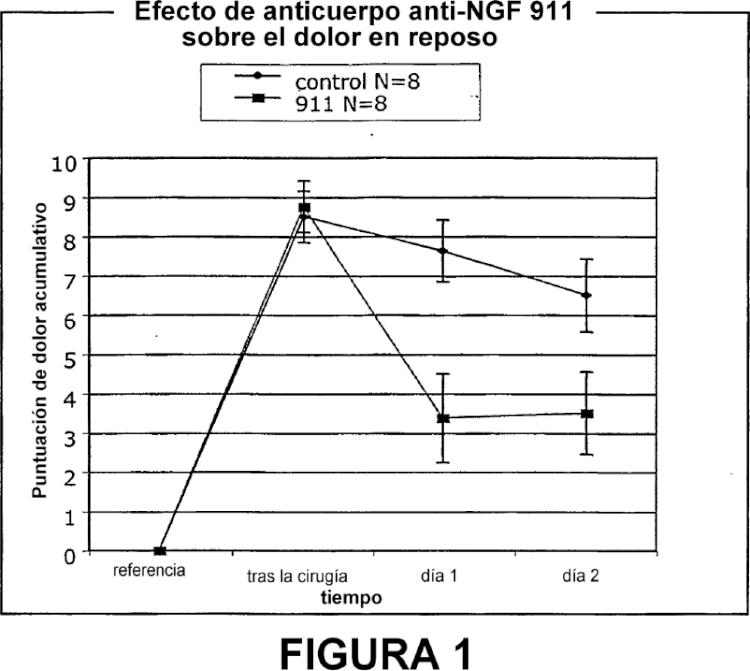
Fragmento de la descripción:
CAMPO DE LA INVENCIÓN
La presente invención se refiere a un anticuerpo anti-factor de crecimiento nervioso (NGF) para su uso en la prevención, la mejora o el tratamiento de dolor postquirúrgico.
ANTECEDENTES DE LA INVENCIÓN 5
El factor de crecimiento nervioso (NGF) fue la primera neurotrofina que se detectó y se ha caracterizado bien su papel en el desarrollo y supervivencia de neuronas tanto periféricas como centrales. Se ha demostrado que NGF es un factor crítico de supervivencia y mantenimiento en el desarrollo de neuronas sensoriales embrionarias y simpáticas periféricas y de neuronas colinérgicas del prosencéfalo basal (Smeyne, et al., Nature 368:246-249 (1994); Crowley, et al., Cell 76:1001-1011 (1994)). El NGF regula por incremento la expresión de neuropéptidos en 10 neuronas sensoriales (Lindsay, et al., Nature 337:362-364 (1989)), y su actividad está mediada a través de dos diferentes receptores unidos a la membrana, el receptor de tirosina cinasa TrkA y el receptor p75 que está estructuralmente relacionado con otros miembros de la familia de receptores del factor de necrosis tumoral (Chao, et al., Science 232:518-521 (1986).
Además de sus efectos en el sistema nervioso, el NGF se ha implicado cada vez más en procesos fuera del 15 sistema nervioso. Por ejemplo, NGF ha mostrado que potencia la permeabilidad vascular (Otten, et al., Eur J Pharmacol. 106:199-201 (1984)), potencia las respuestas inmunitarias de células T y B (Otten, et al., Proc. Natl. Acad. Sci. USA 86:10059-10063 (1989)), induce la diferenciación de linfocitos y la proliferación de mastocitos y provoca la liberación de señales biológicas solubles a partir de mastocitos (Matsuda, et al., Proc. Natl. Acad. Sci. USA 85:6508-6512 (1988); Pearce, et al., J. Physiol. 372:379-393 (1986); Bischoff, et al., Blood 79:2662-2669 20 (1992); Horigome, et al., J. Biol. Chem. 268:14881-14887 (1993)). Aunque el NGF añadido de manera exógena ha demostrado que puede tener todos estos efectos, es importante observar que se ha demostrado sólo pocas veces que el NGF endógeno es importante en cualquiera de estos procesos in vivo (Torcia, et al., Cell. 85(3): 345-56 (1996)). Por tanto, no está claro cuál puede ser el efecto, si lo hay, de inhibir la bioactividad de NGF endógeno.
El NGF se produce mediante varios tipos de células incluyendo mastocitos (Leon, et al., Proc. Natl. Acad. 25 Sci. USA 91: 3739-3743 (1994)), linfocitos B (Torcia, et al., Cell 85:345-356 (1996), queratinocitos (Di Marco, et al., J. Biol. Chem. 268:22838-22846)), células de músculo liso (Ueyama, et al., J. Hypertens. 11:1061-1065 (1993)), fibroblastos (Lindholm, et al., Eur. J. Neurosci. 2:795-801 (1990)), células epiteliales bronquiales (Kassel, et al., Clin, Exp. Allergy 31:1432-40 (2001)), células mesangiales renales (Steiner, et al., Am. J. Physiol. 261:F792-798 (1991)) y miotubos del músculo esquelético (Schwartz, et al., J Photochem, Photobiol. B 66:195-200 (2002)). Se han 30 encontrado receptores de NGF en una variedad de tipos de células fuera del sistema nervioso. Por ejemplo, se ha encontrado TrkA en mastocitos, linfocitos T y B y monocitos humanos.
Se ha observado una asociación entre un aumento de los niveles de NGF y una variedad de estados inflamatorios en pacientes humanos así como también en varios modelos animales. Éstos incluyen lupus eritematoso sistémico (Bracci-Laudiero, et al., Neuroreport 4:563-565 (1993)), esclerosis múltiple (Bracci-Laudiero, et 35 al., Neurosci. Lett. 147:9-12 (1992)), psoriasis (Raychaudhuri, et al., Acta Derm. l'enereol. 78:84-86 (1998)), artritis (Falcimi, et al., Ann. Rheum. Dis. 55:745-748 (1996)), cistitis intersticial (Okragly, et al., J. Urology 161:438-441 (1991)) y asma (Braun, et al., Eur. J Immunol. 28:3240-3251 (1998)).
Consecuentemente, un nivel elevado de NGF en tejidos periféricos está asociado con la inflamación y se ha observado en varias formas de artritis. El sinovio de pacientes afectados por artritis reumatoide expresa altos niveles 40 de NGF, mientras que se ha notificado que en el sinovio no inflamado NGF es indetectable (Aloe, et al., Arch. Rheum. 35:351-355 (1992)). Se observaron resultados similares en ratas con artritis reumatoide inducida experimentalmente (Aloe, et al., Clin. Exp. Rheumatol. 10:203-204 (1992)). Se han notificado niveles elevados de NGF en ratones artríticos transgénicos junto con un aumento del número de mastocitos. (Aloe, et al., Int. J. Tissue Reactions-Exp. Clin. Aspects 15:139-143 (1993)). 45
El tratamiento con NGF exógeno conduce aun aumento del dolor y sensibilidad al dolor. Esto se ilustra mediante el hecho de que la inyección de NGF conduce a un aumento significativo del dolor y la sensibilidad al dolor tanto en modelos animales (Amann, et al., Pain 64, 323-329 (1996); Andreev, et al., Pain 63, 109-115 (1995)) como ser humano (Dyck, et al., Neurology 48, 501-505 (1997); Petty, et al., Annals Neurol. 36, 244-246 (1994)). El NGF parece actuar mediante múltiples mecanismos incluyendo la inducción de la neurotrofina BDNF (Apfel, et al., Mol. 50 Cell. Neurosci. 7(2), 134-142 (1996); Michael, et al., J. Neurosci 17, 8476-8490 (1997)) que a su vez cambia el procesamiento de señal de dolor en la médula espinal (Hains, et al., Neurosci Lett. 320(3), 125-8 (2002); Miletic, et al., Neurosci Lett. 319(3), 137-40 (2002); Thompson, et al., Proc Natl Acad Sci USA 96(14), 7714-8 (1999)), la inducción de cambios en las conexiones central y periférica de las neuronas sensoriales y otras neuronas de transmisión de dolor en la médula espinal (Lewin, et al., European Journal of Neuroscience 6, 1903-1912 (1994); 55 Thompson, et al., Pain 62, 219-231 (1995)), la inducción de cambios en el crecimiento axonal (Lindsay, RM, J Neurosci. 8(7), 2394-405 (1988)), la inducción dela expresión del receptor de bradicinina (Peterson et al., Neuroscience 83:161-168 (1998)), la inducción de cambios en la expresión de genes responsables de la conducción y activación nerviosa tales como canales iónicos (Boettger, et al., Brain 125(Pt 2), 252-63 (2002); Kerr, et al., Neuroreport 12(14), 3077-8 (2001); Gould, et al., Brain Res 854(1-2), 19-29 (2000)), la potenciación del receptor VR1 60
relacionado con el dolor (Chuang, et al., Nature 411 (6840), 957-62 (2001); y la provocación de cambios patológicos en músculos (Foster, et al., J Pathol 197(2), 245-55 (2002)). Muchos de estos cambios tienen lugar directamente en las neuronas sensoriales que transmiten el dolor y aparentemente no dependen de la inflamación concomitante. Además, existen al menos otros dos tipos de células que se sabe que responden a NGF y que pueden estar implicadas en cambios de sensibilidad al o sensación de dolor. Se ha notificado que el primero de ellos, el mastocito, 5 responde a NGF con desgranulación (Yan, et al., Clin. Sci. (Lond) 80:565-569 (1991)) o, en otros estudios, provoca o aumenta la producción o liberación de mediador en colaboración con otros agentes (Pearce y Thompson, J. Physiol. 372:379-393 (1986), Kawamoto, et al., J. Immunol. 168:6412-6419 (2002)). Se ha demostrado claramente en la rata que las respuestas al dolor mediadas con NGF están al menos un tanto mediadas por mastocitos (Lewin, et al., Eur. J. Neurosci. 6:1903-1912 (1994), Woolf, et al., J. Neurosci. 16:2716-2723 (1996) aunque la posible relevancia de 10 esto queda por demostrarse en seres humanos. También se sabe que las neuronas simpáticas primarias responden a NGF y que también están implicadas en la señalización del dolor (Aley, et al., Neuroscience 71:1083-1090 (1996)). Está claro que la eliminación de inervación simpática modifica la hiperalgesia normalmente observada en respuesta al tratamiento con NGF (Woolf, et al., J. Neurosci. 16: 2716-2723 (1996)).
Cada año se someten a procedimientos quirúrgicos veintitrés millones de pacientes. El dolor está localizado 15 normalmente dentro de la proximidad del sitio quirúrgico. El dolor postquirúrgico puede tener dos aspectos clínicamente importantes, concretamente el dolor en reposo, o dolor que se produce cuando el paciente no está moviéndose y el dolor mecánico que se exacerba mediante el movimiento (toser/estornudar, salir de la cama, fisioterapia, etc.). El principal problema con la gestión del dolor postquirúrgico para cirugía mayor es que los fármacos usados actualmente tienen una variedad de efectos secundarios prominentes que retrasan la 20 recuperación, prolongan la hospitalización y someten a ciertos grupos de pacientes vulnerables al riesgo de complicaciones graves. El dolor postquirúrgico, o dolor que se produce tras cirugía o lesión traumática es un problema médico grave y con frecuencia intratable.
Existen... [Seguir leyendo]
Reivindicaciones:
1. Un anticuerpo anti-NGF para su uso en el tratamiento de dolor postquirúrgico.
2. Un anticuerpo anti-NGF según la reivindicación 1, en el que el anticuerpo anti-NGF es para su uso para suprimir o mejorar el dolor en reposo.
3. Un anticuerpo anti-NGF según la reivindicación 1, en el que el anticuerpo anti-NGF es para su uso para 5 suprimir o mejorar el dolor inducido mecánicamente.
4. Un anticuerpo anti-NGF según una cualquiera de las reivindicaciones 1 a 3, en el que el anticuerpo anti-NGF es un anticuerpo humano.
5. Un anticuerpo anti-NGF según una cualquiera de las reivindicaciones 1 a 3, en el que el anticuerpo anti-NGF es un anticuerpo humanizado. 10
6. Un anticuerpo anti-NGF según una cualquiera de las reivindicaciones 1 a 3, en el que el anticuerpo anti-NGF está unido a NGF humano.
7. Un anticuerpo anti-NGF según la reivindicación 6, en el que el anticuerpo anti-NGF está unido a NGF humano con una afinidad de unión de aproximadamente 0,1 nM.
8. Un anticuerpo anti-NGF según la reivindicación 6, en el que el anticuerpo anti-NGF está unido a NGF humano 15 con una afinidad de unión de entre aproximadamente 2 pM y 22 pM.
9. Un anticuerpo anti-NGF según la reivindicación 8, en el que el anticuerpo anti-NGF está unido a un epítopo de NGF que comprende uno o más: residuos K32, K34 y E35 dentro de la región variable 1 (aminoácidos 23-35) de hNGF, residuos F79 y T81 dentro de la región variable 4 (aminoácidos 81-88) de hNGF; residuos H84 y K88 dentro de la región variable 4; residuo R103 entre la región variable 5 (aminoácidos 94-98) de hNGF y el extremo C-20 terminal (aminoácidos 111-118) de hNGF; residuo E11 dentro de la región prevariable 1 (aminoácidos 10-23) de hNGF; Y52 entre la región variable 2 (aminoácidos 40-49) de hNGF y la región variable 3 (aminoácidos 59-66) de hNGF; residuos L112 y S113 dentro del extremo C-terminal de hNGF; residuos R59 y R69 dentro de la región variable 3 de hNGF; o residuos V18, V20 y G23 dentro de la región prevariable 1 de hNGF.
10. Uso de un anticuerpo anti-NGF en la fabricación de un fármaco para tratar el dolor postquirúrgico. 25
11. Una composición farmacéutica para su uso en el tratamiento de dolor postquirúrgico que comprende un anticuerpo anti-NGF y un vehículo farmacéuticamente aceptable.
Patentes similares o relacionadas:
 Métodos para producir proteínas bicatenarias en bacterias, del 29 de Julio de 2020, de GENENTECH, INC.: Un método para producir un receptor de linfocitos T monoclonal de movilización inmunitaria contra el cáncer (ImmTAC) que comprende una cadena alfa del receptor de linfocitos […]
Métodos para producir proteínas bicatenarias en bacterias, del 29 de Julio de 2020, de GENENTECH, INC.: Un método para producir un receptor de linfocitos T monoclonal de movilización inmunitaria contra el cáncer (ImmTAC) que comprende una cadena alfa del receptor de linfocitos […]
Método para el tratamiento de la osteoporosis, del 22 de Julio de 2020, de AMGEN INC.: Un anticuerpo antiesclerostina que comprende una CDR-H1 de la SEQ ID NO: 245, una CDR-H2 de la SEQ ID NO: 246, una CDR-H3 de la SEQ ID NO: 247, […]
Anticuerpo anti-FGF23 y composición farmacéutica que comprende el mismo, del 15 de Julio de 2020, de Kyowa Kirin Co., Ltd: Anticuerpo o fragmento funcional del mismo que se une a la totalidad o a una parte del epítopo de FGF23 humano, al que se une un anticuerpo producido […]
Anticuerpos scFv que pasan las capas epitelial y/o endotelial, del 1 de Julio de 2020, de ESBATech, an Alcon Biomedical Research Unit LLC: Un anticuerpo monocatenario (scFv) que comprende: (a) un dominio variable de la cadena ligera (VL) que tiene tres regiones CDR de VL no […]
 Tratamiento del cáncer usando inhibidores de TGF-beta y PD-1, del 24 de Junio de 2020, de XOMA TECHNOLOGY LTD.: Un inhibidor del factor de crecimiento transformante beta (TGFβ) y un inhibidor de la proteina de muerte celular programada 1 (PD-1) para usar en un metodo […]
Tratamiento del cáncer usando inhibidores de TGF-beta y PD-1, del 24 de Junio de 2020, de XOMA TECHNOLOGY LTD.: Un inhibidor del factor de crecimiento transformante beta (TGFβ) y un inhibidor de la proteina de muerte celular programada 1 (PD-1) para usar en un metodo […]
Métodos para el tratamiento de la enfermedad ocular en sujetos humanos, del 10 de Junio de 2020, de Clearside Biomedical, Inc: Una formulación farmacéutica que comprende un fármaco para su uso en un método de tratamiento de un trastorno ocular posterior en un sujeto humano que […]
Método para tratar la pérdida de hueso alveolar mediante el uso de anticuerpos antiesclerostina, del 3 de Junio de 2020, de AMGEN INC.: Un anticuerpo antiesclerostina para su uso en un método para aumentar la altura del hueso alveolar en un sujeto que padece pérdida de hueso alveolar, donde […]
Proteínas de captura de la superficie celular recombinantes, del 13 de Mayo de 2020, de REGENERON PHARMACEUTICALS, INC.: Un método para detectar y aislar células que producen altos niveles de una proteína heterodimérica que tiene una primera subunidad y una segunda subunidad, […]