Procedimientos para el cribado de fármacos utilizando formación de imágenes in vivo no invasivas.
Procedimiento para el desarrollo de fármacos, que comprende:
(a) injertar células diana dentro de la cámara anterior ocular de un animal de prueba,
seleccionado de entre elgrupo constituido por ratón, mono, perro, gato y cerdo, en el que uno o más componentes celulares de interésterapéutico en las células diana trasplantadas son marcados de manera fluorescente;
(b) poner en contacto las células diana con uno o más compuestos de prueba; y
(c) llevar a cabo la formación de imágenes fluorescentes no invasiva en el ojo del animal de prueba, en el que laformación de imágenes fluorescentes es utilizada para detectar cambios inducidos en el compuesto deprueba en una o varias actividades, localización, y cantidad de componentes celulares marcadosfluorescentemente de interés terapéutico en las células diana injertadas, identificando los cambios aquelloscompuestos de prueba que pueden proporcionar un beneficio terapéutico a las células diana.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2008/007130.
Solicitante: BIOCRINE AB.
Nacionalidad solicitante: Suecia.
Dirección: JOHN ERIKSSONSGATAN 9 112 22 STOCKHOLM SUECIA.
Inventor/es: BERGGREN,Per Olof, CAICEDO,ALEJANDRO.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A01K67/027 NECESIDADES CORRIENTES DE LA VIDA. › A01 AGRICULTURA; SILVICULTURA; CRIA; CAZA; CAPTURA; PESCA. › A01K CRÍA DE ANIMALES; AVICULTURA; APICULTURA; PISCICULTURA; PESCA; ANIMALES PARA CRIA O REPRODUCCIÓN, NO PREVISTOS EN OTRO LUGAR; NUEVAS VARIEDADES DE ANIMALES. › A01K 67/00 Cría u obtención de animales, no prevista en otro lugar; Nuevas razas de animales. › Nuevas razas de vertebrados.
- A61K35/39 A […] › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 35/00 Preparaciones medicinales que contienen sustancias de constitución indeterminada o sus productos de reacción. › Páncreas; Islotes of Langerhans (Células de Langerhans de la epidermis A61K 35/36).
- A61K49/00 A61K […] › Preparaciones para examen in vivo.
- A61P3/10 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › A61P 3/00 Medicamentos para el tratamiento de trastornos del metabolismo (de la sangre o de fluido extracelular A61P 7/00). › para la hiperglucemia, p.ej. antidiabéticos.
- C12N5/06
- G01N33/50 FISICA. › G01 METROLOGIA; ENSAYOS. › G01N INVESTIGACION O ANALISIS DE MATERIALES POR DETERMINACION DE SUS PROPIEDADES QUIMICAS O FISICAS (procedimientos de medida, de investigación o de análisis diferentes de los ensayos inmunológicos, en los que intervienen enzimas o microorganismos C12M, C12Q). › G01N 33/00 Investigación o análisis de materiales por métodos específicos no cubiertos por los grupos G01N 1/00 - G01N 31/00. › Análisis químico de material biológico, p. ej. de sangre o de orina; Ensayos mediante métodos en los que interviene la formación de uniones bioespecíficas con grupos coordinadores; Ensayos inmunológicos (procedimientos de medida o ensayos diferentes de los procedimientos inmunológicos en los que intervienen enzimas o microorganismos, composiciones o papeles reactivos a este efecto, procedimientos para preparar estas composiciones, procedimientos de control sensibles a las condiciones del medio en los procedimientos microbiológicos o enzimáticos C12Q).
PDF original: ES-2447069_T3.pdf
Fragmento de la descripción:
Procedimientos para el cribado de fármacos utilizando formación de imágenes in vivo no invasivas.
Antecedentes de la invención El conocimiento fundamental de los procesos celulares en la salud y la enfermedad se ha obtenido estudiando las células de varios tejidos in vitro. Sin embargo, los resultados obtenidos a partir de los experimentos in vitro no son suficientes, a menudo, para explicar el funcionamiento de las células en más configuraciones fisiológicas como los órganos enteros o los organismos vivientes. Para situar las observaciones llevadas a cabo en un sistema in vitro, en un contacto fisiológico los estudios tienen que llevarse a cabo bajo condiciones in vivo. Recientemente, se han realizado un número creciente de aproximaciones para investigar la función celular in situ, empleando técnicas de imagen. Desafortunadamente, a las técnicas no invasivas de imagen, como la tomografía computacional (CT) , la imagen mediante resonancia magnética (MRI) , la tomografía de emisión de positrones (PET) o la imagen bioluminiscente (BLI) , les falta resolución celular. Por otra parte, la microscopía confocal y la de cribado láser bifotónico mediante láser (LSM) , proporcionan una resolución subcelular pero muestran una distancia de actuación y una profundidad de imagen bastante limitada. El acceso de las células diana para la aplicación de LSM es más invasivo y a menudo excluye la posibilidad de exámenes repetidos.
ARBUZOVA M.I. et al.; PROBLEMY ENDOKRINOLOGII 1991 JAN-FEB, vol. 37, no 1. Enero 1991, p. 42-44 da a conocer el trasplante del páncreas embriónico a la cámara anterior del ojo.
BRAGIN A.G. et al., SU 1.369.039 A (AS BIOL PHYSICS INS) 7 septiembre 1988, da a conocer la compensación de la diabetes mellitus trasplantando la parte de la cola del páncreas embriónico al ojo de una rata de ensayo.
KULIKOV A V et al., MEMBRANE CELL BIOLOGY, vol. 11, no 6, 1998, páginas 737-742, da a conocer el trasplante de varios tejidos biológicos a la cámara anterior del ojo.
TRUBETSKAIA O.E. et al., IZVESTIIA AKADEMII NAUK. SERIIA BIOLOGICHESKAIA/ROSSI SKAIA AKADEMIIA NAUK 1994 JAN-FEB. no 1 Enero 1994, páginas 152-155, da a conocer el trasplante del páncreas embriónico a la cámara anterior ocular.
La patente US no 5.650.435 describe procedimientos y composiciones para detectar y localizar la luz que se origina a partir de un mamífero. Se describen los modelos animales para los estados patológicos y los procedimientos para el cribado de compuestos terapéuticos putativos efectivos para inhibir la enfermedad o el patógeno.
DE 197 03 734 A1 da a conocer un aparato utilizado para el examen no invasivo de células en un ojo viviente, las cuales células pueden trasplantarse.
Sumario de la invención La presente invención proporciona procedimientos para el desarrollo de fármacos, que comprenden;
(a) injertar células diana en el ojo de un animal de prueba, en el que uno o varios componentes celulares de interés terapéutico en las células diana trasplantadas, están marcadas de forma fluorescente;
(b) poner en contacto las células diana con uno o más compuestos de prueba; y
(c) llevar a cabo la formación de imágenes, fluorescente y no invasiva en el ojo del animal de prueba,
en el que la imagen fluorescente se utiliza para detectar cambios inducidos en el compuesto de prueba, en una o más actividades, localizaciones y cantidades de los componentes celulares marcados de forma fluorescente, de interés terapéutico en las células diana injertadas, donde los cambios identifican a los compuestos de prueba que pueden proporcionar un beneficio terapéutico a las células diana.
Breve descripción de las figuras
Figura 1: Islotes pancreáticos trasplantados a la cámara anterior ocular.
(a) Trasplantar islotes a la cámara anterior ocular. (b) Establecer la formación de imágenes no invasivas in vivo.
(c) Fotografía digital de los islotes injertados en el iris en la cámara ocular anterior (d-g) . Cortes oculares que contienen injertos de islotes que muestran células º inmunorreactivas a la insulina (en rojo) y células º glucagoinmunorreactivas (en verde) en puntos temporales distintos después del trasplante.
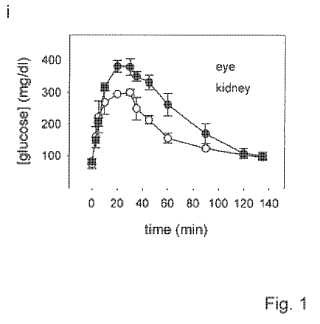
(h) Proporción de insulina a las células inmunorreactivas al glucagón en los islotes pancreáticos y en la cámara anterior ocular, en los tiempos indicados después del trasplante. (i) Niveles plasmáticos de glucosa durante
un ensayo intraperitoneal de tolerancia a la glucosa en ratones tratados con estreptozotocina trasplantados con islotes en los ojos (n = 8, negro) y por debajo de la cápsula renal (n = 2, rojo) .
Figura 2: Imagen no invasiva del injerto de los islotes y vascularización.
Imágenes de un injerto individual de islotes RIP-GFP 4 meses después del trasplante de un corte óptico capturado a una profundidad de 51 !m. (a) Fluorescencia de células GFP (verde) , (b) fluorescencia Rojo Texas, inyectada intravenosamente (rojo) y (c-d) proyección 2D de un montón de imágenes correspondientes a un grosor de 100 !m. Proyecciones (e-p) de las imágenes (grosor de 110 !m) de un injerto individual de los islotes RIP-GFP en los días 3, 7, 14 y 28 después del trasplante. La fluorescencia GFP de las células (e, h, k, n) y la fluorescencia Rojo Texas en los vasos sanguíneos (f, i, l, o) se muestran separadamente y como una capa (g, j, m, p) . Barras escalares, 100 !m. (q-r) Cuantificación de los resultados mostrados en (e-p) . El número de injertos de los islotes analizados se indica entre paréntesis en los tiempos respectivos.
Figura 3: Imágenes in vivo de la función de las células (a-e) . Imágenes de la fluorescencia de Fluo-4 y Fura-Red en los tiempos indicados después de la aplicación sistémica de glibenclamida (1 mg/kg) a los 3 minutos. (f) Cambio proporcional del marco total Fluo 4/Fura-Red en respuesta a un estímulo dado de glibenclamida, indicándose el principio de la estimulación por la flecha (g) . Cambio proporcional en las células individuales a través del islote, tal como se indica en el cuadro (a) . (h-i) proyecciones máximas de las fluorescencias Fluo-4 (verde) y Fura-Red (rojo) de un islote entero, antes (h) y después de la estimulación con glibenclamida (I) . (j-k) Exhibición proporciométrica de Fluo-4/Fura-Red del islote en el cuadro (h) e (i) . Barras escalares, 50 !m.
Figura 4: Imágenes no invasivas in vivo de la muerte de las células . (a-h) Proyecciones de las imágenes de un islote individual RIP-GFP en la cámara anterior ocular. Bajo condiciones normales, (a) fluorescencia de células GFP, (b) reflejo de las células endocrinas y (c) Marcado de la anexina V-APC indetectable del injerto. (d) Imagen en capa de (a-c) con la imagen de reflejo en azul. Veinticuatro horas después de la inducción de la muerte de las células , (e) Fluorescencia de las células (f) , reflejo y (G) fluorescencia intensa de la anexina V-APC del injerto de los islotes. (h) Imagen en capa de (e-g) con la imagen del reflejo en azul. (i-j) Imágenes de alta amplificación de un área de injerto de los islotes marcada intensamente con la anexina V-APC después de la inducción de la muerte de las células (i) fluorescencia de las células GFP, (j) fluorescencia de la anexina V-APC y (k) capa de (i-j) , (I) capa de (k) con la imagen de reflejo (azul) . Barras de escalares, 100 !m.
Figura 5: Imagen no invasiva del injerto de los islotes y vascularización. Se muestran proyecciones (a-f) de la imagen (110 !m de grosor) del mismo injerto de los islotes RIP-GFP, tal como se exponen en la figura 2, se muestran a los 2 y 4 meses después del trasplante. La fluorescencia GFP de las células (a, d) y la fluorescencia Rojo Texas en los vasos sanguíneos (b, e) se muestran separadamente y como una capa (c, f) . Barras escalares de, 100 !m.
Descripción detallada de la invención En un aspecto, la presente invención proporciona procedimientos para el desarrollo de fármacos, que comprenden:
(a) injertar células diana en el ojo de un animal de prueba, donde uno o varios compuestos celulares de interés terapéutico en las células diana trasplantadas, están marcadas fluorescentemente;
(b) poner en contacto de las células diana con uno o más compuestos de prueba, y
(c) llevar a cabo la formación de imágenes fluorescentes no invasiva en el ojo del animal de prueba,
en el que la imagen fluorescente se utiliza para detectar cambios inducidos en el compuesto de prueba en una o varias actividades, localización y cantidad de los componentes celulares marcados fluorescentemente de interés terapéutico en las células diana injertadas, donde los cambios identifican aquellos compuestos de prueba que pueden... [Seguir leyendo]
Reivindicaciones:
1. Procedimiento para el desarrollo de fármacos, que comprende:
(a) injertar células diana dentro de la cámara anterior ocular de un animal de prueba, seleccionado de entre el grupo constituido por ratón, mono, perro, gato y cerdo, en el que uno o más componentes celulares de interés terapéutico en las células diana trasplantadas son marcados de manera fluorescente;
(b) poner en contacto las células diana con uno o más compuestos de prueba; y 10
(c) llevar a cabo la formación de imágenes fluorescentes no invasiva en el ojo del animal de prueba, en el que la formación de imágenes fluorescentes es utilizada para detectar cambios inducidos en el compuesto de prueba en una o varias actividades, localización, y cantidad de componentes celulares marcados fluorescentemente de interés terapéutico en las células diana injertadas, identificando los cambios aquellos compuestos de prueba que pueden proporcionar un beneficio terapéutico a las células diana.
2. Procedimiento según la reivindicación 1, en el que las células diana son derivadas de un tejido seleccionado de entre el grupo constituido por células endocrinas, grasas, músculos, cerebro, hígado, corazón, riñón y pulmones.
3. Procedimiento según cualquiera de las reivindicaciones 1 a 2, en el que uno o más compuestos de prueba son aplicados por vía tópica en el ojo del animal de prueba.
4. Procedimiento según cualquiera de las reivindicaciones 1 a 2, en el que uno o más de los compuestos de prueba son inyectados dentro de la cámara anterior ocular del animal de prueba. 25
5. Procedimiento según cualquiera de las reivindicaciones 1 a 4, en el que la formación de imágenes fluorescentes comprende microscopía de cribado por láser.
6. Procedimiento según cualquiera de las reivindicaciones 1 a 5, en el que la formación de imágenes fluorescentes
es utilizada para detectar los cambios inducidos por el compuesto de prueba en uno o varios de entre la actividad, la localización y la cantidad de los componentes celulares marcados de forma fluorescente de interés terapéutico en las células diana injertadas en múltiples puntos temporales distintos.
7. Procedimiento según cualquiera de las reivindicaciones 1 a 6, en el que las células diana comprenden células 35 beta pancreáticas.
8. Procedimiento según cualquiera de las reivindicaciones 1 a 7, en el que las células diana son células individuales.
Patentes similares o relacionadas:
Cultivo de tejido tridimensional heterogéneamente diferenciado, del 22 de Julio de 2020, de IMBA-INSTITUT FÜR MOLEKULARE BIOTECHNOLOGIE GMBH: Un cultivo de tejido neuronal tridimensional artificial cultivado in vitro que comprende una población heterogénea de células humanas o células de primate no humanas […]
Gangliósidos para estandarizar y aumentar la sensibilidad de las células a las neurotoxinas botulínicas en los sistemas de prueba in vitro, del 15 de Julio de 2020, de MERZ PHARMA GMBH & CO. KGAA: Un método para determinar la actividad biológica de un polipéptido de neurotoxina, que comprende las etapas de: a) cultivar neuronas de diferentes […]
Procedimiento para evaluación de la función hepática y el flujo sanguíneo portal, del 15 de Julio de 2020, de The Regents of the University of Colorado, a body corporate: Procedimiento in vitro para la estimación del flujo sanguíneo portal en un individuo a partir de una única muestra de sangre o suero, comprendiendo el procedimiento: […]
ANTICUERPO MONOCLONAL O UNA PORCIÓN DE UNIÓN A ANTÍGENO DEL MISMO QUE SE UNE A LA PROTEÍNA L DEL VIRUS PARAINFLUENZA HUMANO (PIV); MÉTODO Y KIT PARA DETECTAR AL VIRUS PIV, del 2 de Julio de 2020, de PONTIFICIA UNIVERSIDAD CATÓLICA DE CHILE: La invención presenta la generación de anticuerpos monoclonales, o fragmentos de los mismos, que reconocen la proteína L del virus parainfluenza humano (PIV), donde dichos […]
ANTICUERPOS MONOCLONALES ESPECÍFICOS PARA EL ANTÍGENO PB2 DEL VIRUS DE LA INFLUENZA HUMANA (FLU), SECUENCIAS NUCLEOTÍDICAS; MÉTODO Y KIT DE DIAGNÓSTICO DE INFECCIÓN PRODUCIDA POR FLU, del 2 de Julio de 2020, de PONTIFICIA UNIVERSIDAD CATÓLICA DE CHILE: La invención presenta la generación de anticuerpos monoclonales, o fragmentos de los mismos, que reconocen la proteína PB2 del virus de la influenza humana (Flu), […]
Nueva inmunoterapia contra diversos tumores como el cáncer gastrointestinal y gástrico, del 24 de Junio de 2020, de IMMATICS BIOTECHNOLOGIES GMBH: Péptido seleccionado del grupo siguiente: a) péptido consistente en la secuencia conforme a la SEQ ID N.º 86, b) el péptido conforme a a), en la […]
Reactivos SIRP-alfa de alta afinidad, del 24 de Junio de 2020, de THE BOARD OF TRUSTEES OF THE LELAND STANFORD JUNIOR UNIVERSITY: Un polipéptido SIRPα de alta afinidad que comprende al menos una y no más de 15 modificaciones de aminoácidos dentro del dominio d1 de una secuencia SIRPα de tipo […]
Diagnóstico y terapia de cáncer que implica células madre cancerosas, del 24 de Junio de 2020, de BioNTech SE: Un anticuerpo que tiene la capacidad de unirse a Claudina 6 (CLDN6) para usar en un método de tratamiento o prevención del cáncer que comprende inhibir y/o eliminar […]