PROCEDIMIENTO PARA LA SÍNTESIS DE 5-(METIL-1H-IMIDAZOL-1-IL)-3-(TRIFLUOROMETIL)-BENCENAMINA.
Un procedimiento para preparar 5-(4-metil-1H-imidazol-1-il)-3-(trifluorometil)-bencenamina (I),
que comprende las etapas de: a) hacer reaccionar, en una reacción de acoplamiento, el compuesto con 4-metil-1H-imidazol (IIIa) para preparar 4-metil-1-(3-nitro-5-trifluorometilfenil)-1H-imidazol (III); y b) reducir el 4-metil-1-(3-nitro-5-trifluorometil-fenil)-1H-imidazol resultante para producir el compuesto de fórmula (I)
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2006/022026.
Solicitante: NOVARTIS AG.
Nacionalidad solicitante: Suiza.
Dirección: LICHTSTRASSE 35 4056 BASEL SUIZA.
Inventor/es: ACEMOGLU, MURAT, WIDMER, ERICH, GARCIA FUENTES,PEDRO, XUE,SONG, SCHENKEL,BERTHOLD, MARTIN MEDINA,JOSE, VICENTE BAUOS,FRANCISCO, SHIEH,WEN-CHUNG.
Fecha de Publicación: .
Fecha Solicitud PCT: 7 de Junio de 2006.
Fecha Concesión Europea: 6 de Octubre de 2010.
Clasificación Internacional de Patentes:
- C07D233/56 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07D COMPUESTOS HETEROCICLICOS (Compuestos macromoleculares C08). › C07D 233/00 Compuestos heterocíclicos que contienen ciclos de diazol-1,3 o diazol-1,3 hidrogenado, no condensados con otros ciclos. › con solamente átomos de hidrógeno o radicales que contienen solamente átomos de carbono o hidrógeno unidos a los átomos de carbono del ciclo.
- C07D233/64 C07D 233/00 […] › con radicales hidrocarbonados sustituidos, unidos a los átomos de carbono del ciclo, p. ej. histidina.
- C07D401/14 C07D […] › C07D 401/00 Compuestos heterocíclicos que contienen dos o más heterociclos, que tienen átomos de nitrógeno como únicos heteroátomos del ciclo, siendo al menos un ciclo de seis miembros con solamente un átomo de nitrógeno. › que contienen tres o más heterociclos.
Clasificación PCT:
- C07D233/54 C07D 233/00 […] › que tienen dos enlaces dobles entre miembros cíclicos o entre miembros cíclicos y miembros no cíclicos.
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Eslovenia, Finlandia, Rumania, Chipre, Lituania, Letonia.
Fragmento de la descripción:
Procedimiento para la síntesis de 5-(metil-1H-imidazol-1-il)-3-(trifluorometil)-bencenamina.
Antecedentes de la invención
La presente invención proporciona un modo eficaz, seguro y económico para preparar 5-(4-metil-1H-imidazol-1-il)-3-(trifluorometil)-bencenamina de la siguiente fórmula (I):
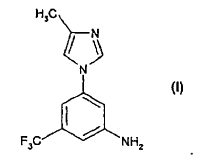
El compuesto de fórmula (I) es un producto intermedio para la preparación de pirimidinilaminobenzamidas sustituidas de fórmula (II):
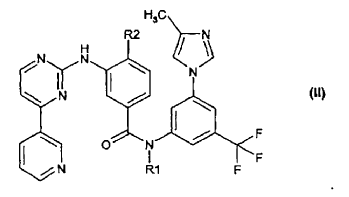
Compuestos de fórmula (II) se han divulgado en W. Breitenstein et al., WO 04/005281 A1, cuya divulgación se incorpora en la presente memoria mediante referencia. Se ha observado que estos compuestos inhiben una o más tirosina quinasas, tales como c-Abl, Bcr-Abl, tirosina quinasas receptoras PDGF-R, Flt3, VEGF-R, EGF-R y c-Kit. Como tales, los compuestos de fórmula (II) pueden usarse para el tratamiento de ciertas enfermedades neoplásticas, tales como leucemia.
La síntesis previa del compuesto (I) implica una ruta sintética de 4 etapas partiendo de una reacción de sustitución aromática del compuesto (IIIa), 4-metil-1H-imidazol, con el compuesto (IV), que requiere emplear alta energía (150ºC) (Esquema 1).
Esquema 1
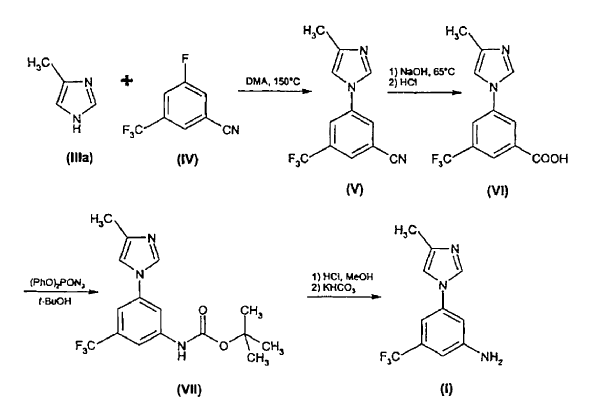
Por otra parte, la transformación del compuesto (VI) en el compuesto (VII) a través de transposición de Curtius utiliza un reactivo seguro, difenilfosforilazida. Esta reacción produce rendimientos y calidad de producto inconsistentes. Además, es difícil retirar el subproducto de ácido difenilfosfórico resultante. El producto de carbamato (VII) necesita purificarse mediante cromatografía, lo que es costoso y requiere mucho tiempo para las operaciones comerciales.
Un objetivo de esta invención es proporcionar procedimientos alternativos para elaborar el compuesto de fórmula (I) eficazmente y con altos rendimientos.
Un objetivo adicional de esta invención es elaborar el compuesto (I) a partir de materiales de partida y reactivos de coste inferior.
Un objetivo adicional más de esta invención es proporcionar un procedimiento para elaborar el compuesto de fórmula (I) usando reactivos más seguros.
La presente invención vence los problemas de la reacción mostrada en el Esquema 1 anteriormente.
Sumario de la invención
La presente invención proporciona nuevos procedimientos sintéticos para la fabricación de 5-(4-metil-1H-imidazol-1-il)-3-(trifluorometil)-bencenamina que tiene la fórmula (I):
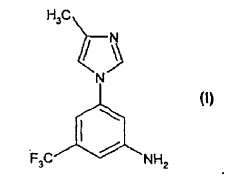
El compuesto de fórmula (I) es un producto intermedio para la preparación de pirimidinilaminobenzamidas de fórmula (II) que se han divulgado en W. Breitenstein et al, WO 04/005281, que se publicó el 15 de enero de 2004, cuya divulgación se incorpora mediante referencia. Un compuesto preferido de fórmula (II) es la 4-metil-3-[[4-(3-piridinil)-2-pirimidinil]amino]-N-[5-(4-metil-1H-imidazol-1-il)-3-(trifluorometil)fenil]benzamida.
Descripción detallada de la invención
El esquema de reacciones general de la invención puede ilustrarse en las siguientes realizaciones:
En una primera realización, la presente invención proporciona el procedimiento general para elaborar el compuesto (I) como sigue:
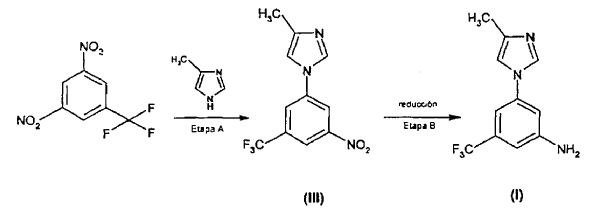
La Etapa A implica una base y una sustitución aromática nucleófila para la síntesis de 4-metil-1-(3-nitro-5-trifluorometil-fenil)-1H-imidazol (III). La etapa B es una reducción que conduce al compuesto (I).
La base puede seleccionarse de un alcóxido, un hidruro, un carbonato o un fosfato. Preferiblemente, la base es alcóxido potásico, alcóxido sódico, hidruro sódico, carbonato potásico o fosfato potásico. El disolvente usado en la Etapa A se selecciona de N,N-dimetilformamida (DMF), N,N-dimetilacetamida (DMA) o 1-metil-2-pirrolidinona (NMP) o mezclas de las mismas.
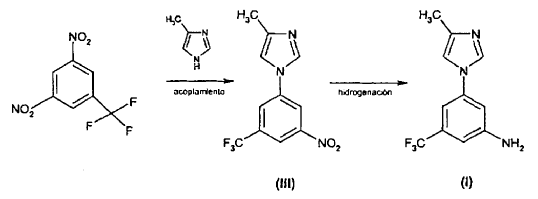
Una segunda realización implica el acoplamiento de dinitrobenzotrifluoruro y 4-metil-1H-imidazol seguido por una reacción de hidrogenación.
Además, una tercera realización implica una etapa adicional para cada uno de los procedimientos descritos anteriormente que implica opcionalmente la transformación del compuesto (III) en una sal de la fórmula (IV), por razones de purificación, según se ilustra mediante el siguiente esquema:
Esquema 7
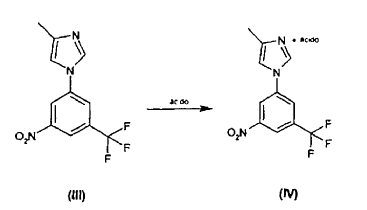
Aquí, una solución del compuesto (III) se trata con un ácido o una solución del mismo en agua o un disolvente orgánico, seguido por el aislamiento de la sal (IV), o. ej. mediante filtración.
El compuesto (III) puede obtenerse tratando la sal (IV) con una base, preferiblemente con solución acuosa de hidróxido sódico, y aislando la base libre (III) mediante extracción o cristalización.
La reacción de acoplamiento funciona en diversos disolventes apróticos polares comunes, incluyendo dimetilsulfóxido (DMSO), DMF, diglime, THF, NMP y DMA.
Se ha encontrado, de acuerdo con la presente invención, que la reacción de acoplamiento de metilimidazol y dinitrobenzotrifluoruro funciona mejor en DMA como disolvente, a una temperatura en el intervalo de 80-150ºC, preferiblemente 90-140ºC. Cuando están presentes K2CO3 u otras bases, la descomposición se produce bastante rápidamente. Puesto que la mezcla de reacción no es estable, la temperatura y el tiempo de reacción deben reducirse tanto como sea posible. Un ciclo de calentamiento y enfriamiento más rápido o intervalos de tiempo de reacción más cortos, p. ej. usando microondas o mediante una capacidad adicional del cambiador de calor en recipientes discontinuos o usando un equipo de reacción continuo, conducirán a menos descomposición y una reacción más limpia.
El K3PO4 tiene un comportamiento similar en comparación con el K2CO3, pero la reacción es más rápida en el segundo caso. Puede obtenerse un rendimiento bruto de >40% de acuerdo con el procedimiento descrito en la presente memoria.
La reducción del producto intermedio de nitroimidazol, compuesto (III), puede realizarse usando hidrógeno gaseoso o agentes de transferencia de hidrógeno tales como ácido fórmico o formiato amónico, en presencia de catalizadores de metal de transición del Grupo VIII soportados comunes, tales como paladio, platino, níquel o cualquier combinación. El metal se incorpora en el soporte en una cantidad de 0,1-20 por ciento en peso, basado en el peso total del metal y el soporte. También puede usarse una combinación de catalizadores. Está dentro del alcance de la presente invención que el catalizador también pueda incluir un promotor o un copromotor. El procedimiento de reducción preferido, la hidrogenación, usa hidrógeno gaseoso y catalizador de paladio. La hidrogenación se realiza habitualmente a una presión de hidrógeno que varía de 1-20 bar, preferiblemente 5-10 bar. El producto en bruto también puede aislarse como la sal de hidrocloruro. La purificación final se alcanza mediante la cristalización de la base libre, compuesto (I).
Los siguientes ejemplos ilustran más particularmente la presente invención, pero no limitan la invención de ningún modo.
Ejemplo 1
En un recipiente de 200 l, se colocan 9 kg de dinitrobenzotrifluoruro, 5,3 kg de carbonato potásico y 84,6 kg de DMA. Después de 10 minutos, agitando para una buena mezcla (color rojo oscuro), se cargan 3,8 kg de 4-metil-1H-imidazol, y la mezcla se calienta bajo agitación hasta 95ºC durante 15-20 horas hasta que el análisis no muestra material de partida. La mezcla roja-marrón oscura se enfría hasta 30ºC, se vierte sobre agua bajo buena agitación, se filtra...
Reivindicaciones:
1. Un procedimiento para preparar 5-(4-metil-1H-imidazol-1-il)-3-(trifluorometil)-bencenamina (I), que comprende las etapas de:
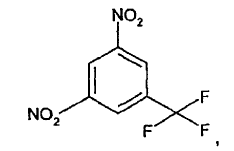
2. El procedimiento de acuerdo con la reivindicación 1, en el que la Etapa a) se realiza a una temperatura en el intervalo de 80-150ºC.
3. El procedimiento de acuerdo con la reivindicación 1, en el que la Etapa a) se realiza a una temperatura en el intervalo de 90-140ºC.
4. El procedimiento de acuerdo con la reivindicación 1, en el que la reacción de reducción, Etapa b), implica catalizadores de metales del Grupo VIII, hidrógeno gaseoso o agentes de transferencia de hidrógeno.
5. El procedimiento de acuerdo con la reivindicación 4, en el que el catalizador es paladio, platino o níquel Raney o combinaciones de los mismos.
6. Un procedimiento para preparar 5-(4-metil-1H-imidazol-1-il)-3-(trifluorometil)-bencenamina (I), que comprende las etapas de:
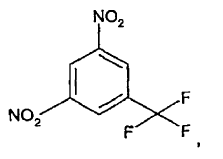
7. Un procedimiento de acuerdo con la reivindicación 6, en el que la base es un alcóxido, un hidruro, un carbonato o un fosfato.
8. El procedimiento de acuerdo con la reivindicación 1 ó 6, en el que la Etapa a) utiliza un disolvente aprótico polar seleccionado de dimetilsulfóxido (DMSO), dimetilformamida (DMF), diglime, THF, N-metilpirrolidona (NMP) y dimetilacetamida (DMA).
9. Un procedimiento de acuerdo con la reivindicación 1, en el que se usan microondas.
10. Un procedimiento de acuerdo con la reivindicación 1, en el que se alcanza un ciclo de calentamiento y enfriamiento más rápido mediante una capacidad adicional del cambiador de calor en recipientes discontinuos o usando un equipo de reacción continuo para obtener una selectividad superior.
Patentes similares o relacionadas:
Compuestos heterocíclicos que activan AMPK y métodos de uso de los mismos, del 29 de Julio de 2020, de RIGEL PHARMACEUTICALS, INC.: Un compuesto que es N-((cis)-1-(4-cianobencil)-3-fluoropiperidin-4-il)-6-(4-(4-metoxibenzoil)piperidin-1-carbonil)nicotinamida; N-((3S,4S)-1-(4-cianobencil)-3-fluoropiperidin-4-il)-6-(4-(4-metoxibenzoil)piperidin-1-carbonil)nicotinamida; […]
Derivados de piperidina 1,4 sustituidos, del 29 de Julio de 2020, de 89Bio Ltd: Un compuesto de acuerdo con la Fórmula I: **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en donde: A se selecciona de […]
Compuestos y procedimientos de uso, del 29 de Julio de 2020, de Medivation Technologies LLC: Un compuesto de fórmula (Aa-1): **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en la que: A representa H, halógeno, amino, […]
Ureas cíclicas como inhibidores de ROCK, del 22 de Julio de 2020, de BRISTOL-MYERS SQUIBB COMPANY: Un compuesto de acuerdo con la Fórmula (I): **(Ver fórmula)** o un enantiómero, un diastereómero, un estereoisómero, un tautómero, una sal farmacéuticamente aceptable […]
Ureas asimétricas p-sustituidas y usos médicos de las mismas, del 22 de Julio de 2020, de Helsinn Healthcare SA: Un compuesto de Fórmula I: **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en donde: una línea discontinua indica un enlace opcional; X es CH; […]
Formas en estado sólido de sales de Nilotinib, del 15 de Julio de 2020, de PLIVA HRVATSKA D.O.O: Una forma cristalina de fumarato de Nilotinib designada como Forma III, caracterizada por datos seleccionados de uno o más de los siguientes: a. un patrón de […]
Inhibidores de Bcl-2/Bcl-xL y su uso en el tratamiento de cáncer, del 15 de Julio de 2020, de THE REGENTS OF THE UNIVERSITY OF MICHIGAN: Compuesto que tiene una estructura **(Ver fórmula)**
Derivado de dihidropiridazin-3,5-diona, del 15 de Julio de 2020, de CHUGAI SEIYAKU KABUSHIKI KAISHA: Un compuesto representado por la fórmula (I) o una sal del mismo, o un solvato del compuesto o la sal: **(Ver fórmula)** en donde R1, R4 y R5 se definen […]