PROCEDIMIENTO PARA LA PREPARACIÓN DE CLORO POR MEDIO DE OXIDACIÓN EN FASE GASEOSA.
Procedimiento para la preparación de cloro por medio de la oxidación catalítica en fase gaseosa de cloruro de hidrógeno con oxígeno,
que comprende al menos: la reacción de cloruro de hidrógeno con oxígeno en al menos dos lechos catalíticos conectados en serie en condiciones adiabáticas
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2007/004368.
Solicitante: BAYER MATERIALSCIENCE AG.
Nacionalidad solicitante: Alemania.
Dirección: 51368 LEVERKUSEN ALEMANIA.
Inventor/es: WOLF, AUREL, SCHUBERT, STEPHAN, MLECZKO,Leslaw, SCHLÜTER,Oliver Felix-Karl.
Fecha de Publicación: .
Fecha Solicitud PCT: 16 de Mayo de 2007.
Clasificación PCT:
- B01J23/46 TECNICAS INDUSTRIALES DIVERSAS; TRANSPORTES. › B01 PROCEDIMIENTOS O APARATOS FISICOS O QUIMICOS EN GENERAL. › B01J PROCEDIMIENTOS QUÍMICOS O FÍSICOS, p. ej. CATÁLISIS O QUÍMICA DE LOS COLOIDES; APARATOS ADECUADOS. › B01J 23/00 Catalizadores que contienen metales, óxidos o hidróxidos metálicos no previstos en el grupo B01J 21/00 (B01J 21/16 tiene prioridad). › Rutenio, rodio, osmio o iridio.
- C01B7/04 QUIMICA; METALURGIA. › C01 QUIMICA INORGANICA. › C01B ELEMENTOS NO METALICOS; SUS COMPUESTOS (procesos de fermentación o procesos que utilizan enzimas para la preparación de elementos o de compuestos inorgánicos excepto anhídrido carbónico C12P 3/00; producción de elementos no metálicos o de compuestos inorgánicos por electrólisis o electroforesis C25B). › C01B 7/00 Halógenos; Acidos de los halógenos. › Preparación del cloro a partir del ácido clorhídrico.
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Eslovenia, Finlandia, Rumania, Chipre, Lituania, Letonia, Ex República Yugoslava de Macedonia, Albania.
PDF original: ES-2361885_T3.pdf
Fragmento de la descripción:
La presente invención se refiere a un procedimiento para preparar cloro mediante la oxidación catalítica en fase gaseosa de cloruro de hidrógeno con oxígeno, en el que la reacción se lleva a cabo en al menos dos lechos catalíticos en condiciones adiabáticas.
El procedimiento, desarrollado por Deacon en 1868, de la oxidación catalítica de cloruro de hidrógeno con oxígeno en una reacción de equilibrio exotérmica se encuentra al comienzo de la química técnica del cloro:
4 HCl + O2 → 2 Cl2 + 2 H2O.
No obstante, debido a la electrolisis alcalina de cloro se relegó profundamente a un segundo plano el uso del procedimiento de Deacon. Casi la totalidad de la producción de cloro se realizó mediante electrolisis de disoluciones acuosas de sal común. No obstante el atractivo del procedimiento de Deacon aumenta de nuevo en tiempos recientes, ya que las necesidades mundiales de cloro crecen más intensamente que la demanda de lejía de hidróxido de sodio, un producto asociado de la electrolisis de NaCl. El procedimiento de preparación de cloro mediante oxidación de cloruro de hidrógeno se adapta a este desarrollo, que no está asociado a la producción de lejía de hidróxido de sodio. Además el subproducto cloruro de hidrógeno se puede obtener fácilmente, se produce en grandes cantidades, por ejemplo en reacciones de fosgenación, por ejemplo en la preparación de isocianato, como producto asociado.
La evacuación y el uso del calor de reacción es un punto importante en la realización del procedimiento de Deacon. Un aumento incontrolado de la temperatura, que del principio al final de la reacción de Deacon podría ser de 600 a 900 ºC, podría causar por una parte un daño permanente en el catalizador y, por otra parte, a altas temperaturas, un desplazamiento del equilibrio de reacción en dirección a los productos de partida con la correspondiente disminución del rendimiento. Por lo tanto, es ventajoso mantener la temperatura de la carga de catalizador del procedimiento en un intervalo de 150 a 600 ºC.
Por lo tanto, en procedimientos establecidos el catalizador se usa en forma de un lecho fluidizado termoestabilizado. Según el documento EP 0 251 731 A2 se regula la temperatura del lecho de catalizador, a este respecto, mediante la pared exterior; según el documento DE 10 2004 006 610 A1 se regula la temperatura del lecho fluidizado por medio de un intercambiador de calor emplazado en el lecho. La evacuación eficaz de calor de este procedimiento genera problemas debido a una distribución irregular del tiempo de residencia y a la abrasión del catalizador, lo que provoca pérdidas de ganancia.
Un distribución estrecha del tiempo de residencia y una abrasión del catalizador reducida son posibles en reacciones con cargas estacionarias de catalizadores. No obstante, en algunas reacciones surgen problemas con la termostatización de los lechos catalíticos. En general, por lo tanto, se usan reactores de haz de tubos que, en particular en el caso de reactores grandes, poseen un circuito de refrigeración muy costoso (WO 2004/052776 A1).
Para mejorar el transporte del calor desde la carga catalítica, se recomienda en R&D-Report, "Sumitomo Kagaku", vol. 2004-I, el uso de un catalizador de lecho fijo de óxido de rutenio sobre óxido de titanio como soporte. Además de la elevada actividad catalítica, se menciona la buena conductividad térmica del sistema catalítico como una ventaja. Dado que también en el caso de conductividades térmicas altas dentro de las pellas de catalizador, la conductividad de la carga permanece reducida, no se mejora sustancialmente la evacuación de calor con esta medida.
En el documento EP 1 170 250 A1 se recomienda usar cargas catalíticas en reactores de haz de tubos que presentan en diferentes regiones de los tubos de contacto enfriados, respectivamente, actividades diferentes. Por ello, el progreso de la reacción se retarda, por lo que el calor de reacción generado puede evacuarse más fácilmente a través de la pared de los tubos de contacto. Un resultado parecido puede lograrse mediante la dilución dirigida de la carga catalítica con material inerte. La desventaja de estas disoluciones es que deben desarrollarse dos o más sistemas catalíticos y usarse en los tubos de contacto o que usando material inerte la capacidad del reactor se reduce.
En las publicaciones para información de solicitud WO 2004/037718 y WO 2004/014845 se menciona concretamente en forma general la posibilidad de una oxidación adiabática catalítica de cloruro de hidrógeno junto con el procedimiento isotermo preferente. No obstante, las formas de realización concretas de una oxidación de cloruro de hidrógeno efectuada adiabáticamente no se describen. Por lo tanto, permanece sin aclarar como puede evacuarse el calor de reacción de la reacción exotérmica en el caso de un modo de realización completamente adiabático de la totalidad del procedimiento y como puede evitarse un daño al catalizador. Realmente, la oxidación de cloruro de hidrógeno según estas etapas se realiza, no obstante, de modo isotermo, como el procedimiento de lecho sólido en reactores de haz de tubos, que como ya se ha mencionado, precisa un enfriamiento de control extraordinariamente caro. Básicamente, todos los reactores de haz de tubos descritos son también muy complejos y precisan de altos costes de inversión. Con el tamaño de construcción los problemas con relación a la estabilidad mecánica y la termostatización simultánea de la carga del catalizador, que aumentan de forma rápida, causan que los agregados grandes de este tipo sean poco económicos.
**(Ver fórmula)**
Por lo tanto, sería ventajoso proporcionar un procedimiento sencillo que pudiera llevarse a cabo en un reactor sencillo sin un sistema costoso para realizar un balance térmico en el reactor. Dichos reactores serían ligeros de transportar en una escala técnica y serían, en todos los tamaños, económicos y robustos. La entalpía de reacción se refleja en este tipo de reactor en la diferencia de temperatura entre la corriente gaseosa de reactante y la de producto cuantitativamente.
Para la oxidación exotérmica en fase gaseosa de cloruro de hidrógeno con una corriente gaseosa que contiene oxígeno no se han descrito hasta la fecha ni el uso de dichos reactores ni se han mostrado catalizadores adecuados ni procedimientos adecuados.
Los catalizadores que se usaron primeramente para el procedimiento de Deacon, por ejemplo catalizadores en soporte con la masa activa CuCl2, presentaban sólo una pequeña actividad. Mediante un aumento de la temperatura de reacción se pudo, ciertamente, aumentar la actividad, no obstante fue desventajoso que la volatibilidad del componente activo a temperatura más elevada provocara una desactivación rápida del catalizador. La oxidación de cloruro de hidrógeno a cloro es, además, una reacción de equilibrio. La posición del equilibrio se desplaza con el aumento de temperatura en perjuicio del producto final deseado.
Habitualmente, por lo tanto, se usan catalizadores con la actividad más alta posible que pueden desarrollar la reacción a temperaturas bajas. Los catalizadores con actividad alta conocidos se basan en rutenio. En el documento DE-A 197 48 299 se describen catalizadores en soporte con la masa activa de óxido de rutenio u óxido mixto de rutenio. A este respecto, el contenido de óxido de rutenio es del 0,1 % en peso al 20 % en peso y el diámetro de partícula promedio del óxido de rutenio de 1,0 nm a 10,0 nm. La reacción se lleva a cabo a una temperatura de entre 90 ºC y 150 ºC. Otros catalizadores en soporte a base de rutenio son conocidos del documento DE-A 197 34 412: catalizadores de cloruro de rutenio que contienen al menos un compuesto de óxido de titanio u óxido de circonio, complejos de rutenio-carbonilo, sales de rutenio de ácidos inorgánicos, complejos de rutenio-nitosilo, complejos de rutenio-amina, complejos de rutenio de aminas orgánicas o complejos de rutenio-acetonato de acetilo. La reacción se lleva a cabo a una temperatura de entre 90 ºC y 150 ºC, preferentemente de entre 200 ºC y 380 ºC. En las dos solicitudes DE-A 197 48 299 y DE-A 197 34 412, el catalizador se usa en un lecho sólido o en lecho fluido. Como sustancia de partida con oxígeno se usa aire u oxígeno puro. La reacción de Deacon sigue siendo, no obstante, una reacción exotérmica y también es necesario un control de temperatura para el uso de catalizadores de alta actividad de este tipo.
Por lo tanto, existía el objetivo de proporcionar un procedimiento para la oxidación... [Seguir leyendo]
Reivindicaciones:
1. Procedimiento para la preparación de cloro por medio de la oxidación catalítica en fase gaseosa de cloruro de hidrógeno con oxígeno, que comprende al menos: la reacción de cloruro de hidrógeno con oxígeno en al menos dos lechos catalíticos conectados en serie en condiciones adiabáticas.
2. Procedimiento según la reivindicación 1, caracterizado porque la temperatura del catalizador en los lechos catalíticos en particular durante la reacción es de 150 ºC a 800 ºC.
3. Procedimiento según al menos una de las reivindicaciones1 ó 2, caracterizado porque la mezcla gaseosa del procedimiento que sale de al menos un lecho catalítico se lleva a continuación a través de un intercambiador de calor posconectado al lecho catalítico.
4. Procedimiento según la reivindicación 3, caracterizado porque después de cada lecho catalítico se encuentra al menos un intercambiador de calor, a través del que se lleva la mezcla gaseosa del proceso que sale.
5. Procedimiento según la reivindicación 3 ó 4, caracterizado porque el calor de reacción evacuado del intercambiador de calor se usa para la obtención de vapor.
6. Procedimiento según al menos una de las reivindicaciones 1 a 5, caracterizado porque la reacción se lleva a cabo a una presión de 100 a 3.000 kPa.
7. Procedimiento según al menos una de las reivindicaciones 1 a 6, caracterizado porque la temperatura de entrada de la mezcla gaseosa que entra en el primer lecho catalítico es de 150 a 400 ºC.
8. Procedimiento según la reivindicación 7, en el que la temperatura de entrada de la mezcla gaseosa que entra en cada uno de los lechos catalíticos es de 150 a 400 ºC.
9. Procedimiento según una de las reivindicaciones 1 a 8, caracterizado porque los lechos catalíticos conectados en serie se operan con una temperatura media que aumenta o disminuye de lecho catalítico a lecho catalítico.
10. Procedimiento según una de las reivindicaciones 1 a 9, caracterizado porque la relación molar entre el oxígeno y el cloruro de hidrógeno antes de la entrada en cada lecho catalítico es de 0,25 a 10 equivalentes de oxígeno por equivalente de cloruro de hidrógeno.
11. Procedimiento según al menos una de las reivindicaciones 1 a 10, caracterizado porque la reacción se lleva a cabo en de 2 a 12 lechos catalíticos conectados en serie.
12. Procedimiento según una de las reivindicaciones 1 a 11, caracterizado porque la corriente gaseosa de entrada que contiene cloruro de hidrógeno y oxígeno sólo se alimenta al primero de los al menos dos lechos catalíticos conectados en serie.
13. Procedimiento según una de las reivindicaciones 1 a 12, caracterizado porque antes de uno o varios de los lechos catalíticos posteriores al primer lecho catalítico se dosifica cloruro de hidrógeno y/o oxígeno fresco a la corriente de gas de proceso.
14. Procedimiento según una de las reivindicaciones 1 a 13, caracterizado porque el catalizador presenta al menos un elemento que está seleccionado del grupo constituido por: cobre, potasio, sodio, cromo, cerio, oro, bismuto, rutenio, rodio, platino, así como un elemento del grupo VIIIb. del sistema periódico de los elementos.
15. Procedimiento según una de las reivindicaciones 1 a 14, caracterizado porque el catalizador es a base de rutenio o de un compuesto de rutenio.
16. Procedimiento según una de las reivindicaciones 1 a 15, caracterizado porque la actividad de los catalizadores en los lechos catalíticos individuales es diferente y, en particular, aumenta de lecho catalítico a lecho catalítico.
17. Procedimiento según una de las reivindicaciones 1 a 16, caracterizado porque el catalizador de los lechos catalíticos está aplicado sobre un soporte inerte.
18. Procedimiento según la reivindicación 17, caracterizado porque el soporte del catalizador está constituido total o parcialmente por óxido de titanio, óxido de estaño, óxido de aluminio, óxido de circonio, óxido de vanadio, óxido de cromo, óxido de silicio, tierra de diatomeas, nanotubos de carbono o una mezcla o compuesto de las sustancias mencionadas.
Patentes similares o relacionadas:
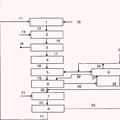 Procedimiento para la producción de cloro a partir de cloruro de hidrógeno y oxígeno, del 26 de Junio de 2019, de Covestro Deutschland AG: Procedimiento para la producción de cloro por medio de oxidación de múltiples etapas mediante
a) reacción térmica de cloruro de hidrógeno […]
Procedimiento para la producción de cloro a partir de cloruro de hidrógeno y oxígeno, del 26 de Junio de 2019, de Covestro Deutschland AG: Procedimiento para la producción de cloro por medio de oxidación de múltiples etapas mediante
a) reacción térmica de cloruro de hidrógeno […]
Catalizador y procedimiento para la preparación de cloro mediante oxidación en fase gaseosa, del 15 de Mayo de 2019, de Covestro Deutschland AG: Composición de catalizador que comprende al menos dióxido de estaño como material de soporte y al menos un compuesto que contiene rutenio […]
Procedimiento para la producción de cloro mediante oxidación en fase gaseosa, del 29 de Noviembre de 2017, de Covestro Deutschland AG: Procedimiento para la producción de cloro mediante oxidación en fase gaseosa catalítica de cloruro de hidrógeno con oxígeno sobre un catalizador sólido, en donde la oxidación […]
Procedimiento para la preparación de carbonatos de diarilo y policarbonatos, del 26 de Julio de 2017, de Covestro Deutschland AG: Procedimiento para la preparación de carbonato de diarilo que comprende las siguientes etapas: (a) preparación de fosgeno por reacción de cloro con monóxido de carbono, […]
Método para la producción de cloro, del 1 de Junio de 2016, de SUMITOMO CHEMICAL COMPANY, LIMITED: Un proceso para la producción de cloro que comprende la etapa de oxidación del cloruro de hidrógeno en un gas que contiene cloruro de hidrógeno con un gas que contiene […]
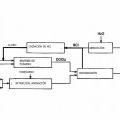 Método para la producción de cloro, del 26 de Marzo de 2015, de SUMITOMO CHEMICAL COMPANY, LIMITED: Un proceso para producir cloro, que comprende hacer reaccionar cloro con monóxido de carbono para producir fosgeno, hacer reaccionar el fosgeno con un amina primaria para […]
Método para la producción de cloro, del 26 de Marzo de 2015, de SUMITOMO CHEMICAL COMPANY, LIMITED: Un proceso para producir cloro, que comprende hacer reaccionar cloro con monóxido de carbono para producir fosgeno, hacer reaccionar el fosgeno con un amina primaria para […]
Proceso para producir óxido de rutenio soportado sobre titania modificada con sílice y proceso para producir cloro, del 9 de Enero de 2015, de SUMITOMO CHEMICAL COMPANY, LIMITED: Proceso para producir óxido de rutenio soportado sobre titania modificada con sílice y proceso para producir cloro. Proceso para producir óxido […]
Aparato para la reacción de oxidación del cloruro de hidrógeno y método de reacción de oxidación del cloruro de hidrógeno, del 9 de Abril de 2014, de SUMITOMO CHEMICAL COMPANY, LIMITED: Un aparato para la reacción de oxidación del cloruro de hidrógeno para producir cloro por oxidación del cloruro de hidrógeno a través de una reacción […]