Procedimiento de cribado.
Un procedimiento para la identificación de un biomarcador que se correlaciona con la sensibilidad de una enfermedad a un fármaco,
comprendiendo el procedimiento:
a) la exposición de una población de células a:
i) el fármaco;
ii) una genoteca de compuestos que tiene como diana varios genes diferentes, inhibiendo los compuestos el nivel o la actividad de una proteína en las células;
b) monitorizar la presencia de un fenotipo en las células que difiere del fenotipo evidente cuando la población de células es tratada solo con el fármaco;
en el que la presencia del fenotipo en una célula que difiere del fenotipo evidente cuando la población de células es tratada solo con el fármaco identifica a la proteína o su gen codificante como un biomarcador que se correlaciona con la sensibilidad a un fármaco.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/GB2007/001086.
Solicitante: ISIS INNOVATION LIMITED.
Nacionalidad solicitante: Reino Unido.
Dirección: UNIVERSITY OFFICES, WELLINGTON SQUARE OXFORD OX1 2JD REINO UNIDO.
Inventor/es: LA THANGUE,Nicholas B, FOTHERINGHAM,Susan.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61P35/00 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › Agentes antineoplásicos.
- C12N15/11 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 15/00 Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K). › Fragmentos de ADN o de ARN; sus formas modificadas (ADN o ARN no empleado en tecnología de recombinación C07H 21/00).
- G01N33/50 FISICA. › G01 METROLOGIA; ENSAYOS. › G01N INVESTIGACION O ANALISIS DE MATERIALES POR DETERMINACION DE SUS PROPIEDADES QUIMICAS O FISICAS (procedimientos de medida, de investigación o de análisis diferentes de los ensayos inmunológicos, en los que intervienen enzimas o microorganismos C12M, C12Q). › G01N 33/00 Investigación o análisis de materiales por métodos específicos no cubiertos por los grupos G01N 1/00 - G01N 31/00. › Análisis químico de material biológico, p. ej. de sangre o de orina; Ensayos mediante métodos en los que interviene la formación de uniones bioespecíficas con grupos coordinadores; Ensayos inmunológicos (procedimientos de medida o ensayos diferentes de los procedimientos inmunológicos en los que intervienen enzimas o microorganismos, composiciones o papeles reactivos a este efecto, procedimientos para preparar estas composiciones, procedimientos de control sensibles a las condiciones del medio en los procedimientos microbiológicos o enzimáticos C12Q).
- G01N33/574 G01N 33/00 […] › para el cáncer.
PDF original: ES-2376912_T3.pdf
Fragmento de la descripción:
Procedimiento de cribado La presente invención versa acerca de un procedimiento novedoso de cribado que identifica marcadores moleculares simples que son predictivos de si una afección particular responde a un tratamiento específico. Así, el procedimiento hace más eficientes los programas de desarrollo de fármacos e informa en cuanto a la manera en que un fármaco puede ser usado en un entorno clínico.
Una proporción significativa de los fármacos terapéuticos candidatos no llega a convertirse en fármacos comercializables debido a su metabolismo adverso o a su toxicidad, descubiertos durante las pruebas clínicas. Además, muchos fármacos que entran en el entorno clínico presentan una eficacia y una toxicidad limitantes. Estos fracasos representan un desperdicio muy significativo en gastos de desarrollo y, en consecuencia, existe la necesidad de nuevas tecnologías que puedan predecir de forma más fiable, rápida y económica, en la fase preclínica de desarrollo, las características metabólicas y toxicológicas de fármacos candidatos y su eficacia probable en la prevención o el tratamiento de una enfermedad.
El desarrollo de nuevas terapias es complicado y caro. Tomando el ejemplo del cáncer, esta es una enfermedad genética compleja para la que se ha demostrado que es difícil de dar con terapias de éxito. Además, en el contexto clínico, los tumores frecuentemente adquieren resistencia a nuevos tratamientos. Así, hay una gran necesidad de desarrollar pruebas simples que predigan la sensibilidad de los tumores a fármacos nuevos y existentes. Lo mismo se aplica a otras afecciones, particularmente a aquellas en las que la proliferación celular contribuye a la patología.
En el documento EP 1.595.952 se describe un procedimiento de estimación del efecto antitumoral de un inhibidor de la histona deacetilasa, que comprende, al menos, (I) una etapa de examen del efecto antitumoral in vivo de un inhibidor de la histona deacetilasa para células tumorales y de la división de las células tumorales en un tipo de célula sensible al inhibidor de la histona deacetilasa (célula tumoral sensible) y en un tipo de célula resistente al mismo (célula tumoral resistente) , y (II) una etapa de examen el patrón de expresión de genes de cada una de la célula tumoral sensible y de la célula tumoral resistente divididas en la etapa (I) recién mencionada, y de cribado (i) de un gen que presente una expresión alta en la célula tumoral sensible y una expresión baja en la célula tumoral resistente, o (ii) de un gen que presente una expresión baja en la célula tumoral sensible y una expresión alta en la célula tumoral resistente.
Resumen de la invención
En su forma más amplia, la invención está definida en la reivindicación independiente 1. En las reivindicaciones dependientes 2-15 se definen realizaciones preferentes.
Según la invención, se proporciona un procedimiento para la identificación de un biomarcador que se correlaciona con la sensibilidad de una enfermedad a un fármaco, comprendiendo el procedimiento:
a) la exposición de una población de células a:
i) el fármaco;
ii) una genoteca de compuestos que tiene como diana varios genes diferentes, inhibiendo los compuestos el nivel o la actividad de una proteína en las células;
b) monitorizar la presencia de un fenotipo en las células que difiere del fenotipo evidente cuando la población de células es tratada solo con el fármaco;
en el que la presencia del fenotipo en una célula que difiere del fenotipo evidente cuando la población de células es tratada solo con el fármaco identifica a la proteína o su gen codificante como un biomarcador que se correlaciona con la sensibilidad a un fármaco.
La invención es una cribado que permite la identificación de biomarcadores de enfermedades. El tipo de biomarcador que puede ser identificado predice la sensibilidad de la enfermedad a fármacos nuevos o existentes y, así, permite la estratificación de pacientes en grupos con respuesta probable y sin respuesta. Estos biomarcadores mejorarán la probabilidad de éxito clínico durante el desarrollo del fármaco y maximizarán el beneficio terapéutico al paciente "diseñando a medida" la terapia a la enfermedad.
La invención es particularmente aplicable a condiciones proliferativas como el cáncer y a enfermedades que implican un cambio en la diferenciación celular o la tasa de crecimiento. Sin embargo, cualquier enfermedad que exprese un biomarcador identificado según la invención es candidata al tratamiento con el fármaco objeto de ensayo.
La tecnología de la invención está idealmente adaptada a fármacos en los que la vía para alcanzar la máxima eficacia clínica es poco clara. Del mismo modo, la cribado facilita información en cuanto a genes vitales que se requieren para la acción del fármaco. Por ejemplo, para los fármacos contra el cáncer, la cribado identifica los sistemas vitales que están implicados en la eliminación de células tumorales.
En el enfoque de la invención, el procedimiento implica la exposición de una población de células a dos entidades. Las células son expuestas a un fármaco, dado que esta es la entidad objeto de la investigación; esto hace que el procedimiento sea específico para ese fármaco particular. En segundo lugar, las células son expuestas a una genoteca de compuestos que tiene como objetivos varios genes diferentes, modulando los compuestos el nivel o la actividad de una proteína que potencialmente hace falta para la susceptibilidad al fármaco. Como consecuencia del diseño de esta metodología, si se manifiesta un fenotipo diferencial como consecuencia de la exposición de las células al fármaco en comparación con células que han sido expuestas al fármaco pero que no han sido expuestas a los compuestos inhibidores, esto indica que la proteína cuyo nivel o cuya actividad han sido modulados puede estar implicada en el mecanismo de acción del fármaco y, así, identifica a esta proteína como un biomarcador útil.
La operación de la metodología puede ejemplificarse con un ejemplo en el que se usa una cribado de interferencia génica de ARNip en todo el genoma para identificar los genes funcionalmente importantes que influyen en la sensibilidad a los inhibidores de la histona deacetilasa (HDAC) . Los inhibidores de HDAC son un grupo particularmente relevante de nuevos agentes anticancerígenos. Hay en desarrollo clínico inhibidores de HDAC químicamente diferenciados que incluyen en particular el linfoma periférico de células T, el linfoma cutáneo de células T, la leucemia linfocítica crónica y el cáncer de próstata independiente de andrógenos. Sin embargo, la utilidad clínica (por ejemplo, tumor sensible, fase de la enfermedad, combinación de fármacos relevantes) es, en el momento actual, imposible de predecir. Serían un paso adelante muy importante biomarcadores que informasen sobre los patrones de sensibilidad del tumor, tanto para maximizar el beneficio clínico del fármaco como para diferenciar entre inhibidores de HDAC. Aunque se centra en los inhibidores de HDAC, el ejemplo descrito tiene idéntica aplicación a otras clases de terapias basadas en mecanismos en las que se requiere una ralentización del crecimiento, la diferenciación o la proliferación celulares para tratar con éxito la enfermedad.
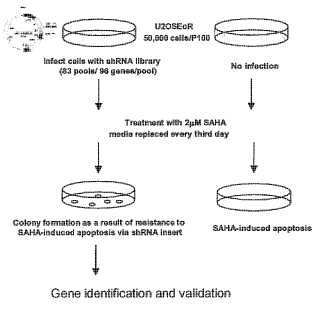
En el presente documento, la plataforma de cribado ha sido validada con estudios sobre los inhibidores de HDAC utilizando una genoteca de ARNip que tiene como diana a genes humanos que han sido seleccionados por la asociación con el cáncer y otras enfermedades humanas. Los inhibidores de HDAC matan células tumorales. Las células tumorales tratadas con la genoteca de ARNip y un inhibidor de HDAC apropiado sobreviven debido a la pérdida de un gen que es diana del ARNip. Sobreviven evitando la apoptosis que, si no, habría sido inducida por el inhibidor de HDAC si el gen hubiera estado presente y activo dentro de la célula. Es decir, es preciso que el gen esté expresado para que confiera sensibilidad al inhibidor de HDAC. En consecuencia, esta metodología identifica como biomarcadores a genes que son diana para los inhibidores de HDAC. La Figura 1 representa una ilustración de cómo opera la metodología.
El procedimiento de la invención evalúa la respuesta de una población de células a un fármaco particular identificando biomarcadores de enfermedad. Así, la invención puede ser usada de muchas maneras diferentes para evaluar la idoneidad de una célula particular al tratamiento con un fármaco... [Seguir leyendo]
Reivindicaciones:
1. Un procedimiento para la identificación de un biomarcador que se correlaciona con la sensibilidad de una enfermedad a un fármaco, comprendiendo el procedimiento:
a) la exposición de una población de células a:
i) el fármaco;
ii) una genoteca de compuestos que tiene como diana varios genes diferentes, inhibiendo los compuestos el nivel o la actividad de una proteína en las células;
b) monitorizar la presencia de un fenotipo en las células que difiere del fenotipo evidente cuando la población de células es tratada solo con el fármaco;
en el que la presencia del fenotipo en una célula que difiere del fenotipo evidente cuando la población de células es tratada solo con el fármaco identifica a la proteína o su gen codificante como un biomarcador que se correlaciona con la sensibilidad a un fármaco.
2. Un procedimiento según la reivindicación 1 en el que los compuestos son ácidos nucleicos.
3. Un procedimiento según las reivindicaciones 1 o 2 en el que los compuestos son ARNip.
4. Un procedimiento según una cualquiera de las reivindicaciones precedentes en el que los compuestos reducen el nivel de expresión de la proteína.
5. Un procedimiento según la reivindicación 4 en el que los compuestos inhabilitan la expresión de la proteína.
6. Un procedimiento según una cualquiera de las reivindicaciones precedentes en el que la etapa de exposición implica incubar la célula en presencia del fármaco.
7. Un procedimiento según una cualquiera de las reivindicaciones precedentes en el que los compuestos están seleccionados de ARNi, ARNhc, ARNip, vectores de ARNip, ribozimas, ácidos nucleicos antisentido, anticuerpos o compuestos de molécula pequeña.
8. Un procedimiento según la reivindicación 1 en el que la genoteca de compuestos es una genoteca de ARNip.
9. Un procedimiento según la reivindicación 1 en el que la genoteca de compuestos es una genoteca vectorizada de interferencia por ARN.
10. Un procedimiento según la reivindicación 8 en el que la genoteca es una genoteca viral vectorizada de interferencia por ARN.
11. Un procedimiento según la reivindicación 1 en el que la genoteca de compuestos es una genoteca de vectores de ARNip y la multiplicidad de infección está organizada de tal modo que, como media, cada célula incorpora un solo vector y este vector expresa una especie de ARNip que inhabilita la expresión de un gen particular.
12. Un procedimiento según una cualquiera de las reivindicaciones precedentes en el que la célula o las células están aisladas de un paciente.
13. Un procedimiento según una cualquiera de las reivindicaciones precedentes en el que el fármaco es un inhibidor de HDAC.
14. Un procedimiento según una cualquiera de las reivindicaciones precedentes en el que la célula o las células están expuestas a una combinación de fármacos.
15. Un procedimiento según una cualquiera de las reivindicaciones precedentes en el que el fenotipo de las características de supervivencia o de crecimiento de la célula o las células.
FIG. 2 (a)
ProbabilidadGenID del genNombreGrupoColoniaNº deaciertosCoincidencia de ID del grupoSecuenciaelevadahHRAD238NM_002874rad humano 23B5212síGATGCAACGAGTGCACTTGRFC1NM_002913factor de replicación C15232síCAGATTAAGGGTGCTATGAMYD88NM_002468gen 88 de respuesta primaria de diferenciación mieloide5241síACACAACTTCAGTCGATAGPTBP1NM_002819proteína 1 de enlace de tracto de polipirimidina5281síGGACCGTTTATCATGAGCPPP4R1NM_005314subunidad 1 reguladora de la proteína fosfatasa 44611síACACAGCTTTCCACAGGGCLIFNM_002309factor inhibidor de la leucemia51411síCAACCTGGACAAGCTATGTLIFRNM_002310receptor del factor inhibidor de la leucemia5191síCAGGCCGTGGTACTGATTA5131síTAATCAGTACCACGGCCTGmediaSCBGB2A2NM_002411secretoglobina, familia 2A, miembro 251191síTTAATATATGACAGCAGTC51201síTTAATATATGACAGCAGTCHLA-0081NM_002123pj p phistocompatibilidad, clase II, DQ beta 151111síGAGATCGTGCGCTTCGACAbaja PVRL1NM_002855receptor atípico 1 de poliovirus5291síGTGCAGTATNAGCCTGAGSERPA10NM_016186serpina A107422síAGATCTCCATGAGGCACGAHEXBNM_000521hexosaminidasa B7011síACATGAGACAAAGAATAGCPPATNM_002703fosforibosilpirofosfato amidotransferasa5251síATCACGTCTTTACTGAAGALDHBNM_002300lactato dehidrogenasa B51152síGGATATACCAACTGGGCTAMAN2A1NM_002372miembro 1 de la manosidasa 2A5123síGTTAAGCCGCCAGTTCACC51141síGTTAAGCCGCCAGTTCACCPLECK2NM_016445pleckstrina 27412síGAAATTAGCCTGAGCACTG2812no (74) GAAATTAGCCTGAGCACTG3721no (74) GAAATTAGCCTGAGCACTGSART2 NM_013352 antígeno del carcinoma de célulasescamosas reconocido por células T 51 7 1 no (56) TTAACNGGACAAACTATGT FIG. 2 (b) GenNombre (s) Función principalLocalizaciónProteínas asociadasRFC-1factor de replicación C1p140facilita la carga de PCNA en sitios de síntesis de ADNnúcleoBRCA1, ATM. Rb, C/EBPa, HDAC1hHR23Brad humano 23Bmodula la transferencia de proteínas del sitio de ubiquitinación al proteasomanúcleo/citoplasmacomponente del proteasoma 19S, hdm2, p53PP4R1subunidad 1 reguladora de laproteína fosfatasa 4se enlaza con la subunidad catalítica PP4 y regula la actividadde la fosfatasa de la mismanúcleo/citoplasmaPP4C, HDAC3MYD88marcador 88 de diferenciación mieloidemolécula adaptadora generalimplicada en la señalización de la familia de receptores Tollnúcleo/citoplasmaNF-__ 1pA pAK PTBP1proteína 1 de enlace de tractode polipirimidinaRNPnh IARN acompañante implicado en el corte y el empalme de preARNmnúcleo/citoplasmaApaf-1, TLS/FUSLIFfactor inhibidor de la leucemiacitoquina polifuncionalcitoplasmaHGF, BMP2LIFR receptor a-subunidad del factorinhibidor de la leucemia dp se combina con gp130 para formar el receptor del LIF, implicado en la señalización devarias citoquinas membrana celular LIF, SHP-2
Patentes similares o relacionadas:
Compuestos de alquinilbenceno heterocíclicos, y composiciones médicas y usos de los mismos, del 29 de Julio de 2020, de Guangzhou Healthquest Pharma Co., Ltd: Un compuesto de alquinilbenceno heterocíclico que tiene la fórmula (I) y una sal farmacéuticamente aceptable, o estereoisómero del mismo, **(Ver […]
 Composiciones y métodos para el tratamiento de trastornos de células plasmáticas y trastornos prolinfocíticos de células b, del 29 de Julio de 2020, de Knopp Biosciences LLC: Una composición que comprende una cantidad terapéuticamente eficaz de dexpramipexol para su uso en el tratamiento de un trastorno de células B caracterizado por niveles elevados […]
Composiciones y métodos para el tratamiento de trastornos de células plasmáticas y trastornos prolinfocíticos de células b, del 29 de Julio de 2020, de Knopp Biosciences LLC: Una composición que comprende una cantidad terapéuticamente eficaz de dexpramipexol para su uso en el tratamiento de un trastorno de células B caracterizado por niveles elevados […]
Derivados de piperidina 1,4 sustituidos, del 29 de Julio de 2020, de 89Bio Ltd: Un compuesto de acuerdo con la Fórmula I: **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en donde: A se selecciona de […]
Profármacos de gemcitabina, del 29 de Julio de 2020, de NuCana plc: Una formulación farmacéutica que comprende gemcitabina-[fenil-benzoxi-L-alaninil)]-(S)-fosfato 3: **(Ver fórmula)** o una sal o solvato […]
Formas cristalinas de 6-((6,7-dimetoxiquinazolin-4-il)oxi)-N,2-dimetilbenzofuran-3-carboxamida, del 29 de Julio de 2020, de Hutchison Medipharma Limited: Forma I de 6-((6,7-dimetoxiquinazolin-4-il)oxi)-N,2-dimetilbenzofuran-3-carboxamida, en donde el difractograma de rayos X de polvo de la Forma […]
Compuestos y procedimientos de uso, del 29 de Julio de 2020, de Medivation Technologies LLC: Un compuesto de fórmula (Aa-1): **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en la que: A representa H, halógeno, amino, […]
Complejos de agentes terapéuticos de base vírica y poli(beta-amino-ésteres) modificados, del 29 de Julio de 2020, de Sagetis Biotech, SL: Un complejo de un agente terapéutico de base vírica con un polímero de fórmula I: **(Ver fórmula)** donde cada L1 y L2 están seleccionados […]
Conectores autoinmolativos no lineales y conjugados de los mismos, del 22 de Julio de 2020, de Byondis B.V: Compuesto conector-farmaco con la formula (I) **(Ver fórmula)** o sal, hidrato o solvato farmaceuticamente aceptables del mismo, donde […]