PREPARACIÓN PARA TRANSFERIR OLIGONUCLEÓTIDOS.
Una preparación para transferir a una cé- lula diana un oligonucleótido deseado,
que contiene como componente esencial colágeno soluble de tipo 1 derivado de dermis o un colágeno soluble de tipo 1 preparado mediante ingeniería genética, liberando dicha preparación un oligonucleótido 5 a 30 mero
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/JP2001/005195.
Solicitante: DAINIPPON SUMITOMO PHARMA CO., LTD.
KOKEN CO., LTD.
NATIONAL CANCER CENTER.
Nacionalidad solicitante: Japón.
Dirección: 6-8, DOSHO-MACHI 2-CHOME CHUO-KU OSAKA-SHI OSAKA-FU JAPON.
Inventor/es: SANO, AKIHIKO, TERADA, MASAAKI, ITOH, HIROSHI, FURUSE, MASAYASU, NAGAHARA,SHUNJI, OCHIYA,TAKAHIRO, KUBOTA,SHUNICHIRO.
Fecha de Publicación: .
Fecha Solicitud PCT: 19 de Junio de 2001.
Fecha Concesión Europea: 25 de Agosto de 2010.
Clasificación Internacional de Patentes:
- A61K31/7105 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › Acidos ribonucleicos naturales, es decir conteniendo unicamente ribosas unidas a la adenina, la guanina, la citosina, o el uracilo y teniendo enlaces 3'-5' fosfodiester.
- A61K31/711 A61K 31/00 […] › Acidos desoxirribonucleicos naturales, es decir conteniendo unicamente 2'-desoxirribosas unidas a la adenina, la guanina, la citosina o la timina y teniendo enlaces 3'-5' fosfodiester.
- A61K47/42 A61K […] › A61K 47/00 Preparaciones medicinales caracterizadas por los ingredientes no activos utilizados, p. ej. portadores o aditivos inertes; Agentes de direccionamiento o agentes modificadores enlazados químicamente al ingrediente activo. › Proteínas; Polipéptidos; Sus productos de degradación; Sus derivados, p. ej. albúmina, gelatina or zeína (oligopéptidos que contienen hasta cinco aminoácidos A61K 47/18; poliaminoácidos A61K 47/34).
- A61K48/00B
- A61K9/00M5
- A61K9/00M5D
Clasificación PCT:
- A61K31/7105 A61K 31/00 […] › Acidos ribonucleicos naturales, es decir conteniendo unicamente ribosas unidas a la adenina, la guanina, la citosina, o el uracilo y teniendo enlaces 3'-5' fosfodiester.
- A61K31/711 A61K 31/00 […] › Acidos desoxirribonucleicos naturales, es decir conteniendo unicamente 2'-desoxirribosas unidas a la adenina, la guanina, la citosina o la timina y teniendo enlaces 3'-5' fosfodiester.
- A61K47/42 A61K 47/00 […] › Proteínas; Polipéptidos; Sus productos de degradación; Sus derivados, p. ej. albúmina, gelatina or zeína (oligopéptidos que contienen hasta cinco aminoácidos A61K 47/18; poliaminoácidos A61K 47/34).
- A61K48/00 A61K […] › Preparaciones medicinales que contienen material genético que se introduce en las células del cuerpo vivo para tratar enfermedades genéticas; Terapia génica.
Clasificación antigua:
- A61K31/7105 A61K 31/00 […] › Acidos ribonucleicos naturales, es decir conteniendo unicamente ribosas unidas a la adenina, la guanina, la citosina, o el uracilo y teniendo enlaces 3'-5' fosfodiester.
- A61K31/711 A61K 31/00 […] › Acidos desoxirribonucleicos naturales, es decir conteniendo unicamente 2'-desoxirribosas unidas a la adenina, la guanina, la citosina o la timina y teniendo enlaces 3'-5' fosfodiester.
- A61K47/42 A61K 47/00 […] › Proteínas; Polipéptidos; Sus productos de degradación; Sus derivados, p. ej. albúmina, gelatina or zeína (oligopéptidos que contienen hasta cinco aminoácidos A61K 47/18; poliaminoácidos A61K 47/34).
- A61K48/00 A61K […] › Preparaciones medicinales que contienen material genético que se introduce en las células del cuerpo vivo para tratar enfermedades genéticas; Terapia génica.
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Eslovenia, Finlandia, Rumania, Chipre, Lituania, Letonia, Ex República Yugoslava de Macedonia, Albania.
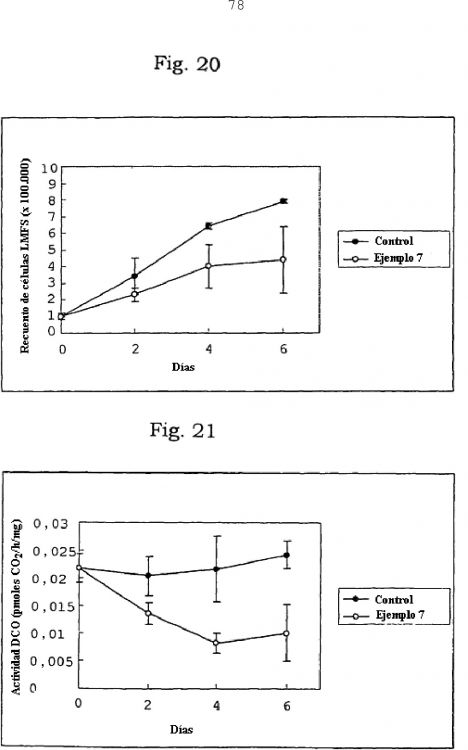
Fragmento de la descripción:
CAMPO DE LA INVENCIÓN
La presente invención se refiere a preparaciones para transferir oligonucleótidos a una célula diana, las cuales contienen un colágeno como componente esencial, siendo utilizadas dichas preparaciones en terapia antisentido. Más específicamente, la presente invención se refiere a una preparación segura que contiene un colágeno como componente esencial, mediante la cual los oligonucleótidos pueden ser transferidos eficazmente a una célula diana. ANTECEDENTES
Con el rápido progreso de la técnica reciente para el análisis de la información genética, se ha acumulado información de genes que causan enfermedades. Por ejemplo, en el campo de las enfermedades infecciosas se ha clarificado la información sobre genes esenciales para el crecimiento o la supervivencia de bacterias y virus. Además, en varias enfermedades, se ha clarificado la información sobre los genes relacionados con la enfermedad y sobre su sobreexpresión y mutaciones, y se ha investigado la relación entre tal información genética y el mecanismo de la patogénesis.
La terapia antisentido sirve para controlar o inhibir la expresión de la información de los genes relacionados con una enfermedad, según se mostró anteriormente, con el fin de tratar o prevenir la enfermedad.
Específicamente, comprende:
(1) la administración de un oligonucleótido 10 a 30 mero aproximadamente que contiene una secuencia de bases complementaria a un ARNm o a un precursor de ARNm de genes cuya expresión va a ser controlada o inhibida;
(2) el permitir que el oligonucleótido forme una doble cadena junto con el ARNm o con el precursor de ARNm en las células y
(3) la inhibición de la traducción del ARNm por los ribosomas, o la inhibición del corte de la doble cadena por la ARNasa H, o del ayuste del precursor de ARNm; suprimiendo de este modo la expresión de los genes.
Además, existe un método que comprende la unión directa del ADN de doble cadena del gen diana para formar una triple hebra, mediante lo cual se inhibe la transcripción a ARNm.
La terapia antisentido ha sido estudiada intensamente desde que fue propuesta al final de los años 70 por Ts'O y Miller y col., Biochemistry, 16, 1988-1996, 1977; y Zamecnik y col., Proc. Natl. Acad. Sci. USA, 75, 280-284, 1978. Originalmente, los estudios sobre terapia antisentido se llevaron a cabo utilizando oligonucleótidos de ADN o ARN nativo. Sin embargo, esto tenía ciertos problemas tales como:
(1) la rápida degradación e inactivación de los oligonucleótidos nativos debido a las nucleasas endógenas;
(2) la dificultad que presentan los oligonucleótidos cargados negativamente para penetrar en las células a través de la membrana celular debido a la membrana cargada negativamente; etcétera.
Considerando tales problemas, se han desarrollado y utilizado varios oligonucleótidos modificados que tienen la estructura básica del ADN o del ARN. Entre estos oligonucleótidos modificados, los más prácticos son los oligonucleótidos de tipo fosforotioato, en los cuales los enlaces diéster entre los nucleósidos respectivos están sustituidos por enlaces fosforotioato (referidos de aquí en adelante como S-oligonucleótidos). Los S-oligonucleótidos han sido utilizados en la mayor parte de los ensayos clínicos que se han realizado hasta ahora.
Sin embargo, incluso los S-oligonucleótidos tienen los problemas siguientes:
(1) que son degradados e inactivados por la nucleasa endógena, aunque no tan rápidamente como los oligonucleótidos nativos;
(2) que tienen menos capacidad para formar una doble cadena junto con el ARNm en comparación con los oligonucleótidos nativos;
(3) que deben ser administrados a la célula diana a una mayor concentración debido a su baja capacidad para formar una doble cadena;
(4) que producen la liberación de citoquinas, la inhibición de la coagulación sanguínea, la activación del complemento y reacciones alérgicas o similares cuando son administrados sistémicamente a una concentración más elevada;
(5) que se unen específicamente o no específicamente a proteínas endógenas y, por consiguiente, no pueden formar una doble cadena con el ARNm diana pero producen efectos no específicos.
Los mismos no satisfacen completamente los requisitos de la terapia antisentido, por lo que prácticamente no han sido utilizados. Estos problemas son ciertos no sólo para los oligonucleótidos utilizados como primera generación de S-oligonucleótidos, sino también para los denominados de segunda y tercera generación para terapia antisentido, que han sido desarrollados hasta ahora (Kazunari Yokoyama, Kagaku-to-Seibutsu, 36, 556559, 1998). Debido a estos problemas, se ha reconocido de manera general que la supresión de la expresión de un gen diana utilizando oligonucleótidos no proporcionará buenos resultados in vivo, particularmente en ensayos clínicos, aunque pudiera proporcionar buenos resultados in vitro. En realidad, los ensayos clínicos para fármacos antisentido son a menudo suspendidos ya que no muestran buenos resultados.
Murakami informó que la suspensión de los ensayos clínicos estaría causada por el problema de la administración de los fármacos antisentido y que el desarrollo con éxito de los fármacos antisentido depende del desarrollo de métodos de administración (Akira Murakami, Seitai-no-Kagaku, 49, 309-314, 1998). Los métodos para administrar oligonucleótidos han sido investigados intensamente dirigiéndose principalmente a la mejora de la penetración y del transporte de los oligonucleótidos en las células. Para solucionar tales problemas, en la revisión de Yokoyama se proponen los métodos siguientes (Kazunari Yokoyama, Cellular Engineering, 16, 1463-1473, 1997):
(1) conjugar los oligonucleótidos con compuestos policargados tales como poli-L-lisina y polietilenimina;
(2) utilizar ADNs conjugados a transferrina/poli-Llisina en presencia de la cápside de adenovirus defectuosos en replicación;
(3) utilizar fragmentos de los dominios homeo del péptido fusionado a la membrana derivado de la proteína de superficie HA del virus de la influenza (Bongartz,
J.P. y col., Nucleic Acids Research, 22, 4681-4688, 1994) y de la proteína Antennapedia de Drosophila;
(4) unir los oligonucleótidos a ácido fólico o al receptor de asialoglicoproteínas, o a transferrina, con el fin de que sean dirigidos hacia receptores específicos de la superficie celular;
(5) conjugar los oligonucleótidos con colesterol;
(6) encapsular los oligonucleótidos en lípidos catiónicos, etcétera. Estas propuestas están encaminadas principalmente a mejorar la penetración y el transporte de los oligonucleótidos a las células, y experimentos in vitro en los cuales los oligonucleótidos pueden ser administrados directamente a las células han proporcionado buenos resultados. Sin embargo, los experimentos in vivo no han sido capaces de mostrar resultados suficientes y han sido difíciles de utilizar en la práctica.
Por ejemplo, los métodos que comprenden la administración de los oligonucleótidos encapsulados en lípidos catiónicos (esto es, liposomas) han sido estudiados intensamente ya que transfieren eficazmente oligonucleótidos a las células. Sin embargo, esos métodos tienen problemas ya que, por ejemplo, esos oligonucleótidos no actúan sobre las células diana a una concentración elevada debido a que se difunden por todo el cuerpo inmediatamente después de la administración; las proteínas que existen en el organismo se unen al liposoma para inhibir la adhesión a las células diana y los lípidos catiónicos que constituyen el liposoma pueden tener citotoxicidad, y por tanto no han sido capaces de proporcionar resultados exitosos en la práctica. En realidad, los ensayos clínicos que utilizan S-oligonucleótidos no han utilizado nunca liposomas (Seitai-no-kagaku, 49, 309-314, 1998). Existe todavía la necesidad de desarrollar métodos prácticos para la administración de oligonucleótidos.
Por otra parte, un método para transferir un gen en el cual un ADN plasmídico o un vector vírico es liberado gradualmente a partir de materiales biocompatibles o compatibles con el hueso, ha sido descrito en la Publicación de Patente Japonesa (kokai) Nº 71542/1997 y en USP Nº 5,763.416. Estos documentos describen que los materiales biocompatibles o compatibles con el hueso liberan gradualmente ADNs plasmídicos con un peso molecular de 2.650.000 a 5.300.000 (correspondiente a 4.000 pb
8.000 pb) o vectores víricos con el peso molecular más grande para presentar buenas eficacias de expresión....
Reivindicaciones:
1. Una preparación para transferir a una célula diana un oligonucleótido deseado, que contiene como componente esencial colágeno soluble de tipo 1 derivado de dermis o un colágeno soluble de tipo 1 preparado mediante ingeniería genética, liberando dicha preparación un oligonucleótido 5 a 30 mero.
2. Una preparación de acuerdo con la Reivindicación 1, en la que la célula diana es una célula animal.
3. Una preparación de acuerdo con la Reivindicación 2, en la que la célula diana es un órgano
o un tejido que requiere ser tratado por una enfermedad del sujeto, o las células de su alrededor.
4. Una preparación de acuerdo con cualquiera de las Reivindicaciones 1 a 3, en la que el colágeno es atelocolágeno.
5. Una preparación de acuerdo con cualquiera de las Reivindicaciones 1 a 4, en la que el peso molecular del colágeno es de 300.000 aproximadamente a 900.000 aproximadamente.
6. Una preparación de acuerdo con cualquiera de las Reivindicaciones 1 a 5, donde la preparación es una formulación de liberación mantenida.
7. Una preparación de acuerdo con la Reivindicación 6, en la cual el oligonucleótido es un ADN
8. Una preparación de acuerdo con la Reivindicación 6, en la que el oligonucleótido es un ARN 9. Una preparación de acuerdo con la Reivindicación 1, en la que el oligonucleótido tiene al menos un enlace fosforotioato. 10. Una preparación de acuerdo con la Reivindicación 1, en la que el oligonucleótido contiene como porción mínima una secuencia de bases que se une de manera complementaria bajo condiciones fisiológicas a una hebra sentido o antisentido de un gen que codifica una proteína que presenta un efecto fisiológico para alterar la homeostasis de un organismo vivo. o un derivado de ADN.
o un derivado de ARN.
Patentes similares o relacionadas:
Preparaciones ácidas de insulina con estabilidad mejorada, del 15 de Julio de 2020, de SANOFI-AVENTIS DEUTSCHLAND GMBH: Formulación farmacéutica que contiene insulina humana Gly(A21),Arg(B31),Arg(B32) y un tensioactivo, elegido de un grupo que contiene Tween 20® y Tween 80®; siendo […]
Marcador molecular para células madre cancerosas, del 29 de Abril de 2020, de Sapporo Medical University: Un péptido seleccionado del grupo que consiste en: DNAJB8 : AFMEAFSSF (SEQ ID NO: 71); DNAJB8 : AYRKLALRW (SEQ ID NO: 68); y DNAJB8 : […]
Variantes de clorotoxina, conjugados y métodos para su utilización, del 8 de Abril de 2020, de FRED HUTCHINSON CANCER RESEARCH CENTER: Conjugado de clorotoxina que comprende un péptido de clorotoxina acoplado covalentemente a un marcador fluorescente seleccionado del grupo que consiste […]
Composición que contiene coenzima Q10, del 25 de Marzo de 2020, de KANEKA CORPORATION: Una composición que contiene coenzima Q10, que comprende 1-70% en peso de coenzima Q10 (A), 15-94% en peso de caseína (B) y al menos 5% en peso de un sacárido […]
Composiciones y métodos para la embolización viral, del 19 de Febrero de 2020, de Sillajen, Inc: Una composición que comprende un virus oncolítico Poxviridae o Herpesviridae y una micropartícula biocompatible o un agente de gel de polímero […]
Cápsulas blandas llenas de líquido, del 12 de Febrero de 2020, de Patheon Softgels Inc: Una composición farmacéutica que comprende una forma de dosificación blanda que comprende un revestimiento que encapsula una matriz líquida, […]
Partículas que contienen un factor de crecimiento y usos de las mismas, del 8 de Enero de 2020, de INSTITUT NATIONAL DE LA SANTE ET DE LA RECHERCHE MEDICALE: Partícula que contiene al menos un polisacárido reticulado covalentemente y al menos un factor de crecimiento, comprendiendo además dicha […]
Un polipéptido de dímero CCL20 bloqueado modificado por ingeniería, del 8 de Enero de 2020, de The Medical College of Wisconsin, Inc: Un polipéptido de dímero CCL20 bloqueado, en donde el dímero comprende dos monómeros unidos covalentemente entre sí, en donde los dos monómeros […]