Polipéptidos con actividad de mejora celulolítica y polinucleótidos que los codifican.
Polipéptido aislado con actividad de mejora celulolítica, y con una secuencia de aminoácidos que tiene al menos 85%,
más preferiblemente al menos 90%, de la forma más preferible al menos 95%, e incluso de forma más preferible al menos 97% de identidad con los aminoácidos 18 a 240 de la SEC ID nº: 4.
Tipo: Patente Europea. Resumen de patente/invención. Número de Solicitud: E10180304.
Solicitante: NOVOZYMES, INC..
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 1445 DREW AVENUE DAVIS, CA 95616 ESTADOS UNIDOS DE AMERICA.
Inventor/es: HARRIS, PAUL, BROWN,KIMBERLY, LOPEZ DE LEON,ALFREDO, VLASENKO,ELENA, ZARETSKY,ELIZABETH, RE,EDWARD, MCFARLAND,KEITH.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C07H21/04 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07H AZUCARES; SUS DERIVADOS; NUCLEOSIDOS; NUCLEOTIDOS; ACIDOS NUCLEICOS (derivados de ácidos aldónicos o sacáricos C07C, C07D; ácidos aldónicos, ácidos sacáricos C07C 59/105, C07C 59/285; cianohidrinas C07C 255/16; glicales C07D; compuestos de constitución indeterminada C07G; polisacáridos, sus derivados C08B; ADN o ARN concerniente a la ingeniería genética, vectores, p. ej. plásmidos o su aislamiento, preparación o purificación C12N 15/00; industria del azúcar C13). › C07H 21/00 Compuestos que contienen al menos dos unidades mononucleótido que tienen cada una grupos fosfato o polifosfato distintos unidos a los radicales sacárido de los grupos nucleósido, p. ej. ácidos nucleicos. › con desoxirribosilo como radical sacárido.
- C07K14/37 C07 […] › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 14/00 Péptidos con más de 20 aminoácidos; Gastrinas; Somatostatinas; Melanotropinas; Sus derivados. › de hongos.
- C11D3/386 C […] › C11 ACEITES, GRASAS, MATERIAS GRASAS O CERAS ANIMALES O VEGETALES; SUS ACIDOS GRASOS; DETERGENTES; VELAS. › C11D COMPOSICIONES DETERGENTES; UTILIZACION DE UNA SOLA SUSTANCIA COMO DETERGENTE; JABON O SU FABRICACION; JABONES DE RESINA; RECUPERACION DE LA GLICERINA. › C11D 3/00 Otros compuestos que entran en las composiciones detergentes cubiertas por C11D 1/00. › Preparaciones que contienen enzimas.
- C12N1/21 C […] › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 1/00 Microorganismos, p.ej. protozoos; Composiciones que los contienen (preparaciones de uso médico que contienen material de protozoos, bacterias o virus A61K 35/66, de algas A61K 36/02, de hongos A61K 36/06; preparación de composiciones de uso médico que contienen antígenos o anticuerpos bacterianos, p. ej. vacunas bacterianas, A61K 39/00 ); Procesos de cultivo o conservación de microorganismos, o de composiciones que los contienen; Procesos de preparación o aislamiento de una composición que contiene un microorganismo; Sus medios de cultivo. › modificados por la introducción de material genético extraño.
- C12N15/74 C12N […] › C12N 15/00 Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K). › Vectores o sistemas de expresión especialmente adaptados a huéspedes procariotas distintos a E. coli, p. ej. Lactobacillus, Micromonospora.
- C12N9/42 C12N […] › C12N 9/00 Enzimas, p. ej. ligasas (6.); Proenzimas; Composiciones que las contienen (preparaciones para la limpieza de los dientes que contienen enzimas A61K 8/66, A61Q 11/00; preparaciones de uso médico que contienen enzimas A61K 38/43; composiciones detergentes que contienen enzimas C11D ); Procesos para preparar, activar, inhibir, separar o purificar enzimas. › actúan sobre los enlaces beta-glucosídicos-1,4, p. ej. celulasa.
- C12P21/06 C12 […] › C12P PROCESOS DE FERMENTACION O PROCESOS QUE UTILIZAN ENZIMAS PARA LA SINTESIS DE UN COMPUESTO QUIMICO DADO O DE UNA COMPOSICION DADA, O PARA LA SEPARACION DE ISOMEROS OPTICOS A PARTIR DE UNA MEZCLA RACEMICA. › C12P 21/00 Preparación de péptidos o de proteínas (proteína monocelular C12N 1/00). › preparados por hidrólisis de un enlace peptídico, p. ej. hidrolizados.
- C12P7/06 C12P […] › C12P 7/00 Preparación de compuestos orgánicos que contienen oxígeno. › Etanol como producto químico y no como bebida alcohólica.
- D21C1/00 TEXTILES; PAPEL. › D21 FABRICACION DEL PAPEL; PRODUCCION DE LA CELULOSA. › D21C PRODUCCION DE CELULOSA POR ELIMINACION DE SUSTANCIAS NO CELULOSICAS DE LAS MATERIAS QUE CONTIENEN LA CELULOSA; REGENERACION DE LIQUIDOS RESIDUALES; APARATOS PARA ESTE EFECTO. › Tratamiento previo de materiales finamente divididos antes de la cocción (de papeles viejos D21C 5/02).
PDF original: ES-2472669_T3.pdf
Fragmento de la descripción:
El0180304
Polipéptidos con actividad de mejora celulolítica y polinucle6lidos que los cod ifican
5 Declaraciones referentes a los Derechos sobre las invenciones hechas mediante
Investigación y Desarrollo patrocinados federalmente
10 [0001] Esta invención se ha hecho con el apoyo del Gobierno bajo el subcontrato NREL Nº ZCO-30017-02, Contrato Principal DE-AC36-98G010337, adjudicado por el Departamento de Energía. El Gobierno tiene ciertos derechos sobre esta invención.
Antecedentes de la invención
15 Campo de la invención
20 [0002] La presente invención se refiere a polipéptidos aislados con actividad de mejora celulolítica y polinucleótidos aislados que codifican los polipéptidos. La invención también se refiere a construcciones de ácidos nucleicos, vectores y células huésped que comprenden los polinucleótidos al igual que métodos para producir y usar los polipéptidos. Descripción de las técnicas relacionadas
25 [0003] La celulosa es un polimero de la glucosa de azúcar simple unida de manera covalente por beta-l, 4-enlaces. Muchos microorganismos producen enzimas que hidrolizan glucanos beta-unidos. Estas enzimas incluyen endoglucanasas, celobiohidrolasas y beta-glucosidasas. Las endoglucanasas digieren el polímero de celulosa en lugares aleatorios, abriéndolo para atacar con celobiohidrolasas. Las celobiohidrolasas liberan secuencialmente moléculas de celobiosa de los extremos del polímero de celulosa . la celobiosa es un dímero de glucosa hidrosoluble beta-l A-unido. Las beta-glucosidasas hidrolizan celobiosa a glucosa.
30 35 [0004] La conversión de materias primas celulósicas en etanol tiene las ventajas de la disponibilidad inmediata de cantidades grandes de materia prima, la conveniencia de evitar quema o vertido de los materiales y la limpieza del combustible de etanol. Madera, residuos agrícolas, brotes herbáceos y desperdicios sólidos municipales se han considerado como materias primas para producción de etanol. Estos materiales principalmente consisten en celulosa, hemicelulosa y lignina. Una vez la celulosa se convierte en glucosa , la glucosa es fácilmente fermentada por levadura en etanol.
[0005] Seria ventajoso en la técnica mejorar la conversión de materias primas celulósicas.
40 [0006] Es un objeto de la presente invención proporcionar polipéptidos aislados con actividad de mejora celulolítica y secuencias de ácidos nucleicos aisladas que codifican los polipéptidos para mejorar la conversión de materias primas celulósicas.
Resumen de la invención
45 [0007] la presente invención se refiere a un polipéptido aislado con actividad de mejora celulol1tica y con una secuencia de aminoácidos que tiene al menos 85%, más preferiblemente al menos 90%, de la forma más preferible al menos 95% e incluso más preferiblemente al menos un 97% de identidad con los aminoácidos 18 a 240 de la SEC ID nO: 4.
SO [0008] La presente invención también se refiere a polinucleótidos aislados que cod ifican un polipéptido con actividad de mejora celulolítica según la reivindicación 1.
[0009] La presente invención también se refiere a construcciones de ácidos nucleicos, recombinantes y células huésped recombinantes comprendiendo los polinucleótidos. vectores de expresión
55 [0010] La presente invención también se refiere a 10 métodos para producir tal polipéptido con actividad de mejora celulolítica comprend iendo (a) cultivo de una célula huésped recombinante comprendiendo una construcción de ácidos nucleicos comprend iendo un polinucleótido que codifica el polipéptido bajo condiciones propicias para la producción del polipéptido; y (b) recuperación del polipéptido.
60 65 [0011] La presente invención también se refiere a métodos para degradar o convertir un material celulósico, que comprenden: tratar el material celulósico con una cantidad efectiva de una proteína celulolítica en presencia de una cantidad efectiva de un polipéptido con actividad de mejora celulolítica, donde la presencia del polipéptido con actividad de mejora celulolítica aumenta la de9radación de material celulósico en comparación con la ausencia del polipéptido que tiene actividad de mejora celulolílica. [0012] La presente invención también se refiere a métodos para producir una sustancia orgánica , que comprenden:
SO
El0180304
(a) sacarificar un material celulósico con una cantidad efectiva de una proteína celulolílica en presencia de una cantidad efectiva del polipéptido con actividad de mejora cetulolitica, donde ta presencia del polipéptico con actividad de mejora celulolítica aumenta la degradación del material celulósico en comparación con la ausencia del polipéptido con actividad de mejora celulolítica;
(b) fermentar et material celutósico sacarificado det paso (a) con uno o más microorganismos de fermentación; y
(c) recuperar la sustancia orgán ica de la fermentación
Breve descripción de las figuras
[oo13[ Las figuras l A y 1 B muestran la secuencia de ADN genómico y la secuencia de aminoácidos deducida de un polipéptido de Thielavia te"estris NRRL 8126 GH61B con actividad de mejora celulolilica (SEC ID nO: 1 y 2, respectivamente) . Intrones predichos están en cursiva. El péptido señal predicho está subrayado.
La figura 2 muestra la secuencia de ADN genómico y la secuencia de aminoácidos deducida de un polipéptido de Thielavia lerreslris NRRL 8126 GH61C con actividad de mejora celulolítica (SEC ID nO: 3 y 4, respectivamente) . Intrones predichos están en cursiva. El péptido señal predicho está subrayado.
La figura 3 muestra la secuencia de ADN genómico y la secuencia de aminoácidos deducida de un polipéptido de Thielavia lerreslris NRRL 8126 GH61 O con actividad de mejora celulolítica (SEC ID nO: 5 y 6, respectivamente) . Intrones predichos están en cursiva. El péptido señal predicho está subrayado.
La figura 4 muestra la secuencia de AONc y la secuencia de aminoácidos deducida de un polipéptido de Thielavía terrestris NRRL 8126 GH61 E con actividad de mejora celulolítica (SEC ID nO: 7 y 8, respectivamente) . El péptido señal pred icho está subrayado.
La figura 5 muestra la secuencia de AONc y la secuencia de aminoácidos deducida de un pol ipéptido Thíelavia ferrestris NRRL 8126 GH61 G con actividad de mejora celulolítica (SEC ID nO: g y lO, respectivamente) . El péptido señal predicho está subrayado.
La Figura 6 muestra un mapa de restricción de pAILol.
La Figura 7 muestra un mapa de restricción de pBANe10.
La Figura 8 muestra un mapa de restricción de pAILo2.
La Figura 9 muestra un mapa de restricción de pPH27.
La Figura 10 muestra un mapa de restricción de pPH29.
La Figura 11 muestra un mapa de restricción de pPH28.
La Figura 12 muestra un mapa de restricción de pEJG120.
La Figura 13 muestra un mapa de restricción de pEJG 111 .
La Figura 14 muestra un mapa de restricción de pEJG 11 2.
La Figura 15 muestra un mapa de restricción de pTter61C.
La Figura 16 muestra un mapa de restricción de pTter610.
La Figura 17 muestra un mapa de restricción de pTter61E.
La Figura 18 muestra un mapa de restricción de pTter61G.
La Figura 19 muestra un mapa de restricción de pEJG108.
La Figura 20 muestra un mapa de restricción de pAILo24.
La Figura 21 muestra un mapa de restricción de pAILo28.
La Figura 22 muestra un mapa de restricción de pMJ04.
La Figura 23 muestra un mapa de restricción de pMJ06.
La Figura 24 muestra un mapa de restricción de pMJ09.
La Figura 25 muestra un mapa de restricción de pEmY10.
La Figura 26 muestra un mapa de restricción de pSMA1155.
La Figura 27 muestra un mapa de restricción de pEJG 11 O.
La Figura 28 muestra un mapa de restricción de pEJG114.
La Figura 29 muestra un mapa de restricción de pCW076.
La Figura 30 muestra un mapa de restricción de pCW078.
La Figura 31 muestra un mapa de restricción de pEJG97. Las Figuras 32A e 32B muestran la secuencia de AON genómico y la secuencia de aminoácidos deducida de una beta glucosidasa de Aspergillus fumigatus (SEC ID nO: 75 y 76, respectivamente) . El péptido señal predicho está subrayado e intrones predichos están en cursiva.
La Figura 33 muestra un mapa de restricción de pEJG107.
La Figura 34 muestra el efecto de un polipéptido Thíela via le"estris GH61 B con actividad de mejora celulolítica (1 mg/g PCS) en la hidrólisis de PCS (1% p/v) por caldo de fermentación de Trichoderma reeseí que expresa actividad y una beta-glucosidasa de Aspergillus fumigalus (5 mg/g PCS) a 50-60Q C.
La Figura 35 muestra el efecto de un polipéptido de Thiela via te"estris GH61B con actividad de mejora celulolitica... [Seguir leyendo]
Reivindicaciones:
1. Polipéptido aislado con aclividad de mejora celulolílica, y con una secuencia de aminoácidos que liene al menos 85%, más preferiblemente al menos 90%, de la forma más preferible al menos 95%, e incluso de forma más preferible al menos 97% de identidad con los aminoácidos 18 a 240 de la SEC ID nO: 4.
2. Polipéptido según la reivindicación 1, que está codificado por el polinucleótido contenido en el plásmido pTter61C que está contenido en E. col; NRRL B-30813.
3. Polinucleótido aislado comprendiendo una secuencia de nucleótidos que codifica el polipéptido según cualquiera de las reivindicaciones 1 02.
4. Construcción de ácidos nucleicos comprendiendo el polinucleótido según la reivindicación 3 unido operativamente a una o más secuencias de control que dirigen la producción del polipéptido en un huésped de expresión.
5. Vector de expresión recombinante comprendiendo la construcción de ácidos nucleicos según la reivindicación 4.
6. Célula huésped recombinante comprendiendo la construcción de ácidos nucleicos según la reivindicación 4.
7. Método para la producción del polipéptido según cualquiera de las reivindicaciones 1 o 2, comprendiendo (a) cultivo de una célula huésped, que comprende una construcción de ácidos nucleicos que comprende una secuencia de nucleólidos que codifica el polipéptido bajo cond iciones propicias para la producción del polipéptido; y (b) recuperación del polipéptido.
8. Composición de detergente que comprende el polipéptido con actividad de mejora celulolitica según cualquiera de las reivindicaciones 1-2, una actividad celulolitica y un tensioactivo.
9. Método para degradación o conversión de un material celulósico, comprendiendo: tratamiento del material celulósico con una cantidad eficaz de una proteína celulolitica en presencia de una cantidad eficaz del polipéptido con actividad de mejorado celulolítica según cualquiera de las reivindicaciones 1 o 2, donde la presencia del polipéptido con actividad de mejora celulolílica aumenla la degradación del malerial celulósico en comparación con la ausencia del polipéplido con actividad de mejora celulolitica.
10. Método según la reivindicación 9, donde una o más enzimas celuloliticas se seleccionan del grupo que consiste en una celulasa, endoglucanasa, celobiohidrolasa y beta-glucosidasa.
11. Método para producir una sustancia orgánica, que comprende:
(a) sacarificar un material celulósico con una cantidad efectiva de una proteína celulolílica en presencia de una cantidad efectiva del polipéptido con actividad de mejora celulolítica según cualquiera de las reivindicaciones 1-2, donde la presencia del polipéptico con actividad de mejora celulol1tica aumenta la degradación del material celulósico en comparación con la ausencia del polipéptido con actividad de mejora celulolitica;
(b) fermentar el material celulósico sacarificado del paso (a) con uno o más microorganismos de fermentación;
y
(c) recuperar la sustancia orgán ica de la fermentación
12. Método según la reivindicación 11, donde el material celulósico son restos de maíz.
13. Método según cualquiera de las reivindicaciones 11-12, donde una o más enzimas celulolíticas son seleccionadas del grupo que consiste en celulasa, endoglucanasa, celobiohidrolasa y beta-glucosidasa.
14. Método según cualquiera de las reivindicaciones 11-13, donde la sustancia orgánica es un alcohol, ácido orgánico, cetona, aminoácido o gas.
15. Método según la reivindicación 14, donde el alcohol es arabinitol, butanol, etanol, glicerol, metanol, 1, 3-propanediol, sorbitol o xilitol.
Patentes similares o relacionadas:
Sistema de expresión bacteriano cistrónico doble, del 25 de Marzo de 2020, de LUPIN LIMITED: Un procedimiento para la producción de un anticuerpo o un fragmento del mismo que comprende las etapas de: (i) transformar una célula hospedadora bacteriana […]
Partículas de transducción no replicativas y sistemas indicadores basados en partículas de transducción, del 15 de Enero de 2020, de Geneweave Biosciences Inc: Un sistema de empaquetamiento de células bacterianas para empaquetar una molécula de ácido nucleico indicadora en una partícula de transducción no replicativa (NRTP) para su introducción […]
Método de construcción de biblioteca de péptidos y vectores relacionados, del 1 de Enero de 2020, de Hunan Zonsen Peplib Biotech Co., Ltd: Método integrado de construcción de una biblioteca de péptidos completa que contiene todos los péptidos posibles para el tamaño específico, comprendiendo el método: (i) […]
 Producción recombinante de péptidos, del 25 de Septiembre de 2019, de BASF SE: Proteina precursora que comprende una secuencia repetitiva escindible de elementos de peptido (Pep) deseados y elementos de peptido auxiliar […]
Producción recombinante de péptidos, del 25 de Septiembre de 2019, de BASF SE: Proteina precursora que comprende una secuencia repetitiva escindible de elementos de peptido (Pep) deseados y elementos de peptido auxiliar […]
Transporte de proteínas basado en bacterias, del 14 de Agosto de 2019, de Universität Basel: Un vector que comprende, en la dirección 5' a 3': un promotor; una primera secuencia de ADN que codifica una señal de transporte procedente […]
Sistema de expresión y secreción, del 26 de Junio de 2019, de F. HOFFMANN-LA ROCHE AG: Una molécula de ácido nucleico que codifica un primer polipéptido y un segundo polipéptido, enlazada de forma funcional a una secuencia señal que codifica […]
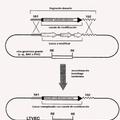 Producción de anticuerpos híbridos que contienen regiones variables humanas y regiones constantes de roedor, del 26 de Junio de 2019, de REGENERON PHARMACEUTICALS, INC.: Un procedimiento para modificar genéticamente un locus génico endógeno de la región variable de cadena pesada de inmunoglobulina en una célula madre embrionaria (ES) de […]
Producción de anticuerpos híbridos que contienen regiones variables humanas y regiones constantes de roedor, del 26 de Junio de 2019, de REGENERON PHARMACEUTICALS, INC.: Un procedimiento para modificar genéticamente un locus génico endógeno de la región variable de cadena pesada de inmunoglobulina en una célula madre embrionaria (ES) de […]
Síntesis microbiana de aldehídos y alcoholes correspondientes, del 17 de Junio de 2019, de Easel Biotechnologies, LLC: Un método para producir un alcohol, que comprende: cultivar una pluralidad de células microbianas en un medio de fermentación, en donde las […]