PEPTIDOS COMO INHIBIDORES DE LA SERINA PROTEASA NS3 DEL VIRUS DE LA HEPATITIS C.
Un compuesto, incluyendo enantiómeros, estereoisómeros, rotámeros,
tautómeros y racematos de dicho compuesto, y sales o solvatos farmacéuticamente aceptables de dicho compuesto, teniendo dicho compuesto la estructura general que se muestra en la Fórmula I:
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US01/22678.
Solicitante: SCHERING CORPORATION
CORVAS INTERNATIONAL, INC.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: PATENT DEPARTMENT - K-6-1 1990, 2000 GALLOPING HILL ROAD,KENILWORTH, NJ 07033-0530.
Inventor/es: NJOROGE, F., GEORGE, CHAN, TIN-YAU, LIU, YI-TSUNG, GANGULY, ASHIT, K., LOVEY, RAYMOND, G., BENNETT, FRANK, SAKSENA, ANIL, K., PIKE, RUSSELL, E., WANG, HAIYAN, PINTO, PATRICK, A., GIRIJAVALLABHAN, VIYYOOR MOOPIL, SANTHANAM,BAMA, CHEN,KEVIN,X, ARASAPPAN,ASHOK, VENKATRAMAN,SRIKANTH, PAREKH,TEJAL,N, ZHU,ZHAONING, BOGEN,STEPHANE,L, VACCARO,HENRY,A, JAO,EDWIN,E, MC CORMICK,JINPING,L, WU,WANLI, HENDRATA,SISKA, HUANG,YUHUA, KEMP,SCOTT JEFFREY, LEVY,ODILE ESTHER, LIM-WILBY,MARGUETITA, TAMURA,SUSAN Y.
Fecha de Publicación: .
Fecha Concesión Europea: 17 de Marzo de 2010.
Clasificación Internacional de Patentes:
- C07K5/08 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 5/00 Péptidos con hasta cuatro aminoácidos en una secuencia totalmente determinada; Sus derivados. › Tripéptidos.
- C07K7/02 C07K […] › C07K 7/00 Péptidos con 5 a 20 aminoácidos en una secuencia totalmente determinada; Sus derivados. › Péptidos lineales que contienen al menos un enlace peptídico anormal.
Clasificación PCT:
- C07K1/00 C07K […] › Procedimientos generales de preparación de péptidos.
Clasificación antigua:
- C07K C07 […] › PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00).
Fragmento de la descripción:
Péptidos como inhibidores de la serina proteasa NS3 del virus de la hepatitis C.
Campo de la invención
La presente invención se refiere a inhibidores novedosos de proteasa del virus de la hepatitis C ("VHC"), a composiciones farmacéuticas que contienen uno o más de dichos inhibidores, a métodos para preparar dichos inhibidores y al uso de dichos inhibidores para tratar la hepatitis C y trastornos relacionados. Esta invención revela específicamente compuestos peptídicos novedosos como inhibidores de la serina proteasa NS3/NS4a del VHC.
Antecedentes de la invención
El virus de la hepatitis C (VHC) es un virus de ARN monocatenario de sentido (+) que se ha implicado como principal agente causante de la hepatitis no A, no B (HNANB), en particular en HNANB asociada con la sangre (BB-HNANB) (véase la Publicación de Solicitud de Patente Internacional No. WO 89/04669 y Publicación de Solicitud de Patente Europea No. EP 381 216). Debe distinguirse la HNANB de otros tipos de enfermedades hepáticas virales, tales como el virus de la hepatitis A (VHA), el virus de la hepatitis B (VHB), el virus de la hepatitis delta (VHD), el citomegalovirus (CMV) y el virus de Epstein-Barr (VEB), así como de otras formas de enfermedad hepática tales como el alcoholismo y la cirrosis biliar primaria.
Recientemente, se ha identificado, clonado y expresado una proteasa del VHC necesaria para el procesamiento de polipéptidos y la replicación viral (véase, por ej., la Patente de los Estados Unidos No. 5.712.145). Esta poliproteína de aproximadamente 3000 aminoácidos contiene, desde el extremo amino terminal hasta el extremo carboxilo terminal, una proteína de nucleocápside (C), proteínas de envoltura (E1 y E2) y varias proteínas no estructurales (NS1, 2, 3, 4a, 5a y 5b). NS3 es una proteína de aproximadamente 68 kda, codificada por aproximadamente 1893 nucleótidos del genoma del VHC, y posee dos dominios distintos: (a) un dominio de serina proteasa formado por aproximadamente 200 de los aminoácidos N-terminales; y (b) un dominio de ATPasa dependiente del ARN en el extremo C-terminal de la proteína. La proteasa NS3 se considera miembro de la familia de quimiotripsinas debido a las similitudes en la secuencia de la proteína, la estructura tridimensional general y el mecanismo de catálisis. Otras enzimas similares a la quimiotripsina son la elastasa, el factor Xa, la trombina, la tripsina, la plasmina, la uroquinasa, tPA y PSA. La serina proteasa NS3 del VHC es responsable de la proteólisis del polipéptido (poliproteína) en las uniones NS3/NS4a, NS4a/NS4b, NS4b/NS5a y NS5a/NS5b y de este modo es responsable de generar cuatro proteínas virales durante la replicación viral. Esto ha hecho de la serina proteasa NS3 del VHC un blanco atractivo para la quimioterapia antiviral.
Se ha determinado que la proteína NS4a, un polipéptido de aproximadamente 6 kda, es un co-factor para la actividad de la serina proteasa NS3. La auto-ruptura de la unión NS3/NS4a producida por la serina proteasa NS3/NS4a ocurre intramolecularmente (es decir, en cis) mientras que otros sitios de ruptura se procesan intermolecularmente (es decir, en trans).
El análisis de los sitios naturales de ruptura para la proteasa del VHC reveló la presencia de cisteína en P1 y serina en P1' y que estos residuos se conservan estrictamente en las uniones NS4a/NS4b, NS4b/NS5a y NS5a/NS5b. La unión NS3/NS4a contiene una treonina en P1 y una serina en P1'. La sustitución Cis
Los inhibidores de la proteasa del VHC que se han informado incluyen antioxidantes (véase la Publicación de Solicitud de Patente Internacional No. WO 98/14181), ciertos péptidos y análogos de péptidos (véase la Publicación de Solicitud de Patente Internacional No. WO 98/17679, Landro et al. (1997) Biochem. 36:9340-9348, Ingallinella et al. (1998) Biochem. 37:8906-8914, Llinàs-Brunet et al. (1998) Bioorg. Med. Chem. Lett. 8:1713-1718), inhibidores basados en el polipéptido eglina c de 70 aminoácidos (Martin et al. (1998) Biochem. 37:11459-11468, inhibidores por afinidad seleccionados del inhibidor de tripsina secretora pancreática humana (hPSTI-C3) y de repertorios de minicuerpos (MBip) (Dimasi et al. (1997) J. Virol. 71:7461-7469), cVHE2 (un fragmento de anticuerpo de dominio variable "camelizado") (Martin et al.(1997) Proten Eng. 10:607-614), y a1-antiquimiotripsina (ACT) (Elzouki et al.) (1997) J. Hepat. 27:42-28). Recientemente se ha descubierto una ribozima diseñada para destruir selectivamente el ARN del virus de la hepatitis C (véase BioWorld Today 9(217): 4 (10 de noviembre de 1998)).
Además, se hace referencia a las publicaciones de PCT, No. WO 98/17679, publicada el 30 de abril de 1998 (Vertex Pharmaceuticals Incorporated); WO 98/22496, publicada el 28 de mayo de 1998 (F. Hoffmann-La Roche AG); y WO 99/07734, publicada el 18 de febrero de 1999 (Boehringer Ingelheim Canada Ltd.).
El VHC se ha implicado en la cirrosis hepática y en la inducción de carcinoma hepatocelular. El pronóstico para pacientes que sufren de infección por VHC actualmente es pobre. La infección por VHC es más difícil de tratar que otras formas de la hepatitis debido a la falta de inmunidad o remisión asociada con la infección por VHC. Datos actuales indican un índice de supervivencia inferior al 50% a los cuatro años posteriores al diagnóstico de cirrosis. Los pacientes con diagnóstico de carcinoma hepatocelular extirpable localizado tienen una tasa de supervivencia del 10-30%, mientras que aquellos con carcinoma hepatocelular no extirpable localizado tienen una tasa de supervivencia a los cinco años inferior al 1%.
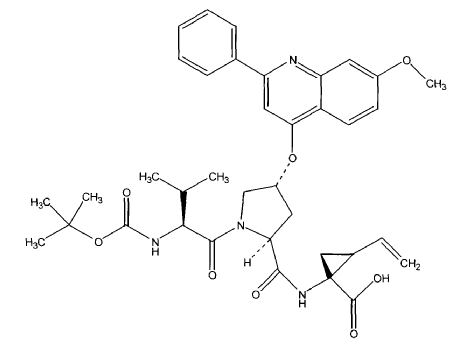
Se hace referencia a A. Marchetti et al, Synlett, S1, 1000-1002 (1999), que describe la síntesis de análogos bicíclicos de un inhibidor de proteasa NS3 del VHC. Un compuesto descrito allí tiene la fórmula:
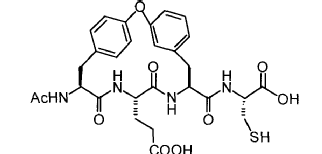
Se hace referencia, además, a W. Han et al, Bioorganic & Medicinal Chem. Lett, (2000) 10, 711-713, que describe la preparación de ciertas a-cetoamidas, a-cetoésteres y a-dicetonas que contienen grupos funcionales alilo y etilo.
Se hace referencia, además, a la WO 00/09558 (Cesionario: Boehringer Ingelheim Limited; Publicada el 24 de febrero de 2000) que describe derivados peptídicos de fórmula:
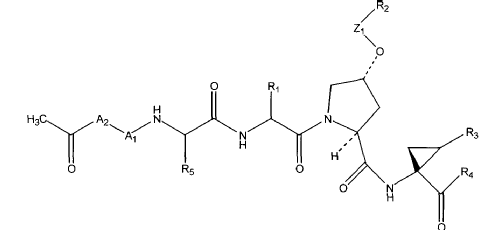
donde los diversos elementos se definen en ella. Un compuesto ilustrativo de esa serie es:
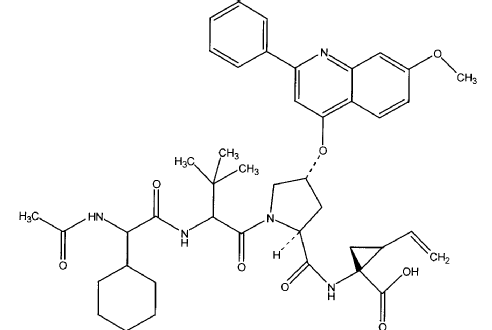
Se hace referencia, además, al documento WO 00/09543 (Cesionario: Boehringer Ingelheim Limited; publicada el 24 de febrero 2000) que divulga derivados peptídicos de fórmula:
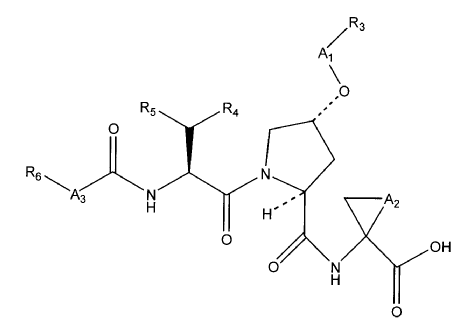
donde los diversos elementos se definen en ella. Un compuesto ilustrativo de esa serie es:
Los tratamientos actuales para la hepatitis C incluyen tratamiento con interferón-a (INFa) y tratamiento combinado con ribavirina e interferón. Véase, por ej., Beremguer et al. (1998) Proc. Assoc. Am. Physicians 110(2):98-112. Estos tratamientos adolecen de una baja tasa de respuesta prolongada y frecuentes efectos colaterales. Véase, por ej., Hoofnagle et al. (1997) N. Engl. J. Med. 336:347. Actualmente, no se dispone de ninguna...
Reivindicaciones:
1. Un compuesto, incluyendo enantiómeros, estereoisómeros, rotámeros, tautómeros y racematos de dicho compuesto, y sales o solvatos farmacéuticamente aceptables de dicho compuesto, teniendo dicho compuesto la estructura general que se muestra en la Fórmula I:
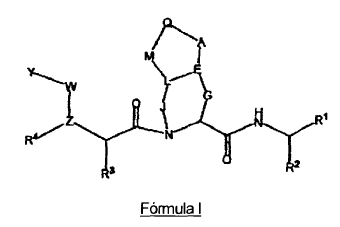
en la que:
Y se selecciona del grupo que consiste en los siguientes restos: alquilo, alquil-arilo, heteroalquilo, heteroarilo, aril-heteroarilo, alquil-heteroarilo, cicloalquilo, alquiloxi, alquil-ariloxi, ariloxi, heteroariloxi, heterocicloalquiloxi, cicloalquiloxi, alquilamino, arilamino, alquil-arilamino, arilamino, heteroarilamino, cicloalquilamino y heterocicloalquilamino, con la salvedad de que Y puede estar sustituido en forma opcional con X11 o X12;
X11 es alquilo, alquenilo, alquinilo, cicloalquilo, cicloalquil-alquilo, heterociclilo, heterociclilalquilo, arilo, alquilarilo, arilalquilo, heteroarilo, alquilheteroarilo o heteroarilalquilo, con la salvedad de que X11 puede además estar sustituido en forma opcional con X12;
X12 es hidroxi, alcoxi, ariloxi, tio, alquiltio, ariltio, amino, alquilamino, arilamino, alquilsulfonilo, arilsulfonilo, alquilsulfonamido, arilsulfonamido, carboxi, carbalcoxi, carboxamido, alcoxicarbonilamino, alcoxicarboniloxi, alquilureido, arilureido, halógeno, ciano o nitro, con la salvedad de que dicho alquilo, alcoxi y arilo pueden además estar sustituidos en forma opcional con restos independientemente seleccionados de X12;
R1 es COCONR9R10, en el que R9 es H, R10 es H, R14, [CH(R1')]pCOOR11, [CH(R1')]pCONR12R13, [CH(R1')]pSO2R11, [CH(R1')]pSO2NR12R13, [CH(R1')]pCOR11, CH(R1')CONHCH(R2')COOR11, CH(R1')CONHCH(R2')CONR12R13 o CH(R1')CONHCH(R2')(R'), donde R1', R2', R11, R12 y R13 se seleccionan en forma independiente del grupo que consiste en H, alquilo, arilo, heteroalquilo, heteroarilo, cicloalquilo, alquil-arilo, alquil-heteroarilo, aril-alquilo y heteroaralquilo, y donde R14 es H, alquilo, arilo, heteroalquilo, heteroarilo, cicloalquilo, alquil-arilo, alquil-heteroarilo, aril-alquilo, alquenilo, alquinilo o heteroaralquilo;
Z se selecciona de O, N, CH o CR;
W puede estar presente o ausente, y si W está presente, W se selecciona de C=O, C=S, C(=N-CN) o SO2;
Q puede estar presente o ausente, y cuando Q está presente, Q es CH, N, P, (CH2)p, (CHR)P, (CRR')P, O, NR, S, o SO2; y cuando Q está ausente, M puede estar presente o ausente; cuando Q y M están ausentes, A está directamente unido a L;
A es O, CH2, (CHR)P, (CHR-CHR')p, (CRR')p, NR, S, SO2 o un enlace;
E es CH, N, CR, o un doble enlace hacia A, L o G;
G puede estar presente o ausente, y cuando G está presente, G es (CH2)P, (CHR)P o (CRR')P; y cuando G está ausente, J está presente y E está directamente conectado al átomo de carbono de la Fórmula I al que está unido G;
J puede estar presente o ausente, y cuando J está presente, J es (CH2)P, (CHR)P, o (CRR')p, SO2, NH, NR u O; y cuando J está ausente, G está presente y E está directamente unido a N como se muestra en la Fórmula I unido a J;
L puede estar presente o ausente, y cuando L está presente, L es CH, CR, O, S o NR; y cuando L está ausente, entonces M puede estar presente o ausente; y si M está presente cuando L está ausente, entonces M está directa e independientemente unido a E, y J está directa e independientemente unido a E;
M puede estar presente o ausente, y cuando M está presente, M es O, NR, S, SO2, (CH2)P, (CHR)P(CHR-CHR') o (CRR')P;
p es un número de 0 a 6; y
R, R1, R2, R3 y R4 se seleccionan en forma independiente del grupo que consiste en H; alquilo C1-C10; alquenilo C2-C10; cicloalquilo C3-C8; heterocicloalquilo C3-C8, alcoxi, ariloxi, alquiltio, ariltio, amino, amido, éster, ácido carboxílico, carbamato, urea, cetona, aldehído, ciano, nitro, halógeno; (cicloalquil)alquilo y (heterocicloalquil)alquilo, donde dicho cicloalquilo está formado por tres a ocho átomos de carbono, y cero a seis átomos de oxígeno, nitrógeno, azufre o fósforo, y dicho alquilo es de uno a seis átomos de carbono; arilo; heteroarilo; alquil-arilo; y alquil-heteroarilo;
donde dichos restos alquilo, heteroalquilo, alquenilo, heteroalquenilo, arilo, heteroarilo, cicloalquilo y heterocicloalquilo pueden estar sustituidos opcionalmente y químicamente en forma apropiada, refiriéndose dicho término "sustituido" a la sustitución opcional y químicamente apropiada con uno o más restos seleccionados del grupo que consiste en alquilo, alquenilo, alquinilo, arilo, aralquilo, cicloalquilo, heterocíclico, halógeno, hidroxi, tio, alcoxi, ariloxi, alquiltio, ariltio, amino, amido, éster, ácido carboxílico, carbamato, urea, cetona, aldehído, ciano, nitro, sulfonamido, sulfóxido, sulfona, sulfonil urea, hidrazida e hidroxamato;
además donde dicha unidad N-C-G-E-L-J-N representa una estructura anular cíclica de cinco o seis miembros con la salvedad de que cuando dicha unidad N-C-G-E-L-J-N representa una estructura anular cíclica de cinco miembros, o cuando la estructura del anillo bicíclico en la Fórmula I que comprende N, C, G, E, L, J, N, A, Q y M representa una estructura anular cíclica de cinco miembros, entonces dicha estructura anular cíclica de cinco miembros carece de un grupo carbonilo como parte del anillo cíclico.
2. El compuesto de la reivindicación 1, en el que R10 es H, R14, CH(R1')COOR11, CH(R1')CH(R1')COOR11, CH(R1')CONR12R13, CH(R1')CH(R1')CONR12R13, CH(R1')CH(R1')SO2R11, CH(R1')CH(R1')SO2NR12R13, CH(R1')CH(R1')COR11, CH(R1')CONHCHC(R2')COOR11, CH(R1')CONHCH(R2')CONR12R13 o CH(R1')CONHCH(R2'KR'), donde R1' es H o alquilo, y R2' es fenilo, fenilo sustituido, fenilo sustituido por heteroátomo, tiofenilo, cicloalquilo, piperidilo o piridilo.
3. El compuesto de la reivindicación 2, en el que R1' es H.
4. El compuesto de la reivindicación 3, en el que R11 es H, metilo, etilo, alilo, terc-butilo, bencilo, a-metilbencilo, a,a-dimetilbencilo, 1-metilcloropropilo o 1-metilciclopentilo;
R' es hidroximetilo o CH2CONR12R13;
R2' se selecciona en forma independiente del grupo que consiste en:
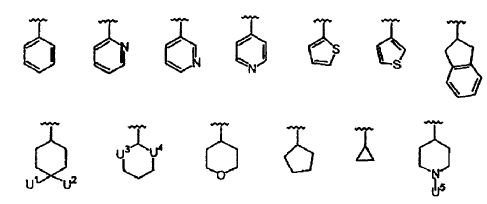
en los que:
U1 y U2 pueden ser iguales o diferentes y se seleccionan de H, F, CH2COOH, CH2COOMe, CH2CONH2, CH2CONHMe, CH2CONMe2, azido, amino, hidroxilo, amino sustituido, hidroxilo sustituido;
U3 y U4 pueden ser iguales o diferentes y se seleccionan de O y S;
U5 se selecciona de los restos que consisten en alquil sulfonilo, aril sulfonilo, heteroalquil sulfonilo, heteroaril sulfonilo, alquil carbonilo, aril carbonilo, heteroalquil carbonilo, heteroaril carbonilo, alcoxicarbonilo, ariloxicarbonilo, heteroariloxicarbonilo, alquilaminocarbonilo, arilaminocarbonilo, heteroarilaminocarbonilo o una combinación de los mismos;
y NR12R13 se seleccionan del grupo que consiste en:

en los que U6 es H, OH o CH2OH y
R14 se selecciona del grupo que consiste en: H, Me, Et, n-propilo, metoxi, ciclopropilo, n-butilo, 1-but-3-inilo, bencilo, a-metilbencilo, fenetilo, alilo, 1-but-3-enilo, OMe, ciclopropilmetilo.
5. El compuesto de la reivindicación 1, en el que R2 se selecciona del grupo que consiste en los siguientes restos:
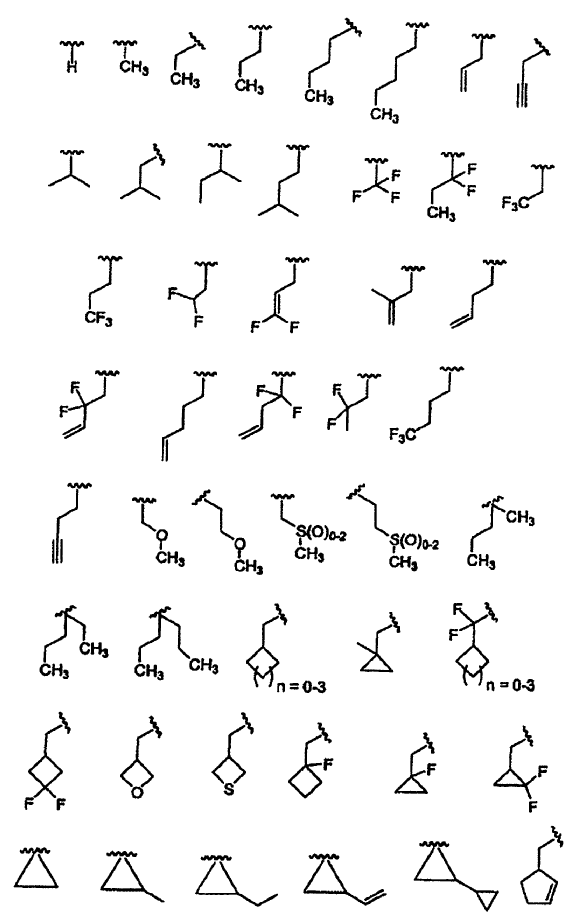
6. El compuesto de la reivindicación 5, en el que R3 se selecciona del grupo que consiste en:
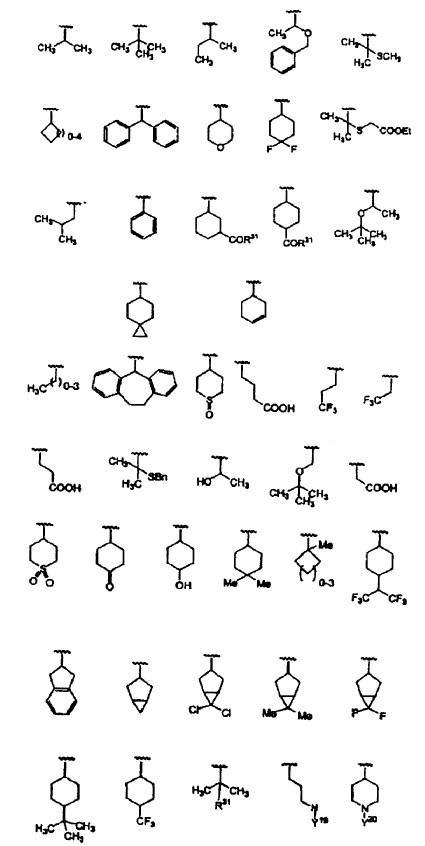
donde R31 = OH u O-alquilo;
Y19 se selecciona de los siguientes restos:
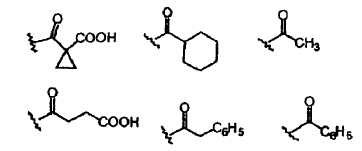
e Y20 se selecciona de los siguientes restos:
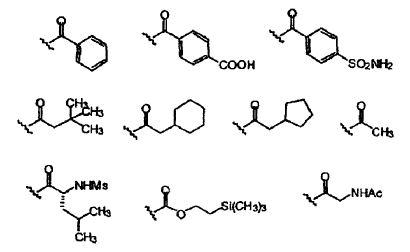
7. El compuesto de la reivindicación 6, en el que R3 se selecciona del grupo que consiste en los siguientes restos:
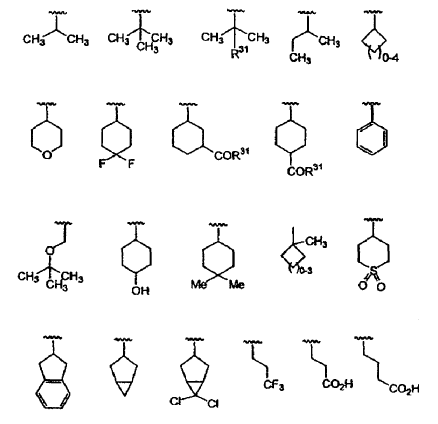
8. El compuesto de la reivindicación 7, en el que Z es N y R4 es H.
9. El compuesto de la reivindicación 8, en el que W es C=O.
10. El compuesto de la reivindicación 9, en el que Y se selecciona de los siguientes restos:
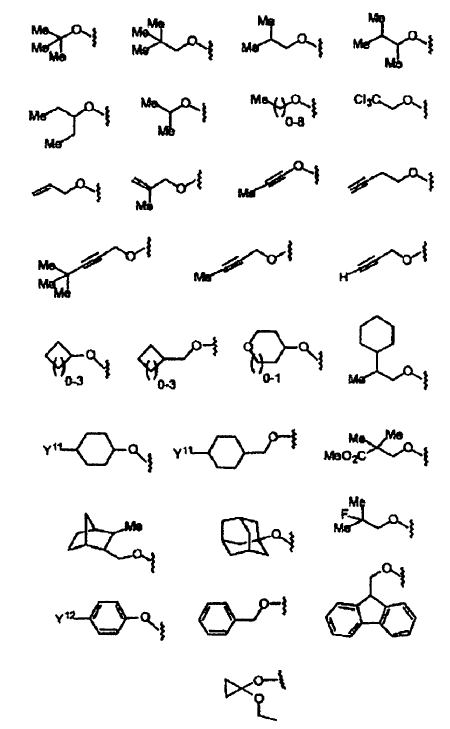
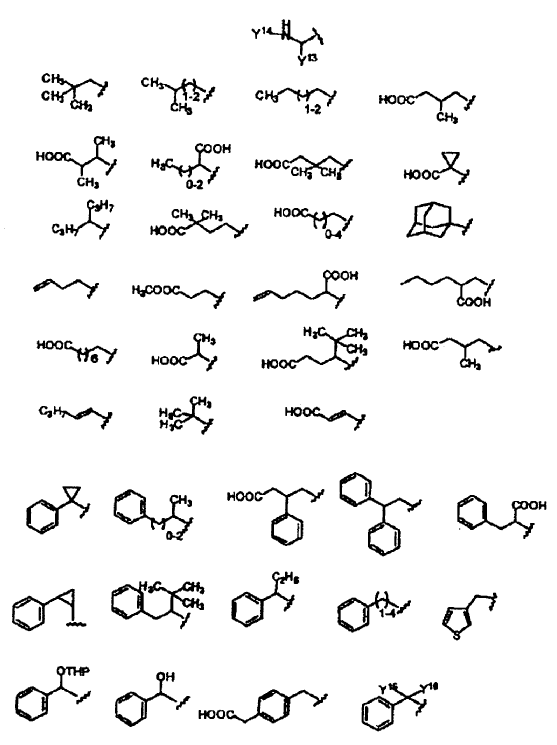
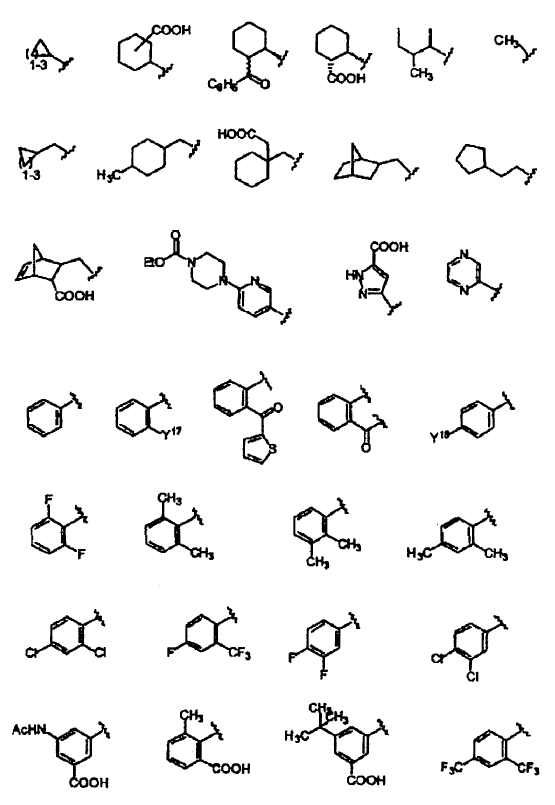
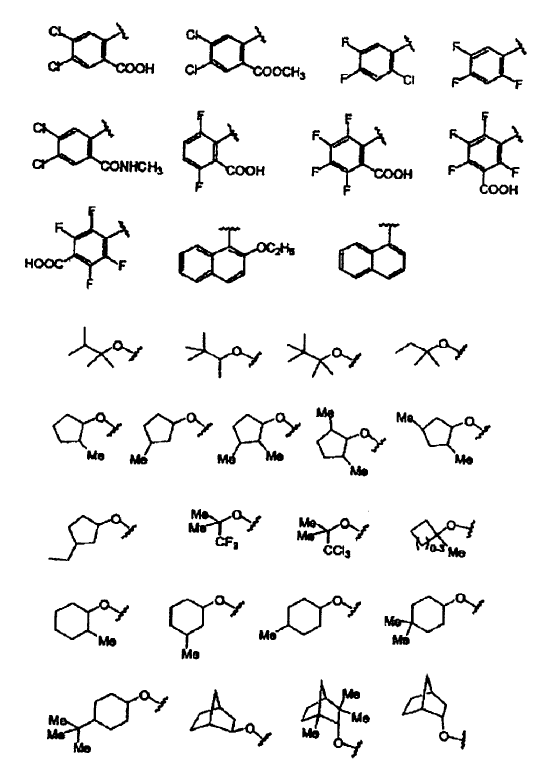
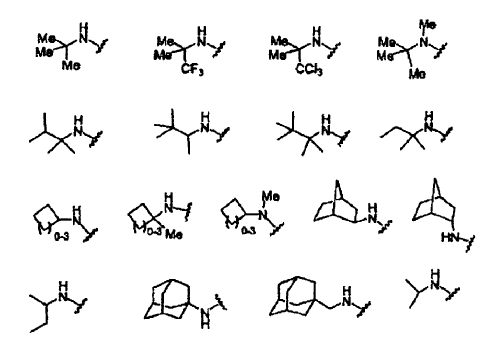
en los que:
Y11 se selecciona de H, COOH, COOEt, OMe, Ph, OPh, NHMe, NHAc, NHPh, CH(Me)2, 1-triazolilo, 1-imidazolilo y NHC2COOH;
Y12 se selecciona de H, COOH, COOMe, OMe, F, Cl o Br;
Y13 se selecciona de los siguientes restos:
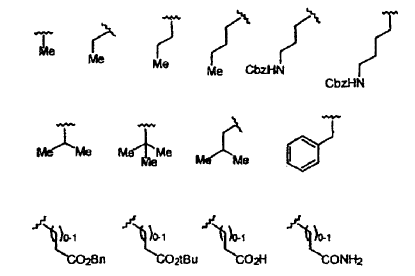
Y14 se selecciona de MeSO2, Ac, Boc, iBoc, Cbz, o Alloc;
Y15 e Y16 se seleccionan en forma independiente de alquilo, arilo, heteroalquilo y heteroarilo;
Y17 es CF3, NO2, CONH2, OH, COOCH3, OCH3, OC6H5, C6H5, COC6H5, NH2 o COOH; e
Y18 es COOCH3, NO2, N(CH3)2, F, OCH3, CH2COOH, COOH, SO2NH2 o NHCOCH3.
11. El compuesto de la reivindicación 10, en el que Y se selecciona del grupo que consiste en:
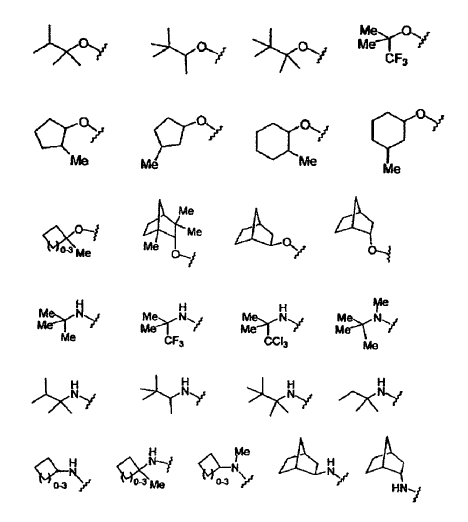
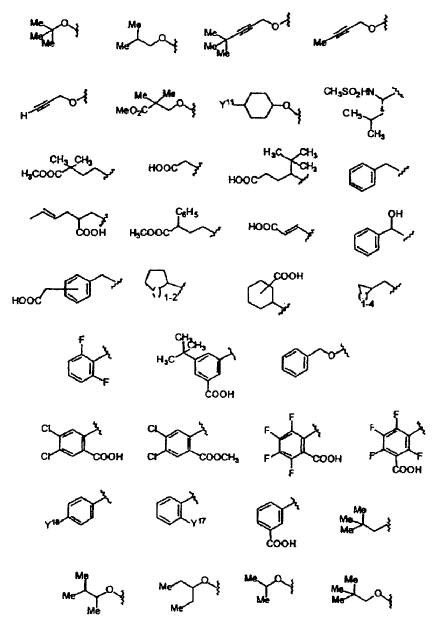
en los que:
Y17 = CF3, NO2, CONH2, OH, NH2 o COOH;
Y18 = F, COOH,
12. El compuesto de la reivindicación 11, en el que Y se selecciona del grupo que consiste en:
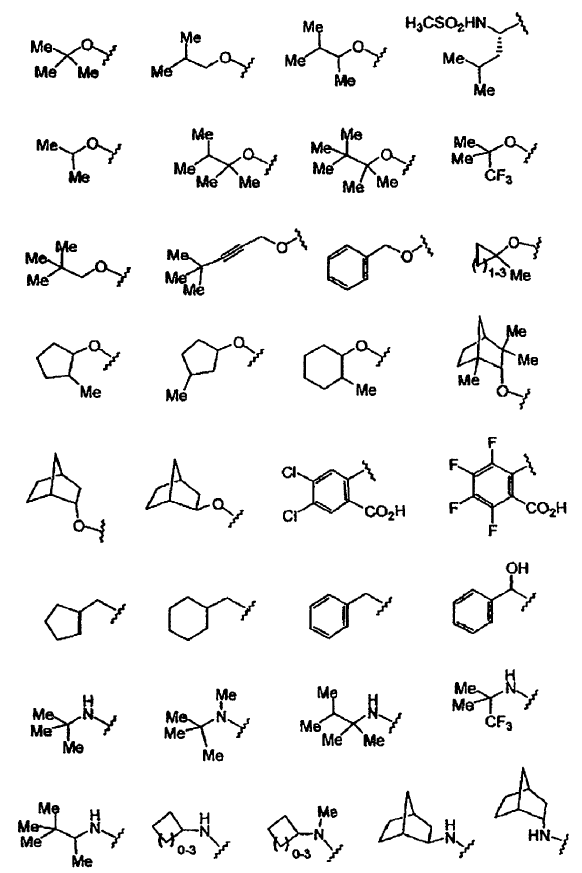
13. El compuesto de la reivindicación 12, en el que L y M están ausentes, y J está directamente unido a E.
14. El compuesto de la reivindicación 12, en el que L, J y M están ausentes y E está directamente unido a N.
15. El compuesto de la reivindicación 12, en el que G y M están ausentes.
16. El compuesto de la reivindicación 12, en el que el resto:
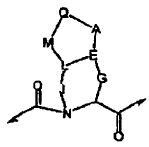

17. El compuesto de la reivindicación 16, en el que la estructura a se selecciona de las siguientes estructuras:

18. El compuesto de la reivindicación 16, en el que la estructura a es:
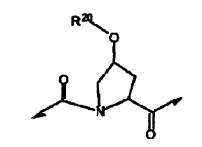
en la que R20 se selecciona de las siguientes estructuras:
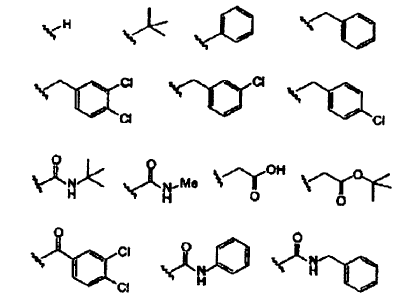
19. El compuesto de la reivindicación 16, en el que la estructura a es:
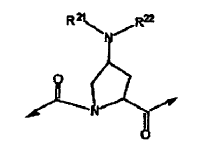
en la que R21 y R22 pueden ser iguales o diferentes y se seleccionan en forma independiente de las siguientes estructuras:
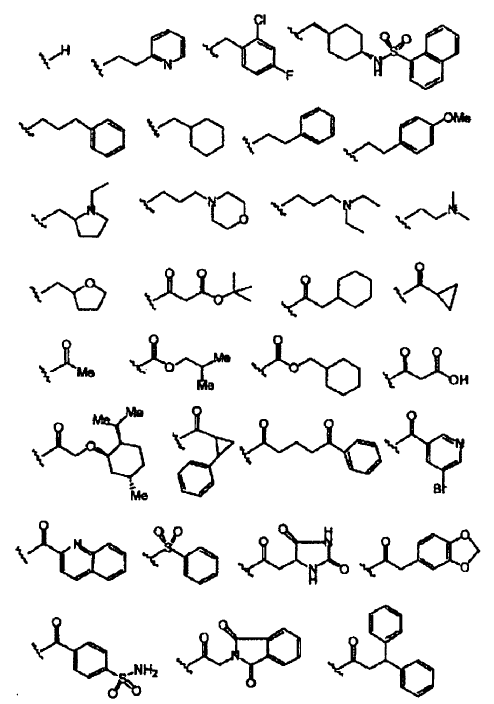
20. El compuesto de la reivindicación 16, en el que la estructura a se selecciona de las siguientes estructuras:

21. El compuesto de la reivindicación 12, en el que:

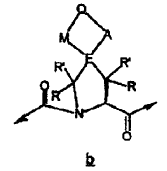
en la que Q puede estar presente o ausente, y si Q está ausente, M está directamente unido a A.
22. El compuesto de la reivindicación 21, en el que la estructura b se selecciona de las siguientes estructuras:
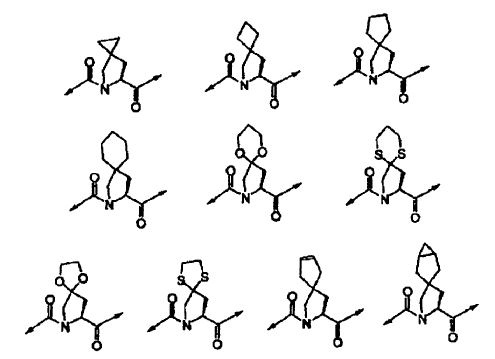
23. El compuesto de la reivindicación 12, en el que:
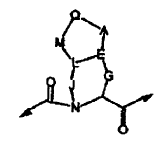
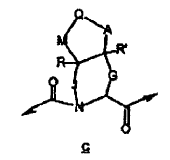
en la que G y J se seleccionan en forma independiente del grupo que consiste en (CH2)p, (CHR)p, (CHR-CHR')p y (CRR')p; A y M se seleccionan en forma independiente del grupo que consiste en O, S, SO2, NR, (CH2)p, (CHR)p, (CHR-CHR')p y (CRR')p; y Q es CH2, CHR, CRR', NH, NR, O, S, SO2, (CH2)p, (CHR)p y (CRR')p.
24. El compuesto de la reivindicación 23, en el que la estructura c se selecciona de las siguientes estructuras:
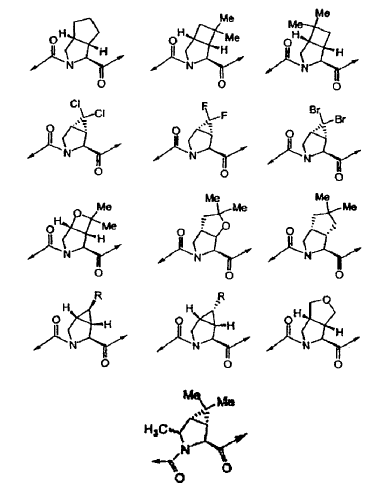
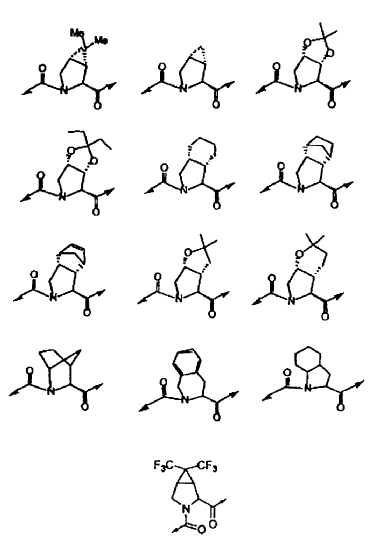
25. El compuesto de la reivindicación 12, en el que:
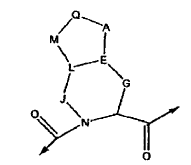
se selecciona de las siguientes estructuras:
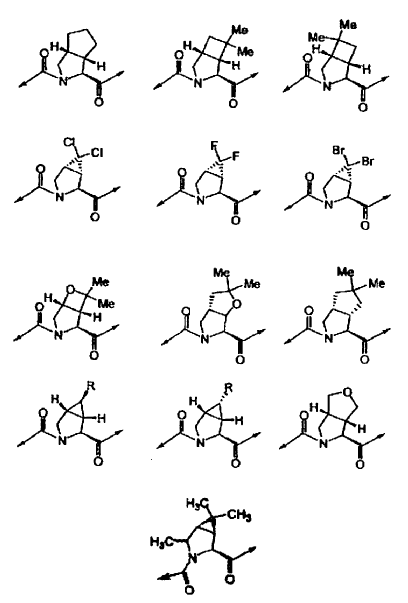
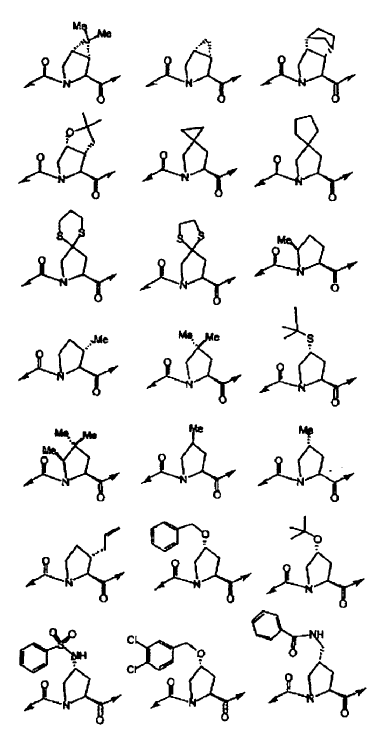
26. El compuesto de la reivindicación 25, en el que:
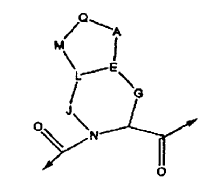
se selecciona de las siguientes estructuras:

27. Una composición farmacéutica que comprende como principio activo un compuesto de cualquiera de las reivindicaciones 1 a 26.
28. La composición farmacéutica de la reivindicación 27 para usar en el tratamiento de trastornos asociados con el VHC.
29. La composición farmacéutica de las reivindicaciones 27 o 28, que además contiene (a) un agente antiviral o (b) un interferón, o ambos (a) y (b).
30. La composición farmacéutica de la reivindicación 29, en la que dicho agente antiviral es ribavirina y dicho interferón es a-interferón o interferón pegilado.
31. El uso de un compuesto de cualquiera de las reivindicaciones 1 a 26 para la fabricación de un medicamento para tratar trastornos asociados con el VHC.
32. Un método para preparar una composición farmacéutica para el tratamiento de los trastornos asociados con el VHC, comprendiendo dicho método poner en íntimo contacto un compuesto de cualquiera de las reivindicaciones 1 a 26 y un vehículo farmacéuticamente aceptable.
33. Un compuesto que exhibe actividad inhibidora de la proteasa del VHC, incluyendo enantiómeros, estereoisómeros, rotámeros, tautómeros y racematos de dicho compuesto, y sales o solvatos farmacéuticamente aceptables de dicho compuesto, seleccionándose dicho compuesto de los compuestos de las estructuras enumeradas a continuación:
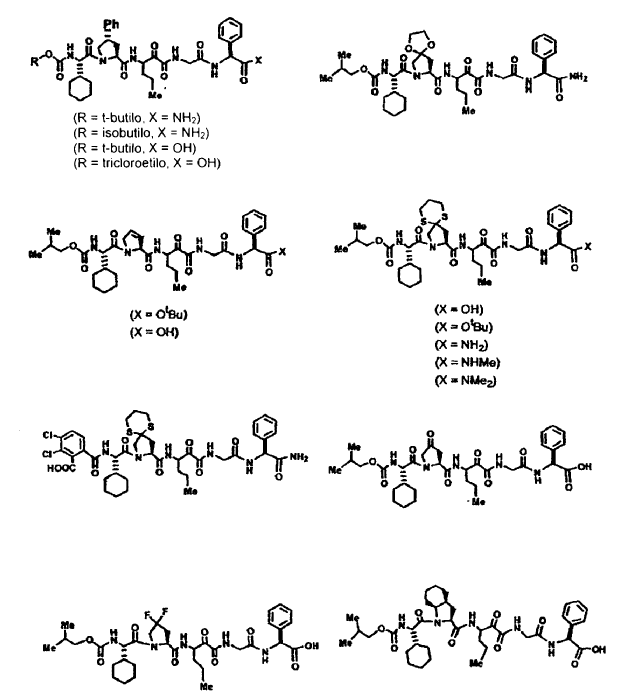
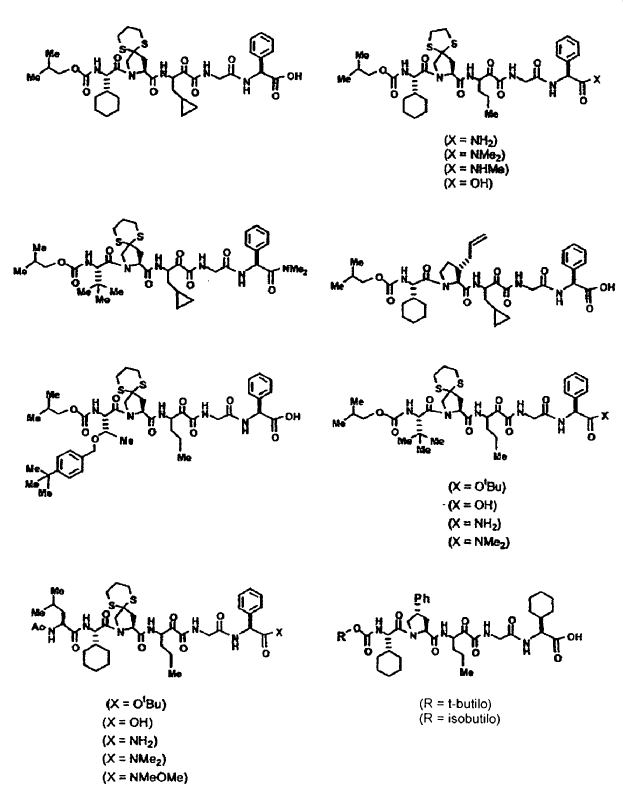
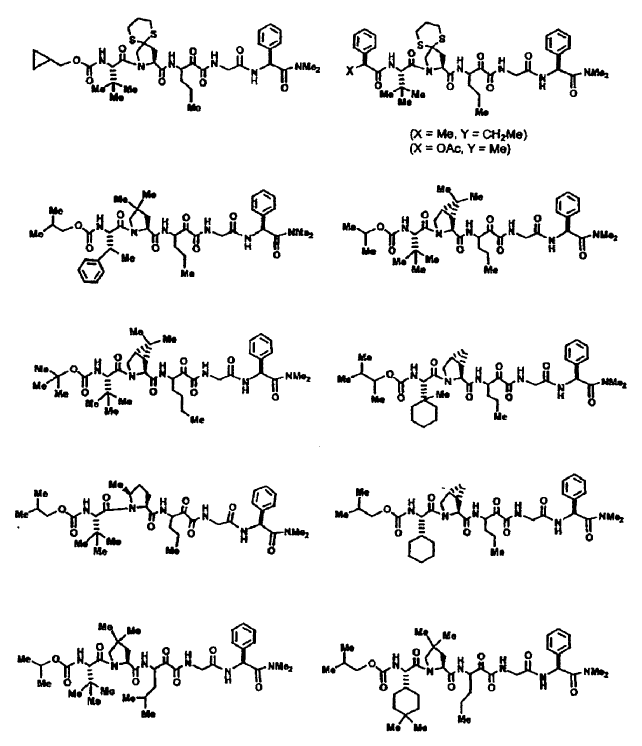
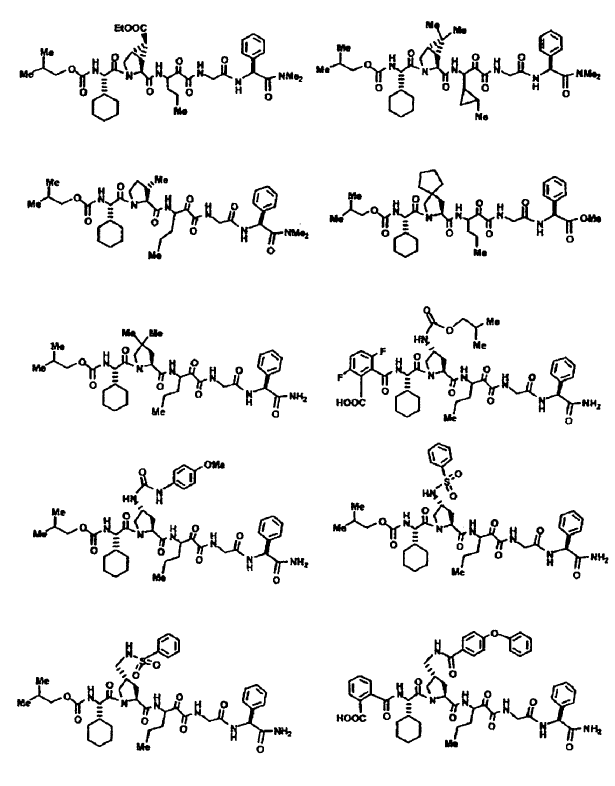
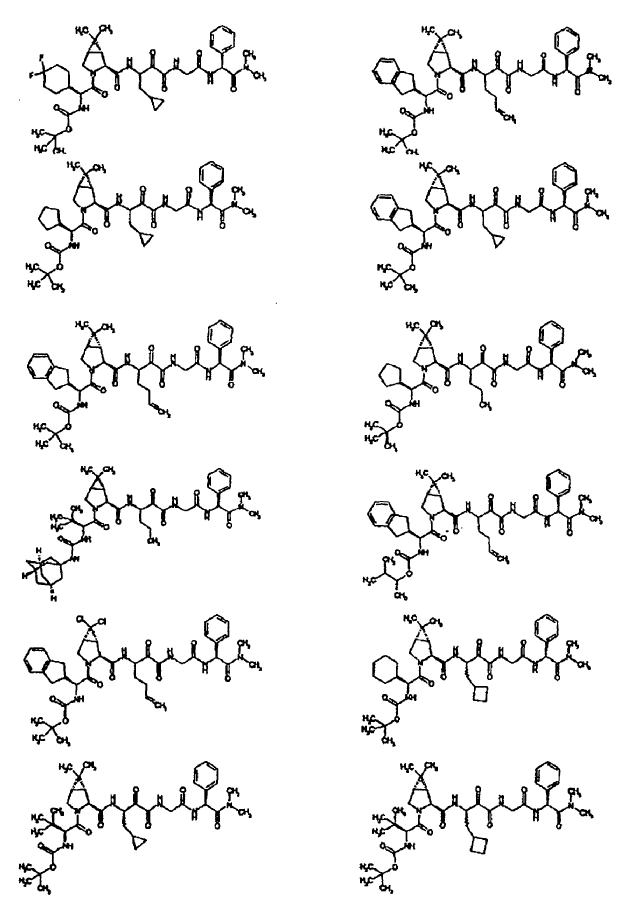
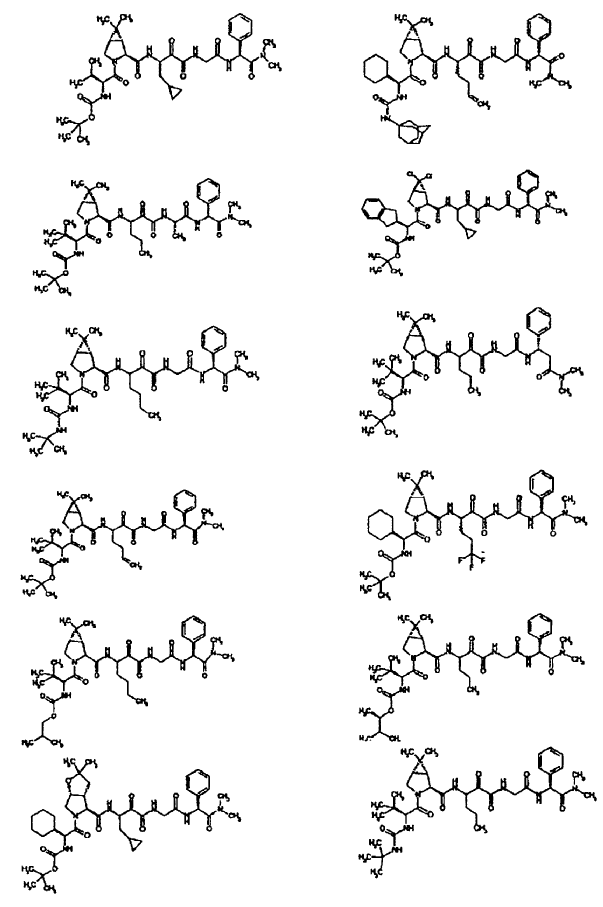
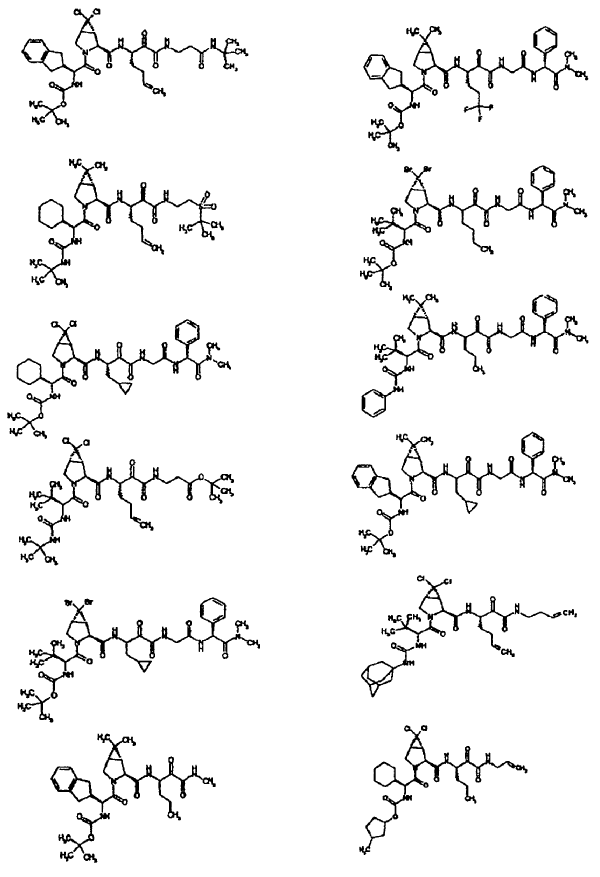
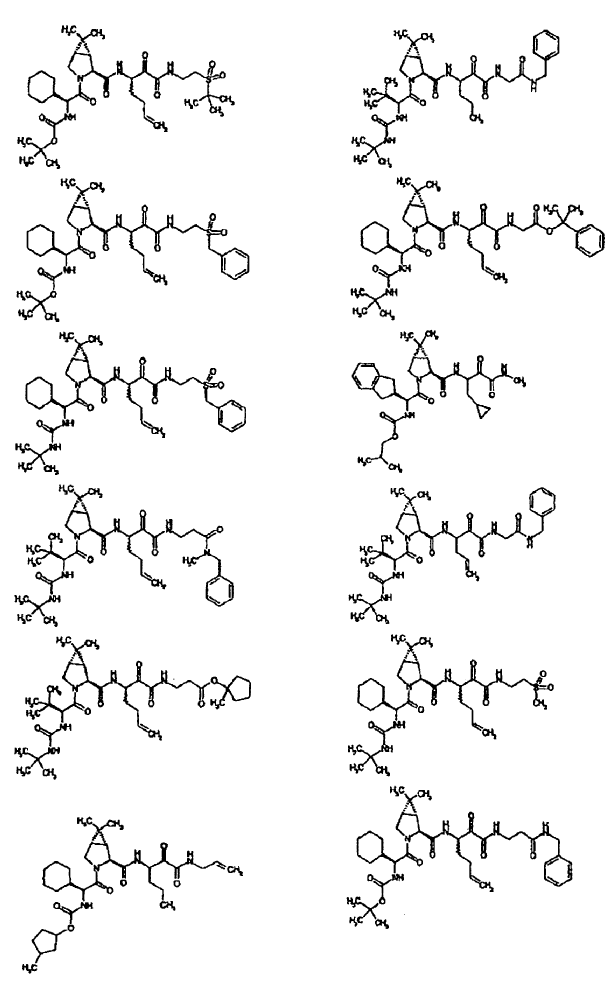
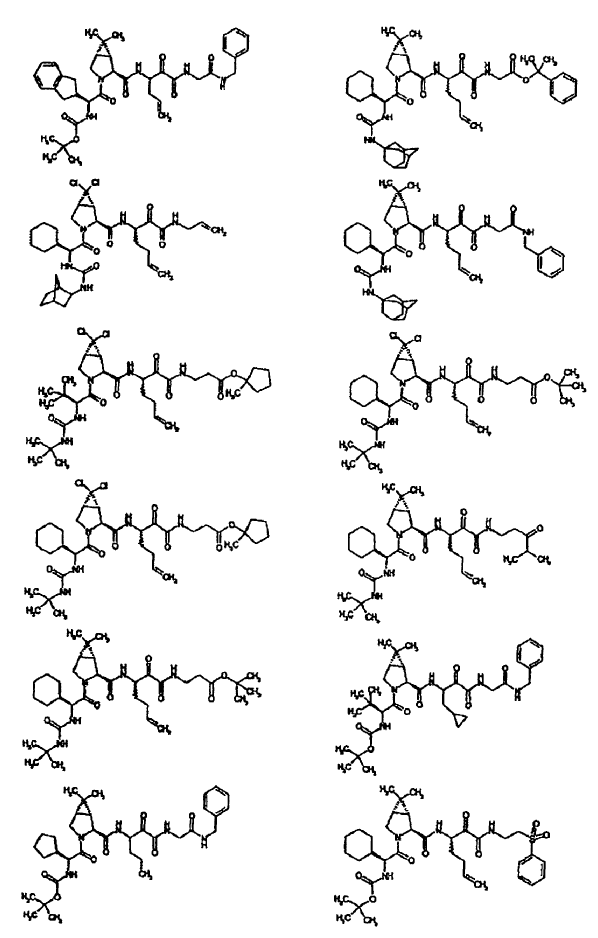
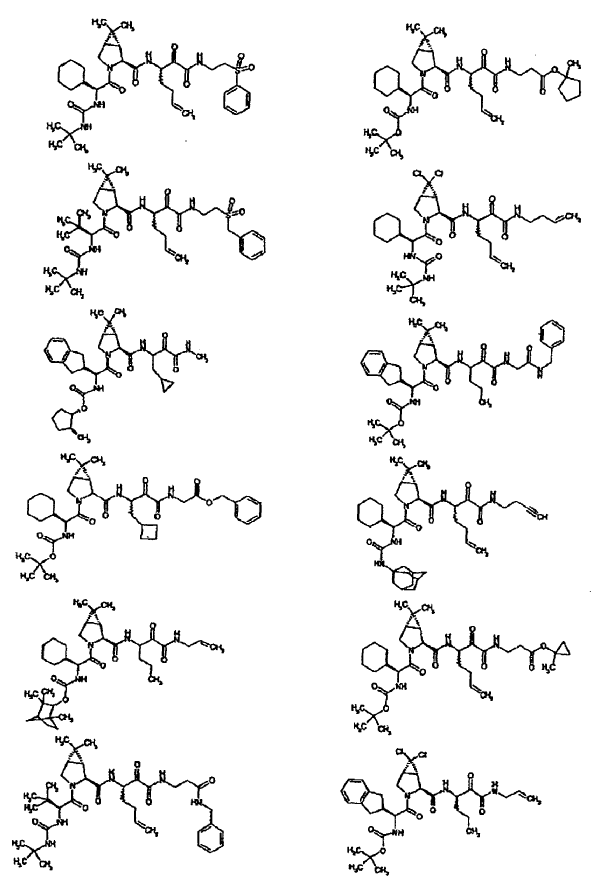
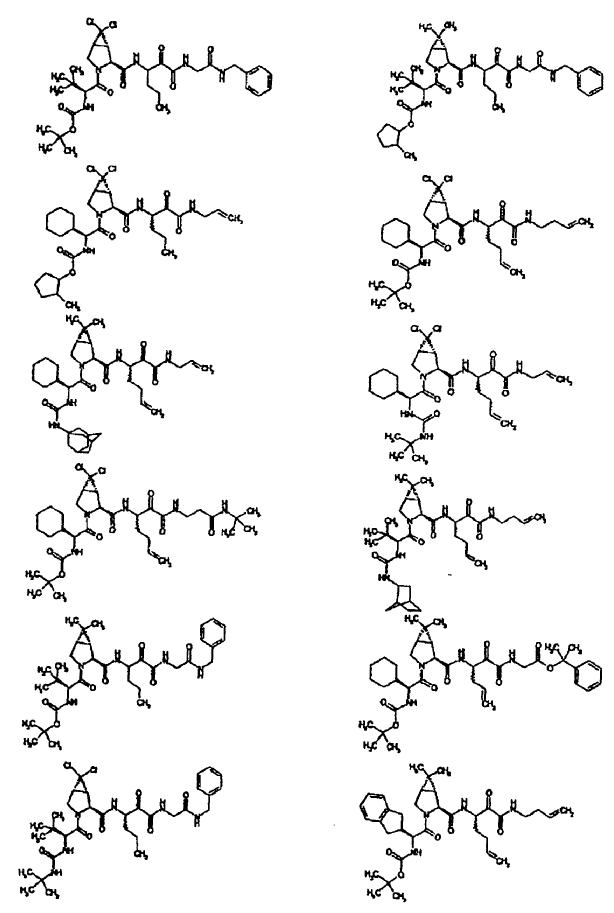
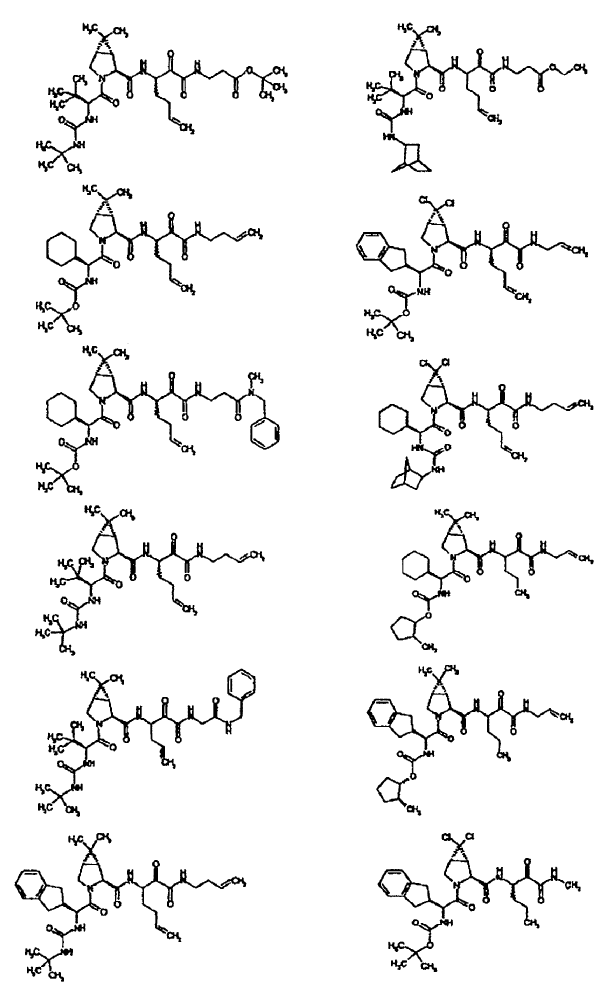
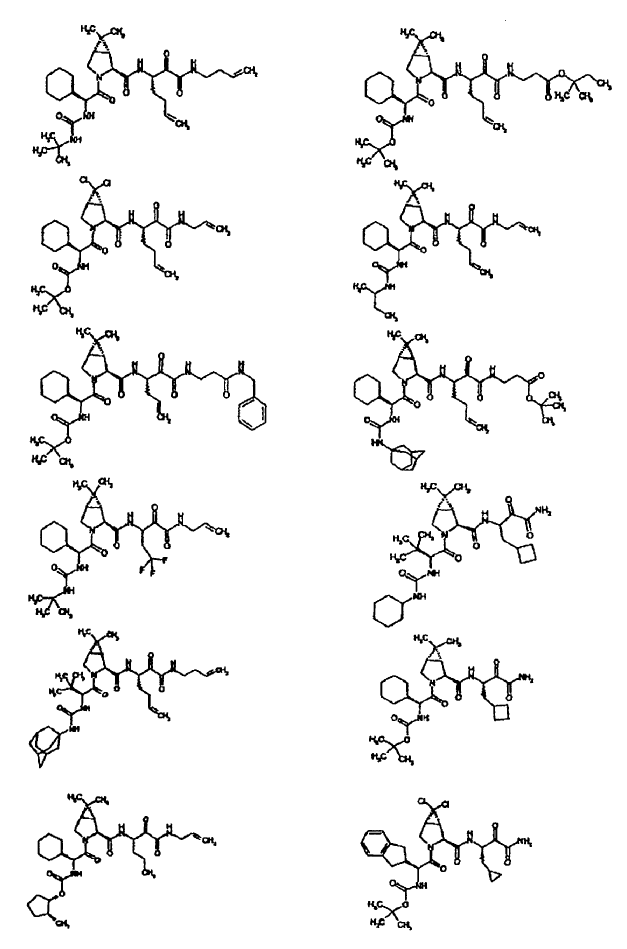

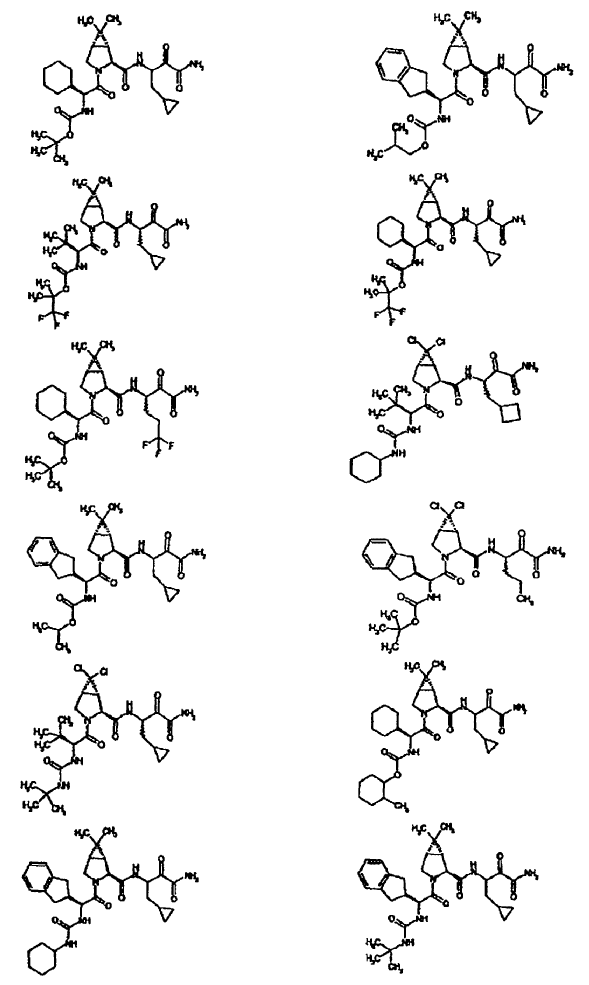
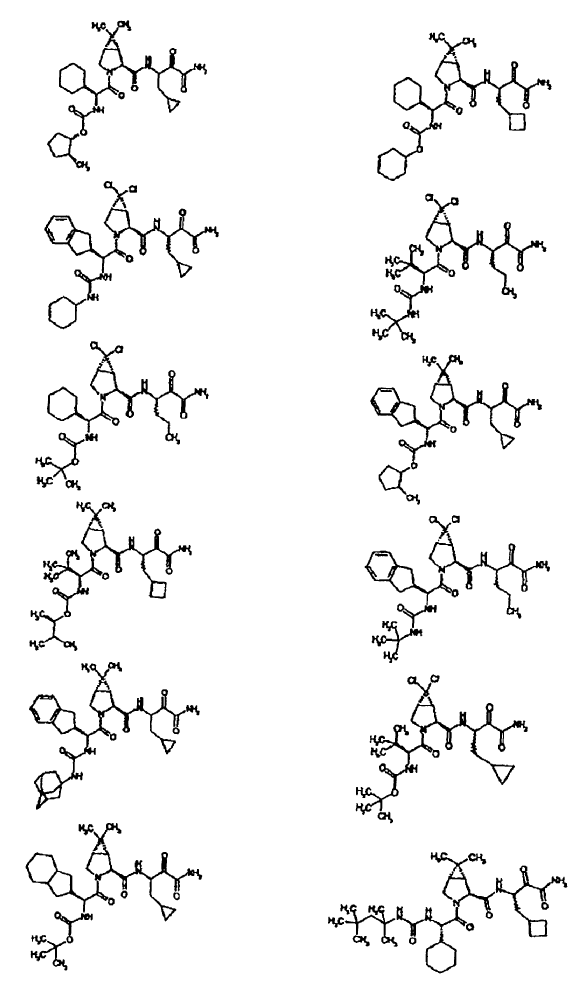
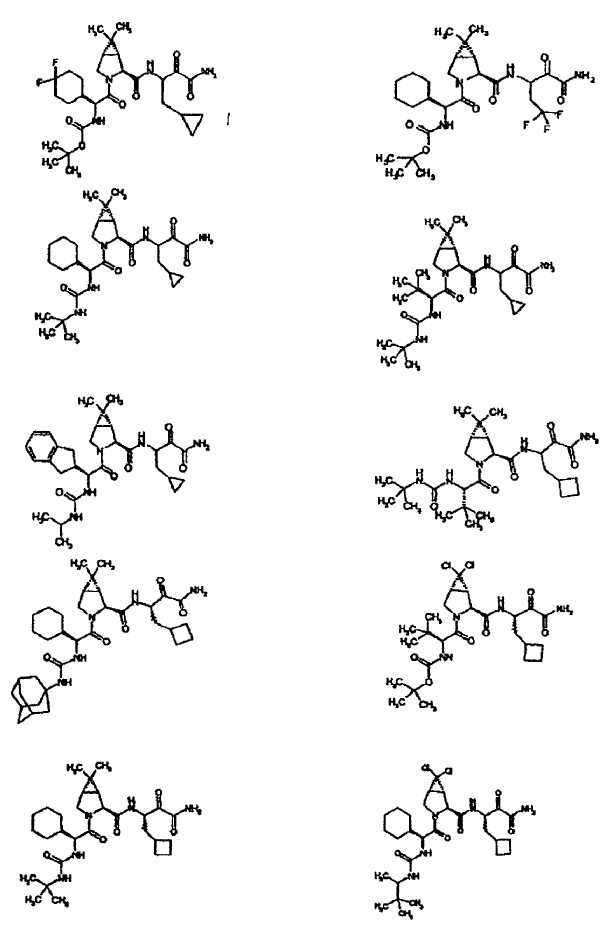
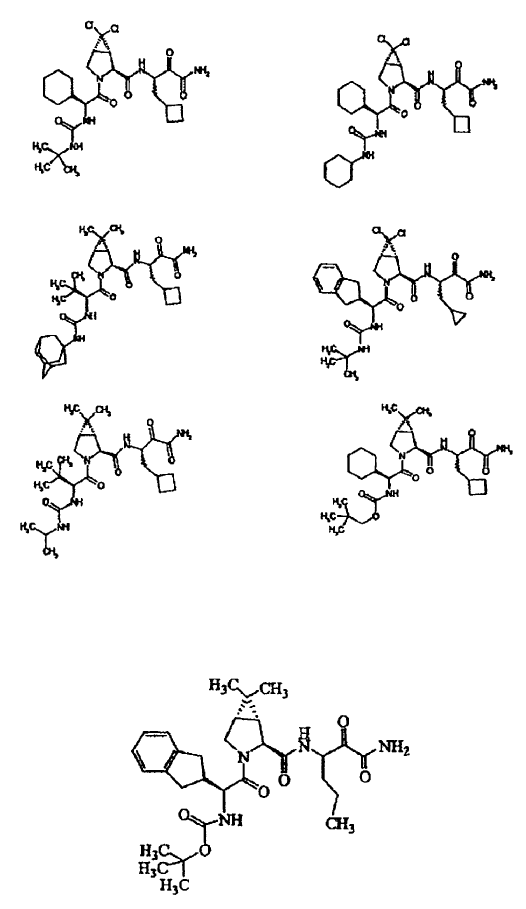
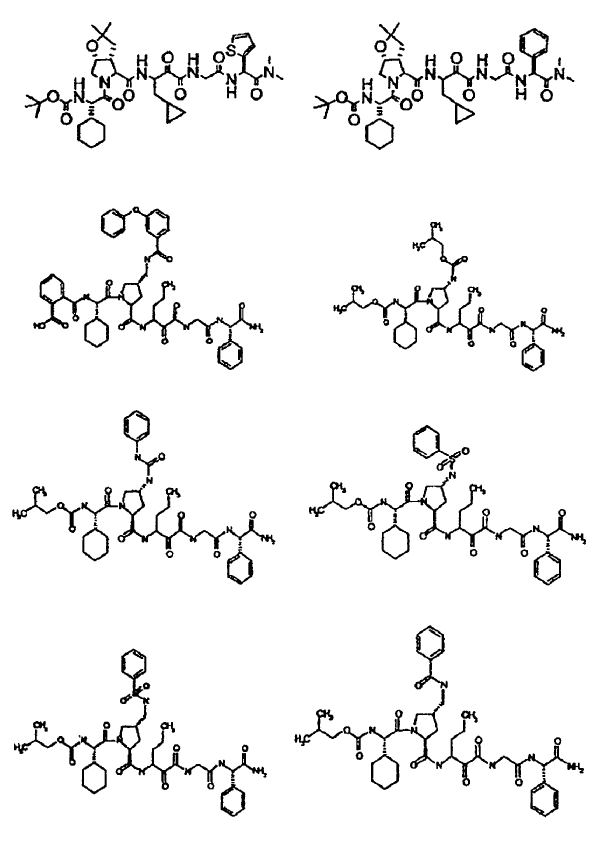
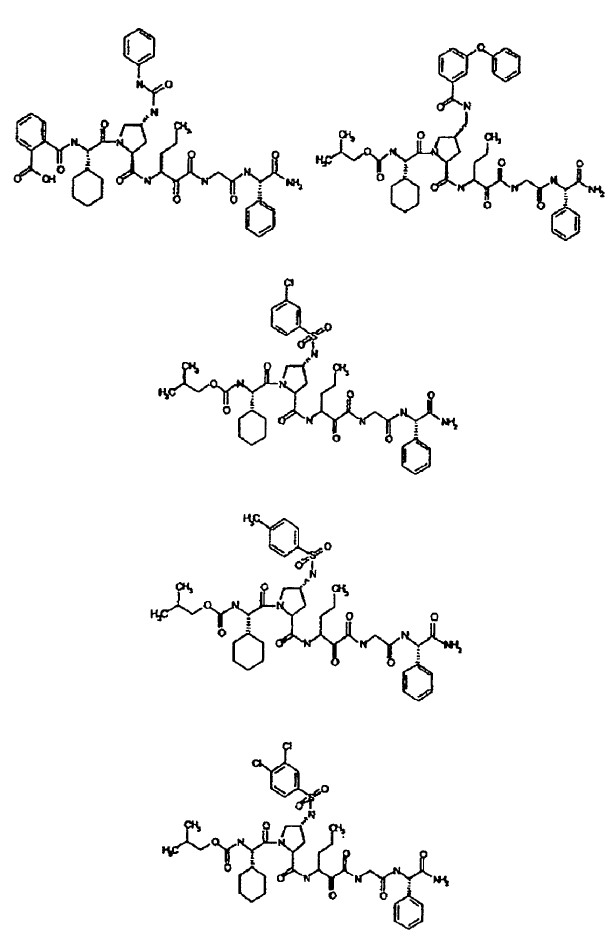
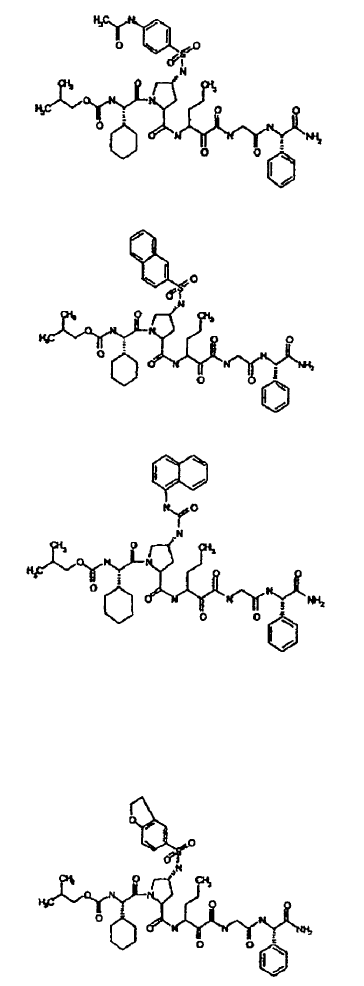

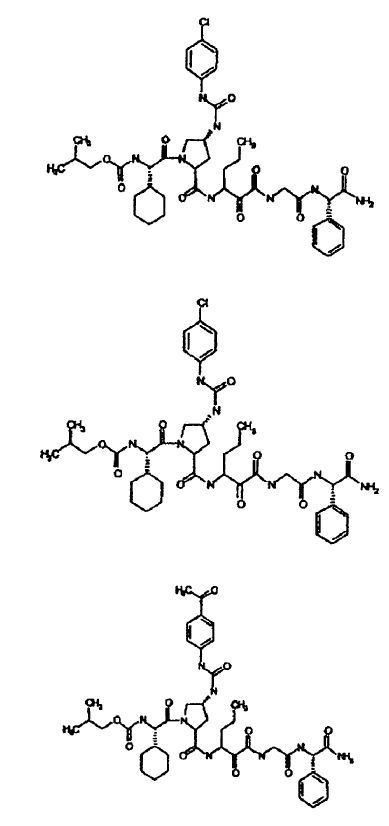
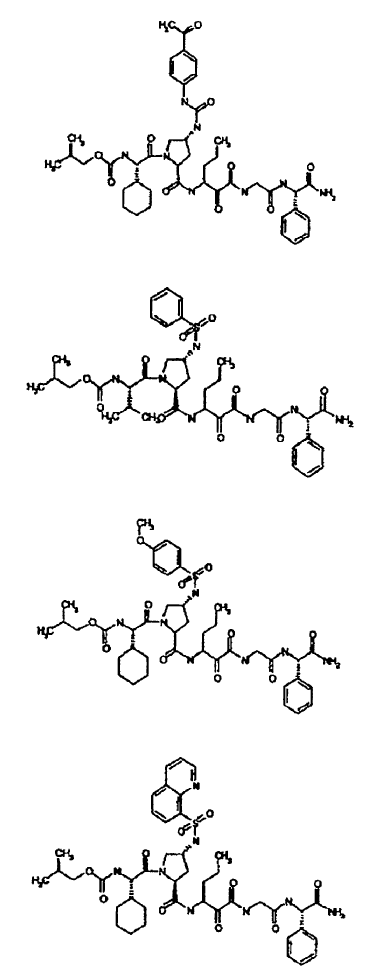
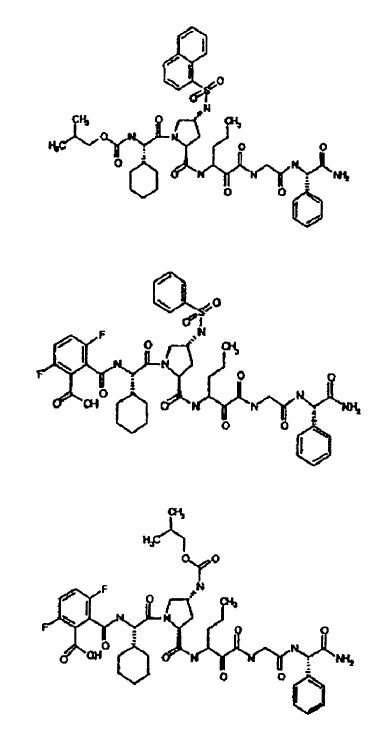
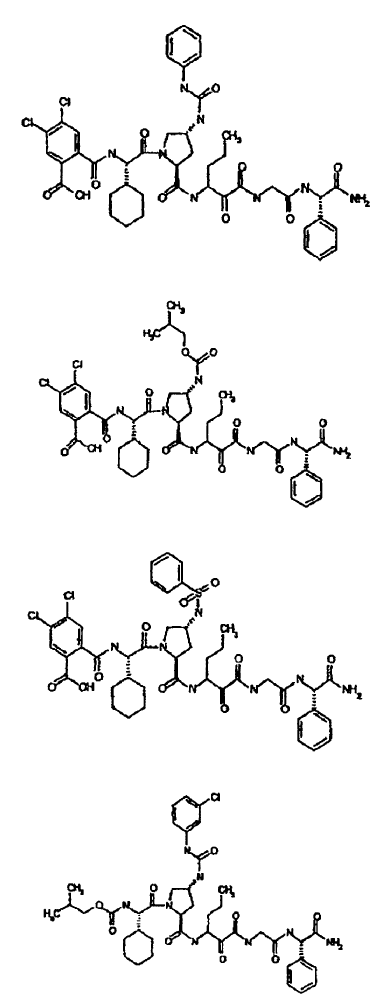
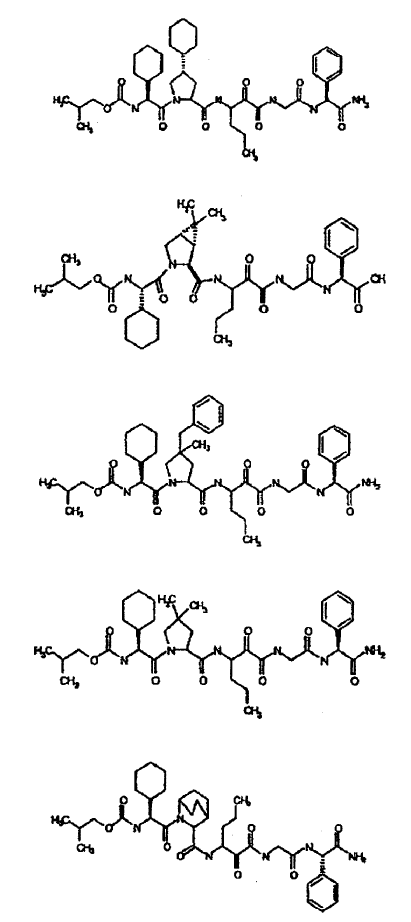
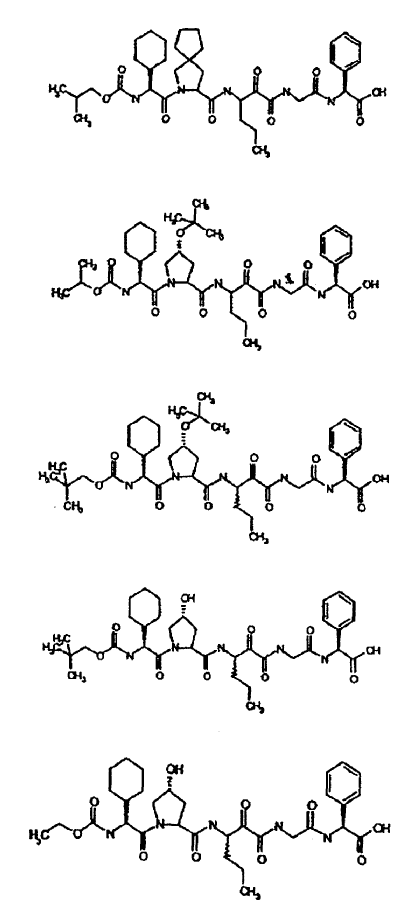
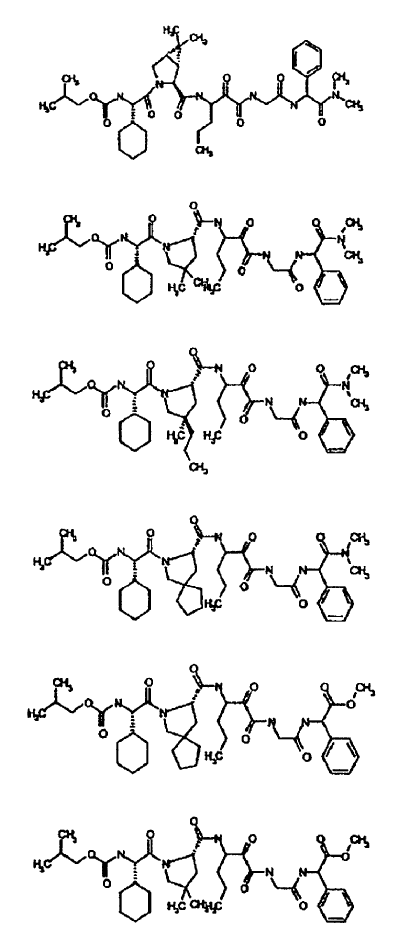
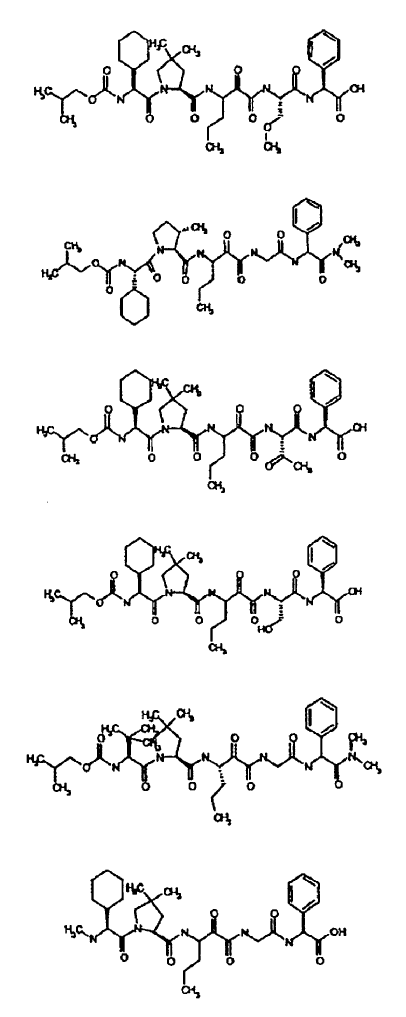
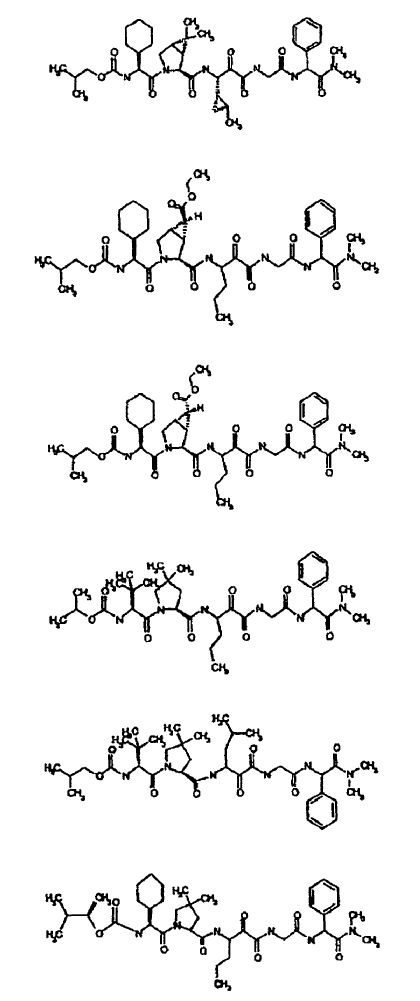
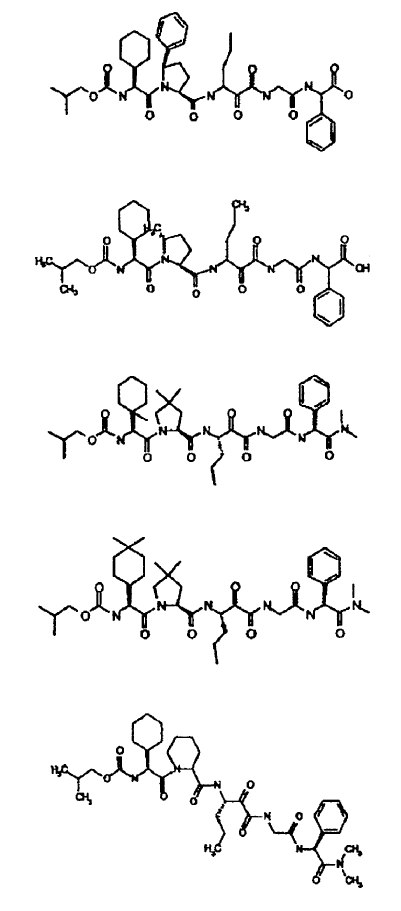





34. Una composición farmacéutica para el tratamiento de trastornos asociados con el VHC, comprendiendo dicha composición una cantidad terapéuticamente efectiva de uno o más compuestos de la reivindicación 33 y un vehículo farmacéuticamente aceptable.
35. La composición farmacéutica de la reivindicación 34, que contiene además (a) un agente antiviral o (b) un interferón o conjugado PEG-interferón alfa, o ambos (a) y (b).
36. La composición farmacéutica de la reivindicación 35, en la que dicho agente antiviral es ribavirina y dicho interferón es a-interferón.
37. Un compuesto que exhibe actividad inhibidora de la proteasa del VHC, incluyendo enantiómeros, estereoisómeros, rotámeros, tautómeros y racematos de dicho compuesto, y sales o solvatos farmacéuticamente aceptables de dicho compuesto, siendo dicho compuesto el compuesto de la estructura que se muestra a continuación:
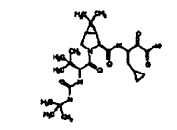
38. Un compuesto que exhibe actividad inhibidora de la proteasa del VHC, incluyendo enantiómeros, estereoisómeros, rotámeros, tautómeros y racematos de dicho compuesto, y sales o solvatos farmacéuticamente aceptables de dicho compuesto, siendo dicho compuesto el compuesto de la estructura que se muestra a continuación:
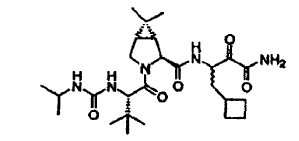
39. Un compuesto que exhibe actividad inhibidora de la proteasa del VHC, incluyendo enantiómeros, estereoisómeros, rotámeros, tautómeros y racematos de dicho compuesto, y sales o solvatos farmacéuticamente aceptables de dicho compuesto, siendo dicho compuesto el compuesto de la estructura que se muestra a continuación:

40. Un compuesto que exhibe actividad inhibidora de la proteasa del VHC, incluyendo enantiómeros, estereoisómeros, rotámeros, tautómeros y racematos de dicho compuesto, y sales o solvatos farmacéuticamente aceptables de dicho compuesto, siendo dicho compuesto el compuesto de la estructura que se muestra a continuación:
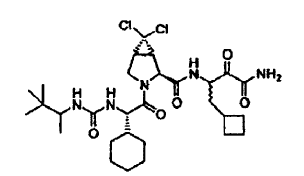
41. Un compuesto que exhibe actividad inhibidora de la proteasa del VHC, incluyendo enantiómeros, estereoisómeros, rotámeros, tautómeros y racematos de dicho compuesto, y sales o solvatos farmacéuticamente aceptables de dicho compuesto, siendo dicho compuesto el compuesto de la estructura que se muestra a continuación:
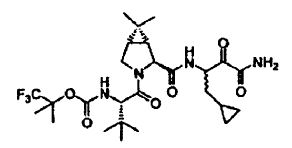
42. Un compuesto que exhibe actividad inhibidora de la proteasa del VHC, incluyendo enantiómeros, estereoisómeros, rotámeros, tautómeros y racematos de dicho compuesto, y sales o solvatos farmacéuticamente aceptables de dicho compuesto, siendo dicho compuesto el compuesto de la estructura que se muestra a continuación:
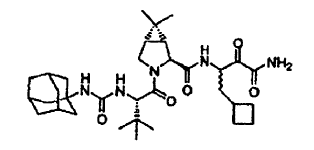
43. Un compuesto que exhibe actividad inhibidora de la proteasa del VHC, incluyendo enantiómeros, estereoisómeros, rotámeros, tautómeros y racematos de dicho compuesto, y sales o solvatos farmacéuticamente aceptables de dicho compuesto, siendo dicho compuesto el compuesto de la estructura que se muestra a continuación:
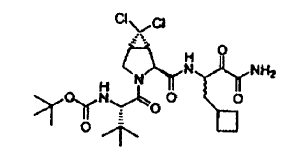
44. Un compuesto que exhibe actividad inhibidora de la proteasa del VHC, incluyendo enantiómeros, estereoisómeros, rotámeros, tautómeros y racematos de dicho compuesto, y sales o solvatos farmacéuticamente aceptables de dicho compuesto, siendo dicho compuesto el compuesto de la estructura que se muestra a continuación:
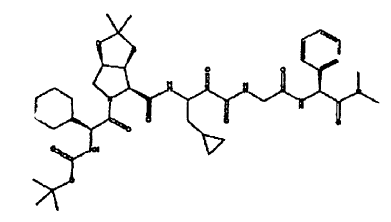
45. Un compuesto que exhibe actividad inhibidora de la proteasa del VHC, incluyendo enantiómeros, estereoisómeros, rotámeros, tautómeros y racematos de dicho compuesto, y sales o solvatos farmacéuticamente aceptables de dicho compuesto, siendo dicho compuesto el compuesto de la estructura que se muestra a continuación:
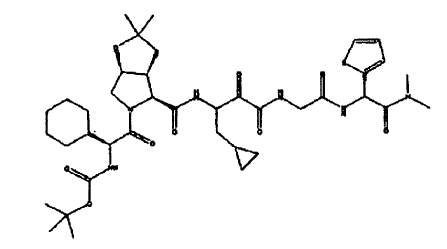
46. Un compuesto que exhibe actividad inhibidora de la proteasa del VHC, incluyendo enantiómeros, estereoisómeros, rotámeros, tautómeros y racematos de dicho compuesto, y sales o solvatos farmacéuticamente aceptables de dicho compuesto, siendo dicho compuesto el compuesto de la estructura que se muestra a continuación:
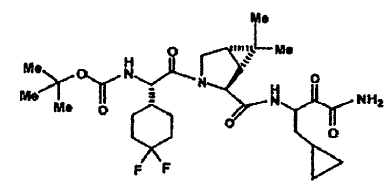
47. Una composición farmacéutica que comprende como principio activo un compuesto, incluyendo enantiómeros, estereoisómeros, rotámeros, tautómeros y racematos de dicho compuesto, y sales o solvatos farmacéuticamente aceptables de dicho compuesto, seleccionándose dicho compuesto de los siguientes:
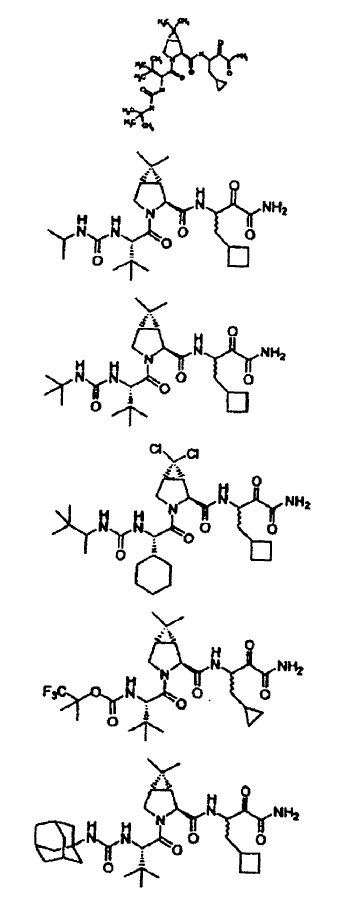
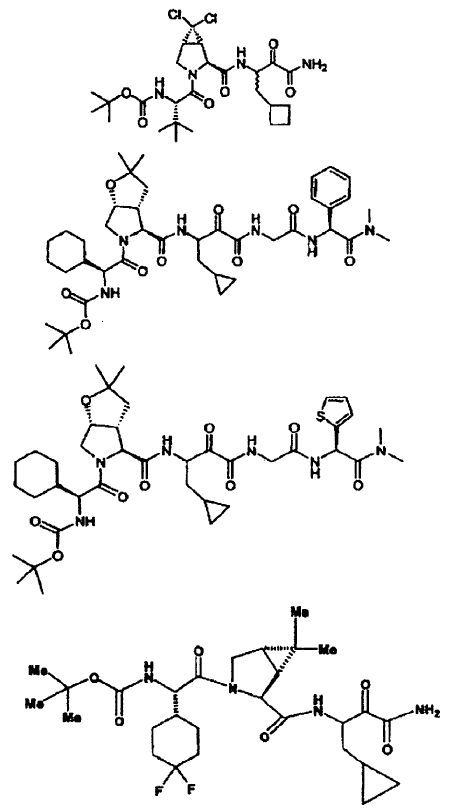
48. La composición farmacéutica de la reivindicación 47, que contiene además (a) un agente antiviral o (b) un interferón o conjugado PEG-interferón alfa, o ambos (a) y (b).
49. La composición farmacéutica de la reivindicación 48, en la que dicho agente antiviral es ribavirina y dicho interferón es a-interferón.
50. Un compuesto de acuerdo con cualquiera de las reivindicaciones 37 a 46, seleccionándose dicho compuesto de los siguientes:
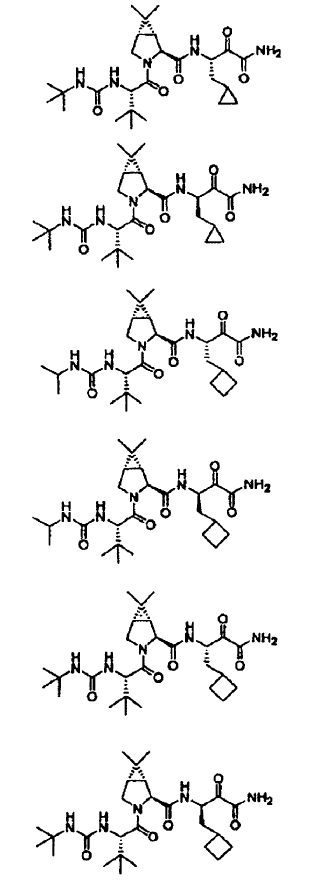
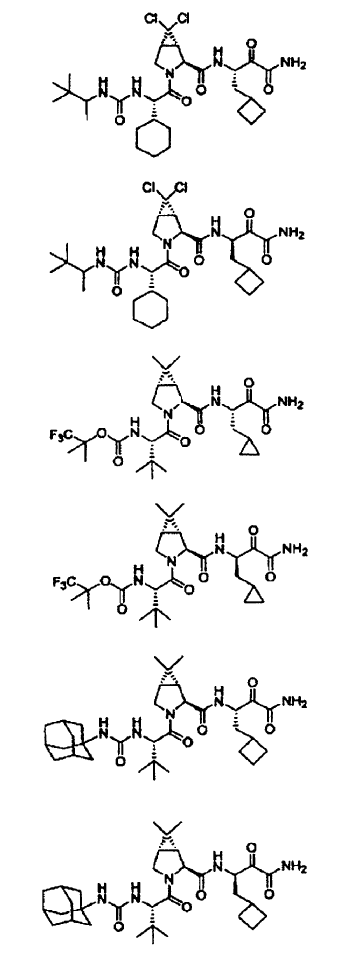
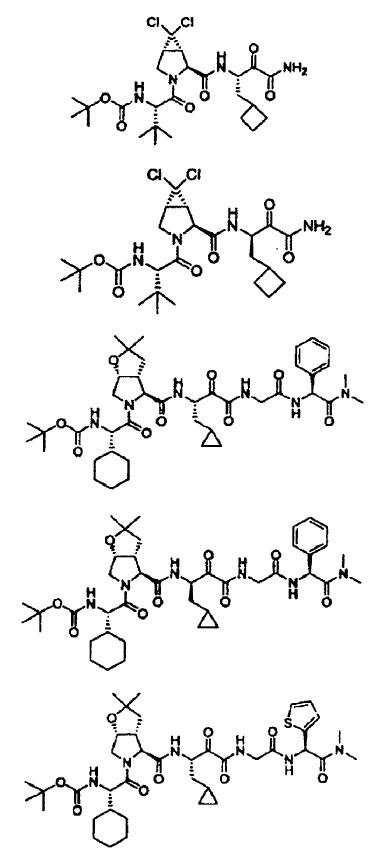

51. La composición farmacéutica de la reivindicación 47, en la que dicho compuesto se selecciona de los siguientes:
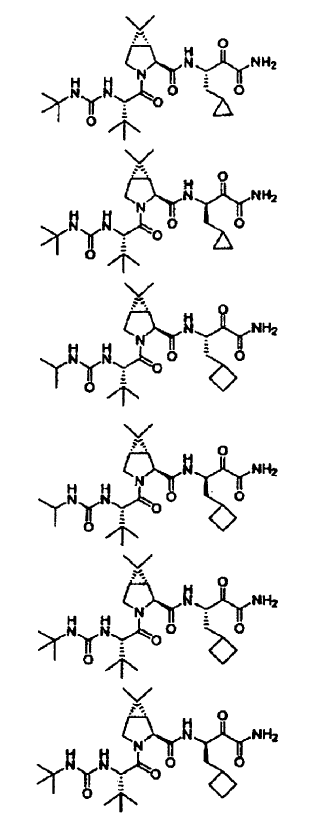
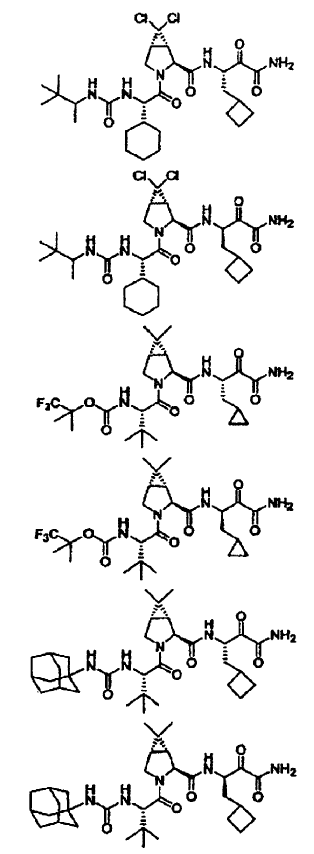
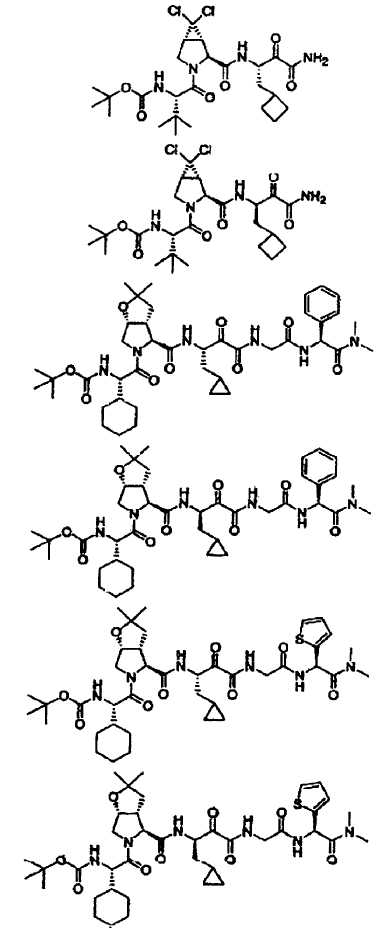
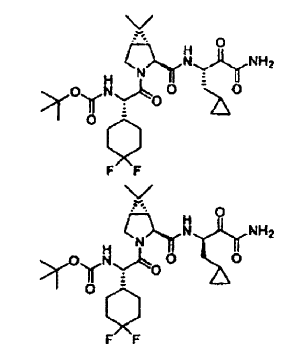
52. La composición farmacéutica de la reivindicación 51, que contiene además (a) un agente antiviral o (b) un interferón o conjugado de interferón alfa pegilado, o ambos (a) y (b).
53. La composición farmacéutica de la reivindicación 52, en la que dicho agente antiviral es ribavirina y dicho interferón es interferón alfa.
54. El uso de un compuesto de acuerdo con cualquiera de las Reivindicaciones 1 a 26, 33, 37 a 46 y 50 en la fabricación de una composición para usar en un tratamiento combinado para tratar trastornos asociados con el virus de la hepatitis C (VHC), comprendiendo dicho tratamiento combinado administrar (i) dicho compuesto y (ii) un interferón.
55. El uso de un interferón en la fabricación de una composición para usar en un tratamiento combinado para tratar trastornos asociados con el virus de la hepatitis C (VHC), comprendiendo dicho tratamiento combinado administrar (i) un interferón y (ii) un compuesto de acuerdo con cualquiera de las reivindicaciones 1 a 26, 33, 37 a 46 y 50.
56. El uso de la reivindicación 54 o 55, en el que dicho interferón es interferón alfa o interferón pegilado.
Patentes similares o relacionadas:
Composiciones enzimáticas líquidas estabilizadas, del 6 de Mayo de 2020, de NOVOZYMES A/S: Aldehído peptídico con la fórmula B2-B1-B0-H, donde: H es hidrógeno; B0 es un residuo de Tyr; B1 es un residuo de aminoácido de alanina, cisteína, glicina, […]
Composición que comprende un péptido derivado de adinopectina, del 11 de Diciembre de 2019, de KNU-Industry Cooperation Foundation: Una composición farmacéutica adecuada para prevenir o tratar una enfermedad de la piel, que comprende un péptido seleccionado del grupo que consiste en los péptidos de las […]
Método para producir un péptido recombinante y péptido resultante, del 6 de Noviembre de 2019, de "IVIX" Company Limited: Una composición farmacéutica que comprende un péptido de fórmula: Thr-Lys-Pro-Arg-Pro-X, en donde X es un grupo OH, OCH3 o NH2.
Formulaciones de tripéptidos liofilizados estables en almacenamiento, del 15 de Octubre de 2019, de DR. AUGUST WOLFF GMBH & CO. KG ARZNEIMITTEL: Formulación liofilizada que comprende lisil-prolil-treonina o una sal farmacéuticamente aceptable de la misma, que comprende además uno o […]
Composiciones de péptidos, del 14 de Mayo de 2019, de DSM IP ASSETS B.V.: Una composición, que comprende: (i) 0,001-12,5% en peso de un péptido con 2-12 aminoácidos sustituido con un resto lipófilo, (ii) 0,00001-2% […]
Inhibidores homomultivalentes y heteromultivalentes de antígeno de membrana específico de próstata (PMSA) y usos de los mismos, del 1 de Mayo de 2019, de THE JOHNS HOPKINS UNIVERSITY: Un compuesto de fórmula II:**Fórmula** - en la que Z es H, CO2H, NH2, SH u OH; - en la que cada R1 es el mismo resto o uno diferente y se selecciona entre el grupo […]
Método de producción de péptidos, del 3 de Abril de 2019, de KANEKA CORPORATION: Método de producción de un péptido mediante un método de síntesis en fase líquida, que comprende etapas de: etapa A: una etapa de hacer […]
Formulación de compuestos de ácido borónico, del 5 de Marzo de 2019, de THE UNITED STATES OF AMERICA, REPRESENTED BY THE SECRETARY, DEPARTMENT OF HEALTH AND HUMAN SERVICES: Procedimiento de preparación de un compuesto lifolizado de la fórmula :**Fórmula** en la que: P es hidrógeno o un resto de protección de grupo amino; R es […]