Métodos para tratar la esteatohepatitis no alcohólica (EHNA) mediante productos basados en cisteamina.
Cisteamina incluyendo sales para su uso en el tratamiento de un paciente que padece esteatohepatitis no alcohólica (NASH) .
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2008/085064.
Solicitante: THE REGENTS OF THE UNIVERSITY OF CALIFORNIA.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 1111 FRANKLIN STREET, 5TH FLOOR OAKLAND, CA 94607-5200 ESTADOS UNIDOS DE AMERICA.
Inventor/es: DOHIL,RANJAN, SCHNEIDER,JERRY.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A01N31/00 NECESIDADES CORRIENTES DE LA VIDA. › A01 AGRICULTURA; SILVICULTURA; CRIA; CAZA; CAPTURA; PESCA. › A01N CONSERVACION DE CUERPOS HUMANOS O ANIMALES O DE VEGETALES O DE PARTES DE ELLOS (conservación de alimentos o productos alimenticios A23 ); BIOCIDAS, p. ej. EN TANTO QUE SEAN DESINFECTANTES, PESTICIDAS O HERBICIDAS (preparaciones de uso médico, dental o para el aseo que eliminan o previenen el crecimiento o la proliferación de organismos no deseados A61K ); PRODUCTOS QUE ATRAEN O REPELEN A LOS ANIMALES; REGULADORES DEL CRECIMIENTO DE LOS VEGETALES. › Biocidas, productos que repelen o atraen los animales perjudiciales, o reguladores del crecimiento de los vegetales, que contienen compuestos orgánicos del oxígeno o del azufre.
- A61K31/095 A […] › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › Compuestos del azufre, del selenio, del teluro, p. ej. tioles.
PDF original: ES-2417179_T3.pdf
Fragmento de la descripción:
Métodos para tratar la esteatohepatitis no alcohólica (EHNA) mediante productos basados en cisteamina
Campo de la invención La invención se refiere en general a materiales y métodos para tratar la enfermedad del hígado graso mediante cisteaminas.
Antecedente de la invención La enfermedad grasa hepática (o esteatohepatitis) está frecuentemente asociada con una ingesta excesiva de alcohol o con la obesidad, pero también tiene otras causas como las deficiencias metabólicas incluyendo resistencia a la insulina y diabetes. El hígado graso es el resultado de la acumulación de triglicéridos grasos en las vacuolas de las células hepáticas, dando como resultado una disminución en la función hepática, y posiblemente conduciendo a cirrosis o cáncer hepático.
La enfermedad grasa hepática no alcohólica (EGHNA) representa una gama de enfermedades que se producen en ausencia de alcoholismo. En la actualidad no se dispone de un tratamiento correcto para la enfermedad grasa hepática, ya sea EGHNA o EHNA.
Un artículo publicado en L’Arcisped S Anna di Ferr por Marras (1955, Vol 8, páginas 639 a 644) divulga la administración de cisteamina (o !-mecaptoetilamina) a ratas alimentadas con una dieta de alto contenido en grasa para determinar el efecto de la cisteamina sobre la esteatosis hepática dietética (enfermedad grasa hepática inducida por una dieta de alto contenido en grasa) . La esteatosis del presente documento se refiere a la acumulación de lípidos en una célula.
Gulbahar Okan y col. han publicado un artículo “Treatment of non-alcoholic steatohepatitis with N-acetyl cystein” en Gastroenterology, Vol. 118, nº 4, (2000, Suplemento 2, Parte 2) que divulga la administración de N-acetil cisteína (NAC) a pacientes que padecen EHNA, que se han sometido a una modificación previa de la dieta. Este documento divulga que el tratamiento con NAC disminuye los niveles de las enzimas hepáticas ALT y AST.
En el World Journal of Gastroenterology (Vol. 13, nº 38, páginas 5127-5132) , Thong-Ngam Duangporn y col. divulgan la administración de NAC a ratas alimentadas con alto contenido en grasa. Este documento divulga que los niveles séricos de ALT no mejoraron significativamente en las ratas tratadas (véase la Tabla 1) . Los niveles de triglicéridos y colesterol no se alteraron en las ratas tratadas. Los análisis histológicos demostraron el tratamiento con NAC mostró una mejora mixta en la esteatosis (deposiciones grasas) y en la necroinflamación (véase la Tabla 2) . El documento confirma que, en un estudio diferente, no se observó mejora en un grupo tratado con NAC comparado con los sujetos que solamente habían experimentado una modificación en la dieta.
La solicitud de patente publicada WO2007/121545 divulga el uso de S-nitrosotioles, particularmente de S-NAC, en el tratamiento de la enfermedad grasa hepática. El documento describe el uso de S-nitrosotioles como donantes de óxido nítrico que pueden actuar como secuestrantes de radicales libres.
En Seminars in Liver Disease (Vol. 21, nº 1, 2001, páginas 81-88) , Paul Angulo y col. proporcionan un artículo de revisión que describe tratamientos para las enfermedades grasas hepáticas y cita los estudios realizados por Gulbahar y col. descritos anteriormente. En Medizinische Monatschrift Pharmazeuten (Vol. 6 nº. 6, 1983, páginas 171-177) , Remmer, divulga que la cisteamina es uno de los diferentes secuestrantes de radicales que son útiles para tratar la toxicidad hepática. La publicación se limita a confirmar la falta de intercambio entre cisteamina, cisteína, glutatión y sus precursores, y enseña además que la administración de glutatión o sus precursores, como la cisteamina, era ineficaz para tratar lesiones hepáticas producidas por intoxicación.
Sumario 55 La divulgación proporciona una cisteamina que incluye sales o ésteres para usar en el tratamiento de un paciente que padece esteatohepatitis no alcohólica (EHNA) . El tratamiento comprende administrar una cantidad terapéuticamente eficaz de una composición de cisteamina. En una realización, la dosis diaria total de composición de cisteamina es de aproximadamente 0, 5-1, 0 g/m2. En otra realización, la composición de cisteamina se administra a una frecuencia de 4 o menos veces al día (por ejemplo, una, dos o tres veces al día) . En una realización, la composición es una forma farmacéutica de liberación retardada o controlada que proporciona un aumento de la administración de la cisteamina o derivado de cisteamina en el intestino delgado. La forma de liberación retardada o controlada puede proporcionar una Cmáx. de la cisteamina o derivado de cisteamina o metabolito biológicamente activo de los anteriores, que es al menos de aproximadamente un 35%, 50%, 75% o superior que la Cmáx. proporcionada por una forma farmacéutica de liberación inmediata que contiene la misma cantidad de cisteamina o 65 derivado de cisteamina. En otra realización más, la forma de liberación retardada o controlada comprende un recubrimiento entérico que libera la composición de cisteamina cuando la composición alcanza el intestino delgado,
o una región del tracto gastrointestinal de un sujeto cuyo pH sea mayor de aproximadamente pH 4, 5. Por ejemplo, el recubrimiento se puede seleccionar del grupo constituido por gelatina polimerizada, shellac, copolímero de ácido metacrílico de tipo C NF, ftalato butirato de celulosa, hidrogenoftalato de celulosa, propionato ftalato de celulosa, acetato ftalato de polivinilo (PVAP) , acetato ftalato de celulosa (CAP) , acetato trimelitato de celulosa (CAT) , ftalato 5 de hidroxipropil metilcelulosa, acetato de hidroxipropil metilcelulosa, succinato de dioxipropil metilcelulosa, carboximetil etilcelulosa (CMEC) , acetato succinato de hidroxipropil metilcelulosa (HPMCAS) , y polímeros y copolímeros de ácido acrílico, formados típicamente a partir de acrilato de metilo, acrilato de etilo, metacrilato de metilo y/o metacrilato de etilo con copolímeros de ésteres de ácido acrílico y metacrílico. La composición se puede administrar por vía oral o parenteral. En otra realización, el método da como resultado la mejora de la fibrosis hepática comparada con los niveles anteriores a la a la administración de la composición de cisteamina. En otra composición adicional, el método da como resultado una reducción en el contenido en grasa del hígado, una reducción en la incidencia o el progreso de la cirrosis, o una reducción en la incidencia de carcinoma hepatocelular. En una realización, el método da como resultado una disminución en los niveles de aminotransferasa hepática comparados con los niveles anteriores a la administración de la composición de cisteamina. En una realización adicional, la administración da como resultado una reducción en la transaminasa hepática de entre aproximadamente 10% y 40% comparada con los niveles anteriores al tratamiento. En otra realización adicional, la administración da como resultado una reducción en los niveles de alanina o aspartato aminotransferasa en un paciente tratado de aproximadamente 30%, 20% o 10% por encima de los niveles de ALT normales, o a los niveles de ALT normales. En otra realización adicional, la administración da como resultado una reducción en los niveles de ferritina sérica comparados con los niveles anteriores al tratamiento con la composición de cisteamina. Los métodos y composición de la divulgación pueden también incluir la administración de un segundo agente combinado con una composición de cisteamina para tratar la EHNA.
El sujeto puede ser un adulto, adolescente o niño.
En un aspecto, la divulgación proporciona un método para tratar a un paciente que padece EHNA, que comprende administrar una cantidad terapéuticamente eficaz de una composición que comprende una cisteamina. Los métodos de la divulgación incluyen también el uso de una cisteamina en la preparación de un medicamento para el tratamiento de la EHNA, y el uso de una cisteamina en la preparación de un medicamento para administrarlo en combinación con un segundo agente para tratar la EHNA. También se ha incluido el uso de un segundo agente para tratar la EHNA en la preparación de un medicamento para administrarlo en combinación con una cisteamina. Se proporcionan además kits que comprenden una cisteamina para el tratamiento de la EHNA, opcionalmente con un segundo agente para tratar la EHNA, e instrucciones para el tratamiento de la EHNA. El término “enfermedad grasa hepática” puede incluir EHNA.
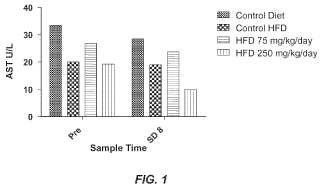
Breve descripción de los dibujos La figura 1 muestra el efecto del tratamiento con cisteína a 0, 75 y 250 mg/kg/día, administrada intraperitonealmente, sobre los niveles de aspartato aminotransferasa (AST) en animales alimentados con... [Seguir leyendo]
Reivindicaciones:
1. Cisteamina incluyendo sales para su uso en el tratamiento de un paciente que padece esteatohepatitis no alcohólica (NASH) . 5
2. Cisteamina para uso de acuerdo con la reivindicación 1 que es cisteamina o una sal de cisteamina.
3. Cisteamina para uso de acuerdo con las reivindicaciones 1 o 2, donde la cisteamina se administra a una dosis diaria total de
i) 0, 5-2, 0 g/m2, o ii) 0, 5-1, 0 g/m2.
4. Cisteamina para uso de acuerdo con una cualquiera de las reivindicaciones 1 a 3, donde la cisteamina se 15 administra a una frecuencia de:
i) cuatro o menos veces al día; o ii) tres veces al día; o iii) dos veces al día; o
iv) una vez al día.
5. Cisteamina para uso de acuerdo con una cualquiera de las reivindicaciones 1 a 4, en una forma de dosificación de liberación retardada o una forma de dosificación de liberación controlada.
6. Cisteamina para uso de acuerdo con una cualquiera de las reivindicaciones 1 a 5, que da como resultado una cualquiera de las siguientes:
i) mejora de la fibrosis hepática en comparación con los niveles antes de la administración de la cisteamina; ii) una reducción del contenido de grasa del hígado; o iii) una reducción de la incidencia de o de la progresión de cirrosis, o iv) una reducción de la incidencia de carcinoma hepatocelular, o v) una reducción de los niveles de aminotransferasa hepática en comparación con los niveles antes de la administración de la cisteamina o vi) una reducción de los niveles de ferritina en suero en comparación con los niveles antes del tratamiento con la cisteamina.
7. Cisteamina para uso de acuerdo con una cualquiera de las reivindicaciones 1 a 5, que da como resultado una respuesta exitosa a la terapia que es una reducción en el nivel de aminotransferasa hepática.
8. Cisteamina para uso de acuerdo con la reivindicación 6 o 7 donde la aminotransferasa hepática se selecciona del grupo que consiste en aspartato aminotransferasa y alanina aminotransferasa.
9. Cisteamina para uso de acuerdo con una cualquiera de las reivindicaciones 1 a 8, donde el paciente es un niño o adolescente. 45
10. Uso de una cisteamina o una sal de cisteamina para la preparación de un medicamento para el tratamiento de esteatohepatitis no alcohólica (NASH) .
11. Uso de la reivindicación 10, donde el medicamento es una forma de dosificación de liberación retardada. 50
12. Uso de la reivindicación 10 u 11, donde la cisteamina o sal de cisteamina se administra a una frecuencia de dos veces al día.
13. Cisteamina para uso de acuerdo con una cualquiera de las reivindicaciones 1-5, donde la cisteamina se 55 administra a una frecuencia de dos veces al día.
Patentes similares o relacionadas:
Método para tratar la fibrosis pulmonar idiopática, del 8 de Abril de 2020, de MEDICINOVA, INC: Un compuesto de Fórmula (I): **(Ver fórmula)** un éster del compuesto de Fórmula (I), o una sal aceptable farmacéuticamente de la misma de […]
Compuestos de sulfuro de hidrógeno para tratar preeclampsia o restricción del crecimiento fetal inducido por hipertensión, del 20 de Noviembre de 2019, de ASTON UNIVERSITY: Sulfuro de hidrógeno (H2S) o compuesto que genera (H2S) para su utilización en el tratamiento de preeclampsia (PE) o restricción del crecimiento fetal inducido por hipertensión.
Derivados de (2-ureidoacetamido)alquilo como moduladores del receptor 2 de péptidos formilados, del 3 de Mayo de 2019, de ALLERGAN, INC.: Un compuesto representado por la Fórmula I, enantiómeros individuales, diastereoisómeros individuales, tautómeros individuales, iones dipolares individuales o una sal farmacéuticamente […]
Nuevos derivados del 4-metoxipirrol o sus sales y composición farmacéutica que los comprende, del 12 de Marzo de 2019, de DAEWOONG PHARMACEUTICAL CO., LTD.: Un compuesto representado por la fórmula química 1 siguiente o una de sus sales farmacéuticamente aceptables:**Fórmula** en la fórmula química 1, R1, R2 […]
Composición farmacéutica para tratar el cáncer que comprende tripsinógeno y quimotripsinógeno, del 3 de Diciembre de 2018, de Propanc Pty Ltd: Una composición farmacéutica que comprende tripsinógeno y quimotripsinógeno, en la que la relación en peso de quimotripsinógeno:tripsinógeno es 4:1, 8:1 o está en […]
Compuestos organosulfurados y métodos de utilización de los mismos, del 7 de Marzo de 2018, de Acea Biosciences, Inc: Un compuesto que es: (a) un compuesto de fórmula : **(Ver fórmula)** en donde cada n es 1-3; y cada R es F, I, etilo, propilo, isopropilo, butilo, sec-butilo, […]
Sales de sulfato como potenciador del tiempo de tránsito, del 4 de Octubre de 2017, de BRAINTREE LABORATORIES, INC.: Uso de una solución oral de sulfato para preparar al tracto gastrointestinal de un paciente para examinar el interior del tracto gastrointestinal del […]
Cisteína y profármacos de cisteína para tratar la esquizofrenia y reducir los deseos compulsivos por los fármacos, del 28 de Diciembre de 2016, de Marquette University: Un profármaco de cisteína que tiene la estructura:**Fórmula** en donde: R1 y R2se seleccionan independientemente de OH, ≥O, o un grupo alcoxilo C1 a C5 de cadena lineal […]