Métodos de reducción de liberación masiva, inducida por el alcohol, en formas posológicas orales con liberación prolongada de opioides. Métodos de reducción de la liberación masiva, inducida por el alcohol, en formas posológicas orales con liberación prolongada de opioides.
Una forma de administración de opioide con liberación prolongada para usar para reducir los efectos adversos asociados a la liberación rápida de la dosis inducida por el alcohol en pacientes que toman por vía oral una forma de administración,
y en donde:
la forma de administración, cuando se somete a ensayo mediante un método de ensayo in vitro en el que se emplea un medio de ensayo que comprende alcohol acuoso a una concentración del 20% en volumen/volumen, libera una cantidad que es inferior o igual al 50% del peso de la dosis del opioide, en un período de 2 horas posterior al inicio del método de ensayo in vitro; y en donde:
(a) la forma de administración comprende una membrana semipermeable;
y/o
(b) la forma de administración comprende al menos un componente hidrófobo que es relativamente insoluble en agua y que se hincha mínimamente en alcohol acuoso, en donde: (i) cuando el componente hidrófobo comprende un polímero hidrófobo, dicho polímero muestra un grado de hinchazón y/o solubilidad en alcohol acuoso igual o inferior al que muestra en agua, y (ii) cuando el componente hidrófobo es no polimérico, dicho componente muestra un grado de hinchazón y/o solubilidad en alcohol acuoso inferior al que muestra en agua.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2006/042687.
Solicitante: ALZA CORPORATION.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 1900 CHARLESTON ROAD MOUNTAIN VIEW, CA 94043-7210 ESTADOS UNIDOS DE AMERICA.
Inventor/es: DAVAR,NIPUN, HASTEDT,JAYNE, CRUZ,Evangeline, SATHYAN,GAYTRI, PORS,LINDA, CASADEVALL,GEMMA.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K9/22 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 9/00 Preparaciones medicinales caracterizadas por un aspecto particular. › del tipo de liberación prolongada o discontinua.
PDF original: ES-2402666_T3.pdf
Fragmento de la descripción:
ÁMBITO DE LA INVENCIÓN
La invención se refiere a métodos de administración con liberación prolongada de opioides, incluidos, entre otros posibles, la hidromorfona y la oxicodona; dichos métodos ofrecen una mejora de las propiedades en caso de coadministración de opioides y alcohol acuoso.
ANTECEDENTES DE LA INVENCIÓN
En los pacientes que toman formas de administración de opioides por vía oral con liberación prolongada, la liberación rápida de la dosis de dichas formas, inducida por el etanol, puede constituir un problema grave.
Las formas de administración oral con liberación prolongada de opioides están concebidas para administrar dichos opioides al paciente a lo largo de un período de tiempo prolongado. A menudo se receta un opioide en formato de administración oral con liberación prolongada para que sustituya a formas de administración oral de opioides con liberación inmediata. Por ejemplo, hay una gran demanda de formas de administración oral con liberación prolongada que se tomen una vez al día (1/d) o dos veces al día (2/d) y que proporcionen alivio del dolor al paciente durante un día entero.
Por eso, la cantidad de opioide contenida en dichas formas de administración, especialmente en las formas de administración oral de opioides con liberación prolongada, de una sola toma al día, es notablemente superior a la contenida tradicionalmente en las formas de administración de opioides con liberación inmediata. Cualquier cosa que ocasione una liberación rápida de la dosis de tales formas de administración oral de opioides con liberación prolongada puede provocar una sobredosis con fármacos opioides, lo que conduciría a depresión respiratoria y posiblemente incluso a la muerte.
Los inventores se han dado cuenta de que una de las causas de liberación rápida (es decir, liberación inmediata) de la dosis la constituyen las velocidades de administración aumentadas ocasionadas por la coadministración de las formas de administración oral de opioides con liberación prolongada y de alcohol acuoso y, en especial, etanol acuoso. Hay diversos alcoholes que pueden aumentar la liberación, hasta velocidades indeseablemente altas, del opioide de las formas de administración oral de opioides con liberación prolongada, llegando incluso a provocar algo similar a la liberación rápida o liberación inmediata de la dosis.
Por lo tanto, sería deseable desarrollar formas de administración oral de opioides con liberación prolongada, y métodos relacionados, que no presenten los problemas asociados a las técnicas conocidas hasta ahora en este campo del conocimiento en lo referente a la liberación rápida de la dosis inducida por alcohol, y en especial, en lo referente a la liberación rápida de la dosis inducida por etanol. Sería asimismo incluso más deseable que dichas formas de administración oral de opioides con liberación prolongada, y los métodos relacionados, comprendieran formas de administración oral de opioides con liberación prolongada que se tomen 1/d o 2/d, y los métodos correspondientes.
RESUMEN DE LA INVENCIÓN
Un aspecto de la presente invención se refiere a un método que comprende: proporcionar una forma de administración con liberación prolongada de hidromorfona, que se toma 1/d y que comprende hidromorfona y una estructura de administración para liberación prolongada que proporciona administración 1/d; la coadministración a un paciente de la forma de administración de hidromorfona 1/d con liberación prolongada, y de alcohol acuoso; la liberación de hidromorfona de la forma de administración de hidromorfona 1/d con liberación prolongada; y en donde el alcohol acuoso comprende alcohol a concentraciones iguales o superiores a un 20% en volumen/volumen, aproximadamente; y en donde la proporción entre una concentración plasmática máxima media obtenida a partir de una única dosis de hidromorfona, alcanzada cuando la forma de administración de hidromorfona 1/d con liberación prolongada se coadministra a un paciente junto con el alcohol acuoso, y una concentración plasmática máxima media obtenida a partir de una única dosis de hidromorfona que se alcanza cuando se administra a un paciente la forma de administración de hidromorfona 1/d con liberación prolongada, sin coadministración del alcohol acuoso, es igual o inferior a 1, 8:1, aproximadamente.
Otro aspecto de la presente invención se refiere a un método que comprende: proporcionar una forma de administración de hidromorfona 1/d con liberación prolongada y que comprende hidromorfona y una estructura de administración para liberación prolongada que proporciona administración 1/d; la coadministración a un paciente de la forma de administración de hidromorfona 1/d con liberación prolongada, y de alcohol acuoso; la liberación de hidromorfona de la forma de administración de hidromorfona 1/d con liberación prolongada; y en donde el alcohol acuoso comprende alcohol a concentraciones iguales o superiores a un 20% en volumen/volumen, aproximadamente; y en donde la proporción entre una concentración plasmática máxima obtenida a partir de una única dosis de hidromorfona en un paciente individual, alcanzada cuando la forma de administración de hidromorfona 1/d con liberación prolongada se coadministra al paciente junto con el alcohol acuoso, y una concentración plasmática máxima obtenida a partir de una única dosis de hidromorfona en unpaciente individual, que se alcanza cuando se administra a un paciente la forma de administración de hidromorfona 1/d con liberación prolongada, sin coadministración del alcohol acuoso, es igual o inferior a 5:1, aproximadamente.
Y otro aspecto de la presente invención se refiere a un método que comprende: proporcionar una forma de administración de hidromorfona 1/d con liberación prolongada y que comprende hidromorfona y una estructura de administración para liberación prolongada que proporciona administración 1/d; la coadministración a un paciente de la forma de administración de hidromorfona 1/d con liberación prolongada, y de alcohol acuoso; la liberación de hidromorfona de la forma de administración de hidromorfona 1/d con liberación prolongada; y en donde la forma de administración de hidromorfona 1/d con liberación prolongada libera una cantidad inferior o igual a aproximadamente el 80% del peso de la dosis de hidromorfona de la forma de administración de hidromorfona 1/d con liberación prolongada, conforme a lo medido (a) mediante un método de ensayo in vitro que comprende medios de ensayo y (b) durante un período de unas 2 horas posteriores al inicio del método de ensayo in vitro; y en donde los medios de ensayo comprenden alcohol acuoso que comprende alcohol a concentraciones iguales o superiores a un 20% en volumen/volumen, aproximadamente.
Otro aspecto de la presente invención se refiere a un método que comprende: proporcionar una forma de administración con liberación prolongada de hidromorfona, que comprende hidromorfona y una estructura de administración para liberación prolongada; la coadministración a un paciente de la forma de administración con liberación prolongada de hidromorfona, y de alcohol acuoso; la liberación de hidromorfona de la forma de administración con liberación prolongada de hidromorfona; y en donde el alcohol acuoso comprende alcohol a concentraciones iguales o superiores a un 20% en volumen/volumen, aproximadamente; y en donde la proporción entre una concentración plasmática máxima media obtenida a partir de una única dosis de hidromorfona, alcanzada cuando la forma de administración se coadministra al paciente junto con el alcohol acuoso, y una concentración plasmática máxima media obtenida a partir de una única dosis de hidromorfona que se alcanza cuando se administra a un paciente la forma de administración, sin coadministración del alcohol acuoso, es igual o inferior a 1, 8:1, aproximadamente.
Y otro aspecto de la presente invención se refiere a un método que comprende: proporcionar una forma de administración con liberación prolongada de hidromorfona, que comprende hidromorfona y una estructura de administración para liberación prolongada; la coadministración a un paciente de la forma de administración con liberación prolongada de hidromorfona, y de alcohol acuoso; la liberación de hidromorfona de la forma de administración con liberación prolongada de hidromorfona; y en donde el alcohol acuoso comprende alcohol a concentraciones iguales o superiores a un 20% en volumen/volumen, aproximadamente; y en donde la proporción entre una concentración plasmática máxima obtenida a partir de una única dosis de hidromorfona en un paciente individual, alcanzada cuando la forma de administración se coadministra al paciente junto con el alcohol... [Seguir leyendo]
Reivindicaciones:
1. Una forma de administración de opioide con liberación prolongada para usar para reducir los efectos adversos asociados a la liberación rápida de la dosis inducida por el alcohol en pacientes que toman por vía oral una forma de administración, y en donde:
la forma de administración, cuando se somete a ensayo mediante un método de ensayo in vitro en el que se emplea un medio de ensayo que comprende alcohol acuoso a una concentración del 20% en volumen/volumen, libera una cantidad que es inferior o igual al 50% del peso de la dosis del opioide, en un período de 2 horas posterior al inicio del método de ensayo in vitro; y en donde:
(a) la forma de administración comprende una membrana semipermeable;
y/o (b) la forma de administración comprende al menos un componente hidrófobo que es relativamente insoluble en agua y que se hincha mínimamente en alcohol acuoso, en donde: (i) cuando el componente hidrófobo comprende un polímero hidrófobo, dicho polímero muestra un grado de hinchazón y/o solubilidad en alcohol acuoso igual o inferior al que muestra en agua, y (ii) cuando el componente hidrófobo es no polimérico, dicho componente muestra un grado de hinchazón y/o solubilidad en alcohol acuoso inferior al que muestra en agua.
2. Una forma de administración conforme con la Reivindicación 1, en donde el opioide es hidromorfona.
3. Una forma de administración, conforme con cualquiera de las reivindicaciones anteriores, que cumple con el ensayo in vitro cuando la concentración de alcohol en el medio de ensayo es del 40% en volumen/volumen.
4. Una forma de administración, conforme con cualquiera de las reivindicaciones anteriores, y que comprende un componente de liberación inmediata para la liberación inmediata del opioide.
5. Una forma de administración, conforme con cualquiera de las reivindicaciones anteriores, que comprende un antagonista de los opioides.
6. Una forma de administración, conforme con cualquiera de las reivindicaciones anteriores, que es una forma de administración que se toma una vez al día.
7. Una forma de administración, conforme con cualquiera de las reivindicaciones anteriores, que es una forma de administración que se toma dos veces al día.
8. Una forma de administración, conforme con cualquiera de las reivindicaciones anteriores, que es una forma de administración osmótica con liberación prolongada.
9. Una forma de administración, conforme con cualquiera de las reivindicaciones anteriores, que se usa en a una población de pacientes que incluye individuos de quienes se puede esperar que coingieran la forma de administración con una bebida alcohólica, al menos ocasionalmente.
10. Una forma de administración, conforme con cualquiera de las reivindicaciones anteriores, que se proporciona a los pacientes sin advertencias especiales en el etiquetado (dirigidas a los médicos y/o a los pacientes) referentes a los posibles efectos mortales que se derivan de tomar la forma de administración con alcohol
Fig. 1
Fig. 2
Orificio de adminiptración Fig.
Membrana pemiaermeab e Caapu a de HPMC
Caaa barrera Caaa de emauuee Po loox0000 gennrico Fig.
Fig. 5a Fig. 5b
Fig. 5c
corcentaje agrega ibero
doado (
de a Caracteristicas agregadas de iberación in vitro de os comprimidos de c orhidrato de hidromorfona 16 mg (de ejemp o 1) en so uciones de etano
Tiempo (h)
Fig. 6
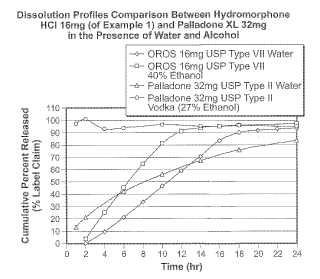
Comparación de as caracteristicas de diso ución de c orhidrato de hidromorfona 16 mg (de ejemp o 1) , y de ca adone XL 32 mg en presencia de agua y a coho
Tiempo (h)
Fig. x
corcentaje agregado iberado (o de a Concentración p asmatica media (SO) de hidromorfona Caracteristicas - Grupo 1 En ayunas
Concentración de hidromorfona (ng-m )
Concentración de hidromorfona (ng-m )
Fig. 8
Concentración p asmatica media (SO) de hidromorfona Caracteristicas - Grupo 1 Con a imento
Fig. 9
croporcionesde Cma> indi.idua es: Grupo 1: Estudio con a coho frente a estudiocon administraciones dup icadas Proaorción correpaondiente a a or a to/bauo en otep A l S adminiptración en dop ocapionep
croporción de Cma>
E a or map bauo epaerado de a aroaorción de Cmao en e ote A l e ote S ep 1 0
Acoho a 4º Acoho a 20º Acoho a 40º Lote A Lote B
Tratamiento Fig. 10
croporciones de Cma> indi.idua es: Grupo 2: Estudio con a coho frente a estudiocon administraciones dup icadas Proaorción correpaondiente a a or a to/bauo en otep A l S
croporción de Cma>
adminiptración en dop ocapionep
E a or map bauo epaerado de a aroaorción de Cmao en e ote A le ote S ep 1 0
Acoho a 4º Acoho a20º Acoho a40º Lote A Lote B
Tratamiento Fig. 11
Liberacióndec orhidrato deo>icodona a partir de formu aciones con ysin a coho esteari ico Liberación de farmaco agregada Liberación de farmaco agregada (o E:)
(o E:)
Tiempo (h)
Fig. 12
Liberación de c orhidrato dehidromorfona a partirde formu aciones con ysin a coho esteari ico
Tiempo (h)
Fig.1
Efecto de Eudragit® RS cP sobre a iberación de farmaco c orhidrato de o>icodona
Tiempo (h)
Fig. 1
Efecto de Eudragit® RS cP sobre a iberación de farmaco c orhidrato de hidromorfona Tiempo (h)
Liberación de farmaco agregada Fig. 15
Efectos re ati.os de a coho esteari ico, de a cera de carnauba y de aceite dericinocon co io>i 60
hidrogenado sobre a funciona idad de a iberación de c orhidrato de o>icodona Liberación de farmaco agregada (o E:)
o zC
Fig. 16
Caracteristicas de diso ución in vitro de os comprimidos de P>yContin® Caracteristicas de diso ución in vitro en agua y en etano a 40º:P>yContin 40 mg
Tiempo (h)
Fig. 1x
Patentes similares o relacionadas:
Dispositivos de administración de fármacos implantables para sitios genitourinarios, del 15 de Julio de 2020, de TARIS Biomedical LLC: Un dispositivo implantable de administración de fármacos que comprende: un depósito de fármaco que tiene una forma alargada […]
Composiciones y métodos no hormonales para la anticoncepción masculina que comprenden (R)-Silodosina, del 1 de Julio de 2020, de Laboratoires Major: Composición para su uso en un método anticonceptivo no hormonal para un sujeto masculino, en la que dicha composición es una formulación de liberación prolongada […]
Métodos para tratar sujetos con síndrome de Prader-Willi o síndrome de Smith-Magenis, del 20 de Mayo de 2020, de ESSENTIALIS, INC: Un agente de apertura del canal KATP para uso en la reducción de uno o más comportamientos agresivos en un sujeto con síndrome de Prader-Willi (PWS), en el que el uso […]
Comunicación inalámbrica para dispositivos médicos sobre el cuerpo, del 13 de Mayo de 2020, de BECTON, DICKINSON AND COMPANY: Un sistema para el suministro de fluidos sobre el cuerpo que comprende: una interfaz de usuario primaria que comprende un reloj de tiempo real de interfaz […]
Formulaciones de liberación controlada de levodopa y usos de las mismas, del 8 de Abril de 2020, de Impax Laboratories, LLC: Formulación sólida oral multiparticulada de liberación controlada que comprende 50 a 600 mg de levodopa y 10 a 80 mg de carbidopa, donde los multiparticulados están en una cápsula […]
Nanopartículas de circulación prolongada para la liberación sostenida de agentes terapéuticos, del 26 de Febrero de 2020, de PFIZER INC.: Una composición de nanopartículas biocompatibles que comprende una pluralidad de nanopartículas de circulación prolongada, comprendiendo cada una: copolímero […]
Composiciones terapéuticas de nanopartículas poliméricas con alta temperatura de transición vítrea o copolímeros de alto peso molecular, del 12 de Febrero de 2020, de PFIZER INC.: Un procedimiento para cribado de suspensiones de nanopartículas para identificar una suspensión que tiene una tasa de liberación de fármaco específica, que comprende: (a) […]
Composición farmacéutica que comprende drospirenona y kit anticonceptivo, del 25 de Diciembre de 2019, de Laboratorios León Farma SA: Kit anticonceptivo que comprende una o más unidades de acondicionamiento, en el que cada unidad de acondicionamiento comprende de 21 a 28 unidades […]