METODO DE PRUEBA BACTERIANA PARA ENZIMAS GLICADAS INTRACELULARES.
Un método para medir el contenido bacteriano de fluidos que comprende:
a. enlazar una cantidad efectiva de una glicoproteína con bacterias contenida en una muestra de fluido, dicha glicoproteína teniendo una funcionalidad enzimática generando una señal para indicar su presencia;
b. separar glicoproteína en exceso no enlazada de dicha muestra fluida después de reaccionar dicha glicoproteína con bacterias en dicha muestra en el paso (a);
c. medir la cantidad de dicho marcador que permanece después de separar dicha glicoproteína en exceso no enlazada de (b); y
d. determinar el contenido bacteriano de dicha muestra como relacionada a la cantidad de dicho marcador medido en el paso (c);
donde dicha glicoproteína es por lo menos un miembro del grupo que consiste de enzimas intracelulares y dichas enzimas inherentemente proveen una fracción de marcador que sirve como dicho marcador directamente enlazando dichas bacterias
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US03/17688.
Solicitante: SIEMENS HEALTHCARE DIAGNOSTICS INC..
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 511 BENEDICT AVENUE,TARRYTOWN, NY 10591.
Inventor/es: PUGIA, MICHAEL J., HATCH, ROBERT P., PROFITT,JAMES,A, BASU,MANJU.
Fecha de Publicación: .
Fecha Concesión Europea: 28 de Abril de 2010.
Clasificación Internacional de Patentes:
- G01N33/569 FISICA. › G01 METROLOGIA; ENSAYOS. › G01N INVESTIGACION O ANALISIS DE MATERIALES POR DETERMINACION DE SUS PROPIEDADES QUIMICAS O FISICAS (procedimientos de medida, de investigación o de análisis diferentes de los ensayos inmunológicos, en los que intervienen enzimas o microorganismos C12M, C12Q). › G01N 33/00 Investigación o análisis de materiales por métodos específicos no cubiertos por los grupos G01N 1/00 - G01N 31/00. › para microorganismos, p. ej. protozoarios, bacterias, virus.
Clasificación PCT:
- G01N33/569 G01N 33/00 […] › para microorganismos, p. ej. protozoarios, bacterias, virus.
Clasificación antigua:
- C12Q1/00 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12Q PROCESOS DE MEDIDA, INVESTIGACION O ANALISIS EN LOS QUE INTERVIENEN ENZIMAS, ÁCIDOS NUCLEICOS O MICROORGANISMOS (ensayos inmunológicos G01N 33/53 ); COMPOSICIONES O PAPELES REACTIVOS PARA ESTE FIN; PROCESOS PARA PREPARAR ESTAS COMPOSICIONES; PROCESOS DE CONTROL SENSIBLES A LAS CONDICIONES DEL MEDIO EN LOS PROCESOS MICROBIOLOGICOS O ENZIMOLOGICOS. › Procesos de medida, investigación o análisis en los que intervienen enzimas, ácidos nucleicos o microorganismos (aparatos de medida, investigación o análisis con medios de medida o detección de las condiciones del medio, p. ej. contadores de colonias, C12M 1/34 ); Composiciones para este fin; Procesos para preparar estas composiciones.
- C12Q1/02 C12Q […] › C12Q 1/00 Procesos de medida, investigación o análisis en los que intervienen enzimas, ácidos nucleicos o microorganismos (aparatos de medida, investigación o análisis con medios de medida o detección de las condiciones del medio, p. ej. contadores de colonias, C12M 1/34 ); Composiciones para este fin; Procesos para preparar estas composiciones. › en los que intervienen microorganismos vivos.
- C12Q1/28 C12Q 1/00 […] › una peroxidasa.
- C12Q1/70 C12Q 1/00 […] › en los que intervienen virus o bacteriófagos.
- G01N33/53 G01N 33/00 […] › Ensayos inmunológicos; Ensayos en los que interviene la formación de uniones bioespecíficas; Materiales a este efecto.
- G01N33/537 G01N 33/00 […] › con separación del complejo inmunológico del antígeno o del anticuerpo no ligados.
- G01N33/542 G01N 33/00 […] › con inhibición estérica o modificación de la señal, p. ej. extinción de fluorescencia.
- G01N33/543 G01N 33/00 […] › con un soporte insoluble para la inmovilización de compuestos inmunoquímicos.
- G01N33/554 G01N 33/00 […] › siendo el soporte una célula o un fragmento de célula biológica, p. ej. células de bacterias, de levadura.
- G01N33/567 G01N 33/00 […] › utilizando un extracto de tejido o de órgano como agente de unión.
- G01N33/569 G01N 33/00 […] › para microorganismos, p. ej. protozoarios, bacterias, virus.
Fragmento de la descripción:
Método de prueba bacteriana para enzimas glicadas intracelulares.
Antecedentes de la invención
Esta invención se relaciona en general con métodos para detectar bacterias en fluidos, particularmente en especímenes biológicos. Mas específicamente, la invención se relaciona con métodos rápidos para la detección de bacterias en orina y otros fluidos con mejorada precisión comparados con aquellos actualmente disponibles. Aunque el análisis de orina es de particular interés, otros fluidos, tales como sangre, suero, agua, y similares pueden ser analizados usando los métodos de la invención.
Es deseable una prueba rápida para bacterias, por ejemplo usando tiras de prueba secas del tipo ahora usado para diversos propósitos. En la actualidad, las tiras de prueba de orina son usadas para explorar muestras y descartar aquellas que no requieren evaluación de laboratorio. Sin embargo, las pruebas actuales, tales como medición de nitritos y leucocitos, no son capaces de proveer rápidamente resultados certeros. A menudo, se obtienen muchos resultados falsos, haciendo innecesarios análisis de seguimiento de laboratorio. Aproximadamente 50% de la carga de trabajo del laboratorio de un hospital involucra especímenes de orina y aproximadamente 90% de estos especímenes son cultivados y analizados para bacterias totales y gran negativas. Sin embargo, sólo aproximadamente 10% de las muestras de orina que son cultivadas para detección de bacterias tienen en efecto una prueba positiva. Claramente, una previa exploración correcta de la orina podría reducir grandemente el número de muestras enviadas al laboratorio para análisis.
La penetración de mercado de las tiras de prueba disponibles actualmente no es grande, en parte porque las pruebas producen resultados positivos falsos, tal como se determina después por análisis de seguimiento en el laboratorio. Por consiguiente, una tira de muestra que provee determinación rápida y certera de la presencia de bacterias reduciría costos y haría posible tratar bacterias en un paciente de inmediato, en lugar de esperar por resultados de laboratorio.
Los presentes inventores estaban investigando métodos por los cuales las bacterias pueden ser detectadas con exactitud. Un acercamiento potencial involucraba encontrar sustancias que podrían enlazarse a bacterias y después ser detectadas y medidas para que la cantidad de bacterias presente pudiera ser determinada. El problema puede ser planteado como sigue: Cómo se enlazan las sustancias a las bacterias y qué sustancias exhiben las propiedades necesarias para que se realicen medidas certeras? El enlace debería ser específico para bacterias. Enlaces no específicos pueden oscurecer los resultados ya que puede variar impredeciblemente y proveer resultados inexactos.
Los anticuerpos son reconocidos por tener la habilidad de unirse a las bacterias y se pensó que si la ALP (fosfatasa alcalina), que puede ser usada para detectar por desarrollo de color los materiales a los cuales se enlaza, podría ser unida a otra sustancia capaz de unirse por sí misma a las bacterias, sería posible medir la cantidad de bacterias presente. Al principio, los experimentos indicaban que la ALP estaba enlazada a bacterias de una forma no específica y por lo tanto se consideraba que presentaba un problema para el desarrollo de un método confiable para medir la cantidad de bacterias presente en una muestra. Posteriores investigaciones fueron dirigidas hacia la eliminación de enlaces no específicos de ALP para que sólo el ALP unido a las sustancias que puedan enlazarse a bacterias sea medidas. Sorprendentemente, se encontró que la creencia que la ALP se enlazaba no específicamente a las bacterias no era correcta y que de hecho, esta sí se enlazaba a bacterias, llevando a la presente invención. Como se verá más abajo, la ALP es una sustancia preferida para medir la cantidad de bacteria, pero pueden usarse otras sustancias, particularmente glicopéptidos y glicoproteínas.
Literatura relacionada y patentes
Se conocen métodos de pruebas rápidas para bacterias, pero difieren del método de la presente invención. En un método, un inmunoensayo para la detección de lipopolisacáridos de bacterias Gram negativas tal como E. coli, Clamidia o Salmonela usa una proteína de enlace lipopolisacárida o un anticuerpo que tiene afinidad de enlace específica al analito lipopolisacárido como un primero o segundo reactivo de enlace (véase WO 00/60354 y US 5,620,845). En US 5,866,344 se describen otros inmunoensayos para detectar polipéptidos de paredes celulares. Las proteínas pueden ser purificadas en un método usando polipéptidos de enlace polisacárido y sus conjugados (véase US 5,962,289; US 5,340,731; y US 5,928,917). En US 5,856,201 se revela la detección de proteínas usando proteínas de enlace polisacárido y sus conjugados. Los métodos descritos en lo anterior difieren de aquellos de la presente invención, como se verá en la discusión de la presente invención más abajo.
Los métodos que se basan en anticuerpos liposacáridos o proteínas de enlace no proveen una medida de las bacterias totales presentes. Estos tampoco usan un glicopéptido o glicoproteína para enlazarse a la célula bacteriana. Los métodos basados en polipéptidos requieren anticuerpos para enlazarse a la pared celular bacteriana en lugar de usar glicopéptidos o glicoproteínas. Los métodos basados en polipéptidos de enlace polisacárido requieren la fusión de secuencias cortas de polipéptidos en analitos de interés y usan polipéptidos no-glicados para enlazarse a un polisacárido.
Se ha demostrado que las glicoproteínas se enlazan a varias biomoléculas. Por ejemplo, se ha mostrado que las glicoproteínas en la superficie celular de hongos se enlazan a las proteínas del huésped. También, se ha demostrado que glicoproteínas excretadas de células epiteliales se enlazan a lípidos y el enlace de glicoproteínas a carbohidratos es bien conocido. Todas estas interacciones de glicoproteínas son dependientes de muchos factores, tales como fuerza iónica y pH, y la afinidad de las proteínas individuales para las biomoléculas. Sin embargo, el uso de glicoproteínas en ensayos para la medición de contenido bacteriano no ha sido descrito hasta el momento.
Se han aislado receptores de glicoproteínas en monocitos humanos. Se ha mostrado que dos proteínas de enlace extraídas de las paredes celulares de monocitos humanos tienen una afinidad de 9x10+6 para enlazar fructosilisina (lisil péptidos glicados con glucosa) con 10,000 sitios de enlace activos por célula. Se piensa que estos sitios receptores de proteína pertenecen a la familia de proteínas de enlace ARN y que están involucradas en el proceso de envejecimiento enlazando proteínas relacionadas con la edad tales como albúmina glicada. Sin embargo, la técnica previa en receptores de glicoproteína no enseña que los receptores sobre las paredes celulares podrían ser usados para la detección de células. No se provee ningún medio para la generación de señal, por partículas de color o reacciones enzimáticas que puedan ser usadas como una medida de la cuenta o detección de células.
Las bacterias son conocidas por unirse al tejido del huésped, usualmente por adhesión de la membrana celular bacteriana a proteínas de matriz extracelulares del huésped. Se conoce que este enlace ocurre a través de varias formas de interacción, por glicoaminoglicanos, colágenos, proteínas e integrinas en su superficie. Por lo tanto, la superficie celular, incluyendo superficies bacterianas celulares, puede ser visualizada como un mosaico de moléculas capaz de enlazarse a proteínas de los tejidos del huésped como también a sitios receptores del huésped.
La interacción entre células bacterianas y glicoproteínas es generalmente conocida, pero el enlace de glicopéptidos específicos a una célula bacteriana no ha sido revelado. Ha sido descrita la adhesión celular bacteriana a proteínas de matriz extra celulares tales como fibronectina y lamina. Se mostró que este enlace ocurre entre las adhesiones celulares y grupos glicados sobre las proteínas. Se han mostrado resultados similares con proteínas de tejido conectivo y células bacterianas. Estructuras de polipéptido y carbohidrato de glicoproteínas pueden tener gran variación y las estructuras químicas de glicopéptidos y glicoproteínas son usualmente desconocidas, tales como aquellas que enlazan células bacterianas.
Se han descrito métodos para medir el enlace de glicoproteínas a células bacterianas; sin embargo, la medida de bacterias por enlace de glicopéptido o glicoproteína no ha...
Reivindicaciones:
1. Un método para medir el contenido bacteriano de fluidos que comprende:
donde dicha glicoproteína es por lo menos un miembro del grupo que consiste de enzimas intracelulares y dichas enzimas inherentemente proveen una fracción de marcador que sirve como dicho marcador directamente enlazando dichas bacterias.
2. Un método de la Reivindicación 1 donde dicha glicoproteína tiene un enlace constante a bacterias de por lo menos 106 y por lo menos 100 sitios de enlace.
3. Un método para la Reivindicación 1 donde dichas enzimas intracelulares son seleccionadas del grupo que consiste de glutamato hidrogenasa, ALP, y lactato deshidrogenasa.
4. Un método para la Reivindicación 1 donde dicha glicoproteína es una enzima intracelular seleccionada del grupo que consiste de fosfatasa alcalina, fosfatasa ácida, fucosidasa, manosidasa, hexaminidasa, alfa-galactosidasa, fosfolipasa, hialuronidasa, glucocerebrosidasa, hidrolasa, arilsulfatasa A, amilasas, celobiohidrolasa, y peroxidasa.
5. Un método de la Reivindicación 3 donde dicha enzima es fosfatasa alcalina (ALP).
6. Un método de la Reivindicación 5 donde dicha ALP es ALP intestinal.
7. Un método de la Reivindicación 5 donde ALP es medida agregando como reactivo PNPP.
8. Un método de la Reivindicación 7 donde el color desarrollado por dicho reactivo es leído a una longitud de onda de 405 nm.
9. Un método de la Reivindicación 1 que comprende adicionalmente agregar a dicha muestra compuestos de bloqueo seleccionados del grupo que consiste de polímeros, proteínas no glicadas, polipéptidos no glicados, y polisacáridos.
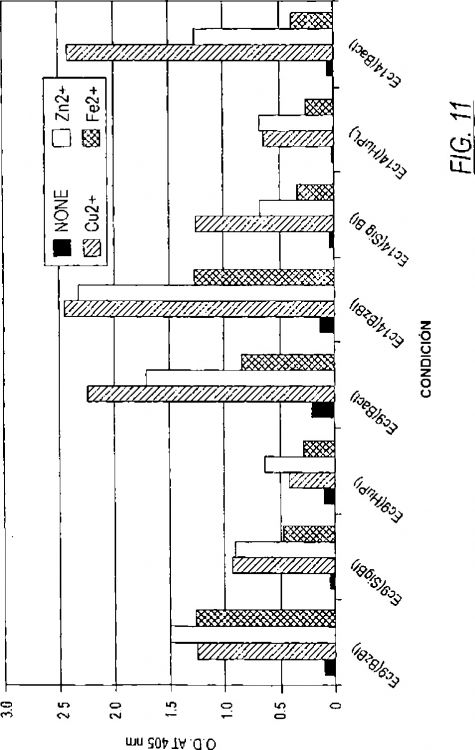
10. Un método de la Reivindicación 1 que comprende adicionalmente agregar por lo menos un catión capaz de aumentar el enlace de dicha glicoproteína a bacteria.
11. Un método de la Reivindicación 10 donde dicho catión es por lo menos un miembro del grupo que consiste de zinc, cobre y hierro.
12. Un método de la Reivindicación 11 donde dicho catión es zinc.
Patentes similares o relacionadas:
Método de determinación de la presencia y/o cantidad de moléculas diana, del 22 de Julio de 2020, de Canopy Biosciences, LLC: Método para el análisis de células individuales en una muestra de sangre mediante la determinación de la presencia y/o cantidad de una o más moléculas […]
Ensayo de toxina botulínica con sensibilidad mejorada, del 1 de Julio de 2020, de BioMadison, Inc: Un método para aumentar la sensibilidad de la detección basada en células de una toxina botulínica, que comprende: (i) proporcionar una célula […]
Bebidas energéticas y otras ayudas nutricionales derivadas de licores a base de agave, del 1 de Julio de 2020, de Roar Holding, LLC: Una composición que comprende compuestos inhibidores de monoamino oxidasa (MAO), cuya composición se prepara mediante la eliminación de etanol de una bebida […]
Evaluación asistida del pronóstico en la enfermedad inflamatoria, del 24 de Junio de 2020, de KINGS COLLEGE LONDON: Un método in vitro de recopilación de información útil para predecir el resultado clínico en un sujeto, en donde el sujeto tiene o se sospecha que tiene una enfermedad […]
Vacunas y diagnóstico de torque teno virus porcino, del 18 de Junio de 2020, de VIRGINIA TECH INTELLECTUAL PROPERTIES, INC.: Composición inmunogénica que comprende una proteína según SEQ ID NO. 16.
Marcadores celulares para el diagnóstico de la enfermedad de Alzheimer y para la progresión de la enfermedad de Alzheimer, del 17 de Junio de 2020, de YEDA RESEARCH AND DEVELOPMENT CO. LTD.: Un método para el diagnóstico de la probabilidad de la enfermedad de Alzheimer (EA) en un individuo examinado, que comprende: (i) medir los […]
Biomarcadores de TB, del 22 de Abril de 2020, de United Kingdom Research and Innovation: Un método para el diagnóstico de TB en un sujeto, comprendiendo el método: (a) proporcionar una muestra de dicho sujeto, siendo dicha muestra seleccionada […]
Procedimiento para detectar bacterias coliformes contenidas en la leche, del 15 de Abril de 2020, de ASAHI KASEI KABUSHIKI KAISHA: Procedimiento para lisar bacterias coliformes contenidas en la leche, que comprende la etapa de mezclar un agente de lisis que contiene lisozima, un surfactante aniónico […]