Un método y un dispositivo para determinar el estado de hidratación y/o nutrición de un paciente.
Un método para determinar un volumen intracelular ICV de un paciente comprendiendo los pasos de:
determinar una resistencia eléctrica intracelular Rmix del paciente,
obtener el volumen intracelular ICV utilizando Rmix teniendo en cuenta que una célula de un primer tipo de tejidocontribuye de manera diferente a la resistencia eléctrica Rmix del volumen intracelular ICV en comparación conuna célula de un segundo tipo de tejido,
en el que el primer tipo de tejido es tejido adiposo y el segundo tipo de tejido es tejido magro,
determinar una resistencia eléctrica extracelular RE del paciente,
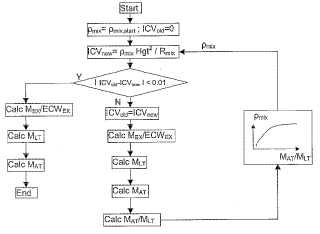
en el que se determina la masa total M del paciente en donde la obtención se lleva a cabo por iteraciónutilizando un valor normal de inicio para el volumen intracelular ICV, la iteración comprendiendo los siguientespasos:
obtener un volumen de agua extracelular ECW del paciente utilizando RE,
obtener el volumen de mal-hidratación ECWEX y así la masa de mal-hidratación MEX del pacienteutilizando el volumen de agua extracelular ECW y la masa total M del paciente,
obtener la masa MLT del compartimento de tejido magro del paciente usando una ecuación basada enla masa de mal-hidratación MEX del paciente, la masa total M del paciente, el volumen intracelular ICVy constantes de proporcionalidad ζLT y ζAT las constantes proporcionalmente relacionando las masasde tejido magro MLT y del compartimento del tejido adiposo MAT con componentes correspondientes detejido magro y de tejido adiposo ICVLT y ICVAT del volumen intracelular ICV, y la ecuación siendoobtener la masa MAT del compartimento de tejido adiposo del paciente por sustracción de las masasMLT y MEX de la masa total M,
obtener la resistividad mezclada ρmix a partir de valores de referencia para sujetos sanos endependencia de la proporción MAT/MLT,
utilizar la resistividad mezclada ρmix así determinada para obtener un nuevo valor para el volumenintracelular ICV y repetir la iteración hasta que se logre convergencia suficiente.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2004/007023.
Solicitante: FRESENIUS MEDICAL CARE DEUTSCHLAND GMBH.
Nacionalidad solicitante: Alemania.
Dirección: ELSE-KRONER-STRASSE 1 61352 BAD HOMBURG V.D.H. ALEMANIA.
Inventor/es: CHAMNEY, PAUL, WABEL,PETER.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61B5/053 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61B DIAGNOSTICO; CIRUGIA; IDENTIFICACION (análisis de material biológico G01N, p.ej. G01N 33/48). › A61B 5/00 Medidas encaminadas a establecer un diagnóstico (diagnóstico por medio de radiaciones A61B 6/00; diagnóstico por ondas ultrasónicas, sónicas o infrasónicas A61B 8/00 ); Identificación de individuos. › Medida de la impedancia o de la conductancia eléctrica de una zona corporal.
PDF original: ES-2396906_T3.pdf
Fragmento de la descripción:
La invención se refiere al campo de vigilancia del estado de hidratación y/o nutrición de un paciente.
Los riñones llevan a cabo diversas funciones para mantener la salud de un cuerpo humano. Primero, controlan el equilibrio de líquidos separando cualquier exceso de líquido del volumen de sangre del paciente. Segundo, sirven para purificar la sangre de cualquier sustancia de desecho como urea o creatinina. Por último pero no menos importante también controlan los niveles de ciertas sustancias en la sangre como electrolitos con el fin de asegurar un nivel de concentración necesario y saludable.
En caso de insuficiencia renal el líquido ingerido se acumula en los tejidos corporales y en el sistema vascular causando aumento de tensión en el sistema circulatorio. Este exceso de líquido tiene que ser eliminado durante un tratamiento de diálisis por ultrafiltración de la sangre. Si se elimina insuficiente líquido las consecuencias a largo plazo pueden ser graves, llevando a alta presión sanguínea e insuficiencia cardíaca. La propia insuficiencia cardiaca tiene mucha mayor probabilidad de ocurrir en pacientes de diálisis y se piensa que los estados de sobrecarga de líquido son uno de los principales factores contribuyentes. La eliminación de demasiado líquido es también peligrosa ya que el paciente de diálisis llega a deshidratarse y esto conduce invariablemente a la hipotensión.
El peso seco (por simplicidad las palabras “peso” y masa” se usarán de forma sinónima en todo este documento de solicitud de patente – lo que es también práctica normal en el campo médico) define el peso de un paciente que se lograría si los riñones funcionaran normalmente. En otras palabras esto representa el peso (o status líquido) objetivo óptimo que debería ser conseguido a fin de minimizar el riesgo cardiovascular. El peso seco ha sido siempre un problema esquivo en la práctica clínica rutinaria debido a la falta de métodos cuantitativos para su evaluación. Actualmente el problema del peso seco es abordado utilizando indicadores indirectos como por ejemplo presión sanguínea, investigaciones ecocardiográficas e información subjetiva como rayos X. Además ha sido particularmente difícil definir un conjunto de condiciones que sean universalmente aceptadas como estándar de peso seco.
Un método prometedor para obtener el status líquido de un paciente implica el uso de medidas de bioimpedancia. Una corriente alterna pequeña se aplica a dos o más electrodos que se unen a un paciente y se mide la correspondiente diferencia de potencial eléctrico. Los diversos compartimentos de líquido de un cuerpo humano contribuyen diferentemente a las señales medidas. El uso de frecuencias múltiples permite determinar el agua en el volumen intracelular (ICV) y el volumen extracelular (ECV) . Un ejemplo de tal dispositivo se describe en la solicitud de patente internacional WO 92/19153. Sin embargo, este documento no revela ningún método relacionado con cómo puede obtenerse el peso seco del paciente particular.
La patente U.S. 5.449.000 describe un sistema de bioimpedancia que también utiliza frecuencias múltiples para determinar la masa de agua en el ECV e ICV. Además se toman ciertos datos dependientes de la población para utilizar y elegir las llamadas fórmulas de predicción de población. La composición corporal se analiza luego utilizando estas fórmulas y con la ayuda de señales de bioimpedancia segmentaria.
La solicitud de patente internacional WO 02/36004 A1 describe un método y un dispositivo para derivar el peso seco de un paciente con insuficiencia renal utilizando un dispositivo de bioimpedancia extrapolando un volumen de exceso de agua en el volumen extracelular a una condición donde no habría insuficiencia renal. Por un procedimiento similar puede obtenerse un término de corrección de masa que tiene en cuenta desviaciones dentro de seres humanos saludables y que se atribuye a ciertos tejidos.
La solicitud de patente internacional WO 03/053239 A1 divulga un modelo compartimental que trata la variación en seres saludables en ciertos compartimentos corporales con el fin de separar mejor un volumen de mal-hidratación y otros componentes de tejidos en particular con la ayuda de mediciones de bioimpedancia. Con tal dispositivo puede obtenerse también información sobre el estado nutricional de un paciente.
La patente U.S. 6, 615, 077 describe un enfoque para supervisar un tratamiento de diálisis por un dispositivo de bioimpedancia con el fin de correlacionar las señales con el progreso del tratamiento.
Kanai et al. : «Electrical measurement of fluid distributions in legs and arms" Medical progress through technology, Springer Verlag Berlin, DE, vol. 12, 1987, páginas 159-170, XP000882965 ISSN: 0047-6552 describe el modelado eléctrico del tejido humano a la vista de la diagnosis médica.
Rigaud et al.: "Bioelectrical Impedance Techniques in Medicine, Critical Review in Biomedical Engineering", 24 (46) , 1996, páginas 257-351, XP000885971 ISSN: 0278-940X es un artículo de revisión dirigido a la modelación de propiedades eléctricas de tejidos biológicos y aspectos instrumentales de la espectrometria de impedancia eléctrica. Se presentan diversos modelos eléctricos de tejido incluyendo el modelo de Kanai y una modificación del mismo.
Un dispositivo de bioimpedancia que realiza cálculos en volúmenes de agua ICV y ECV es distribuido por Xitron Technologies bajo la marca Hydra™. Los detalles sobre el dispositivo son divulgados en la solicitud de patente internacional WO 92/19153. Este dispositivo se basa en un modelo de locus de impedancia que relaciona los valores de impedancia medidos a componentes resistivos que simulan las contribuciones de los volúmenes de agua en los espacios intra y extracelulares - ICW y ECW – con el fin de obtener y aislar cualquier valor para el ICW y ECW. En el caso del dispositivo existente este modelo es el llamado modelo Hanai.
Aplicando el modelo Hanai el ECW se determina aprovechando el hecho de que la impedancia eléctrica de los tejidos corporales cambia cuando se aplican corrientes alternas de diferentes frecuencias al paciente por medio de electrodos. A bajas frecuencias las membranas celulares se comportan como aislantes y la corriente aplicada pasa únicamente a través de los espacios ECV. A altas frecuencias las membranas celulares se vuelven más conductoras y por ello la corriente pasa través de tanto los espacios ICV como ECV. El locus de impedancia correspondiente por tanto consiste en dos ramas paralelas, la primera representando el espacio ECV por una resistencia óhmica RE, la segunda representando el espacio ICV por una resistencia óhmica RI, y una capacitancia conectada en serie. Los volúmenes de agua de los respectivos compartimentos pueden entonces ser calculados a partir de la información de resistencia, en base a constantes de resistividad del compartimento disponibles a partir de estudios anteriores para los cuales los volúmenes fueron también determinados por mediciones de dilución.
La exactitud de los métodos que se basan en los resultados así obtenidos para el ECW y el ICW, por ejemplo métodos como los divulgados en WO 02/36004 A1 o WO 03/053239 A1, entonces depende de la exactitud del modelo inicial, por ejemplo el modelo Hanai. Los inventores de la presente invención han notado que ciertas deficiencias en la precisión de los resultados de los métodos actuales de bioimpedancia para evaluar el agua corporal y el tejido corporal tienen su origen en las limitaciones del modelo Hanai.
Por lo tanto existe una necesidad de un método y dispositivo de biimpedancia que haga uso de un modelo refinado por el cual las contribuciones del agua y el tejido a los espacios de ECV y ICV pueden ser separadas más precisamente para permitir una evaluación mejorada de la composición corporal de un paciente con mayor precisión, proporcionando una mejor comprensión del estado de hidratación, nutrición y capacitación del paciente. Es un objeto de la invención proporcionar tales métodos.
El problema de la invención se soluciona por un método de acuerdo a la reivindicación 1 para determinar un volumen intracelular ICV de un paciente que comprende los pasos de determinar una resistencia eléctrica intracelular Rmix del paciente y obtener el volumen intracelular ICV utilizando Rmix teniendo en cuenta que una célula de un primer tipo de tejido contribuye de forma diferente a la resistencia eléctrica Rmix del volumen intracelular ICV en comparación con una célula de un segundo tipo de tejido. Como un volumen intracelular ICV puede considerarse el espacio completo ICV o sólo una parte como el espacio ICW o un parámetro directamente relacionado... [Seguir leyendo]
Reivindicaciones:
1. Un método para determinar un volumen intracelular ICV de un paciente comprendiendo los pasos de:
determinar una resistencia eléctrica intracelular Rmix del paciente,
obtener el volumen intracelular ICV utilizando Rmix teniendo en cuenta que una célula de un primer tipo de tejido contribuye de manera diferente a la resistencia eléctrica Rmix del volumen intracelular ICV en comparación con una célula de un segundo tipo de tejido,
en el que el primer tipo de tejido es tejido adiposo y el segundo tipo de tejido es tejido magro,
determinar una resistencia eléctrica extracelular RE del paciente,
en el que se determina la masa total M del paciente en donde la obtención se lleva a cabo por iteración utilizando un valor normal de inicio para el volumen intracelular ICV, la iteración comprendiendo los siguientes pasos:
obtener un volumen de agua extracelular ECW del paciente utilizando RE,
obtener el volumen de mal-hidratación ECWEX y así la masa de mal-hidratación MEX del paciente utilizando el volumen de agua extracelular ECW y la masa total M del paciente,
obtener la masa MLT del compartimento de tejido magro del paciente usando una ecuación basada en la masa de mal-hidratación MEX del paciente, la masa total M del paciente, el volumen intracelular ICV y constantes de proporcionalidad iLT y iAT las constantes proporcionalmente relacionando las masas de tejido magro MLT y del compartimento del tejido adiposo MAT con componentes correspondientes de tejido magro y de tejido adiposo ICVLT y ICVAT del volumen intracelular ICV, y la ecuación siendo obtener la masa MAT del compartimento de tejido adiposo del paciente por sustracción de las masas MLT y MEX de la masa total M,
obtener la resistividad mezclada Pmix a partir de valores de referencia para sujetos sanos en dependencia de la proporción MAT/MLT,
utilizar la resistividad mezclada Pmix así determinada para obtener un nuevo valor para el volumen intracelular ICV y repetir la iteración hasta que se logre convergencia suficiente.
2. El método según la reivindicación 1 caracterizado porque además comprende los pasos de determinar al menos una medida antropométrica X del paciente y obtener el volumen intracelular ICV también utilizando la medida antropométrica X.
3. El método según la reivindicación 2 caracterizado porque la al menos una medida antropométrica X es la altura Hgt del paciente.
4. El método según cualquiera de las reivindicaciones precedentes caracterizado porque el tejido magro se define por el tejido del paciente que no es tejido adiposo.
5. Un dispositivo (10) para llevar a cabo el método según cualquiera de las reivindicaciones precedentes que comprende
una unidad de medición (5) , en donde la unidad de medición comprende un dispositivo de bioimpedancia para determinar una resistencia eléctrica intracelular Rmix del paciente y
una unidad de evaluación (1) configurada para llevar a cabo los pasos del método según cualquiera de las reivindicaciones 1-4,
en el que la unidad de evaluación es una unidad de microprocesador (1) que a su vez comprende una unidad de almacenamiento de programa de microprocesador (1a) ,
medios de entrada (5) para introducir la masa total M del paciente en la unidad de evaluación (1) ,
en donde la unidad de medición (5) está también configurada para determinar una resistencia eléctrica extracelular RE del paciente.
6. El dispositivo según la reivindicación 5 caracterizado porque el dispositivo además comprende medios de entrada (2) para introducir una medida antropométrica X del paciente en la unidad de evaluación (1) y que la unidad de evaluación está configurada para obtener el volumen intracelular ICV utilizando X.
7. El dispositivo según cualquiera de las reivindicaciones 5 o 6 caracterizado porque además comprende una unidad
de salida (9) conectada a la unidad de evaluación (1) para la salida, preferiblemente por visualización, de cualquier dato obtenido de la unidad de evaluación.
8. Un producto de programa de ordenador caracterizado porque comprende un medio de almacenamiento comprendiendo código del software adaptado para realizar los pasos del método según cualquiera de las reivindicaciones 1-4.
Parámetro Valor Descripción Unidad
AICW, LT 0.425 Volumen de agua intracelular por unidad de masa de tejido magro Litros/kg
AICW, AT 0.154 Volumen de agua intracelular por unidad de masa de tejido adiposo Litros/Kg
AECW, LT 0.290 Volumen de agua extracelular por unidad de masa de tejido magro Litros/kg
AICW, AT 0.096 Volumen de agua extracelular por unidad de masa de tejido adiposo Litros/kg
iLT 0.620 Volumen intracelular por unidad de masa de tejido magro Litros/kg
iAT 0.987 Volumen intracelular por unidad de masa de tejido adiposo Litros/kg
DECW 1.020 Densidad del líquido total extracelular Kg/litros
Patentes similares o relacionadas:
Sistemas para electroporación mejorada basada en la detección de tejidos, del 20 de Mayo de 2020, de OncoSec Medical Incorporated: Un dispositivo para la administracion de restos terapeuticos a las celulas en una zona de tratamiento de un tejido, dicho dispositivo que comprende: a) una sonda […]
Mapeo cognitivo utilizando estimulación magnética transcraneal, del 29 de Abril de 2020, de Nexstim Oy: Un método de mapeo cognitivo que comprende las etapas de: - determinar una respuesta de línea de base cognitiva para una función cognitiva de un sujeto como respuesta […]
Procedimiento para determinar un continente de volumen corregido de un paciente amputado, dispositivo para realizar el procedimiento y producto de programa informático, del 29 de Abril de 2020, de FRESENIUS MEDICAL CARE DEUTSCHLAND GMBH: Procedimiento para determinar un continente de volumen corregido V(t) de un paciente en el instante t, donde al paciente le faltan miembros individuales o partes […]
Dispositivo para la determinación no invasiva de la presión arterial, del 15 de Abril de 2020, de Heller, Arnulf: Dispositivo para la determinación no invasiva de la presión arterial de un cuerpo humano o animal, que comprende al menos un equipo de medición de bioimpedancia con […]
Dispositivo para la neuroestimulación efectiva no invasiva de dos etapas, del 1 de Enero de 2020, de FORSCHUNGSZENTRUM JULICH GMBH: Dispositivo para la estimulación de neuronas , que comprende - una unidad de estimulación no invasiva para la generación de estímulos […]
Un sistema de seguimiento para detectar el útero de manera continua, del 1 de Enero de 2020, de Fertigo Medical Ltd: Un sistema de seguimiento continuo del útero, que comprende: un inserto uterino , un módulo de despliegue , un dispositivo de control […]
Procedimiento y dispositivo para la determinación de datos de bioimpedancia de una persona, del 11 de Diciembre de 2019, de seca ag: Procedimiento para la determinación de datos de bioimpedancia de una persona que se encuentra de pie, en cuyo caso se mide al menos un valor de bioimpedancia mediante […]
Dispositivo y método para evaluar el nivel de consciencia, dolor y nocicepción durante el estado de vigilia, la sedación y la anestesia general, del 27 de Noviembre de 2019, de QUANTIUM MEDICAL S.L: Dispositivo para evaluar en tiempo real el efecto hipnótico y analgésico en un sujeto durante el estado de vigilia, la sedación y la anestesia general, que […]