MEJORADORES DE LA TRANSCRIPCION DE ENOS PARA USO EN LA TERAPIA CELULAR DE ENFERMEDADES CARDIACAS ISQUEMICAS.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2004/011944.
Solicitante: SANOFI-AVENTIS DEUTSCHLAND GMBH.
Nacionalidad solicitante: Alemania.
Dirección: BRUNINGSTRASSE 50,65929 FRANKFURT AM MAIN.
Inventor/es: HEESCHEN,CHRISTOPHER, DIMMELER,STEFANIE, ZEIHER,ANDREAS, RUETTEN,HARTMUT.
Fecha de Publicación: .
Fecha Concesión Europea: 6 de Enero de 2010.
Clasificación Internacional de Patentes:
- A61K31/00 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › Preparaciones medicinales que contienen ingredientes orgánicos activos.
- A61K31/165 A61K […] › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › teniendo ciclos aromáticos, p. ej. colchicina, atenolol, progabide.
Clasificación PCT:
- A61K31/167 A61K 31/00 […] › teniendo el átomo de nitrogeno de un grupo carboxiamida unido directamente al ciclo aromático, p. ej. lidocaina, paracetamol.
- A61P9/10 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › A61P 9/00 Medicamentos para el tratamiento de trastornos en el aparato cardiovascular. › para enfermedades isquémicas o ateroscleróticas, p.ej. medicamentos antianginosos, vasodilatadores coronarios,medicamentos para el tratamiento del infarto de miocardio, de la retinopatía, de la insuficiencia cerebrovascular, de la arterioesclerosis renal.
Clasificación antigua:
- A61K31/167 A61K 31/00 […] › teniendo el átomo de nitrogeno de un grupo carboxiamida unido directamente al ciclo aromático, p. ej. lidocaina, paracetamol.
- A61P9/10 A61P 9/00 […] › para enfermedades isquémicas o ateroscleróticas, p.ej. medicamentos antianginosos, vasodilatadores coronarios,medicamentos para el tratamiento del infarto de miocardio, de la retinopatía, de la insuficiencia cerebrovascular, de la arterioesclerosis renal.
Fragmento de la descripción:
Mejoradores de la transcripción de eNOS para uso en la terapia celular de enfermedades cardíacas isquémicas.
La presente invención se refiere al uso de compuestos que mejoran la transcripción de sintasa de óxido nítrico endotelial (eNOS) para tratar células estaminales y madre en la terapia celular de pacientes con enfermedades cardíacas isquémicas tales como enfermedad cardíaca coronaria o cardiomiopatía isquémica. El tratamiento de tales células que pueden aislarse, por ejemplo, de médula ósea, con un mejorador de la transcripción de eNOS antes de su administración aumenta su actividad funcional y mejora la neovascularización del corazón y la regeneración cardíaca.
El fallo cardiaco post-infarto continúa siendo una causa principal de morbidez y mortalidad en pacientes con una enfermedad cardíaca isquémica tal como enfermedad cardíaca coronaria o cardiomiopatía isquémica. Aunque la reperfusión rápida de la arteria ocluída ha reducido significativamente las proporciones de mortalidad temprana, los procedimientos de remodelación ventricular caracterizados por una expansión progresiva del área de infarto y la dilatación de la cavidad ventricular izquierda producen a menudo el desarrollo de fallo cardíaco en pacientes que sobreviven a un infarto de miocardio agudo. El principal fin para invertir la remodelación sería el estímulo de la neovascularización así como la mejora de la regeneración de miocitos cardíacos dentro del área de infarto.
Los resultados de investigaciones recientes han establecido un papel fundamental para las células estaminales y madre endoteliales en neovascularización postnatal y regeneración cardíaca. La mejora de la neovascularización después de isquemia crítica es una opción terapéutica importante después de sucesos tales como infarto de miocardio o isquemia de miembros, por ejemplo. Hasta hace poco, se creía que la neovascularización de tejido isquémico en el adulto estaba restringida a la migración y proliferación de células endoteliales maduras, un proceso denominado angiogénesis. Entre tanto, una evidencia creciente sugiere que las células madre endoteliales (EPCs) circulantes vuelven a lugares de isquemia y contribuyen a la formación de nuevos vasos sanguíneos (C. Kalka et al., Transplantation of ex vivo expanded endothelial progenitor cells for therapeutic neovascularization, Proc. Natl. Acad. Sci. USA 2000, 97:3422-7). Por analogía al desarrollo embriónico de vasos sanguíneos a partir de madres endoteliales primitivas (angioblastos), se hace referencia a ste proceso como vasculogénesis.
La importancia de las células madre circulantes se demuestra por el hecho de que la inhibición genética de su reclutamiento inhibe la angiogénesis de tumores. Las EPCs pueden movilizarse desde la médula ósea a la circulación por el factor de crecimiento endotelial vascular (VEGF) o el factor derivado de células estromales (SDF)-1. VEGF y SDF-1 están profundamente sobrerregulados en tejido hipóxico, sugiriendo que VEGF y SDF-1 constituyen señales de vuelta para reclutar células madre circulantes a fin de aumentar los mecanismos de reparación endógenos después de isquemia crítica (S.H. Lee et al., Early expression of angiogenesis factors in acute myocardial ischemia and infarction, N. Engl. J. Med. 2000, 342:626-33).
Estudios experimentales recientes sostienen que células madre obtenidas de la médula ósea o la sangre contribuyen a la regeneración del miocardio infartado y aumentan la neovascularización del miocardio isquémico (A.A. Kocher et al., Neovascularization of ischemic myocardium by human bone-marrow-derived angioblasts prevents cardiomyocyte apoptosis, reduces remodeling and improves cardiac function, Nat. Med. 2001, 7:430-6; D. Orlic et al., Bone marrow cells regenerate infarcted myocardium, Nature 2001, 410:701-5; S. Fuchs et al., Catheter-based autologous bone marrow myocardial injection in no-option patients with advanced coronary artery disease: a feasibility study, J. Am. Coll. Cardiol. 2003, 41:1721-4). Además, la infusión intravenosa o la inyección intramiocárdica de células madre de adulto produjo una mejora sostenida de la función cardíaca después de infarto de miocardio inducido experimentalmente y en pacienes con enfermedad cardíaca isquémica crónica. Se ha demostrado clínicamente que la infusión intracoronaria de células estaminales y madre de adulto es factible y segura en pacientes con infarto de miocardio agudo y en pacientes con cardiomiopatía isquémica crónica (B. Assmus et al., Transplantation of progenitor cells and regeneration enhancement in acute myocardial infarction (TOPCARE-AMI), Circulation 2002, 106:3009-17; B.E. Strauer et al., Repair of infarcted myocardium by autologous intracoronary mononuclear bone marrow cell transplantation in humans, Circulation 2002, 106:1913-8). Tal terapia celular, que en un paciente se realiza como una terapia celular autóloga, está asociada con mejoras significativas de la función ventricular izquierda regional y global.
Un prerrequisito para el éxito de la terapia celular en pacientes con una enfermedad cardíaca isquémica es la vuelta y, así, el injerto de las células trasplantadas en el área objetivo del corazón, especialmente si se escoge una vía intravascular de administración. Mientras que el número de células estaminales y madre de la médula ósea de diversos tipos tales como células estaminales y madre mesenquémicas y hematopoyéticas es similar en pacientes con una enfermedad cardíaca isquémica y testigos sanos, desgraciadamente la actividad funcional de las células estaminales y madre de pacientes con una enfermedad cardíaca isquémica está deteriorada y su capacidad de vuenta disminuida. Este deterioro funcional de las células estaminales y madre de pacientes con enfermedad cardíaca coronaria limita su potencial terapéutico para terapia celular clínica. Esto es de aplicación especialmente cuando se usa una vía intravascular de administración que requiere que se extravasen las células madre frente a un gradiente quimioatractivo con el fin de invadir y volver a tejido isquémico. La actividad funcional y la capacidad de vuelta de células estaminales y madre pueden valorarse determinando su actividad de formación de colonias o actividad migratoria, por ejemplo en respuesta a VEGF o SDF-1. Vigilar la actividad migratoria o de formación de colonias de células estaminales y madre antes de la terapia celular puede servir como un ensayo sustituto para identificar pacientes que pueden obtener mayor beneficio de la terapia celular. Por otra parte, se ha descrito recientemente que EPCs derivadas de médula ósea totalmente funcionales de ratones donantes sanos restablecen la angiogénesis cardíaca de hospedantes senescentes en un modelo de ratón de neovascularización deteriorada (J.M. Edelberg et al., Young adult bone marrow-derived endothelial precursor cells restore aging-impaired cardiac angiogenic function, Circ. Res. 2002, 90:e89-e93). Así, sería ventajoso si pudiera restablecerse la actividad de las células estaminales y madre deterioradas funcionalmente por medios adecuados, por ejemplo por manipulación farmacológica o genética antes de la administración, y por ello mejorarse el beneficio terapéutico de los pacientes de la terapia celular.
Sorprendentemente, se ha encontrado que puede mejorarse considerablemente la función deteriorada de células estaminales y madre de pacientes con una enfermedad cardíaca isquémica por incubación con un mejorador de transcripción de sintasa de óxido nítrico endotelial. La expresión mejorada de sintasa de óxido nítrico endotelial, producida por tratamiento ex vivo de las células de pacientes con un mejorador de la transcripción de ENOs antes de su readministración, mejora o restablece la actividad funcional de estas células, como se ha demostrado in vitro usando un ensayo de transmigración e in vivo en un modelo de ratón de isquemia de miembro trasero como se indica después. En este último modelo, la neovascularización después de la ligación de la arteria femoral se determina mediante medida del flujo sanguíneo, y se ha encontrado que el efecto beneficioso de células estaminales y madre administradas de pacientes con enfermedad cardíaca isquémica si se ha aumentado sustancialmente después del pretratamiento con un mejorador de la transcripción de ENOs. Se ha probado que el efecto observado es causada realmente por la actividad mejorada de sintasa de NO endotelial y formación de NO por el efecto de abrogación de NG-monometil-L-arginina (L-NMMA), que se sabe que es un inhibidor de la formación de eNOS y NO. La incubación...
Reivindicaciones:
1. Uso de un mejorador de transcripción de sintasa de óxido nítrico endotelial para la producción de un medicamento para el tratamiento ex vivo de células estaminales y/o madre en la terapia celular de un paciente con una enfermedad cardíaca isquémica.
2. Uso según la reivindicación 1, en el que el mejorador de transcripción de sintasa de óxido nítrico endotelial es un compuesto de fórmula I
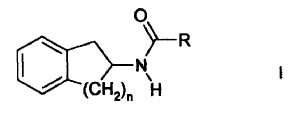
en la que
3. Uso según la reivindicación 1 y/o la reivindicación 2, en el que el mejorador de transcripción de sintasa de óxido nítrico endotelial se selecciona entre 4-fluoro-N-(indan-2-il)benzamida e indan-2-ilamida de ácido 2,2-difluorobenzo[1,3]dioxol-5-carboxílico.
4. Uso según una o más de las reivindicaciones 1 a 3, en el que las células estaminales y/o madre se obtienen de la médula ósea del paciente.
5. Uso según una o más de las reivindicaciones 1 a 4, en el que las células estaminales y/o madre se incuban con un mejorador de transcripción de sintasa de óxido nítrico endotelial durante un período de 6 horas a 48 horas.
6. Uso según una o más de las reivindicaciones 1 a 5, en el que la enfermedad cardíaca isquémica es enfermedad cardíaca coronaria, enfermedad de arterias coronarias, síndrome coronario agudo, angina de pecho, infarto de miocardio, cardiomiopatía isquémica o fallo cardíaco congestivo.
7. Uso según una o más de las reivindicaciones 1 a 6, en el que las células estaminales y/o madre tratadas se administran al paciente por inyección o infusión intravenosa, intracoronaria o intramiocárdica.
8. Un procedimiento para producir un medicamento para tratar células estaminales y/o madre en la terapia celular de un paciente con una enfermedad cardíaca isquémica, que comprende emplear un mejorador de transcripción de sintasa de óxido nítrico endotelial.
9. Un procedimiento para producir células estaminales y/o madre con actividad funcional aumentada que comprende tratar células estaminales y/o madre de un paciente con una enfermedad cardíaca isquémica con un mejorador de transcripción de sintasa de óxido nítrico endotelial.
10. Una composición farmacéutica para el tratamiento ex vivo de células estaminales y/o madre en la terapia celular de un paciente con una enfermedad cardíaca isquémica, que comprende un mejorador de transcripción de sintasa de óxido nítrico endotelial.
11. Una composición farmacéutica para uso en el tratamiento ex vivo de células estaminales y/o madre en la terapia celular de un paciente con una enfermedad cardíaca isquémica, que comprende un mejorador de transcripción de sintasa de óxido nítrico endotelial según se define en la reivindicación 2 y/o la reivindicación 3.
12. Un mejorador de transcripción de sintasa de óxido nítrico endotelial para uso en el tratamiento ex vivo de células estaminales y/o madre en la terapia celular de un paciente con una enfermedad cardíaca isquémica.
13. Un mejorador de transcripción de sintasa de óxido nítrico endotelial de la fórmula I
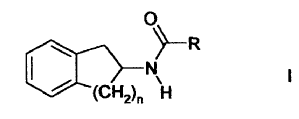
en la que
14. Un mejorador de transcripción de sintasa de óxido nítrico endotelial para uso en el tratamiento ex vivo de células estaminales y/o madre en la terapia celular de un paciente con una enfermedad cardíaca isquémica, que es 4-fluoro-N-(indan-2-il)benzamida.
15. Un mejorador de transcripción de sintasa de óxido nítrico endotelial para uso en el tratamiento ex vivo de células estaminales y/o madre en la terapia celular de un paciente con una enfermedad cardíaca isquémica, que es indan-2-ilamida de ácido 2,2-difluorobenzo[1,3]dioxol-5-carboxílico.
Patentes similares o relacionadas:
Métodos y composiciones para trastornos relacionados con la proliferación celular, del 27 de Mayo de 2020, de Agios Pharmaceuticals, Inc: Un método in vitro para diagnosticar a un sujeto que tiene un trastorno relacionado con la proliferación celular o que se sospecha que tiene un trastorno relacionado con […]
Uso de inhibidores de la PDE4 para la profilaxis y/o la terapia de la dislipoproteinemia y trastornos relacionados, del 27 de Mayo de 2020, de Albert-Ludwigs-Universität Freiburg: Inhibidor específico de la fosfodiesterasa 4 (PDE 4) para uso en el tratamiento profiláctico o terapéutico de la dislipoproteinemia, en donde el inhibidor […]
Un canal catiónico no selectivo en células neurales y compuestos que bloquean el canal para su uso en el tratamiento de la inflamación del cerebro, del 6 de Mayo de 2020, de UNIVERSITY OF MARYLAND, BALTIMORE: Un antagonista de SUR1 que bloquea el canal de NCCa-ATP para su uso en (a) la prevención o el tratamiento de la inflamación de las células neurales […]
Inhibidores de ERK y sus usos, del 8 de Abril de 2020, de Celgene CAR LLC: Un compuesto de fórmula VIII: **(Ver fórmula)** o una de sus sales farmacéuticamente aceptables, en donde: el anillo A se selecciona de **(Ver fórmula)** […]
Procedimiento de uso de inmunoconjugados anti-CD79b, del 8 de Abril de 2020, de F. HOFFMANN-LA ROCHE AG: Un inmunoconjugado que comprende un anticuerpo anti-CD79b unido a un agente citotóxico para su uso en un procedimiento para tratar un trastorno proliferativo […]
IMIPRAMINA PARA USO COMO INHIBIDOR DE LA SOBREXPRESIÓN DE LA FASCINA 1, del 2 de Abril de 2020, de FUNDACION UNIVERSITARIA SAN ANTONIO: La presente invención se refiere a imipramina para su uso como inhibidor de la sobreexpresión de la fascina 1, preferiblemente dicha sobreexpresión de la fascina 1 está asociada […]
Composiciones y métodos para la distribución de moléculas en células vivas, del 25 de Marzo de 2020, de THE TEXAS A & M UNIVERSITY SYSTEM: Un compuesto que tiene la fórmula: **(Ver fórmula)** En donde X es un resto de unión, Y es un residuo de aminoácido acoplado de forma covalente […]
Mutación novedosa del receptor de andrógenos, del 25 de Marzo de 2020, de NOVARTIS AG: Una composicion terapeutica para su uso en el tratamiento de un paciente que padece cancer de prostata o de mama, asociado con una mutacion del receptor de […]