INHIBIDORES DE PARP TRICICLICOS.
Un compuesto de Fórmula I, II o III, o su sal farmacéuticamente aceptable,
para su uso como medicamento citotóxico para el tratamiento del cáncer, en el que el cáncer está causado por un defecto genético en un gen que media la recombinación homóloga.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/GB2004/003183.
Solicitante: CANCER RESEARCH TECHNOLOGY LIMITED
PFIZER, INC.
Nacionalidad solicitante: Reino Unido.
Dirección: SARDINIA HOUSE, SARDINIA STREET,LONDON WC2A 3NL.
Inventor/es: HELLEDAY,THOMAS, CURTIN,NICOLA.
Fecha de Publicación: .
Fecha Concesión Europea: 13 de Enero de 2010.
Clasificación Internacional de Patentes:
- A61K31/5517 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › condensadas con ciclos de cinco eslabones teniendo el nitrógeno como heteroátomo de un ciclo, p. ej. imidazobenzodiazepinas, triazolam.
- A61K38/00A
- C07D487/06 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07D COMPUESTOS HETEROCICLICOS (Compuestos macromoleculares C08). › C07D 487/00 Compuestos heterocíclicos que contienen átomos de nitrógeno como únicos heteroátomos del ciclo en el sistema condensado, no previstos por los grupos C07D 451/00 - C07D 477/00. › Sistemas peri-condensados.
- C12N15/113D
Clasificación PCT:
- A61K31/5517 A61K 31/00 […] › condensadas con ciclos de cinco eslabones teniendo el nitrógeno como heteroátomo de un ciclo, p. ej. imidazobenzodiazepinas, triazolam.
- A61P35/00 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › Agentes antineoplásicos.
- C07D487/06 C07D 487/00 […] › Sistemas peri-condensados.
Clasificación antigua:
- A61K31/5517 A61K 31/00 […] › condensadas con ciclos de cinco eslabones teniendo el nitrógeno como heteroátomo de un ciclo, p. ej. imidazobenzodiazepinas, triazolam.
- A61P35/00 A61P […] › Agentes antineoplásicos.
- C07D487/06 C07D 487/00 […] › Sistemas peri-condensados.
Fragmento de la descripción:
Inhibidores de PARP tricíclicos.
Compuestos terapéuticos.
Esta invención se refiere a una serie de compuestos que son derivados de índoles de lactama tricíclicos y benzimidazoles de lactama tricíclicos y que inhiben a la poli(ADP-ribosa)polimerasa (PARP) y a su uso en el tratamiento del cáncer, en particular, el cáncer de mama.
Se ha demostrado que la recombinación homóloga (RH) desempeña un papel importante en la reparación del daño que se da en horquillas de replicación del ADN en células de mamíferos (2). Por eso, las células deficientes en RH muestran un crecimiento retardado y exhiben unos niveles más altos de inestabilidad genética. Se piensa que la inestabilidad genética debida a la pérdida de la reparación de RH en cánceres humanos contribuye considerablemente al desarrollo del cáncer en estas células (1).
La modificación post-transcripcional de proteínas nucleares por poli(ADP-ribosil)ación como respuesta a roturas en las cadenas de ADN desempeña un papel importante en la reparación del ADN, la regulación de la apoptosis y el mantenimiento de la estabilidad genómica.
La poli(ADP-ribosa)polimerasa (PARP-1) es un miembro principal de la familia de enzimas PARP y es una proteína nuclear abundante en células de mamíferos. La PARP-1 cataliza la formación de polímeros de poli(ADP-ribosa) (PAR) usando NAD+ como sustrato. Cuando se produce el daño del ADN, la PARP-1 se une rápidamente a una rotura monocatenaria del ADN (SSB) y cataliza la adición de cadenas de PAR negativamente cargadas a sí misma (automodificación) y otras proteínas [véase (3, 4) para revisiones]. Se piensa que la unión de PARP-1 a las SSB protege las lesiones de ADN de un procesamiento posterior hasta que la PARP-1 sea disociada de la rotura por la carga negativa acumulada que resulta de polímeros PAR (5, 6).
Aunque se haya implicado a PARP-1 en varios procesos nucleares, tales como la modulación de la estructura de cromatina, la replicación del ADN, la reparación del ADN y la transcripción, los ratones genéticamente modificados con PARP-1 se desarrollan normalmente (7). Las células aisladas de estos ratones muestran un fenotipo de hiper-recombinación y una inestabilidad genética en la forma de mayores niveles de micronúcleos de intercambios de cromátides hermanas (SCE) y tetraploidía (8, 10). También puede darse inestabilidad genética en estos ratones genéticamente modificados con PARP-1 por acortamiento del telómero, mayor frecuencia de la fusión cromosómica y aneuploide (11), aunque todos estos resultados no pudieran ser repetidos en otro grupo de ratones genéticamente modificados con PARP-1 (12). En el primer ratón genéticamente modificado, la mutación nula de PARP-1 rescató la recombinación V (D) J perjudicada en ratones SCID (13).
Estos resultados apoyan la opinión sugerida por Lindahl y colaboradores de que PARP-1 tiene una función protectora frente a la recombinación (5). Se propuso que la unión de PARP-1 a roturas de ssDNA impide el reconocimiento y el procesamiento de las lesiones de ADN por la maquinaria de recombinación o, por otro lado que las cargas negativas acumuladas después de la poli(ADP-ribosil)ación repelen las secuencias de ADN recombinogénicas adyacentes. Sólo el último modelo es consecuente con la inhibición de la propia PARP-1 y la expresión de un mutante negativo dominante PARP-1, incluyendo SCE, la amplificación de genes y la recombinación homóloga (14-18).
Los estudios basados en el tratamiento de células con inhibidores de PARP-1 o células derivadas de ratones genéticamente modificados con PARP-1 indican que la supresión de la actividad de PARP-1 aumenta la susceptibilidad de las células frente a agentes perjudiciales del ADN e inhibe la reincorporación de la rotura de la cadena (3, 4, 8-11, 19, 20).
Los documentos WO 01/16136 A y WO 00/42040 A describen una variedad de compuestos tricíclicos diferentes que inhiben la actividad de PARP. Canon Koch et al. (Journal of Medicinal Chemistry, Vol. 45, 2002, pps. 4961-4974) muestran la actividad quimiopotenciadora anticáncer de inhibidores de PARP-1.
Se han usado inhibidores de la actividad de PARP-1 junto con regímenes de tratamiento del cáncer tradicionales tales como radioterapia y quimioterapia (21). Cuando se usaron los inhibidores en combinación con agentes metilantes, venenos de topoisomerasa y radiaciones ionizantes, se encontró que se realzaba la eficacia de estas formas de tratamiento. Sin embargo, tales tratamientos no son selectivos y como tal, causan daños y muerte a las células no cancerosas o "sanas". Además, se sabe que tales tratamientos dan ocasión a efectos secundarios desagradables.
Por lo tanto, es muy deseable proporcionar un tratamiento para el cáncer que sea tanto eficaz como selectivo en la eliminación de células cancerígenas y que no tenga que ser administrado en combinación con tratamientos quimioterapéuticos o radioterapéuticos.
Sorprendentemente, se ha encontrado que células deficientes en recombinación homóloga (RH) son hipersensibles a inhibidores de PARP con relación a células tipo silvestres.
Por lo tanto, según un primer aspecto de la presente invención, se proporciona un compuesto de Fórmula I, II o III, o su sal farmacéuticamente aceptable, para su uso como medicamento citotóxico para el tratamiento del cáncer, en el que el cáncer está causado por un defecto genético en un gen que media la recombinación homóloga.
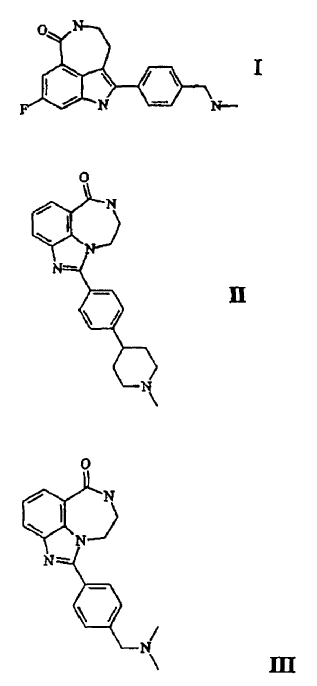
Los compuestos descritos en este documento pueden prepararse por rutas sintéticas basadas en las descritas en los documentos WO 00/42040 y WO 01/16136.
Se sobrentenderá que cuando se haga referencia en esta memoria descriptiva a compuestos de fórmulas I a III, la referencia debería interpretarse como que se amplía también a sus sales farmacéuticamente aceptables.
Según se indica en este documento, las sales farmacéuticamente aceptables incluyen sales metálicas, fosfatos y aminas cuaternarias. Las sales metálicas pueden estar formadas por metales alcalinos tales como litio, sodio o potasio.
Preferiblemente, la fórmula I, más arriba, se administra en la forma de una sal de fosfato farmacéuticamente aceptable que tiene la fórmula siguiente:
Fórmula I
Fosfato

La presente invención se refiere a la utilidad terapéutica de los compuestos descritos en este documento.
Según un aspecto adicional de la presente invención, se proporciona el uso de una cantidad terapéutica de un compuesto de fórmula I, II o III, o su sal farmacéuticamente aceptable, en la fabricación de un medicamento citotóxico para el tratamiento de un cáncer, en el que el cáncer está causado por un defecto genético en un gen que media la recombinación homóloga.
El cáncer causado por un defecto genético en un gen que media la recombinación homóloga incluye, en particular, el cáncer de mama.
Según se describen en este documento, "cáncer" o "tumor" incluyen, aunque no limitados, cáncer de pulmón, colon, páncreas, estómago, ovario, cerviz, pecho, próstata, hueso, cerebro o piel.
Los inhibidores de PARP se usan en el tratamiento del cáncer que está causado por un defecto genético en un gen en el que dicho gen media recombinaciones homólogas. Las células cancerígenas de este tipo tienden a ser defectuosas en RH.
La sensibilidad específica de los tumores defectuosos en RH respecto a la inhibición de PARP significa que las células "sanas" que se dividen normalmente en pacientes que tienen cantidades adecuadas de RH no estarán, en gran parte, afectadas por el tratamiento.
Una ventaja adicional del tratamiento que usa inhibidores de PARP consiste en que los inhibidores de PARP no tienen que ser administrados como una terapia de combinación junto con tratamientos de radioterapia o quimioterapia convencionales, evitándose así los efectos secundarios asociados a estas formas convencionales de tratamiento.
Un defecto en un gen que media la recombinación homóloga puede ser debido a una mutación en un gen que codifica una proteína implicada en la RH, a su ausencia, o a su expresión defectuosa.
Las células cancerígenas adecuadas para el tratamiento con los compuestos descritos en este documento pueden ser deficientes,...
Reivindicaciones:
1. Un compuesto de Fórmula I, II o III, o su sal farmacéuticamente aceptable, para su uso como medicamento citotóxico para el tratamiento del cáncer, en el que el cáncer está causado por un defecto genético en un gen que media la recombinación homóloga.

2. Un compuesto según la reivindicación 1, en el que el compuesto es el compuesto de Fórmula I.
3. Un compuesto según la reivindicación 2, en el que el compuesto de Fórmula I está en la forma de una sal de fosfato.
4. Un compuesto según cualquiera de las reivindicaciones 1 a 3, en el que el cáncer es cáncer de mama.
5. Un compuesto según cualquiera de las reivindicaciones 1 a 4, en el que el defecto genético es la ausencia de un gen que codifica una proteína implicada en la recombinación homóloga.
6. Un compuesto según cualquiera de las reivindicaciones 1 a 4, en el que el defecto genético está en la expresión de un gen que codifica una proteína implicada en la recombinación homóloga.
7. Un compuesto según la reivindicación 6, en el que el gen que media la recombinación homóloga se selecciona entre el grupo que consiste en XRCC1, CTPS, RPA, RPA1, RPA2, RPA3, XPD, ERCC1, XPF, MMS19, RAD51, RAD51ß, RAD51C, RAD51D, DMC1, XRCCR, XRCC3, BRCA1, BRCA2, RAD52, RAD54, RAD50, MRE11, NB51, WRN, BLM KU70, KU80, ATM, ATR CHK1, CHK2, FANCA, FANCB, FANCC, FANCD1, FANCD2, FANCE, FANCF, FANCG, RAD1 y RAD9.
8. Un compuesto según la reivindicación 6 o la reivindicación 7, en el que el gen que media la recombinación homóloga es un gen supresor de tumor.
9. Un compuesto según la reivindicación 8, en el que el gen supresor de tumor es BRCA1 y/o BRCA2.
10. El uso de una cantidad terapéutica de un compuesto de Fórmula I, II o III, o su sal farmacéuticamente aceptable, en la fabricación de un medicamento citotóxico para el tratamiento del cáncer, en el que el cáncer está causado por un defecto genético en un gen que media la recombinación homóloga.
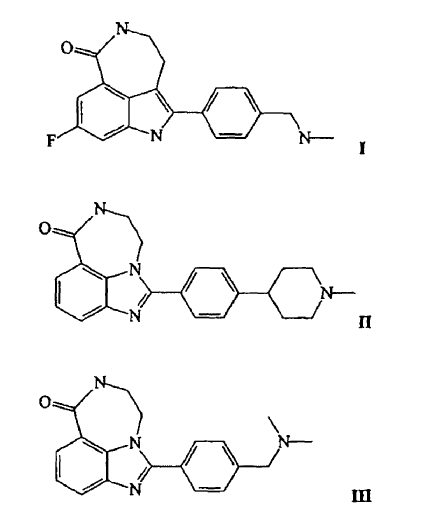
11. El uso según la reivindicación 10, en el que el compuesto es el compuesto de Fórmula I.
12. El uso según la reivindicación 11, en el que el compuesto de Fórmula I está en la forma de una sal de fosfato.
13. El uso según cualquiera de las reivindicaciones 10 a 12, en el que el cáncer es cáncer de mama.
14. El uso según cualquiera de las reivindicaciones 10 a 13, en el que el defecto genético es la ausencia de un gen que codifica una proteína implicada en la recombinación homóloga.
15. El uso según cualquiera de las reivindicaciones 10 a 14, en el que el defecto genético está en la expresión de un gen que codifica una proteína implicada en la recombinación homóloga.
16. El uso según la reivindicación 15, en el que el gen que media la recombinación homóloga se selecciona entre el grupo que consiste en XRCC1, CTPS, RPA, RPA1, RPA2, RPA3, XPD, ERCC1, XPF, MMS19, RAD51, RAD51ß, RAD51C, RAD51D, DMC1, XRCCR, XRCC3, BRCA1, BRCA2, RAD52, RAD54, RAD50, MRE11, NB51, WRN, BLM KU70, KU80, ATM, ATR CHK1, CHK2, FANCA, FANCB, FANCC, FANCD1, FANCD2, FANCE, FANCF, FANCG, RAD1 y RAD9.
17. El uso según la reivindicación 15 o la reivindicación 16, en el que el gen que media la recombinación homóloga es un gen supresor de tumor.
18. El uso según la reivindicación 17, en el que el gen supresor de tumor es BRCA1 y/o BRCA2.
Patentes similares o relacionadas:
COMPOSICIONES DE ALPRAZOLAM AMORFO CON ACTIVIDAD ANSIOLÍTICA, CON ETILCELULOSA Y CROSPOVIDONA, Y PROCEDIMIENTOS CORRESPONDIENTES, del 18 de Junio de 2020, de LABORATORIOS BAGO S.A.: Composición de alprazolam amorfo con actividad ansiolítica que comprende: a) una premezcla que contiene: - entre 0,33 y 0,66% p/p de alprazolam; - entre […]
Antagonistas de V1a para tratar trastornos del sueño por desplazamiento de fase, del 25 de Marzo de 2020, de F. HOFFMANN-LA ROCHE AG: Un antagonista de V1a para su uso en el tratamiento y/o prevención de trastornos del sueño por desplazamiento de fase, en el que el antagonista de V1a es […]
Composiciones farmacéuticas que comprenden esteres de ácidos grasos, del 13 de Noviembre de 2019, de Alkermes Pharma Ireland Limited: Una composición farmacéutica que comprende: (a) un agente antipsicótico insoluble en agua, en donde el agente antipsicótico insoluble en agua es aripiprazol, un […]
Composiciones farmacéuticas que comprenden ésteres de glicerol, del 6 de Noviembre de 2019, de Alkermes Pharma Ireland Limited: Una composición farmacéutica que comprende: (a) un agente antipsicótico insoluble en agua, en donde el agente antipsicótico insoluble en agua es aripiprazol, […]
Nuevos derivados de octahidro-pirrolo[3,4-c]-pirrol y análogos de los mismos como inhibidores de autotaxina, del 23 de Octubre de 2019, de F. HOFFMANN-LA ROCHE AG: Compuestos de fórmula (I) **Fórmula** en la que R1 es cicloalquilo C3-10 sustituido, cicloalquil C3-10-alquilo C1-12 sustituido, fenilo sustituido, fenil-alquilo […]
Compuestos inhibidores de bromodominios y composición farmacéutica que los comprende para prevenir o tratar un cáncer, del 26 de Junio de 2019, de Kainos Medicine, Inc: Compuesto de fórmula (I), o sal, hidrato, solvato o estereoisómero farmacéuticamente aceptable del mismo: **Fórmula** en la que, R1 se selecciona […]
Composiciones de midazolam para administración bucal en el tratamiento de convulsiones para obtener comienzo de acción rápido, del 29 de Mayo de 2019, de SWIPP AB: Composición de dosificación unitaria en forma de una película que contiene desde 0,25 mg hasta 2 mg de midazolam o una sal farmacéuticamente aceptable del […]
Forma de dosificación sólida de disolución rápida, del 17 de Mayo de 2019, de IX Biopharma Ltd: Una forma de dosificacion de oblea porosa liofilizada de desintegracion y disolucion rapidas, adecuada para la liberacion de un material biologicamente activo […]