Haces de hélices superenrolladas de lipopéptido y partículas pseudovíricas sintéticas.
Bloque constructivo de lipopéptido que consiste de una cadena peptídica de entre 21 y 80 residuos aminoácidos,
que comprende un dominio superenrollado unido covalentemente a una fracción lípido que comprende dos o tres cadenas hidrocarbilo largas y opcionalmente unido a un antígeno.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2007/010601.
Solicitante: UNIVERSITÄT ZÜRICH PROREKTORAT FORSCHUNG.
Nacionalidad solicitante: Suiza.
Dirección: RÄMISTRASSE 71 8006 ZÜRICH SUIZA.
Inventor/es: BOATO,FRANCESCA, FREUND,ANNABELLE, GHASPARIAN,ARIN, MÖHLE,KERSTIN, ROBINSON,JOHN A, THOMAS,RICHARD M.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K39/00 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › Preparaciones medicinales que contienen antígenos o anticuerpos (materiales para ensayos inmunológicos G01N 33/53).
- C07K14/005 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 14/00 Péptidos con más de 20 aminoácidos; Gastrinas; Somatostatinas; Melanotropinas; Sus derivados. › de origen vírico.
PDF original: ES-2392080_T3.pdf
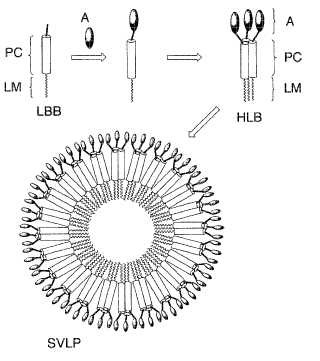
Fragmento de la descripción:
Haces de helices superenrolladas de lipopeptido y particulas pseudoviricas sinteticas
Campo de la invencion La invencion se refiere a bloques constructivos de lipopeptido que comprenden un dominio superenrollado y opcionalmente un antigeno, los cuales se agregan formando haces de lipopeptidos helicoidales y particulas pseudoviricas sinteticas. Las particulas pseudoviricas sinteticas que portan antigenos resultan utiles como vacunas.
Antecedentes de la invencion Es bien conocido que los peptidos y proteinas de pequeno tamano habitualmente solo son pobremente inmunogenicos. Los adyuvantes toxicos, tales como el bien conocido adyuvante completo de Freund, han sido
ampliamente utilizados para inducir respuestas inmunologicas contra vacunas de subunidades en animales, aunque muchas no pueden utilizarse en el ser humano debido a sus efectos secundarios toxicos. La situacion ideal seria evitar por completo la utilizacion de adyuvantes externos, pero esto tipicamente resulta en respuestas inmunologicas pobres. Sin embargo, el sistema inmunologico (humano) genera respuestas inmunologicas robustas contra patogenos que expresan estructuras antigenicas repetidas sobre una superficie, por ejemplo las superficies de un
virus [Zinkernagel R., Science 171:173-178, 1996]. Los liposomas han sido intensamente investigados durante los ultimos 30 anos como portadores para productos farmaceuticos, entre ellos farmacos, acidos nucleicos y biofarmacos, y son bien conocidas las aplicaciones de los mismos, por ejemplo los vehiculos de administracion para antigenos, acidos nucleicos y farmacos. Las propiedades
de los liposomas pueden alterarse mediante el acoplamiento de peptidos o proteinas a la superficie de los mismos con el fin de reconocer receptores especificos, creando sistemas conocidos como proteoliposomas. Tambien se han incorporado peptidos y proteinas en liposomas con el fin de generar respuestas inmunologicas [Leserman L., J. Liposome Res. 14:175-189, 2004; Frisch B. et al., Methods Enzymol. 373:51-73, 2003]. El conjugado de peptidos con lipidos facilita su insercion en los liposomas, con el lipido anclado en la membrana bicapa, permitiendo de esta
manera el reconocimiento del peptido por parte de anticuerpos en la superficie del liposoma. Una de las desventajas de los liposomas como vehiculo general de administracion es su inestabilidad in vivo, debido a su rapida eliminacion de la sangre y la captura por parte de las celulas del sistema reticuloendotelial [Torchilin V.P., Nat. Rev. Drug Discov. 4:145-160, 2005].
Las potenciales ventajas de la utilizacion de particulas pseudoviricas, compuestas de virus naturales o modificados geneticamente y las quimeras, incluyendo fagos o componentes viricos naturales o modificados geneticamente, tales como las proteinas de capside, las proteinas de superficie y las glucoproteinas, o fragmentos de los mismos, en el diseno de las vacunas, han sido reconocidas desde hace ya cierto tiempo [Felnerova D. et al., Curr. Opin. Biotechnol. 15:518-529, 2004; Garcea R.L. et al., Curr. Opin. Biotechnol. 15:513
517, 2004; Doan L.
. et al., Rev. Med. Virol. 15:75-88, 2005]. La produccion de dichas particulas pseudoviricas utiliza los procesos viricos naturales de autoensamblaje. Pueden aprovecharse las estructuras nucleares autoensamblantes naturales de muchos virus utilizando tecnologia de ADN recombinante para expresar uno o mas antigenos sobre la superficie de dichas particulas. Estas particulas pseudoviricas no son accesibles mediante sintesis quimica debido a su gran tamano y complejidad estructural. Las solicitudes de patente WO n°
98/014564 y n° 00/035479 se refieren a "particulas pseudoviricas sinteticas", aunque las particulas a las que se hace referencia en ellas se basan en particulas viricas naturales o modificadas geneticamente, o a componentes de las mismas, construidas mediante metodos de ADN recombinante y basados en celulas, no materiales producidos mediante sintesis quimica. La patente WO n° 00/32227 describe la utilizacion de particulas nucleares de origen natural o no natural a la que se unen antigenos de modo ordenado y repetitivo, ejemplificadas por la
utilizacion del virus recombinante Sindbis. Tambien se han realizado esfuerzos considerables para disenar peptidos y proteinas autoensamblantes para aplicaciones nanotecnologicas. Se han producido morfologias a escala nanometrica basadas en peptidos anfifilicos de diseno [Lowik D.W.P.M. et al., Chem. Soc. Rev. 33:234-245, 2004], incluyendo las presentan estructuras
secundarias de cadenas º, laminas º y helices a] [Rajagopal K. et al., Curr. Opin. Struct. Biol. 14:480-486, 2004; Tu
R.S.et al., Adv. Drug Deliv. Revs. 56:1537-1563, 2004]. Pueden encontrarse ejemplos adicionales de la utilizacion de lipopeptidos para preparar materiales compuestos nanoestructurados en el trabajo de Stupp y colaboradores [Behanna H.A. et al., J. Am. Chem. Soc. 127:1193-1200, 2005]. Anteriormente se ha demostrado el autoensamblaje de un peptido anfifilo en nanofibras [Hartgerink J.D. et al., Science 294:1684-1688, 2001].
Uno de los problemas principales durante el diseno de vacunas efectivas basadas en antigenos sinteticos ha sido su baja inmunogenicidad. Las moleculas sinteticas relativamente pequenas tienden a ser poco inmunogenicas. Un enfoque para superar dicha baja inmunogenicidad es conjugar covalentemente el antigeno sintetico con un portador, tal como una proteina como la toxina tetanica o la hemocianina de lapa americana (KLH) [Herrington D.A. et al.,
Nature 328:257-259, 1987]. Sin embargo, el conjugado todavia debe administrarse en el animal conjuntamente con un adyuvante (por ejemplo alum o adyuvante de Freund) para inducir una respuesta inmunologica fuerte. Se han descrito otros metodos para producir constructos multiepitopo que incorporan epitopos de celulas B y de celulas T (revisados en [Jackson D.C. et al., Vaccine 18:355-361, 1999].
Los analogos sinteticos de lipopeptidos bacterianos han recibido mucha atencion en la investigacion sobre vacunas, por sus efectos adyuvantes y como portadores para peptidos antigenicos [Ghielmetti M. et al., Immunobiology 210:211-215, 2005]. Es conocido que los lipidos y lipopeptidos pueden actuar como adyuvantes de inmunogenos peptidicos que de otra manera serian debiles [Jung G. et al., Angew. Chem. Int. Ed. 10:872, 1985; Martinon F. et al.,
J. Immunol. 149:3416, 1992]. Se ha informado de muchos constructos lipopeptidos, en los que un lipido con efectos adyuvantes conocidos se acopla con un peptido para generar candidatos a vacunas autoadyuvantes. Han sido particularmente bien estudiados la tripalmitoil-S-gliceril-cisteina (N-palmitoil-S- (2, 3-bis- (O-palmitoiloxi) -propil) cisteinilo o Pam3Cys) y la dipalmitoil-S-gliceril-cisteina (2, 3-bis- (O-palmitoiloxi) -propil) -cisteinilo o Pam2Cys) [Ghielmetti M. et al., Immunobiology 210:211-215, 2005]. Dichas fracciones lipidicas se encuentran en componentes lipoproteina de las membranas interna y externa de las bacterias Gram-negativas. Los lipopeptidos sinteticos que portan dichos u otros residuos S-gliceril-cisteina diacilados o triacilados en el extremo N-terminal se ha demostrado que son ligandos especificos de receptores de tipo Toll [Reutter F. et al., J. Pept. Res. 65:375-383, 2005; Buwitt-Beckmann U. et al., Eur. J. Immunol. 35:1-8, 2005]. Ademas, la conjugacion de peptidos antigenicos con Pam3Cys o Pam2Cys se ha aplicado al diseno de candidatos a vacuna sintetica autoadyuvante [Bessler W.G. et al., Int. J. Immunopharmac. 19:547-550, 1998; Loleit M. et al., Biol. Chem. Hoppe-Seyler, 371:967-975, 1990; Muller C.P. et al., Clin. Exp. Immunol. 78:499-504, 1989]. La solicitud de patente WO n° 98/07752 describe la utilizacion para el direccionamiento de farmacos, de lipopeptidos en los que la parte peptido puede ser una secuencia de tipo colageno capaz de inducir la formacion de estructuras de triple helice.
Recientemente han aparecido varias revisiones sobre el diseno de helices superenrolladas [Woolfson D.N., Adv. Prot. Chem. 70:79-112, 2005], incluyendo un volumen de Advances in Protein Chemistr y dedicado a las helices superenrolladas, el colageno y los elastomeros [Parr y D.A.D. et al., Advances in Protein Chemistr y 70, 2005]. Muchos virus y microbios naturales contienen secuencias peptidicas con estructura de helice superenrollada dentro de sus propias proteinas de superficie (por ejemplo la hemaglutinina del virus Influenza o gp41 del virus 1 de la inmunodeficiencia humana (VIH-1) o la glucoproteina F del virus sincitial respiratorio (VSR)... [Seguir leyendo]
Reivindicaciones:
1. Bloque constructivo de lipopeptido que consiste de una cadena peptidica de entre 21 y 80 residuos
aminoacidos, que comprende un dominio superenrollado unido covalentemente a una fraccion lipido que 5 comprende dos o tres cadenas hidrocarbilo largas y opcionalmente unido a un antigeno.
2. Bloque constructivo de lipopeptido segun la reivindicacion 1, en el que la cadena peptidica comprende un dominio superenrollado que consiste de tres a ocho motivos heptadas.
3. Bloque constructivo de lipopeptido segun la reivindicacion 1, en el que la cadena peptidica comprende un dominio superenrollado que forma dimeros, trimeros, tetrameros, pentameros, hexameros o heptameros.
4. Bloque constructivo de lipopeptido segun la reivindicacion 2, en el que, en el dominio superenrollado las posiciones a y d en cada motivo heptada (abcdefg) comprenden a-aminoacidos con cadenas laterales hidrofobicas de tamano pequeno a intermedio y/o cadenas laterales aromaticas o heteroaromaticas; en cero, una o dos de todas las posiciones a y d, un aminoacido con un residuo no cargado polar y en cero o una de todas las posiciones a y d un aminoacido con un residuo cationico polar o un derivado acilado del mismo, o con
un residuo anionico polar, o glicina.
5. Bloque constructivo de lipopeptido segun la reivindicacion 4, en el que la cadena lateral hidrofobica de tamano pequeno a intermedio es R1, en la que R1 es alquilo inferior, alquenilo inferior, - (CH2) a (CHR2) bOR3, (CH2) a (CHR2) bSR3, - (CHR2) OR3, - (CH2) aSR3, - (CH2) aR4 o -CH (CF3) 2; en el que R2 es alquilo inferior, R3 es alquilo inferior, R4 es ciclohexilo, ciclopentilo o ciclobutilo, a es 1 a 4, y b es 0 o 1,
la cadena lateral aromatica o heteroaromatica es R5, en la que R5 es - (CH2) aR6, - (CH2) cO (CH2) dR6, (CH2) cS (CH2) dR6, o - (CH2) cNR7 (CH2) dR6; en las que R7 es H, alquilo inferior, arilo o aril-alquilo inferior, R6 es fenilo opcionalmente sustituido de formula -C6R8R9R10R11R12 o un grupo arilo o heteroarilo de una de las formulas H1 a H14,
30 35 40 6. en la que cada uno de R8, R9, R10, R11 y R12 es, independientemente, H, F, Br, Cl, I, NO2, CF3, NR7R14 , N7COR14, alquilo inferior, arilo o OR7; R13 es H, Cl, Br, I, NO2, alquilo inferior o arilo; R14 es H, alquilo inferior o arilo; a es 1 a 4; c es 1 o 2; y d es 0 a 4; el residuo no cargado polar es R15, en el que R15 es (CH2) d (CHR16) bOR17, - (CH2) d (CHR16) bSR17, - (CH2) aCONR17R18 o - (CH2) aCOOR19; en el que R16 es alquilo inferior, arilo, arilo-alquilo inferior, - (CH2) aOR17, - (CH2) aNR17R18, - (CH2) aNR17R18 o - (CH2) aCOOR19; R17 y R18 son, independientemente, H, alquilo inferior, arilo, o arilo-alquilo inferior, o R17 y R18 conjuntamente son - (CH2) e-, - (CH2) 2-O- (CH2) 2-o - (CH2) 2-NR17- (CH2) 2-; R19 es alquilo inferior, arilo, arilo-alquilo inferior; y en el que a, b y d presentan los significados definidos anteriormente y e es 2 a 6; el residuo cationico polar o un derivado acilado del mismo es R20 , en el que R20 es - (CH2) aNR17R18 , - (CH2) aN=C (NR21R22) NR17R18 , - (CH2) aNR21C (=NR22) NR17R18, - (CH2) aNR21COR19 o - (CH2) aNR21CONR17R18; en el que R21 es H o alquilo inferior y R22 es H o alquilo inferior; y R17, R18 y R19 presentan los mismos significados que los definidos anteriormente y a es 1 a 4; y el residuo anionico polar es R23 , en el que R23 es - (CH2) aCOOH, en el que a es 1 a 4. Bloque constructivo de lipopeptido segun la reivindicacion 4, en el que: los a-aminoacidos con cadena lateral hidrofobica de tamano pequeno a intermedio son la alanina, la isoleucina, la leucina, la metionina y la valina, los a-aminoacidos con cadena lateral aromatica o heteroaromatica son la fenilalanina, la tirosina, el triptofano y 45 la histidina, los a-aminoacidos con un residuo no cargado polar son la asparagina, la cisteina, la glutamina, la serina y latreonina, los a-aminoacidos con residuo cationico polar son la arginina, la lisina y la histidina, y los a-aminoacidos con un residuo anionico polar son el acido aspartico y el acido glutamico.
7. Bloque constructivo de lipopeptido segun la reivindicacion 1, en el que la cadena peptidica comprende un 5 peptido de SEC ID n° 1 a n° 29.
8. Bloque constructivo de lipopeptido segun cualquiera de las reivindicaciones 1 a 7, en el que la fraccion lipido es una de entre los tipos Z1 a Z8,
en el que R1 y R2 son hidrocarbilos largos o hidrocarbil-C=O largo e Y es H o COOH.
en el que R1, R2 y R3 son hidrocarbilos largos o R1 y R2 son hidrocarbil-C=O largo y R3 es H o acetilo,
en el que R1 y R2 son hidrocarbil-C=O largo y n es 1, 2, 3 o 4,
en el que R1 y R2 son hidrocarbilos largos, es O o NH, y n es 1, 2, 3 o 4, o
en el que R1 y R2 son hidrocarbilos largos, y en el que el hidrocarbilo largo es alquilo o alquenilo lineal o ramificado que consiste de entre 8 y 25 atomos de carbono y opcionalmente uno, dos o tres dobles enlaces en la cadena.
9. Bloque constructivo de lipopeptido segun cualquiera de las reivindicaciones 1 a 8, en el que la cadena peptidica CP se encuentra unida covalentemente a la fraccion lipido FL en el extremo N-terminal o en el extremo Cterminal o en una posicion proxima a cualquiera de los mismos.
10. Bloque constructivo de lipopeptido segun cualquiera de las reivindicaciones 1 a 8, en el que la cadena peptidica
CP se encuentra unida covalentemente a la fraccion lipido FL en el extremo N-terminal o en el extremo C10 terminal o mediante un conector tal como en la formula (2) o (3) ,
en el que L es un conector L1 a L10,
en el que es O o NH, m esta comprendido entre 1 y 20 y n esta comprendido entre 1 y 20.
11. Bloque constructivo de lipopeptido segun cualquiera de las reivindicaciones 1 a 10, en el que un antigeno seleccionado de entre un peptido, una proteina, un mimetico de epitopo, un carbohidrato o un hapteno se une covalentemente en el otro extremo de la cadena peptidica o en una posicion proxima al mismo.
12. Haces de lipopeptido helicoidal que comprenden dos, tres, cuatro, cinco, seis o siete bloques constructivos de lipopeptido segun cualquiera de las reivindicaciones 1 a 11.
13. Particulas pseudoviricas sinteticas que consiste de haces de lipopeptido helicoidal segun la reivindicacion 12.
14. Preparacion farmaceutica que comprende un haz de lipopeptidos helicoidales y/o una particula pseudovirica sintetica segun las reivindicaciones 12 y 13 portadores de antigenos.
15. Preparacion farmaceutica segun la reivindicacion 14, en la que el antigeno se deriva de la proteina circunsporozoito (CS) del parasito del paludismo Plasmodium falciparum.
16. Utilizacion de un haz de lipopeptidos helicoidales y/o una particula pseudovirica sintetica segun la reivindicacion 13 portador de antigenos a modo de vacuna.
45
46
47
48
49
50
51
52
53
54
Patentes similares o relacionadas:
Eliminación de impurezas de cultivos celulares residuales, del 29 de Julio de 2020, de NOVARTIS AG: Un método para eliminar la Proteína Nuclear (NP) de la Gripe de una preparación que comprende proteínas del virus de la gripe de interés que incluyen hemaglutinina […]
 Cepas de Bordetella vivas atenuadas como vacuna de dosis única contra la tos ferina, del 29 de Julio de 2020, de INSTITUT PASTEUR DE LILLE: Una vacuna que comprende una cepa viva, atenuada y mutada de Bordetella pertussis que comprende al menos una mutación del gen (ptx) de la toxina […]
Cepas de Bordetella vivas atenuadas como vacuna de dosis única contra la tos ferina, del 29 de Julio de 2020, de INSTITUT PASTEUR DE LILLE: Una vacuna que comprende una cepa viva, atenuada y mutada de Bordetella pertussis que comprende al menos una mutación del gen (ptx) de la toxina […]
Inmunoterapia novedosa contra diversos tumores, entre ellos tumores cerebrales y neuronales, del 22 de Julio de 2020, de IMMATICS BIOTECHNOLOGIES GMBH: Péptido que comprende una secuencia de aminoácidos acorde con la SEQ ID N.º 19, en que dicho péptido tiene una longitud total de entre 9 y 16 aminoácidos.
Método para producir inmunoconjugados de anticuerpo-SN-38 con un enlazador CL2A, del 22 de Julio de 2020, de IMMUNOMEDICS, INC.: Un método para producir un compuesto, CL2A-SN-38, que presenta la estructura, **(Ver fórmula)** que comprende realizar un esquema de reacción como el que se muestra: **(Ver […]
Composición de vacuna que contiene un adyuvante sintético, del 22 de Julio de 2020, de INFECTIOUS DISEASE RESEARCH INSTITUTE: Una composición farmacéutica que comprende: un adyuvante lípido de glucopiranosilo (GLA), que tiene la fórmula: **(Ver fórmula)** en la que: […]
Arenavirus trisegmentados como vectores de vacunas, del 22 de Julio de 2020, de UNIVERSITE DE GENEVE: Una partícula de arenavirus trisegmentada infecciosa y competente para la replicación que comprende un segmento L y dos segmentos S, en donde uno de los dos segmentos […]
Anticuerpo anti-FGF23 y composición farmacéutica que comprende el mismo, del 15 de Julio de 2020, de Kyowa Kirin Co., Ltd: Anticuerpo o fragmento funcional del mismo que se une a la totalidad o a una parte del epítopo de FGF23 humano, al que se une un anticuerpo producido […]
Composiciones para inducir la diferenciación de células supresoras derivadas mieloides para tratar el cáncer y las enfermedades infecciosas, del 15 de Julio de 2020, de OSE Immunotherapeutics: Un compuesto seleccionado del grupo que consiste en un anticuerpo y un fragmento de unión a antígeno del mismo que se une específicamente a la proteína […]