Fragmentos proteicos poliepitópicos de las proteínas E6 y E7 del HPV, su obtención y sus usos particularmente en vacunación.
Fragmentos poliepitópicos de la proteína E6 de HPV humano caracterizados por el hecho de que comprenden:
- una secuencia peptídica de aproximadamente 15 a 30 aminoácidos, preferiblemente con un número de aminoácidos superior o igual a 17 e inferior o igual a 30 para los fragmentos poliepitópicos delimitados por los aminoácidos situados en 118 y 139: (118)CPEEKQRHLDKKQRFHNIRGRW(139) (o SEC ID Nº :10),
- esta secuencia peptídica contiene las secuencias de aminoácidos de por lo menos 3 epítopos diferentes que se enlazan de manera estable a las moléculas de HLA de tipo idéntico o diferente, cuando estos epítopos se obtienen por degradación enzimática de dicha secuencia peptídica, particularmente en el proteasoma, de manera que al menos 4 moléculas de HLA de diferentes tipos se enlazan a estos epítopos, estas 4 moléculas de HLA se seleccionan de entre las de tipo A1, A2, A3, A11, A24, A29, B7, 88, B18, B27, B35, B44, B51 y B62 para los fragmentos poliepitópicos de la proteína E6.
Tipo: Patente Europea. Resumen de patente/invención. Número de Solicitud: E10177363.
Solicitante: Assistance Publique-Hopitaux.
Nacionalidad solicitante: Francia.
Dirección: 3, Avenue Victoria 75100 Paris RP FRANCIA.
Inventor/es: BOURGAULT-VILLADA, ISABELLE, CHOPPIN,Jeannine, CONNAN,Francine, FERRIES,Estelle, GUILLE,JEAN-GÉRARD.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K38/00 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00).
- A61K39/00 A61K […] › Preparaciones medicinales que contienen antígenos o anticuerpos (materiales para ensayos inmunológicos G01N 33/53).
- A61K39/12 A61K […] › A61K 39/00 Preparaciones medicinales que contienen antígenos o anticuerpos (materiales para ensayos inmunológicos G01N 33/53). › Antígenos virales.
- A61P31/18 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › A61P 31/00 Antiinfecciosos, es decir antibióticos, antisépticos, quimioterápicos. › para el VIH.
- C07K14/025 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 14/00 Péptidos con más de 20 aminoácidos; Gastrinas; Somatostatinas; Melanotropinas; Sus derivados. › Papovaviridae, p. ej. virus de papiloma, virus del polioma, SV40, virus BK, virus JC.
- C07K14/16 C07K 14/00 […] › VIH-1.
- C07K16/08 C07K […] › C07K 16/00 Inmunoglobulinas, p. ej. anticuerpos mono o policlonales. › contra materiales víricos.
- C12N15/12 C […] › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 15/00 Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K). › Genes que codifican proteínas animales.
- C12N15/33 C12N 15/00 […] › Genes que codifican proteínas virales.
- C12N15/37 C12N 15/00 […] › Papovaviridae, p. ej. virus del papiloma, virus del polioma, SV 40.
PDF original: ES-2509901_T3.pdf
Fragmento de la descripción:
Fragmentos proteicos poliepitópicos de las proteínas E6 y E7 del HPV, su obtención y sus usos particularmente en vacunación [0001] La presente invención se refiere a fragmentos proteicos poliepitópicos, tales como los de la proteína E6 de los papilomavirus humanos, su procedimiento de obtención y sus usos, particularmente en el dominio de la vacunación terapéutica o preventiva.
La invención se refiere de una forma más particular al uso de fragmentos poliepitópicos de una proteína determinada para la preparación de medicamentos destinados a la prevención o al tratamiento de patologías en las que dicha proteína es reconocida por el sistema inmunitario celular.
Ventajosamente, dichos fragmentos poliepitópicos son tales que su aminoácido N-terminal corresponde al aminoácido N-terminal del epítopo situado en sentido ascendente de uno o más epítopos de una región poliepitópica de dicha proteína, y su aminoácido C-terminal corresponde al aminoácido C-terminal del epítopo situado en sentido descendente del o de los epítopos anteriormente mencionados de dicha región poliepitópica.
Así, los fragmentos proteicos poliepitópicos anteriormente mencionados de la presente invención corresponden ventajosamente a las regiones poliepitópicas de una proteína determinada, a saber a las regiones que contienen varios epítopos reconocidos por las células T en asociación con las diferentes moléculas del complejo mayor de histocompatibilidad (CMH) , dichas regiones se seleccionan entre las que tienen la característica de ser degradadas in vitro en péptidos más cortos por proteasomas, tales como el proteasoma 205, cuando el fragmento proteico testado se pone en presencia de dicho proteasoma, particularmente según el método detallado siguiente. El fragmento proteico (aproximadamente 75 μg cuando se trata de un polipéptido de aproximadamente 30 aminoácidos) se incuba a 37º C con aproximadamente 15μg de proteasoma 20S (Calbiochem Ref 539150, La Jolla, CA, EEUU) en 500 μ l del tampón siguiente: 20 mM de Tris-HCl pH8, 0, 5 mM de EDTA. Alícuotas de 50 μl son recogidos después del tiempo de incubación de 24 y 48 horas y se analizan por cromatografía líquida de alta presión (HPLC) . Los productos de digestión de los proteasomas se separan por RP-HPLC (Perkin Elmer) utilizando una columna C18 y un gradiente acetonitrilo (de 0 a 100 % que contiene 0, 1 % de ácido trifluoroacético, en 90 mn, índices de elución 0, 8 ml/mn) . Los productos de división se detectan a 214 nm por un detector de absorción (759A, Applied Biosystems) .
Ventajosamente, las regiones poliepitópicas definidas anteriormente poseen la característica de contener aminoácidos hidrófobos.
Los diferentes epítopos de la región poliepitópica de la proteína determinada, y que delimitan los fragmentos proteicos poliepitópicos, se seleccionan ventajosamente entre los péptidos;
- que se unen a una molécula determinada del CMH, particularmente a una molécula de tipo HLA determinada, y hasta concentraciones de aproximadamente 10-6 M a aproximadamente 10-10 M en péptido para unas concentraciones de aproximadamente 10-7 M en molécula de HLA, particularmente en las condiciones descritas a continuación,
- y que forman un complejo estable con esta molécula del CMH, a saber particularmente un complejo en el que dicho péptido permanece unido a dicha molécula durante al menos aproximadamente 3 horas a 37º C.
A modo de ilustración, los epítopos anteriormente mencionados de la invención se seleccionan de entre los péptidos susceptibles:
- por una parte, de asociarse con las moléculas del CMH, particularmente por ejecución del método siguiente:
â?¢ incubación (particularmente durante aproximadamente 2 horas a 25º C, luego aproximadamente 15 horas a 4º C) del péptido en presencia de moléculas del CMH, provenientes de la lisis de células humanas o animales o purificadas particularmente por cromatografía de afinidad a partir de líneas celulares humanas
o animales,
â?¢ captura de los complejos formados en la etapa precedente en un soporte sólido recubierto de un primer anticuerpo, particularmente monoclonal, que reconoce específicamente las moléculas del CMH en su conformación dependiente de su enlace a dicho péptido,
â?¢ adición sobre el soporte sólido precedente de un segundo anticuerpo marcado, particularmente por acoplamiento a un marcador radioactivo, enzimático o fluorescente, dichos anticuerpos marcados reconocen específicamente bien las cadenas pesadas del CMH en su conformación dependiente de su enlace al péptido, bien la cadena ligera del CMH o la β-microglobulina que se enlaza específicamente a las diferentes cadenas pesadas del CMH en su conformación anteriormente mencionada,
â?¢ detección, después del aclarado del soporte sólido, de la eventual presencia de segundos anticuerpos marcados que quedan fijados sobre el soporte sólido, testimoniando un efecto de asociación entre las moléculas del CMH y el péptido estudiado, - y, por otra parte, de formar un complejo con dichas moléculas del CMH, cuya estabilidad se puede evaluar por ejecución de un método de seguimiento a la vez que el enlace establecido entre el péptido y las moléculas del CMH, este método se realiza ventajosamente según un protocolo idéntico al método precedente, pero en el que la etapa de incubación del péptido en presencia de las moléculas del CMH sobre el soporte sólido recubierto de dicho primer anticuerpo está precedida de una etapa previa de eliminación del péptido libre susceptible de estar presente en el medio reactivo, particularmente por lavado del soporte sólido, dicha etapa de incubación se lleva a cabo (ventajosamente a una temperatura de 37º C) durante tiempos variables de 1h, 3h, 5h, 24h y 48h.az<
Como se ha mencionado anteriormente, los epítopos de la invención deben ser reconocidos por las células T en asociación con las moléculas del CMH y asociarse a estas últimas, particularmente en el marco de la ejecución de la prueba de reconocimiento descrita anteriormente. Esta asociación puede ser baja (detectable a concentraciones en análogos peptídicos del orden de 10-4 a 10-5 M) , intermedia (detectable a concentraciones en análogos peptídicos del orden de 10-6 a 10-7 M) o fuerte (detectable a concentraciones en análogos peptídicos del orden de 10-8 a 10-9 M) . Los péptidos asociados a las moléculas del CMH en el marco de la presente invención son preferiblemente susceptibles de unirse durante al menos aproximadamente 3 horas a dichas moléculas del CMH.
La invención tiene de una forma más particular como objetivo los epítopos (también designados péptidos anteriormente y a continuación) tales como los descritos anteriormente y que están caracterizados por el hecho de que se seleccionan de entre los que son susceptibles:
- de inducir in vitro la citólisis a través de linfocitos T citotóxicos, de células objetivo que presentan en su superficie el péptido anteriormente mencionado asociado a las moléculas del CMH, dichos linfocitos T citotóxicos se recogen ventajosamente de un paciente que sufre una patología en la que está implicado el péptido estudiado,
- y de inducir in vitro la secreción de citocinas (o interleuquinas) por los linfocitos T citotóxicos anteriormente mencionados, particularmente IL-2, IL-4 o el interferón γ.
En su caso, los epítopos anteriormente mencionados son elegidos de entre los que son capaces de inducir in vitro la aparición y el crecimiento de linfocitos T citotóxicos a partir de células humanas o animales, particularmente a partir de células mononucleares de la sangre periférica (PBMC) , en presencia de factores necesarios para el crecimiento y la diferenciación de las células T citotóxicas.
Los fragmentos proteicos poliepitópicos de la invención se caracterizan además por el hecho de que son susceptibles de contener epítopos CD4 reconocidos por las células T auxiliares en asociación con las moléculas del CMH de clase II, esta propiedad favorece la inducción y el mantenimiento de las células T CD8+ que reconocen los epítopos comprendidos en dichos fragmentos.
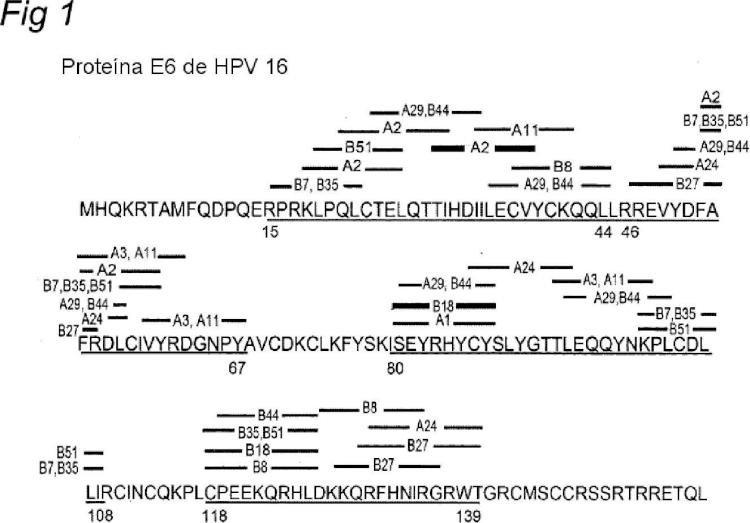
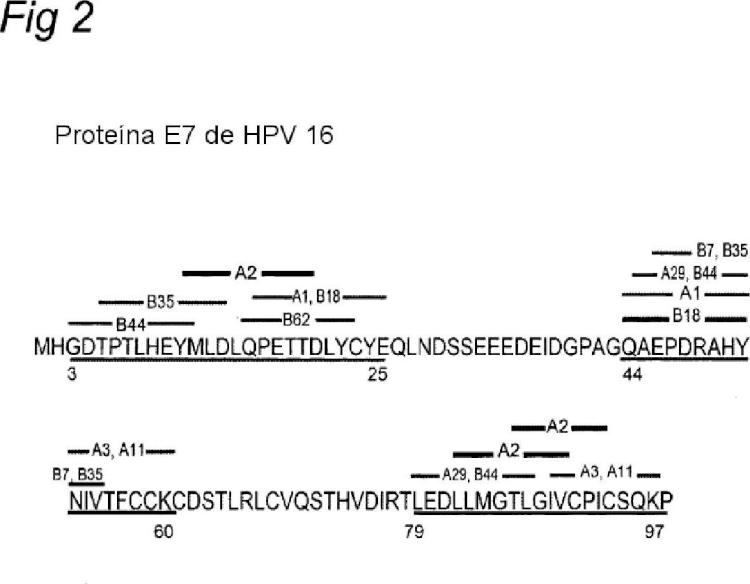
La presente invención se ilustra con ayuda de las figuras 1 y 2, que representan respectivamente las secuencias peptídicas de la proteína E6 y E7 de la cepa 16 de los papilomavirus humanos (HPV 16) , así como los fragmentos poliepitópicos de la invención y los epítopos dentro de estos fragmentos.
La invención tiene de una forma más particular como objetivo los fragmentos poliepitópicos de la proteína E6 de HPV y, más particularmente, los de la proteína E6 representada en la figura 1 o por SEC ID Nº : 2, de HPV 16, caracterizados por el hecho de que comprenden... [Seguir leyendo]
Reivindicaciones:
1. Fragmentos poliepitópicos de la proteína E6 de HPV humano caracterizados por el hecho de que comprenden:
- una secuencia peptídica de aproximadamente 15 a 30 aminoácidos, preferiblemente con un número de aminoácidos superior o igual a 17 e inferior o igual a 30 para los fragmentos poliepitópicos delimitados por los aminoácidos situados en 118 y 139: (118) CPEEKQRHLDKKQRFHNIRGRW (139) (o SEC ID Nº :10) ,
- esta secuencia peptídica contiene las secuencias de aminoácidos de por lo menos 3 epítopos diferentes que se enlazan de manera estable a las moléculas de HLA de tipo idéntico o diferente, cuando estos epítopos se obtienen por degradación enzimática de dicha secuencia peptídica, particularmente en el proteasoma, de manera que al menos 4 moléculas de HLA de diferentes tipos se enlazan a estos epítopos, estas 4 moléculas de HLA se seleccionan de entre las de tipo A1, A2, A3, A11, A24, A29, B7, 88, B18, B27, B35, B44, B51 y B62 para los fragmentos poliepitópicos de la proteína E6.
2. Fragmentos poliepitópicos de la proteína E6 de HPV según la reivindicación 1, caracterizados por el hecho de que comprenden una secuencia peptídica de aproximadamente 15 a 30 aminoácidos, esta secuencia peptídica contiene las secuencias de aminoácidos de por lo menos 5 epítopos diferentes que se enlazan de manera estable a las moléculas de HLA de tipo idéntico o diferente, cuando estos epítopos se obtienen por degradación enzimática de dicha secuencia peptídica, particularmente en el proteasoma, de manera que al menos 6 moléculas de HLA de diferentes tipos se enlazan a estos epítopos, estas 6 moléculas de HLA se seleccionan de entre las de tipo A1, A2, A3, A11, A24, A29, B7, B8, B18, B27, B35, B44 y B51.
3. Fragmentos poliepitópicos de la proteína E6 de HPV según la reivindicación 1 o 2, caracterizados por el hecho de que comprenden todos un epítopo que se enlaza a la molécula de HLA de tipo B35, un epítopo que se enlaza a la molécula de HLA de tipo B44 y un epítopo que se enlaza a la molécula de HLA de tipo B51.
4. Fragmento poliepitópico de la proteína E6 de HPV según una de las reivindicaciones 1 a 3, caracterizado por el hecho de que corresponden al fragmento de 22 aminoácidos delimitado por los aminoácidos situados en las posiciones 118 y 139 de la secuencia peptídica de la proteína E6 de HPV, este último fragmento está caracterizado por la secuencia peptídica SEC ID Nº : 10 siguiente:
(118) CPEEKQRHLDKKQRFHNIRGRW (139)
dicho fragmento contiene 6 epítopos que se unen de manera estable a por lo menos una de las 7 moléculas de HLA de los siguientes tipos: A24, B8, B18, B27, B35, B44 o B51, dichos epítopos son los siguientes:
- (118) CPEEKQRHL (126) se une de manera estable a las moléculas de HLA de tipo B8, B18, B35, B51,
- (119) PEEKQRHL (126) se une de manera estable a las moléculas de HLA de tipo B44,
- (127) DKKQRFHNI (135) se une de manera estable a las moléculas de HLA de tipo B8,
- (128) KKQRFHNIR (136) se une de manera estable a las moléculas de HLA de tipo B27,
- (130) QRFHNIRGRW (139) se une de manera estable a las moléculas de HLA de tipo B27,
- (131) RFHNIRGRW (139) se une de manera estable a las moléculas de HLA de tipo A24.
5. Fragmentos poliepitópicos de la proteína E6 humana según una de las reivindicaciones 1 a 4, caracterizados por el hecho de que corresponden a las secuencias peptídicas derivadas de los fragmentos poliepitópicos definidos en una de las reivindicaciones 1 a 4, particularmente,
- por sustitución y/o supresión y/o adición de uno o varios aminoácidos, los fragmentos anteriormente mencionados, y/o
- por modificación de al menos un enlace peptídico -CO-NH- de la cadena peptídica de los fragmentos anteriormente mencionados, particularmente por introducción de un enlace del tipo retro o retro-inverso, y/o
- por sustitución de al menos un aminoácido de la cadena peptídica de la secuencia o del fragmento anteriormente mencionados, por un aminoácido no proteinogénico,
dichas secuencias derivadas contienen los péptidos o pseudopéptidos que se unen específicamente a la o a las mismas moléculas del CMH que las que se unen a los péptidos contenidos en los fragmentos poliepitópicos anteriormente mencionados de los que derivan.
6. Secuencias nucleótidas que codifican para un fragmento poliepitópico o para una secuencia peptídica derivada según una de las reivindicaciones 1 a 5, dichas secuencias nucleótidas derivan de la secuencia SEC ID Nº : 1 que codifica para la proteína E6.
7. Secuencias nucleótidas según la reivindicación 6, seleccionadas de entre las siguientes:
- la secuencia SEC ID Nº : 3, que codifica para el fragmento poliepitópico SEC ID Nº : 4 según la reivindicación 4, - la secuencia SEC ID Nº : 7, que codifica para el fragmento poliepitópico SEC ID Nº : 8 según la reivindicación 4, 10
- la secuencia SEC ID Nº : 9, que codifica para el fragmento poliepitópico SEC ID Nº : 10 según la reivindicación 4, 8. Anticuerpos, policlonales o monoclonales, dirigidos contra un fragmento poliepitópico o contra una secuencia peptídica derivada según una de las reivindicaciones 1 a 5. 15
9. Lipopéptido caracterizado por el hecho de que comprende:
- una parte peptídica que comprende uno o varios fragmentos proteicos poliepitópicos o una secuencia peptídica derivada de dichos fragmentos, tal y como se han definido en una de las reivindicaciones 1 a 5, 20
- y una o varias partes lipófilas, tales como las que incluyen:
* una cadena hidrocarbonada en C4 a C20, saturada o insaturada, lineal o ramificada, * o un grupo esteroide, en su caso enlazado a la cadena hidrocarbonada arriba mencionada, dichas partes lipófilas están eventualmente asociadas a un péptido de vector corto que comporta una o varias funciones ionizadas a pH fisiológico, y una función que permite la fijación covalente de dicha cadena hidrocarbonada y/o de dicho grupo esteroide.
10. Composición farmacéutica, o vacuna, caracterizada por el hecho de que comprende:
* a)
- al menos un fragmento poliepitópico de la proteína E6 humana definido en una de la reivindicaciones 1 a 4, 35
- y/o al menos una secuencia peptídica derivada de este fragmento, tal y como se define en la reivindicación 5,
- y/o al menos un vector apropiado, particularmente de los lipopéptidos según la reivindicación 9 y/o micelas,
que contienen al menos un fragmento poliepitópico anteriormente mencionado de la proteína E6 humana, y/o al menos una secuencia derivada arriba mencionada de estos fragmentos, en asociación con un vehículo fisiológicamente aceptable, dicho fragmento proteico poliepitópico y/o su secuencia derivada está, en su caso, asociado a uno o más epítopos exógenos reconocidos por las células T auxiliares, tales 45 como el fragmento peptídico delimitado por los aminoácidos situados en las posiciones 830 y 846 de la secuencia peptídica de la toxina tetánica, la hemaglutinina, o el epítopo PADRE, * o b)
- al menos una secuencia nucleótida según la reivindicación 6 o 7, que codifica para un fragmento poliepitópico anteriormente mencionado de la proteína E6 humana, - y/o al menos una secuencia nucleótida que codifica para una secuencia peptídica derivada de este fragmento, tal y como se ha definido anteriormente, 55
- y/o al menos un vector apropiado anteriormente mencionado, elegido particularmente de entre los virus, que contiene al menos una secuencia nucleótida mencionada arriba, en asociación con un vehículo fisiológicamente aceptable, 60 * o c)
- anticuerpos según la reivindicación 8, dirigidos contra un fragmento poliepitópico de la proteína E6 humana, y/o contra una secuencia peptídica derivada de estos fragmentos, tal y como se ha definido anteriormente. 65
11. Utilización de fragmentos poliepitópicos de la proteína E6 humana definidos en una de las reivindicaciones 1 a 4, o secuencias peptídicas derivadas según la reivindicación 5, o secuencias nucleótidas según la reivindicación 6 o 7, o anticuerpos según la reivindicación 8, o lipopéptidos según la reivindicación 9, para la preparación de un medicamento o vacuna destinada a la prevención o al tratamiento de patologías relacionadas con la infección de individuos por los papilomavirus humanos, tales como las neoplasias cervicales intraepiteliales (CIN) , el cáncer invasivo del cuello del útero, las neoplasias vulvares intraepiteliales (VIN) en el caso de la proteína E6.
12. Epítopos de la proteína E6 del HPV humano elegidos de entre los siguientes.
10. (118) CPEEKQRHL (126) se une de manera estable a las moléculas de HLA de tipo B8, B18, B35, B51, - (119) PEEKQRHL (126) se une de manera estable a las moléculas HLA de tipo B44, - (127) DKKQRFHNI (135) se une de manera estable a las moléculas HLA de tipo B8, 15
- (128) KKQRFHNIR (136) se une de manera estable a las moléculas HLA de tipo B27,
- (130) QRFHNIRGRW (139) se une de manera estable a las moléculas HLA de tipo B27.
Patentes similares o relacionadas:
Eliminación de impurezas de cultivos celulares residuales, del 29 de Julio de 2020, de NOVARTIS AG: Un método para eliminar la Proteína Nuclear (NP) de la Gripe de una preparación que comprende proteínas del virus de la gripe de interés que incluyen hemaglutinina […]
 Cepas de Bordetella vivas atenuadas como vacuna de dosis única contra la tos ferina, del 29 de Julio de 2020, de INSTITUT PASTEUR DE LILLE: Una vacuna que comprende una cepa viva, atenuada y mutada de Bordetella pertussis que comprende al menos una mutación del gen (ptx) de la toxina […]
Cepas de Bordetella vivas atenuadas como vacuna de dosis única contra la tos ferina, del 29 de Julio de 2020, de INSTITUT PASTEUR DE LILLE: Una vacuna que comprende una cepa viva, atenuada y mutada de Bordetella pertussis que comprende al menos una mutación del gen (ptx) de la toxina […]
Inmunoterapia novedosa contra diversos tumores, entre ellos tumores cerebrales y neuronales, del 22 de Julio de 2020, de IMMATICS BIOTECHNOLOGIES GMBH: Péptido que comprende una secuencia de aminoácidos acorde con la SEQ ID N.º 19, en que dicho péptido tiene una longitud total de entre 9 y 16 aminoácidos.
Método para producir inmunoconjugados de anticuerpo-SN-38 con un enlazador CL2A, del 22 de Julio de 2020, de IMMUNOMEDICS, INC.: Un método para producir un compuesto, CL2A-SN-38, que presenta la estructura, **(Ver fórmula)** que comprende realizar un esquema de reacción como el que se muestra: **(Ver […]
Composición de vacuna que contiene un adyuvante sintético, del 22 de Julio de 2020, de INFECTIOUS DISEASE RESEARCH INSTITUTE: Una composición farmacéutica que comprende: un adyuvante lípido de glucopiranosilo (GLA), que tiene la fórmula: **(Ver fórmula)** en la que: […]
Arenavirus trisegmentados como vectores de vacunas, del 22 de Julio de 2020, de UNIVERSITE DE GENEVE: Una partícula de arenavirus trisegmentada infecciosa y competente para la replicación que comprende un segmento L y dos segmentos S, en donde uno de los dos segmentos […]
Composiciones para inducir la diferenciación de células supresoras derivadas mieloides para tratar el cáncer y las enfermedades infecciosas, del 15 de Julio de 2020, de OSE Immunotherapeutics: Un compuesto seleccionado del grupo que consiste en un anticuerpo y un fragmento de unión a antígeno del mismo que se une específicamente a la proteína […]
Polipéptidos biparatópicos antagonistas de la señalización WNT en células tumorales, del 15 de Julio de 2020, de Boehringer Ingelheim International GmbH & Co. KG: Un polipéptido que se une específicamente a LRP5 o LRP6, que comprende - un primer dominio variable individual de inmunoglobulina seleccionado del grupo de dominios […]