Formulaciones terapéuticas del factor de crecimiento de queratinocitos.
Una composición liofilizada del factor de crecimiento de queratinocitos (KGF) que consiste en:
* KGF en una concentración entre 3 mg/mL y 15 mg/mL;
* el tampón de histidina;
* el incrementador del volumen manitol en una concentración entre 2% y 5% p/v;
* sacarosa en una concentración entre 1% y 3% p/v;
* polisorbato en una concentración en el rango entre 0.004% y 0.1% p/v; y donde el pH se encuentra en el rango entre 6.0 y 8.0.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2005/045169.
Solicitante: Swedish Orphan Biovitrum AB (publ).
Nacionalidad solicitante: Suecia.
Dirección: 112 76 Stockholm SUECIA.
Inventor/es: TREUHEIT,MICHAEL,J, DHARMAVARAM,VASUMATHI, PURTELL,JUDITH, ROY,SUZANNE E.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K38/18 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 38/00 Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00). › Factores de crecimiento; Reguladores de crecimiento.
- A61K47/18 A61K […] › A61K 47/00 Preparaciones medicinales caracterizadas por los ingredientes no activos utilizados, p. ej. portadores o aditivos inertes; Agentes de direccionamiento o agentes modificadores enlazados químicamente al ingrediente activo. › Aminas; Amidas; Ureas; Compuestos de amonio cuaternario; Aminoácidos; Oligopéptidos que tienen hasta cinco aminoácidos.
- A61K47/26 A61K 47/00 […] › Hidratos de carbono, p. ej. alcoholes de azúcares, amino azúcares, ácidos nucleicos, mono-, di- u oligo-sacáridos; Sus derivados, p. ej. polisorbatos, ésteres de ácidos grasos sorbitano o glicirricina.
PDF original: ES-2504441_T3.pdf
Fragmento de la descripción:
Formulaciones terapéuticas del factor de crecimiento de queratinocitos Campo de la invención La presente invención se refiere a formulaciones del factor de crecimiento de queratinocitos liofilizado y a métodos para hacer una composición liofilizada compuesta por el factor de crecimiento de queratinocitos.
Antecedentes de la invención El factor de crecimiento de queratinocitos (KGF) es un factor de crecimiento específico de las células epiteliales que fue identificado primero en medio acondicionado de una línea celular de fibroblastos embrionarios pulmonares humanos [Rubin et al., Proc. Natl. Acad. Sci. USA 86:802-806 (1989) ]. La expresión del ARN mensajero para KGF se detectó en varias líneas celulares de fibroblastos estromales derivados de tejidos epiteliales en diversas etapas de desarrollo. La transcripción para KGF también fue evidente en el ARN extraído de riñón de adulto normal y órganos del tubo gastrointestinal [Finch et al., Science 245:752-755 (1989) ]. La evidencia de que KGF es segregado por los fibroblastos en cultivo y se expresa in vivo en la dermis, pero no en la epidermis, indica que KGF puede ser un efector paracrino normal importante de la proliferación de queratinocitos. Los estudios han demostrado que KGF es tan potente como el factor de crecimiento epidérmico (EGF) para estimular la proliferación de los queratinocitos humanos primarios o secundarios en cultivo tisular [Marchese et al., J. Cell Phys. 144:326-332 (1990) ]. KGF es producido por las células mesenquimatosas cerca del epitelio de muchos órganos que incluyen la epidermis, el epitelio gastrointestinal oral e inferior, el páncreas, el hígado, el pulmón, el urotelio, el epitelio prostático y otros [Finch et al, supra, Housley et al., J Clin Invest. 94:1764-77, (1994) ; Yi et al., Am J Path. 145:80-85, (1994) ; Pierce et al., J Exp. Med. 179831-40, (1994) ; Yi et al, J Urol. 154:1566-70, (1995) ; y Ulich et al., J Clin Invest. 93:1298-1306, (1994) ].
La purificación de KGF del medio acondicionado de una línea celular de fibroblastos de embrionarios humanos, así como la secuenciación parcial de aminoácidos del KGF purificado, la clonación del gen de KGF y la expresión del gen en células bacterianas para producir KGF biológicamente activo recombinante se describen en la publicación de patente internacional WO 90/08771. Esta publicación también da a conocer que KGF o polipéptidos tipo KGF son útiles como agentes curativos de heridas por quemaduras o para estimular el tejido córneo trasplantado.
Estudios ex vivo e in vivo en animales adultos normales han demostrado que KGF-1 (en lo sucesivo "KGF") produce cambios en la morfogénesis del folículo piloso, la proliferación de hepatocitos y la proliferación de células epiteliales en pulmón, mama, páncreas, estómago, intestino delgado e intestino grueso [Panos et al., J. Clin. Invest. 92:969-977 (1993) ; Ulich et al., Am. J. Path. 144:862-868 (1994) ; Yi et al., Am. J. Path. 145:80-85 (1994) ; y Ulich et al., J. Clin. Invest. 93:1298-1306 (1994) ]. El papel de KGF en el desarrollo embrionario o neonatal está actualmente en investigación; sin embargo, se ha documentado que KGF es un mediador importante del desarrollo de la vesícula seminal en el ratón recién nacido [Alarid et al., Proc. Natl. Acad. Sci. USA 91:1074-1078 (1994) ]. Además, los ratones que sobreexpresan KGF en los hepatocitos tienen riñones poliquísticos [Nguyen et al., Oncogene 12:210919, (1996) ], mientras que la sobreexpresión de KGF en el pulmón utilizando un promotor surfactante da lugar a ratones con cistoadenomas pulmonares [Simonet et al., Proc. Natl. Acad. Sci. USA 92:12461-65, (1995) ], lo que demuestra la importancia de KGF en el desarrollo renal y pulmonar normal.
Se ha demostrado que KGF aumenta la reepitelización y que aumentó el espesor del epitelio cuando se aplicó tópicamente KGF recombinante a heridas inducidas quirúrgicamente en oreja de conejo o en piel porcina [Pierce et al., J. Exp. Med. 179:831-840 (1994]) ; y Staiano-Coico et al., J. Exp. Med. 178:865-878 (1993) ]. Bosch, et al., [J. Clin. Invest. 98:2683-2687 (1996) ] informaron que la administración del factor de crecimiento de queratinocitos inducirá la proliferación de células hepáticas.
Habitualmente, los polipéptidos purificados son sólo marginalmente estables en estado acuoso y sufren degradación química y física lo que resulta en una pérdida de actividad biológica durante el procesamiento y el almacenamiento. Además, las composiciones de polipéptidos en solución acuosa sufren hidrólisis, como desamidación y escisión del enlace peptídico. Estos efectos representan un problema serio para los polipéptidos terapéuticamente activos destinados a ser administrados a humanos en un rango de dosis definido basado en la actividad biológica.
La administración del factor de crecimiento de queratinocitos sigue siendo una estrategia promisoria para tratar muchas enfermedades que afectan a la población humana. No obstante, no se ha abordado la capacidad de KGF para permanecer como una composición farmacéutica estable en el tiempo en diversas condiciones de almacenamiento y ser por lo tanto eficaz para los pacientes in vivo. Por consiguiente, sigue existiendo la necesidad en el área de proporcionar el factor de crecimiento de queratinocitos en formulaciones estables que sean útiles como agentes terapéuticos para el tratamiento de diversas enfermedades que se benefician de la estimulación mediada por KGF de la multiplicación de células epiteliales.
Resumen de la invención La presente invención proporciona una novedosa formulación útil para la liofilización del factor de crecimiento de queratinocitos (KGF) , que resulta en un producto de KGF sumamente estable. El producto de KGF estable es útil como agente terapéutico en el tratamiento de individuos que sufren de trastornos o afecciones que se pueden beneficiar de la administración de KGF.
En un aspecto, la invención proporciona una composición liofilizada del factor de crecimiento de queratinocitos que contiene histidina, un incrementador del volumen, un surfactante y un azúcar, por ej. un azúcar estabilizante, como el que se reivindica en la reivindicación 1.
En una realización, la composición de KGF comprende la secuencia de aminoácidos de SEC. ID Nº : 2 o una variante de ésta. Una variante de proteínas KGF incluye variaciones alélicas o una o más deleciones, sustituciones o inserciones de aminoácidos, incluidos fragmentos y moléculas quiméricas o híbridas del KGF nativo. Por ejemplo, la invención propone que el KGF sea ºN23 KGF (SEC. ID Nº : 3) , en el cual se eliminaron los primeros 23 aminoácidos del KGF nativo. Las variantes incluyen las moléculas descritas en este documento como los polipéptidos que cambian de carga, donde uno o más residuos de los aminoácidos 41-154 del KGF nativo (SEC. ID Nº : 2) son eliminados o sustituidos con un residuo neutro o un residuo cargado negativamente elegido para efectuar una proteína con una carga positiva menor. Aún otro ejemplo de KGF incluye, pero no exclusivamente, las proteínas generadas mediante la sustitución de al menos un aminoácido que tenga un mayor potencial de formación de bucle para al menos un aminoácido dentro de una región de formación de bucle de Asn115 -His116 -Tyr117 -Asn118 -Thr119 del KGF nativo. Aún otro ejemplo incluye proteínas que tienen una o más sustituciones, deleciones o adiciones de aminoácidos dentro de la región de los aminoácidos 123-133 (aminoácidos 154-164 de SEC. ID Nº : 2) del KGF nativo.
En un aspecto, la invención proporciona una composición que contiene un incrementador del volumen/regulador de la osmolaridad. Específicamente el incrementador del volumen es manitol, incorporado en una concentración entre aproximadamente 2% y aproximadamente 5% p/v. Aún en otra realización, la concentración es entre aproximadamente 3% y aproximadamente 4.5% p/v. En otra realización, el manitol está en una concentración de 4% p/v.
En otro aspecto, la invención proporciona una composición que contiene un azúcar estabilizante. Específicamente, el azúcar es sacarosa en una concentración entre aproximadamente 1% y 3% p/v. En otra realización, la sacarosa está en una concentración de 2%.
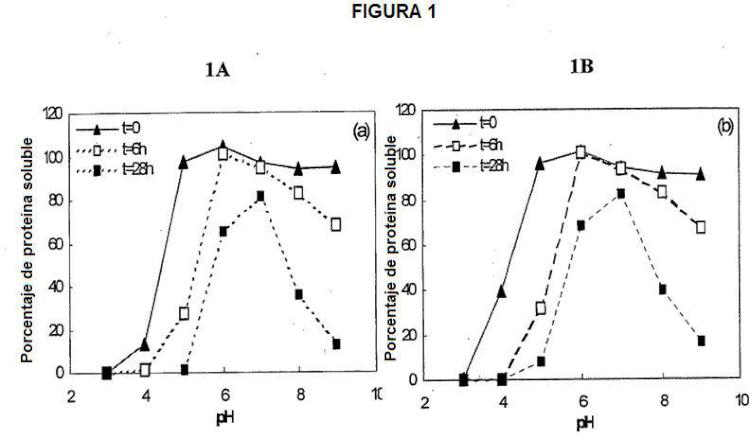
La composición de la invención se ajusta a un pH en el rango de 6.0 a 8.0. En otra realización, la composición tiene un pH en el rango entre aproximadamente 6.0 y aproximadamente 7.0. En otra realización, la composición tiene un pH de aproximadamente 6.5.
En otra realización más, la invención proporciona una composición que contiene el surfactante polisorbato 20 en un rango entre aproximadamente 0.1% y aproximadamente 0.004% p/v. En otra realización, el polisorbato 20 está en una concentración... [Seguir leyendo]
Reivindicaciones:
1. Una composición liofilizada del factor de crecimiento de queratinocitos (KGF) que consiste en:
• KGF en una concentración entre 3 mg/mL y 15 mg/mL;
• el tampón de histidina;
• el incrementador del volumen manitol en una concentración entre 2% y 5% p/v;
• sacarosa en una concentración entre 1% y 3% p/v;
• polisorbato 20 en una concentración en el rango entre 0.004% y 0.1% p/v; y donde el pH se encuentra en el rango entre 6.0 y 8.0.
2. La composición de la reivindicación 1, en la cual el KGF se elige del grupo que consiste en SEC. ID Nº : 2 y SEC. ID Nº : 3.
3. La composición de la reivindicación 1, en la cual el KGF consiste en la secuencia de aminoácidos de SEC. ID Nº :
2.
4. La composición de la reivindicación 1, en la cual el KGF consiste en ºN23 KGF indicado en SEC. ID Nº : 3.
5. La composición de la reivindicación 1, en la cual el manitol está en una concentración de 4% p/v.
6. La composición de la reivindicación 1, en la cual la sacarosa está en una concentración de 2% p/v.
7. La composición de la reivindicación 1, en la cual el pH está en el rango de 6.0 a 7.0.
8. La composición de la reivindicación 7, en la cual el pH es 6.5.
9. La composición de la reivindicación 1, en la cual la concentración de polisorbato 20 es de 0.01% p/v.
10. La composición de la reivindicación 1, en la cual la concentración de KGF es de 5 mg/mL.
11. La composición liofilizada de KGF de la reivindicación 1 que contiene histidina 10 mM, 4% p/v de manitol, 2% p/v de sacarosa y 0.01% p/v de polisorbato 20, donde la composición tiene un pH de 6.5.
12. Un método para preparar una composición liofilizada de KGF de acuerdo con la reivindicación 1 que comprende los pasos de:
a) preparar una solución de KGF a una concentración entre 3 mg/mL y 15 mg/mL; tampón de histidina; manitol a una concentración entre 2% y 5% p/v; sacarosa a una concentración entre 1% y 3% p/v; polisorbato 20 a una concentración en un rango entre 0.004% y 0.1% p/v, en la cual el pH está dentro del rango de 6.0 a 8.0; y b) liofilizar dicha solución de KGF para obtener dicha composición liofilizada de KGF.
13. El método de la reivindicación 12, donde el KGF se elige del grupo que consiste en SEC. ID Nº : 2 y SEC. ID Nº :
3.
14. El método de la reivindicación 12, donde el KGF consiste en la secuencia de aminoácidos de SEC. ID Nº : 2.
15. El método de la reivindicación 12, donde el KGF consiste en ºN23 KGF indicado en SEC. ID Nº : 3.
16. El uso de una composición liofilizada de KGF de la reivindicación 1 para la preparación de un medicamento destinado al tratamiento de la toxicidad intestinal; la mucositis; una quemadura u otras lesiones de espesor parcial y total; la repoblación de folículos pilosos, glándulas sudoríparas y glándulas sebáceas; la proliferación de estructura anexas; la epidermólisis ampollosa; la alopecia inducida por quimioterapia; la calvicie hipocrática; las úlceras gástricas; las úlceras duodenales; la gastritis erosiva, la esofagitis o el reflujo esofágico; la enfermedad inflamatoria intestinal; la enfermedad de la membrana hialina; las lesiones por inhalación de humo; el enfisema; la cirrosis hepática, la insuficiencia hepática, la hepatitis viral aguda, otras agresiones tóxicas para el hígado; o la enfermedad injerto contra huésped (EICH) , mediante el aumento de la estimulación mediada por KGF de la multiplicación de células epiteliales.
17. La composición liofilizada de KGF de la reivindicación 1, para usar en el tratamiento de la toxicidad intestinal; la mucositis; una quemadura u otras lesiones de espesor parcial y total; la repoblación de folículos pilosos, glándulas sudoríparas y glándulas sebáceas; la proliferación de estructura anexas; la epidermólisis ampollosa; la alopecia inducida por quimioterapia; la calvicie hipocrática; las úlceras gástricas; las úlceras duodenales; la gastritis erosiva, la esofagitis o el reflujo esofágico; la enfermedad inflamatoria intestinal; la enfermedad de la membrana hialina; las lesiones por inhalación de humo; el enfisema; la cirrosis hepática, la insuficiencia hepática, la hepatitis viral aguda,
otras agresiones tóxicas para el hígado; o la enfermedad injerto contra huésped (EICH) , mediante el aumento de la estimulación mediada por KGF de la proliferación de células epiteliales.
Patentes similares o relacionadas:
Neuregulina para tratar la insuficiencia cardíaca, del 29 de Julio de 2020, de Zensun (Shanghai) Science & Technology, Co., Ltd: Neuregulina para usar en un método para tratar la insuficiencia cardíaca crónica en un paciente, donde el paciente tiene un nivel plasmático de NT-proBNP […]
Dispositivo médico que tiene un revestimiento que comprende ACCS, del 15 de Julio de 2020, de Noveome Biotherapeutics, Inc: Un dispositivo médico implantable que tiene un revestimiento en su superficie, útil para la implantación quirúrgica en el cuerpo de un sujeto, […]
Composiciones que comprenden cócteles de fagos antibacterianos y usos de las mismas para el tratamiento de infecciones bacterianas, del 24 de Junio de 2020, de Tecnifar-Indústria Técnica Farmacêutica, S.A: Una composicion que comprende: una primera y una segunda cepa purificada de bacteriofago, cada una de dichas cepas que tiene un genoma que comprende […]
Trampas de GDF, del 3 de Junio de 2020, de ACCELERON PHARMA, INC: Un polipéptido aislado que comprende la secuencia de aminoácidos de SEQ ID NO: 28.
Combinacion de peptidos tolerogenos con TFG-â para inducir y mantener la tolerancia oral en mamiferos jovenes, del 3 de Junio de 2020, de SOCIETE DES PRODUITS NESTLE S.A.: Una composición nutricional - que contiene al menos un péptido de cinco hasta doce aminoácidos de longitud e incluye una secuencia elegida entre […]
Formulaciones con oxidación reducida, del 3 de Junio de 2020, de F. HOFFMANN-LA ROCHE AG: Una formulación líquida que comprende un anticuerpo y un compuesto que previene la oxidación del anticuerpo en la formulación líquida, en la que el compuesto es […]
Modulación de la actividad del factor de crecimiento epidérmico de unión a heparina para la curación de la membrana timpánica, del 6 de Mayo de 2020, de THE BOARD OF TRUSTEES OF THE LELAND STANFORD JUNIOR UNIVERSITY: Un agente que proporciona actividad de factor de crecimiento epidérmico de unión a heparina (HB-EGF) para su uso en el tratamiento de una perforación crónica de la membrana […]
Composiciones para lograr niveles plasmáticos deseados del factor 2 de crecimiento glial, del 6 de Mayo de 2020, de ACORDA THERAPEUTICS, INC: Factor de crecimiento glial 2 (GGF2) para su uso en la promocion de la remielinizacion celular en un paciente, donde el GGF2 se administra al paciente en una cantidad de […]