FORMULACIONES FARMACÉUTICAS DE FSH Y/O LH LÍQUIDAS O LIOFILIZADAS JUNTO CON EL TENSIOACTIVO NO IÓNICO POLOXÁMERO 188 Y UN AGENTE BACTERIOSTÁTICO.
Una composición farmacéutica líquida que comprende la hormona estimulante de folículo (FSH) o uno de sus variantes,
así como un tensioactivo que es poloxámero 188 y que además comprende metionina y un agente bacteriostático elegido entre fenol y m-cresol
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2004/050432.
Solicitante: ARES TRADING S.A..
Nacionalidad solicitante: Suiza.
Dirección: ZONE INDUSTRIELLE DE L'OURIETTAZ 1170 AUBONNE SUIZA.
Inventor/es: SAMARITANI, FABRIZIO, DONATI,Piergiorgio.
Fecha de Publicación: .
Fecha Solicitud PCT: 2 de Abril de 2004.
Clasificación PCT:
- A61K38/24 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 38/00 Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00). › Hormona folículo-estimulante [FSH]; Gonadotropinas coriónicas, p. ej.: HCG; Hormona luteinizante [LH]; Hormona estimulante de la tiroides [TSH].
- A61K47/10 A61K […] › A61K 47/00 Preparaciones medicinales caracterizadas por los ingredientes no activos utilizados, p. ej. portadores o aditivos inertes; Agentes de direccionamiento o agentes modificadores enlazados químicamente al ingrediente activo. › Alcoholes; Fenoles; Sus sales, p. ej. glicerol; Polietilenglicoles [PEG]; Poloxámeros; Éteres alquílicos PEG/POE.
Clasificación antigua:
- A61K38/24 A61K 38/00 […] › Hormona folículo-estimulante [FSH]; Gonadotropinas coriónicas, p. ej.: HCG; Hormona luteinizante [LH]; Hormona estimulante de la tiroides [TSH].
- A61K47/10 A61K 47/00 […] › Alcoholes; Fenoles; Sus sales, p. ej. glicerol; Polietilenglicoles [PEG]; Poloxámeros; Éteres alquílicos PEG/POE.
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Eslovenia, Finlandia, Rumania, Chipre, Lituania, Letonia, Ex República Yugoslava de Macedonia, Albania.
PDF original: ES-2358330_T3.pdf
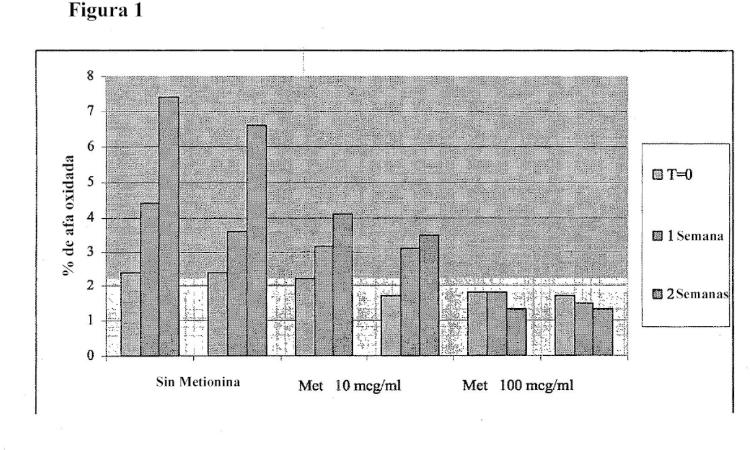
Fragmento de la descripción:
Campo de la invención
La invención se refiere al campo de las formulaciones farmacéuticas de la hormona estimulante del folículo (abreviada generalmente como FSH por sus iniciales en inglés: follicle-stimulating hormone), formulaciones de la hormona luteinizante, (abreviada generalmente como LH por sus iniciales en inglés: luteinising hormone) y mezclas de FSH y 5 hormona luteinizante (LH), así como a métodos para producir dichas formulaciones.
Antecedentes de la invención
La hormona estimulante del folículo (FSH), la hormona luteinizante (LH) y la gonadotropina coriónica (CG) son proteínas inyectables que entran dentro de la clase de las gonadotropinas. La FSH, LH y hCG se usan solas y en combinación en el tratamiento de la infertilidad y los trastornos reproductivos en pacientes tanto hembras como machos. 10
En la naturaleza, la FSH y la LH son producidas por la glándula pituitaria. Para uso farmacéutico, la FSH y la LH y sus variantes se pueden producir por recombinación (rFSH y rLH) o se pueden producir a partir de la orina de mujeres post-menopáusicas (uFSH y uLH).
La FSH se usa en pacientes hembras para inducir la ovulación (OI) y en hiperestimulación ovárica controlada (COH) para técnicas de reproducción asistida (ART). En un régimen de tratamiento típico para la inducción de la ovulación, al 15 paciente se le administran inyecciones diarias de FHS o de un variante (aproximadamente 75 a 300 UI de FSH/día) durante un periodo de aproximadamente 6 a aproximadamente 12 días. En un régimen de tratamiento típico para la hiperestimulación ovárica controlada, al paciente se le administran inyecciones diarias de FHS o de un variante (aproximadamente 150-600 UI de FSH/día) durante un periodo de aproximadamente 6 a aproximadamente 12 días.
La FSH también se usa para inducir la espermatogénesis en hombres que padecen oligospermia. Se ha usado con éxito 20 un régimen que usa 150 UI de FSH 3 veces a la semana en combinación con 2.500 UI de hCG dos veces a la semana para obtener una mejora en el recuento del esperma en hombres que padecen hipogonadismo hipogonadotrópico1.
La LH se usa en pacientes hembras en combinación con la FSH en OI y en COH, particularmente en aquellas pacientes que tienen niveles muy bajos de LH endógena o resistencia a la LH, tales como mujeres que padecen hipogonadismo hipogonadotrópico (HH, Grupo I de la OMS) o pacientes mayores (es decir, de 35 años de edad o mayores) y en 25 pacientes en las que la implantación embrionaria o el aborto temprano plantean problemas. La LH en combinación con la FSH ha estado disponible tradicionalmente en una preparación denominada gonadotropinas menopáusicas humanas (hMG) extraídas de la orina de mujeres post-menopáusicas. LA hMG tiene una relación de actividad FSH:LH de 1:1.
La CG actúa en el mismo receptor que la LH y produce las mismas respuestas. La CG tiene una semivida en la circulación mayor que la LH y por lo tanto se usa generalmente como una fuente de actividad LH de acción prolongada. 30 La CG se usa en regímenes de OI y COH para imitar el pico natural de la LH y activar la ovulación. Una inyección de gonadotropina coriónica humana (hCG) se usa para activar la ovulación al final de la estimulación con FSH o con una mezcla de FSH y LH. La CG también se puede usar junto con la FSH durante la estimulación para la OI y la COH con el fin de proporcionar actividad LH durante la estimulación en pacientes en los que se desea tener actividad LH, tales como los que se han mencionado anteriormente. 35
La FSH, la LH y la CG son miembros de la familia de las hormonas de glicoproteína, heterodímeros, que también incluye la hormona estimuladora del tiroides (abreviada generalmente como TSH por sus iniciales en inglés: thyroid stimulating hormone). Los miembros de esta familia son heterodímeros que comprenden una subunidad y una . Las subunidades se mantienen unidas mediante interacciones no covalentes. El heterodímero de la FSH humana (hFSH) consiste en: (i) una subunidad alfa de glicoproteína madura de 92 aminoácidos que también es común en los otros 40 miembros de la familia humana (es decir, la gonadotropina coriónica (CG), la hormona luteinizante (LH) y la hormona estimulante del tiroides (TSH)); y (ii) una subunidad beta madura de 111 aminoácidos que es característica de la FSH2. El heterodímero de LH humana consiste en (i) la subunidad alfa de glicoproteína madura de 92 aminoácidos; y (ii) una subunidad beta madura de 112 aminoácidos que es característica de la LH3. Las subunidades alfa y beta de las glicoproteínas pueden tener tendencia a disociarse en las formulaciones debido a la interacción con un conservante, un 45 tensioactivo y otros excipientes. La disociación de las subunidades lleva a la pérdida de potencia biológica4.
La FSH se formula para inyección intramuscular (IM) o subcutánea (SC). La FSH se suministra en forma liofilizada (sólida) en frascos o ampollas de 75 UI/frasco y 150 UI/frasco con una durabilidad de un año y medio a dos años si se almacena a 2-25ºC. La disolución para la inyección se forma reconstituyendo el producto liofilizado con agua para inyección (API). Para la inducción de la ovulación o la hiperestimulación ovárica controlada, se recomiendan inyecciones 50 diarias con dosis iniciales de 75 a 600 UI hasta aproximadamente diez días. Dependiendo de la respuesta del paciente, se pueden usar hasta tres ciclos de tratamiento con dosis crecientes de FSH. Con las formulaciones liofilizadas se pide al paciente que reconstituya un frasco de material liofilizado nuevo con diluyente y que se lo administre inmediatamente después de su reconstitución diariamente [Prospecto N1700101A, publicado en Febrero de 1996 por Fertinex® (urofolitropina para inyección, purificada) para inyección subcutánea, por Serono Laboratorios, Inc., Randolph, MA]. 55
La FSH también se ha formulado en formatos líquidos bien para dosis única o bien para dosis múltiples, en frascos o ampollas. Los formatos para dosis única deben permanecer estables y potentes durante el almacenamiento antes de su utilización. Los formatos para dosis múltiples no solo deben permanecer estables y potentes durante el almacenamiento antes de su utilización, sino que también deben permanecer estables, potentes y relativamente libres de bacterias durante el periodo de administración en régimen de uso en dosis múltiples, después de que el precinto de la ampolla 5 haya sido roto. Por esta razón, los formatos para dosis múltiples contienen a menudo un agente bacteriostático.
La LH se formula para inyección intramuscular (IM) o subcutánea (SC). La LH se suministra en forma liofilizada (sólida) en frascos o ampollas de 75 UI/frasco con una durabilidad de un año y medio a dos años si se almacena a 2-25ºC. La disolución para inyección se forma reconstituyendo el producto liofilizado con agua para inyección (API). Para la inducción de la ovulación o la hiperestimulación ovárica controlada, junto con la FSH, se recomiendan inyecciones 10 diarias con dosis iniciales de 75 a 600 UI de LH hasta aproximadamente diez días.
El documento EP 0618808 (Applied Research Systems ARS Holding N.V.) describe una composición farmacéutica que comprende una mezcla íntima sólida de gonadotropina y una cantidad estabilizante de sacarosa sola o combinada con glicina.
El documento EP 0814841 (Applied Research Systems ARS Holding N.V.) describe una composición farmacéutica 15 líquida estable que comprende gonadotropina coriónica humana (hCG) recombinante y una cantidad estabilizante de manitol.
El documento EP 0448146 (AZKO N.V.) describe un liofilizado que contiene gonadotropina estabilizada que comprende una parte en peso de gonadotropina; y 200 a 10.000 partes en peso de un estabilizante de una sal de ácido dicarboxílico asociado con la gonadotropina. 20
El documento EP 0853945 (Akzo Nobel N.V.) describe una formulación líquida que contiene gonadotropina caracterizada porque la formulación comprende una gonadotropina y cantidades estabilizantes de un ácido policarboxílico o una de sus sales y de un compuesto de tioéter.
El documento WO 00/04913 (Eli Lilly and Co.) describe una formulación que comprende FSH o un variante de la FSH que contiene una subunidad alfa y una beta y un conservante elegido entre el grupo que consiste en fenol, m-cresol, p-25 cresol, o-cresol, clorocresol, alcohol bencílico, alquil-parabeno (metil, etil, propil, butil y similares), cloruro de benzalconio, cloruro de bencetonio, deshidroacetato... [Seguir leyendo]
Reivindicaciones:
1. Una composición farmacéutica líquida que comprende la hormona estimulante de folículo (FSH) o uno de sus variantes, así como un tensioactivo que es poloxámero 188 y que además comprende metionina y un agente bacteriostático elegido entre fenol y m-cresol.
2. Una composición farmacéutica líquida que comprende la hormona estimulante de folículo (FSH) o un variante y la 5 hormona luteinizante (LH) o uno de sus variantes, así como un tensioactivo que es poloxámero 188 y que además comprende metionina y un agente bacteriostático elegido entre fenol y m-cresol.
3. Una composición farmacéutica líquida que comprende la hormona luteinizante (LH) o uno de sus variantes, así como un tensioactivo que es poloxámero 188 y que además comprende metionina y un agente bacteriostático elegido entre fenol y m-cresol. 10
4. Una composición farmacéutica líquida según cualquiera de las reivindicaciones precedentes, en la que la hormona estimulante de folículo (FSH) está presente en una concentración de o de aproximadamente 150 UI/ml hasta o hasta aproximadamente 1.200 UI/ml.
5. Una composición farmacéutica líquida según la reivindicación 4, en la que la hormona estimulante de folículo (FSH) está presente en una concentración de o de aproximadamente 300 UI/ml hasta o hasta aproximadamente 900 UI/ml. 15
6. Una composición farmacéutica líquida según la reivindicación 5, en la que la hormona estimulante de folículo (FSH) está presente en una concentración de o de aproximadamente 600 UI/ml.
7. Una composición farmacéutica líquida según cualquiera de las reivindicaciones 2 ó 3, en la que la hormona luteinizante (LH) está presente en una concentración de o de aproximadamente 150 UI/ml hasta o hasta aproximadamente 1.200 UI/ml. 20
8. Una composición farmacéutica líquida según la reivindicación 7, en la que la hormona luteinizante (LH) está presente en una concentración de o de aproximadamente 300 UI/ml hasta o hasta aproximadamente 750 UI/ml.
9. Un artículo elaborado que comprende una formulación liofilizada que comprende la hormona estimulante de folículo (FSH) o uno de sus variantes, un tensioactivo que es poloxámero 188 así como metionina, comprendiendo además el artículo elaborado un disolvente para reconstitución que contiene un agente bacteriostático elegido entre fenol y m-25 cresol.
10. Un artículo elaborado que comprende una formulación liofilizada que comprende la hormona luteinizante (LH) o uno de sus variantes, un tensioactivo que es poloxámero 188 así como metionina, comprendiendo además el artículo elaborado un disolvente para reconstitución que contiene un agente bacteriostático elegido entre fenol y m-cresol.
11. Un artículo elaborado que comprende una formulación liofilizada que comprende la hormona estimulante de folículo 30 (FSH) o uno de sus variantes así como la hormona luteinizante (LH) o uno de sus variantes, un tensioactivo que es poloxámero 188 así como metionina, comprendiendo además el artículo elaborado un disolvente para reconstitución que contiene un agente bacteriostático elegido entre fenol y m-cresol.
12. El artículo elaborado según cualquiera de las reivindicaciones 9 a 11, en el que la hormona estimulante del folículo (FSH) está presente en una concentración (peso/peso) de o de aproximadamente 0,1 a 10 g/mg de la formulación 35 total.
13. El artículo elaborado según la reivindicación 12, en el que la hormona estimulante del folículo (FSH) está presente en una concentración de o de aproximadamente 0,3 a 5 g/mg de la formulación total.
14. El artículo elaborado según la reivindicación 13, en el que la hormona estimulante del folículo (FSH) está presente en una concentración de o de aproximadamente 0,37 a 2 g/mg de la formulación total. 40
15. El artículo elaborado según cualquiera de las reivindicaciones 9 a 11, en el que la hormona luteinizante (LH) está presente en una concentración de o de aproximadamente 0,1 a 3 g/mg de la formulación total.
16. El artículo elaborado según la reivindicación 15, en el que la hormona luteinizante (LH) está presente en una concentración de o de aproximadamente 0,1 a 1 g/mg de la formulación total.
17. El artículo elaborado según la reivindicación 16, en el que la hormona luteinizante (LH) está presente en una 45 concentración de o de aproximadamente 0,1 a 0,6 g/mg de la formulación total.
18. Una composición farmacéutica o artículo elaborado según cualquiera de las reivindicaciones precedentes, en la que la hormona estimulante del folículo es una hormona estimulante del folículo humana y/o la hormona luteinizante (LH) es una hormona luteinizante (LH) humana.
19. Una composición farmacéutica o artículo elaborado según la reivindicación 18, en la que la hormona estimulante del folículo es una hormona estimulante del folículo humana urinaria y/o la hormona luteinizante (LH) es una hormona luteinizante (LH) humana urinaria.
20. Una composición farmacéutica o artículo elaborado según la reivindicación 18, en la que la hormona estimulante del folículo es una hormona estimulante del folículo humana recombinante y/o la hormona luteinizante (LH) es una hormona 5 luteinizante (LH) humana recombinante.
21. Una composición farmacéutica o artículo elaborado según cualquiera de las reivindicaciones precedentes, en la que la relación entre la FSH y la LH está en el intervalo de o de aproximadamente 6:1 hasta o hasta aproximadamente 1:6.
22. Una composición farmacéutica o artículo elaborado según la reivindicación 21, en la que la relación entre la FSH y la LH está en el intervalo de o de aproximadamente 4:1 hasta o hasta aproximadamente 1:2. 10
23. Una composición farmacéutica o artículo elaborado según la reivindicación 22, en la que la relación entre la FSH y la LH está en el intervalo de o de aproximadamente 3:1 hasta o hasta aproximadamente 1:1.
24. Una composición farmacéutica o artículo elaborado según la reivindicación 23, en la que la relación entre la FSH y la LH está en el intervalo de o de aproximadamente 2:1 y 1:1.
25. Una composición farmacéutica o artículo elaborado según cualquiera de las reivindicaciones precedentes, en la que 15 el agente bacteriostático es m-cresol.
26. Una composición farmacéutica o artículo elaborado según la reivindicación 25, que comprende m-cresol a una concentración de o de aproximadamente 0,3% (masa/masa de disolvente).
27. Una composición farmacéutica o artículo elaborado según cualquiera de las reivindicaciones precedentes que comprende además sacarosa. 20
28. Una composición farmacéutica o artículo elaborado según cualquiera de las reivindicaciones precedentes que comprende además un tampón de fosfato a un pH de o de aproximadamente 6,0 hasta o hasta aproximadamente 8,0.
29. Una composición farmacéutica o artículo manufactura según la reivindicación 28, que comprende además un tampón de fosfato a un pH de o de aproximadamente 7,0.
30. Una composición farmacéutica o artículo manufactura según la reivindicación 29, que comprende los siguientes 25 ingredientes: rFSH, poloxámero 188, sacarosa, metionina, m-cresol y una disolución acuosa tampón de fosfato de pH a o a aproximadamente 7,0.
31. Una composición farmacéutica o artículo elaborado según la reivindicación 30, en la que la rFSH está presente a una concentración de o de aproximadamente 600 UI/ml, el poloxámero 188 está presente a una concentración de o de aproximadamente 0,1 mg/ml, la sacarosa está presente a una concentración de o de aproximadamente 60 mg/ml, la 30 metionina está presente a una concentración de o de aproximadamente 0,1 mg/ml, el m-cresol está presente a una concentración de o de aproximadamente 3 mg/ml y el tampón de fosfato es de o de aproximadamente 10mM en fosfato.
32. Un artículo elaborado según la reivindicación 11, que comprende 32,75 g de FSH recombinante, 9,0 g de LH recombinante, 15,0 mg de sacarosa, 0,052 mg de NaH2PO4 H2O, 0,825 mg de Na2HPO4 2H2O, 0,05 mg de poloxámero 188 y 0,05 mg de L-metionina. 35
33. Un artículo elaborado según la reivindicación 11, que comprende 65,5 g de FSH recombinante, 18,0 g de LH recombinante, 30,0 mg de sacarosa, 0,104 mg de NaH2PO4 H2O, 1,65 mg de Na2HPO4 2H2O, 0,10 mg de poloxámero 188 y 0,10 mg de L-metionina.
34. Un método para elaborar una composición farmacéutica que comprende la etapa de formar una disolución de FSH, un tensioactivo que es poloxámero 188 y un diluyente líquido y añadir además metionina y un agente bacteriostático 40 elegido entre fenol y m-cresol.
35. Un método para elaborar una composición farmacéutica envasada que comprende colocar una disolución que comprende FSH, un tensioactivo que es poloxámero 188 y colocar además metionina y un agente bacteriostático elegido entre fenol y m-cresol, en un frasco, ampolla o cartucho.
36. Un método para elaborar un artículo elaborado según cualquiera de las reivindicaciones 9 a 11, que comprende la 45 etapa de formar una mezcla de FSH con o sin LH, o LH sola, así como un tensioactivo que es poloxámero 188, añadir metionina y someter la mezcla a liofilización, y proporcionar un disolvente para reconstitución que contiene un agente bacteriostático elegido entre fenol y m-cresol.
Patentes similares o relacionadas:
Uso de cannabinoides en el tratamiento de convulsiones atónicas en el síndrome de Lennox-Gastaut, del 29 de Julio de 2020, de GW Research Limited: Cannabidiol (CBD) para su uso en el tratamiento de las convulsiones en el síndrome de Lennox-Gastaut en el que el CBD está en forma de un extracto de cannabis […]
Preparación sólida que contiene colorante, del 29 de Julio de 2020, de DAIICHI SANKYO COMPANY, LIMITED: Preparación farmacéutica sólida que comprende monobencenosulfonato de ácido [(1R,5S,6S)-6-(aminometil)-3- etilbiciclo[3.2.0]hept-3-en-6-il]acético […]
Potenciador de la conservación, del 29 de Julio de 2020, de DSM IP ASSETS B.V.: Una composición tópica que comprende fitantriol y eritrulosa.
Reducción de tejido adiposo, del 22 de Julio de 2020, de Dobak, John, Daniel: Una formulacion farmaceutica inyectable que comprende: (i) polidocanol en una cantidad del 0,5 % p/v al 2,0 % p/v; e (ii) un alcohol C3-C6 en una cantidad del […]
Preparaciones ácidas de insulina con estabilidad mejorada, del 15 de Julio de 2020, de SANOFI-AVENTIS DEUTSCHLAND GMBH: Formulación farmacéutica que contiene insulina humana Gly(A21),Arg(B31),Arg(B32) y un tensioactivo, elegido de un grupo que contiene Tween 20® y Tween 80®; siendo […]
Composición calmante para animales que comprende al menos un ácido graso y nepetalactona, del 15 de Julio de 2020, de VIRBAC: Composición calmante para mamíferos no humanos, que comprende entre 1% y 50% en peso/peso de al menos un ácido graso que comprende entre 5 […]
Macrogols para aplicación a la mucosa, y sus usos terapéuticos, del 15 de Julio de 2020, de S.I.I.T. S.R.L.-SERVIZIO INTERNAZIONALE IMBALLAGGI TERMOSALDANTI: Composición farmacéutica en forma sólida que comprende, por unidad de dosificación, entre 5 y 400 mg de un PEG con un grado de 3000 o más, para uso en el tratamiento […]
Preparaciones de hidrogel térmico reversible para su uso en el tratamiento de trastornos del urotelio, del 15 de Julio de 2020, de UroGen Pharma Ltd: Una composición de hidrogel termorreversible mucoadhesiva biocompatible que incorpora toxina botulínica y que comprende al menos un agente de gelificación […]