FORMULACIONES FARMACEUTICAS QUE CONTIENEN SUSTANCIAS SABORIZANTES CON PROPIEDADES FARMACEUTICAS MEJORADAS.
Formulación farmacéutica sólida que contiene:
- un antibiótico de quinolona como principio activo farmacéutico,
- de 4 a 20% en peso, respecto al peso total de la formulación acabada, de una sustancia aromatizante y/o sustancia saborizante, siendo la sustancia saborizante o aromatizante una mezcla de proteínas, grasas e hidratos de carbono; y
- de 1,5 a 15% en peso de dióxido de silicio de alta dispersión, respecto al peso total de la formulación acabada, presentándose el dióxido de silicio de alta dispersión y la sustancia saborizante o aromatizante en una relación en peso de 1:4 a 1:1
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2004/012327.
Solicitante: BAYER ANIMAL HEALTH GMBH.
Nacionalidad solicitante: Alemania.
Dirección: BAYER ANIMAL HEALTH GMBH08670820BHC 03 1062-EP,51368 LEVERKUSEN.
Inventor/es: BOSCHE, PATRICK, KANIKANTI, VENKATA-RANGARAO, BONGAERTS,SABINE.
Fecha de Publicación: .
Fecha Concesión Europea: 13 de Enero de 2010.
Clasificación Internacional de Patentes:
- A61K31/495 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › que tienen ciclos con seis eslabones con dos nitrógenos como únicos heteroátomos de un ciclo, p. ej. piperazina (A61K 31/48 tiene prioridad).
- A61K9/00M18B
Clasificación PCT:
- A61K31/495 A61K 31/00 […] › que tienen ciclos con seis eslabones con dos nitrógenos como únicos heteroátomos de un ciclo, p. ej. piperazina (A61K 31/48 tiene prioridad).
Clasificación antigua:
- A61K31/495 A61K 31/00 […] › que tienen ciclos con seis eslabones con dos nitrógenos como únicos heteroátomos de un ciclo, p. ej. piperazina (A61K 31/48 tiene prioridad).
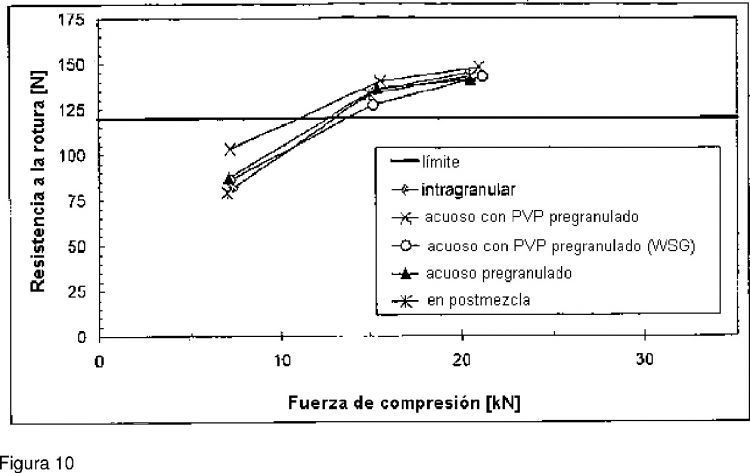
Fragmento de la descripción:
Formulaciones farmacéuticas que contienen sustancias saborizantes con propiedades farmacéuticas mejoradas.
La invención se refiere a formulaciones farmacéuticas que contienen sustancias saborizantes con propiedades farmacéuticas mejoradas así como a procedimientos para su preparación.
El uso de sustancias aromatizantes en formulaciones farmacéuticas se está haciendo cada vez más importante en el sector de la veterinaria. Las sustancias aromatizantes deben facilitar la administración de formas farmacéuticas sólidas a animales, por ejemplo perros o gatos. Las sustancias aromatizantes presentes en el mercado como, por ejemplo, Trigarol Bayopal P® (Haarmann und Reimer GmbH, Holzminden, Alemania) o aroma cárnico artificial (Pharma Chemie, Syracuse, Nebraska, EE.UU.) tienen una influencia negativa sobre las propiedades farmacéuticas de los comprimidos. Así, por ejemplo, reducen la dureza de los comprimidos (determinación de la dureza de los comprimidos descrita, por ejemplo, en Bauer, Kurt H.; Frömming, Karl-Heinz; Führer, Claus: "Lehrbuch der Pharmazeutischen Technologie", 6ª edición revisada y corregida, 1999) o influyen negativamente en la estabilidad de los comprimidos por una liberación o dureza de comprimidos empeorada. Por estas modificaciones, resultan desventajas para la calidad del producto farmacéutico.
Botzolakis, Harris y Nesbitt describen en Pharm. Res. (5, Nº 10, supl. S253, 1988) y en los documentos EP-A-0345787 o US 04910023 formulaciones con principios activos de mal sabor y procedimientos para su preparación. A este respecto, se suspenden principios activos higroscópicos de mal sabor en agua y se secan en combinación con dióxido de silicio de alta dispersión. De este modo, se obtienen comprimidos de buen sabor y menos higroscópicos.
Los requisitos para una formulación farmacéutica sólida adecuada para administración a animales son numerosos:
La aceptación elevada puede alcanzarse mediante la adición de sustancias aromatizantes y saborizantes. A este respecto, existía hasta ahora el problema de que estas sustancias aromatizantes empeoraran las propiedades farmacéuticas de las correspondientes formulaciones sólidas.
Se ha encontrado ahora sorprendentemente que mediante la adición de cantidades comparativamente altas de dióxido de silicio de alta dispersión, pueden reducirse o equilibrarse totalmente las influencias desventajosas de las sustancias saborizantes o aromatizantes y se obtienen formulaciones farmacéuticas sólidas que presentan en todos los criterios anteriormente citados buenas o muy buenas propiedades. A este respecto, es destacable que el dióxido de silicio de alta dispersión apenas influye en el efecto de las sustancias saborizantes o aromatizantes, aunque se propone en el estado de la técnica para enmascarar el sabor.
La invención se refiere por tanto a formulaciones farmacéuticas sólidas que contienen un principio activo farmacéutico, una sustancia saborizante y al menos un 1,5% en peso de dióxido de silicio de alta dispersión respecto al peso total de la formulación acabada.
Las formulaciones farmacéuticas según la invención contienen habitualmente el principio activo farmacéutico en una cantidad de 0,001-90% en peso.
Se tienen en cuenta generalmente todos los principios activos farmacéuticos habituales en veterinaria. Se citan como ejemplos: antibióticos de quinolona.
Se describen inhibidores de quinolona, entre otros, en los siguientes documentos: US 4.670.444 (Bayer AG), US 4.472.405 (Riker Labs), US 4.730.000 (Abbott), US 4.861 779 (Pfizer), US 4.382.892 (Daiichi), US 4.704.459 (Toyama), se citan como ejemplos concretos de antibióticos de quinolona: ciprofloxacino, enrofloxacino, ibafloxacino, sarafloxacino, difloxacino, binfloxacino, danofloxacino, marbofloxacino, benofloxacino, ofloxacino, orbifloxacino, tosufloxacino, temafloxacino, ácido pipemídico, norfloxacino, pefloxacino, ofloxacino y fleroxacino. Además, se citan como antibióticos de quinolona adecuados los compuestos descritos en el documento WO 97/31001, particularmente pradofloxacino (ácido 8-ciano-1-ciclopropil-7-((1S,6S)-2,8-diazabiciclo[4.3.0]nonan-8-il)-6-fluoro-1,4-dihidro-4-oxo-3-quinolincarboxílico) de fórmula
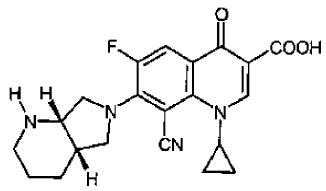
Se representan antibióticos de quinolona preferidos en general mediante las fórmulas (I) y (II)
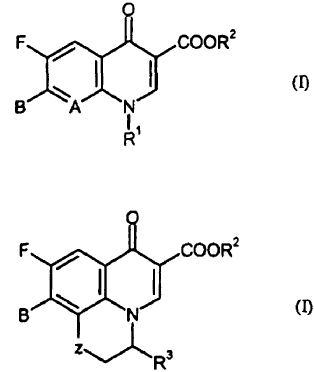
en las que
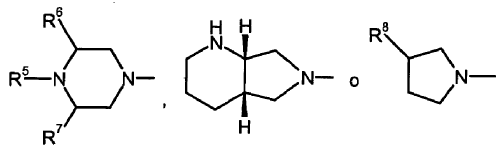
y
Se prefieren como principios activos ácidos quinolonocarboxílicos y sus derivados de fórmula (Ia)
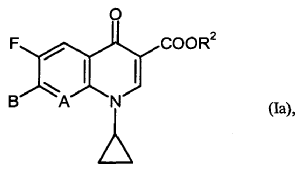
en la que
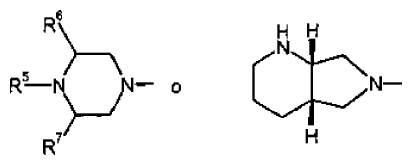
y
A, R2, R5, R6 y R7 tienen el significado anteriormente dado.
Se prefieren especialmente como principios activos ácidos quinolonocarboxílicos y sus derivados de fórmula (Ia)
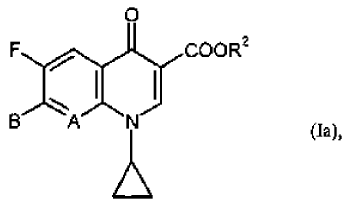
en la que
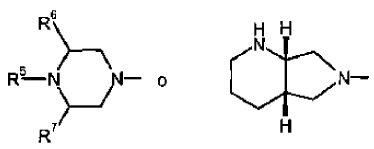
Reivindicaciones:
1. Formulación farmacéutica sólida que contiene:
2. Formulación farmacéutica sólida según una de las reivindicaciones precedentes, que contiene como principio activo enrofloxacino, una sal de enrofloxacino o un hidrato de enrofloxacino o su sal.
3. Formulación farmacéutica según una de las reivindicaciones precedentes, que contiene como principio activo farmacéutico pradofloxacino, una sal de pradofloxacino o un hidrato de pradofloxacino o su sal.
4. Formulación farmacéutica sólida según una de las reivindicaciones precedentes, que contiene al menos un 4% en peso de dióxido de silicio de alta dispersión respecto al peso total de la formulación acabada.
5. Formulación farmacéutica sólida según una de las reivindicaciones precedentes, que contiene no más de un 10% en peso de dióxido de silicio de alta dispersión.
6. Procedimiento para la preparación de la formulación farmacéutica sólida según la reivindicación 1, en el que la sustancia saborizante se granula con el dióxido de silicio de alta dispersión así como uno o varios principios activos y aditivos y/o coadyuvantes farmacéuticos habituales.
7. Uso de las formulaciones farmacéuticas sólidas según una de las reivindicaciones 1 a 5 para la preparación de medicamentos para empleo en veterinaria.
8. Uso según la reivindicación 7 para la preparación de medicamentos para perros o gatos.
Patentes similares o relacionadas:
Análogos de (E)-N''-(1-feniletiliden) benzohidrazida sustituida como inhibidores de desmetilasas de histonas, del 15 de Julio de 2020, de UNIVERSITY OF UTAH RESEARCH FOUNDATION: Un compuesto que tiene una estructura representada por una fórmula: **(Ver fórmula)** en donde m es 1; n es un número entero de 0 a […]
Antagonista del receptor NK1, del 27 de Mayo de 2020, de KISSEI PHARMACEUTICAL CO., LTD.: Un compuesto representado por la fórmula (I): **(Ver fórmula)** donde W es un átomo de hidrógeno o un átomo de flúor; el anillo A es un […]
Formulación granular compleja con estabilidad mejorada, que comprende levocetirizina y montelukast, del 13 de Mayo de 2020, de HANMI PHARM. CO., LTD.: Una formulación granular compleja que comprende: (a) una primera parte granular que comprende levocetirizina o una sal farmacéuticamente aceptable de la misma, ciclodextrina […]
Composiciones y compuestos terapéuticos, del 6 de Mayo de 2020, de Agios Pharmaceuticals, Inc: Un compuesto de Fórmula (I) o una sal del mismo farmacéuticamente aceptable, en donde: **(Ver fórmula)** A es arilo o heteroarilo, en donde el arilo o heteroarilo […]
Combinaciones de inhibidores de histona desacetilasa y fármacos inmunomoduladores, del 29 de Abril de 2020, de Acetylon Pharmaceuticals, Inc: Una combinación farmacéutica para su uso en el tratamiento del linfoma que comprende una cantidad terapéuticamente eficaz de un inhibidor específico de histona desacetilasa […]
Composiciones farmacéuticas para terapia de combinación, del 29 de Abril de 2020, de Acesion Pharma ApS: Una combinación de (i) un inhibidor del canal de potasio (SK) activado por calcio de pequeña conductancia, o una sal o solvato farmacéuticamente aceptable de este; […]
Formulaciones farmacéuticas de liberación controlada de nitazoxanida, del 15 de Abril de 2020, de ROMARK LABORATORIES, L.C.: Composición farmacéutica en forma de una forma de dosificación oral sólida que comprende: (a) una primera parte que comprende una primera […]
Composiciones congeladas fluidas que comprenden un agente terapéutico, del 8 de Abril de 2020, de Tavakoli, Zahra: Una composición fluida congelada que comprende un agente terapéutico y al menos un agente aromatizante para su uso en terapia, donde dicha composición […]