ESTs 5¿PARA PROTEÍNAS SECRETADAS, EXPRESADAS EN DIVERSOS TEJIDOS.
Un péptido señal que tiene la secuencia de aminoácidos -26 a -1 del SEQ ID NO: 306
Tipo: Patente Europea. Resumen de patente/invención. Número de Solicitud: E03016783.
Solicitante: MERCK SERONO BIODEVELOPMENT.
Nacionalidad solicitante: Francia.
Dirección: 37, TUE SAINT ROMAIN 69008 LYON FRANCIA.
Inventor/es: DUMAS MILNE EDWARDS, JEAN-BAPTISTE, DUCLERT, AYMERIC, LACROIX, BRUNO.
Fecha de Publicación: .
Fecha Solicitud PCT: 31 de Julio de 1998.
Clasificación Internacional de Patentes:
- C07K14/47 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 14/00 Péptidos con más de 20 aminoácidos; Gastrinas; Somatostatinas; Melanotropinas; Sus derivados. › de mamíferos.
Clasificación PCT:
- A61K38/17 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 38/00 Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00). › que provienen de animales; que provienen de humanos.
- A61K48/00 A61K […] › Preparaciones medicinales que contienen material genético que se introduce en las células del cuerpo vivo para tratar enfermedades genéticas; Terapia génica.
- C07K14/47 C07K 14/00 […] › de mamíferos.
- C07K16/18 C07K […] › C07K 16/00 Inmunoglobulinas, p. ej. anticuerpos mono o policlonales. › contra materiales animales o humanos.
- C12N15/10 C […] › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 15/00 Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K). › Procedimientos para el aislamiento, la preparación o la purificación de ADN o ARN (preparación química de ADN o ARN C07H 21/00; preparación de polinucleótidos no estructurales a partir de microorganismos o con la ayuda de enzimas C12P 19/34).
- C12N15/12 C12N 15/00 […] › Genes que codifican proteínas animales.
- C12N15/66 C12N 15/00 […] › Métodos generales para insertar un gen en un vector para formar un vector recombinante, utilizando la escisión y la unión; Utilización de "linkers" no funcionales o de adaptadores, p. ej. "linkers" que contienen la secuencia para una endonucleasa de restricción.
- C12Q1/68 C12 […] › C12Q PROCESOS DE MEDIDA, INVESTIGACION O ANALISIS EN LOS QUE INTERVIENEN ENZIMAS, ÁCIDOS NUCLEICOS O MICROORGANISMOS (ensayos inmunológicos G01N 33/53 ); COMPOSICIONES O PAPELES REACTIVOS PARA ESTE FIN; PROCESOS PARA PREPARAR ESTAS COMPOSICIONES; PROCESOS DE CONTROL SENSIBLES A LAS CONDICIONES DEL MEDIO EN LOS PROCESOS MICROBIOLOGICOS O ENZIMOLOGICOS. › C12Q 1/00 Procesos de medida, investigación o análisis en los que intervienen enzimas, ácidos nucleicos o microorganismos (aparatos de medida, investigación o análisis con medios de medida o detección de las condiciones del medio, p. ej. contadores de colonias, C12M 1/34 ); Composiciones para este fin; Procesos para preparar estas composiciones. › en los que intervienen ácidos nucleicos.
- G01N33/50 FISICA. › G01 METROLOGIA; ENSAYOS. › G01N INVESTIGACION O ANALISIS DE MATERIALES POR DETERMINACION DE SUS PROPIEDADES QUIMICAS O FISICAS (procedimientos de medida, de investigación o de análisis diferentes de los ensayos inmunológicos, en los que intervienen enzimas o microorganismos C12M, C12Q). › G01N 33/00 Investigación o análisis de materiales por métodos específicos no cubiertos por los grupos G01N 1/00 - G01N 31/00. › Análisis químico de material biológico, p. ej. de sangre o de orina; Ensayos mediante métodos en los que interviene la formación de uniones bioespecíficas con grupos coordinadores; Ensayos inmunológicos (procedimientos de medida o ensayos diferentes de los procedimientos inmunológicos en los que intervienen enzimas o microorganismos, composiciones o papeles reactivos a este efecto, procedimientos para preparar estas composiciones, procedimientos de control sensibles a las condiciones del medio en los procedimientos microbiológicos o enzimáticos C12Q).
- G01N33/53 G01N 33/00 […] › Ensayos inmunológicos; Ensayos en los que interviene la formación de uniones bioespecíficas; Materiales a este efecto.
Clasificación antigua:
- A61K38/17 A61K 38/00 […] › que provienen de animales; que provienen de humanos.
- A61K48/00 A61K […] › Preparaciones medicinales que contienen material genético que se introduce en las células del cuerpo vivo para tratar enfermedades genéticas; Terapia génica.
- C07K14/47 C07K 14/00 […] › de mamíferos.
- C07K16/18 C07K 16/00 […] › contra materiales animales o humanos.
- C12N15/10 C12N 15/00 […] › Procedimientos para el aislamiento, la preparación o la purificación de ADN o ARN (preparación química de ADN o ARN C07H 21/00; preparación de polinucleótidos no estructurales a partir de microorganismos o con la ayuda de enzimas C12P 19/34).
- C12N15/12 C12N 15/00 […] › Genes que codifican proteínas animales.
- C12N15/66 C12N 15/00 […] › Métodos generales para insertar un gen en un vector para formar un vector recombinante, utilizando la escisión y la unión; Utilización de "linkers" no funcionales o de adaptadores, p. ej. "linkers" que contienen la secuencia para una endonucleasa de restricción.
- C12Q1/68 C12Q 1/00 […] › en los que intervienen ácidos nucleicos.
- G01N33/50 G01N 33/00 […] › Análisis químico de material biológico, p. ej. de sangre o de orina; Ensayos mediante métodos en los que interviene la formación de uniones bioespecíficas con grupos coordinadores; Ensayos inmunológicos (procedimientos de medida o ensayos diferentes de los procedimientos inmunológicos en los que intervienen enzimas o microorganismos, composiciones o papeles reactivos a este efecto, procedimientos para preparar estas composiciones, procedimientos de control sensibles a las condiciones del medio en los procedimientos microbiológicos o enzimáticos C12Q).
- G01N33/53 G01N 33/00 […] › Ensayos inmunológicos; Ensayos en los que interviene la formación de uniones bioespecíficas; Materiales a este efecto.
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Finlandia, Chipre.
PDF original: ES-2359401_T3.pdf



Fragmento de la descripción:
Antecedentes de la Invención
Los 50.000-100.000 genes estimados diseminados a lo largo de los cromosomas humanos ofrecen una promesa tremenda para la comprensión, diagnóstico y tratamiento de enfermedades humanas. Además, las sondas que son capaces de hibridarse específicamente con loci distribuidos a lo largo del genoma humano encuentran aplicación en la construcción de mapas cromosómicos de alta resolución y en la identificación de individuos.
En el pasado, la caracterización de incluso un solo gen humano era un proceso laborioso, que requería años de esfuerzo. Recientes progresos en las áreas de vectores de clonación, secuenciación de ADN y tecnología informática se han fundido para acelerar en gran medida la velocidad a la que los genes humanos pueden aislarse, secuenciarse, cartografiarse y caracterizarse. Los vectores de clonación, tales como cromosomas artificiales de levaduras (YAC) y cromosomas artificiales bacterianos (BAC) son capaces de aceptar insertos de ADN que varían de 300 a 1000 kilobases (kb) o 100-400 kb de longitud, respectivamente, facilitando, con ello, la manipulación y ordenación de secuencias de ADN distribuidas a lo largo de grandes distancias sobre los cromosomas humanos. Las máquinas de secuenciación de ADN automáticas permiten la rápida secuenciación de genes humanos. Los programas bioinformáticos permiten la comparación de secuencias de ácidos nucleicos y proteínas, ayudando, con ello, a la caracterización de productos génicos humanos.
En la actualidad se siguen dos líneas diferentes para identificar y caracterizar los genes distribuidos a lo largo del genoma humano. En una línea, fragmentos grandes de ADN genómico se aíslan, se clonan y se secuencian. Se identifican los marcos de lectura abiertos potenciales de estas secuencias genómicas utilizando programas bioinformáticos. Sin embargo, esta línea supone secuenciar tramos largos de ADN humano que no codifican proteínas para encontrar las secuencias codificantes de proteínas dispersas a lo largo del genoma. Además de requerir una extensa secuenciación, los programas bioinformáticos pueden caracterizar erróneamente las secuencias genómicas obtenidas. Así, el programa puede producir falsos positivos en los que se caracteriza erróneamente un ADN que no codifica como un ADN codificante, o falsos negativos en los que un ADN codificante se designa erróneamente como un ADN no codificante.
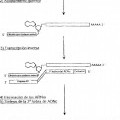
Una línea alternativa toma una ruta más directa para identificar y caracterizar genes humanos. En esta línea, se sintetizan ADN complementarios (ADNc) a partir de ARN mensajeros (ARNm) aislados que codifican proteínas humanas. Utilizando esta línea, sólo se realiza la secuenciación sobre el ADN que se deriva de porciones codificantes de proteínas del genoma. A menudo, sólo se secuencian tramos cortos del ADNc para obtener secuencias denominadas etiquetas de secuencia expresada (EST, “expressed sequence tags”). Las EST a continuación pueden utilizarse para aislar o purificar ADNc extendido que incluye secuencias adyacentes a las secuencias de EST. Los ADNc extendidos pueden contener la secuencia completa de la EST que se utilizó para obtenerlos, o sólo una porción de la secuencia de la EST que se utilizó para obtenerlos. Además, los ADNc extendidos pueden contener la secuencia completa del gen a partir del cual se derivó la EST o, como alternativa, los ADNc extendidos pueden incluir porciones de la secuencia codificante del gen a partir del cual se derivó la EST. Se apreciará que pueden existir varios ADNc extendidos que incluyen la secuencia EST como resultado de un corte y empalme alternativo o de la actividad de promotores alternativos.
En el pasado, estas secuencias EST cortas a menudo se obtenían de bancos de ADNc cebados con oligo-dT. Por consiguiente, corresponden principalmente a la región 3' no traducida del ARNm. En parte, el predominio de secuencias EST derivadas del extremo 3' del ARNm es un resultado del hecho de que las técnicas típicas para obtener ADNc no son adecuadas para aislar secuencias de ADNc derivadas de los extremos 5' de los ARNm (Adams et al., Nature, 377: 3-174, 1996; Hillier et al., Genome Res., 6: 807-828, 1996).
Además, en los casos indicados en los que se han obtenido secuencias de ADNc más largas, las secuencias indicadas corresponden, de forma típica, a secuencias codificantes y no incluyen la región 5' completa no traducida del ARNm a partir del cual se deriva el ADNc. Estas secuencias incompletas pueden no incluir el primer exón del ARNm, en particular en situaciones en las que el primer exón es corto. Además, pueden no incluir algunos exones, a menudo los que son cortos, que están colocados aguas arriba de los sitios de corte y empalme. Por tanto, existe la necesidad de obtener secuencias derivadas de los extremos 5' de los ARNm.
Aunque muchas secuencias derivadas de cromosomas humanos tienen aplicaciones prácticas, las líneas basadas en la identificación y caracterización de aquellas secuencias cromosómicas que codifican un producto proteico son particularmente relevantes para usos de diagnóstico y terapéuticos. De los 50.000-100.000 genes codificantes de proteínas, aquellos genes que codifican proteínas que se secretan desde la célula en la que se sintetizan, así como las proteínas secretadas en sí mismas, son particularmente valiosos como agentes terapéuticos potenciales. Estas proteínas a menudo están implicadas en la comunicación de célula a célula, y pueden ser responsables de producir una respuesta clínicamente importante en sus células diana.
De hecho, varias proteínas de secreción, incluyendo el activador de plasminógeno tisular, G-CSF, GMCSF, eritropoyetina, hormona del crecimiento humana, insulina, interferón-α, interferón-β, interferón-γ e interleuquina-2, tienen un uso clínico en la actualidad. Estas proteínas se utilizan para tratar una amplia gama de trastornos, incluyendo infarto agudo de miocardio, ictus isquémico agudo, anemia, diabetes, deficiencia de la hormona del crecimiento, hepatitis, carcinoma renal, neutropenia inducida por quimioterapia, y esclerosis múltiple. Por estas razones, los ADNc extendidos que codifican proteínas secretadas, o porciones de éstas, representan una fuente particularmente valiosa de agentes terapéuticos. Por tanto, existe la necesidad de identificar y caracterizar proteínas secretadas y los ácidos nucleicos que las codifican.
Además de ser terapéuticamente útiles en sí mismas, las proteínas de secreción incluyen péptidos cortos, denominados péptidos señal, en sus extremos amino, que dirigen su secreción. Estos péptidos señal son codificados por las secuencias señal colocadas en los extremos 5' de las secuencias codificantes de genes que codifican proteínas secretadas. Debido a que estos péptidos señal dirigirán la secreción extracelular de cualquier proteína a la que estén operablemente conectados, las secuencias señal pueden aprovecharse para dirigir la secreción eficaz de cualquier proteína mediante la conexión operable de las secuencias señal a un gen que codifica la proteína cuya secreción se desea. Además, también pueden utilizarse porciones de secuencias señal para dirigir la importación intracelular de un péptido o una proteína de interés. Esto puede resultar beneficioso en estrategias de terapia génica, en las que se desea dirigir un producto génico concreto a células distintas a la célula en la que se produce. Las secuencias señal que codifican péptidos señal también tienen aplicación para simplificar las técnicas de purificación de proteínas. En estas aplicaciones, la secreción extracelular de la proteína deseada facilita en gran medida la purificación mediante la reducción del número de proteínas no deseadas, a partir de las cuales debe seleccionarse la proteína deseada. Por tanto, existe la necesidad de identificar y caracterizar las porciones 5' de los genes para proteínas de secreción que codifican péptidos señal.
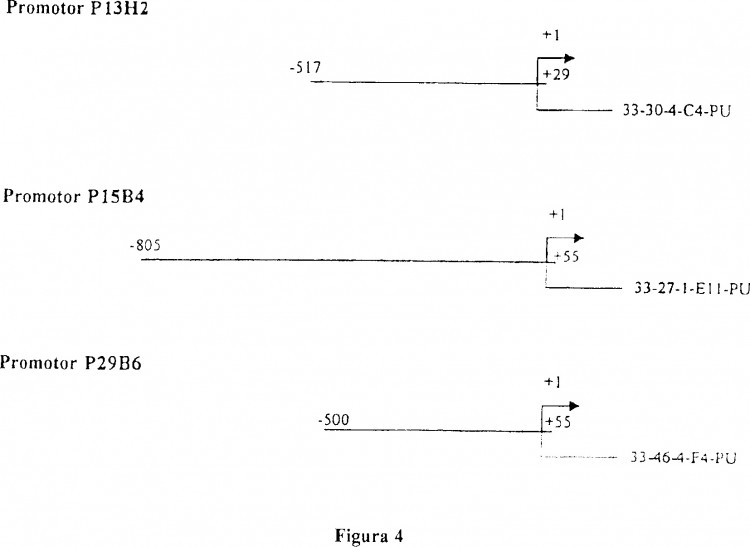
La información pública sobre el número de genes humanos para los que se han identificado y caracterizado los promotores y las regiones reguladoras aguas arriba es bastante limitada. En parte, esto puede ser debido a la dificultad de aislar estas secuencias reguladoras. Las secuencias reguladoras aguas arriba, tales como los sitios de unión del factor de transcripción, son, de forma típica, demasiado cortas para ser utilizadas como sondas para aislar promotores... [Seguir leyendo]
Reivindicaciones:
1. Un péptido señal que tiene la secuencia de aminoácidos -26 a -1 del SEQ ID NO: 306.
2. Una secuencia señal aislada que codifica el péptido señal de la reivindicación 1.
3. La secuencia señal de la reivindicación 2, que tiene la secuencia de nucleótidos 151 a 228 del SEQ ID NO: 73.
4. Un ácido nucleico purificado y aislado que codifica un polipéptido que comprende el péptido señal según la reivindicación 1 en el extremo 5' de la secuencia codificante.
5. Un ácido nucleico según la reivindicación 4, en el que el ácido nucleico comprende una secuencia señal que tiene la secuencia de nucleótidos 151 a 228 del SEQ ID NO: 73.
6. El ácido nucleico según la reivindicación 4, en el que el extremo amino de dicho polipéptido está codificado por los nucleótidos 151 a 315 del SEQ ID NO: 73.
7. El ácido nucleico según la reivindicación 4, en el que el extremo amino de dicho polipéptido está codificado por los nucleótidos 114 a 224 del SEQ I D NO: 75.
8. El ácido nucleico según la reivindicación 4, en el que dicha secuencia señal está fusionada en marco al extremo 5' de una secuencia que codifica un polipéptido que es heterólogo a un polipéptido que comprende los aminoácidos 1 a 29 del SEQ ID NO: 306.
9. Un vector de expresión que comprende la secuencia señal según la reivindicación 2 ó 3 conectado operablemente a un promotor.
10. Un vector de expresión que comprende el ácido nucleico de uno cualquiera de los ácidos nucleicos según las reivindicaciones 4 a 8 conectado operablemente a un promotor
11. El vector de expresión según la reivindicación 9 o 10, en el que dicho vector es un vector de secreción.
12. El vector de expresión según la reivindicación 9 o 10, en el que dicho vector es un vector de terapia génica.
13. Un polipéptido codificado por un polinucleótido de una cualquiera según las reivindicaciones 4 a 8.
14. El polipéptido según la reivindicación 13, en el que dicho polipéptido es una proteína secretada humana.
15. El polipéptido según la reivindicación 13 o la reivindicación 14, en el que dicho polipéptido comprende los aminoácidos 1 a 29 del SEQ ID NO: 306.
16. El polipéptido según la reivindicación 13 o la reivindicación 14, en el que dicho polipéptido comprende los aminoácidos 1 a 11 del SEQ ID NO: 308.
17. Una proteína de fusión codificada por el ácido nucleico según la reivindicación 8.
18. El uso in vitro del péptido señal según la reivindicación 1, para dirigir la secreción extracelular de un polipéptido.
19. El uso del péptido señal según la reivindicación 1, para simplificar la purificación de proteínas de un polipéptido deseado.
20. El uso in vitro del vector según una cualquiera de las reivindicaciones 9 a 12, para dirigir la secreción extracelular de un polipéptido.
21. El uso del vector según una cualquiera de las reivindicaciones 9 a 12, para simplificar la purificación de proteínas de un polipéptido deseado.
22. El uso de un vector según una cualquiera de las reivindicaciones 18 a 21, en el que dicho polipéptido es el polipéptido de una cualquiera de las reivindicaciones 13 a 17.
23. Un método para producir una proteína secretada, que comprende la etapa de insertar un gen que codifica una proteína no secretada en marco con la secuencia señal de la reivindicación 2 ó 3 en un vector de modo que la proteína codificada por el gen insertado es expresada a partir de del ARNm transcrito.
24. El método de la reivindicación 23, que comprende, además, la etapa de introducir dicho vector en una célula hospedante, tejido no humano u organismo no humano.
Patentes similares o relacionadas:
Detección de interacciones proteína a proteína, del 15 de Julio de 2020, de THE GOVERNING COUNCIL OF THE UNIVERSITY OF TORONTO: Un método para medir cuantitativamente la fuerza y la afinidad de una interacción entre una primera proteína de membrana o parte de la misma y una […]
Polipéptidos de unión específica novedosos y usos de los mismos, del 15 de Julio de 2020, de Pieris Pharmaceuticals GmbH: Muteína de lipocalina lagrimal humana que tiene especificidad de unión para IL-17A, en la que la muteína se une a IL-17A con una KD de aproximadamente 1 nM o menos, en la que […]
Biomarcador de enfermedad autoinmunitaria, del 15 de Julio de 2020, de Tzartos, Socrates: Un método de diagnóstico o pronóstico de una enfermedad autoinmunitaria asociada con la formación de lesiones desmielinizadas del sistema nervioso central (SNC) […]
Composiciones útiles en el tratamiento de la deficiencia de ornitina transcarbamilasa (OTC), del 8 de Julio de 2020, de THE TRUSTEES OF THE UNIVERSITY OF PENNSYLVANIA: Un vector vírico recombinante que comprende una secuencia de ácido nucleico que codifica la proteína ornitina transcarbamilasa humana (hOTC) y secuencias […]
Procedimientos y composiciones para el tratamiento de una afección genética, del 24 de Junio de 2020, de Sangamo Therapeutics, Inc: Una célula precursora de glóbulos rojos genomanipulada caracterizada por una modificación genómica dentro del exón 2 o el exón 4 de BCL11A o dentro de BCL11A-XL […]
Reactivos SIRP-alfa de alta afinidad, del 24 de Junio de 2020, de THE BOARD OF TRUSTEES OF THE LELAND STANFORD JUNIOR UNIVERSITY: Un polipéptido SIRPα de alta afinidad que comprende al menos una y no más de 15 modificaciones de aminoácidos dentro del dominio d1 de una secuencia SIRPα de tipo […]
Estructuras artificiales de poliepítopos para uso en inmunoterapia, del 17 de Junio de 2020, de Invectys: Un vector de expresión de ADN o una mezcla de vectores de expresión de ADN que codifica al menos dos epítopos de CD4 de la transcriptasa inversa de la telomerasa […]
Inmunoterapia WT1 para enfermedad angiogénica intraocular, del 17 de Junio de 2020, de INTERNATIONAL INSTITUTE OF CANCER IMMUNOLOGY, INC.: Una composición farmacéutica que comprende un péptido WT1 o péptido WT1 variante para su uso en el tratamiento y/o prevención de una enfermedad […]