Derivados de piperidina como antagonistas del receptor de CGRP.
Un compuesto de fórmula I
en la que:
R1 es hidrógeno, ciano,
halo, alquilo, haloalquilo, alcoxi, haloalcoxi, alquilSO2, amino, alquilamino, dialquilamino, azetidinilo, pirrolidinilo, piperidinilo, piperazinilo, N-alquilpiperazinilo o morfolinilo;
R2 es N-piperidinilo y está sustituido en 4 con 1 sustituyente seleccionado del grupo constituido por
R3 es hidrógeno, halo, ciano, alquilo, haloalquilo, alcoxi o haloalcoxi;
R4 es hidrógeno, halo, ciano, alquilo, haloalquilo, alcoxi o haloalcoxi;
Ar1 es fenilo sustituido con 0-3 sustituyentes seleccionados del grupo constituido por ciano, halo, alquilo, haloalquilo, alcoxi, haloalcoxi y alquilSO2;
X es O, CH2 o NH; y
Y es un enlace, O, CH2 o NH;
o una sal farmacéuticamente aceptable del mismo.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2009/039444.
Solicitante: BRISTOL-MYERS SQUIBB COMPANY.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: ROUTE 206 AND PROVINCE LINE ROAD P.O. BOX 4000 PRINCETON, NJ 08543-4000 ESTADOS UNIDOS DE AMERICA.
Inventor/es: LUO, GUANGLIN.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K31/435 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › que tienen ciclos con seis eslabones con un nitrógeno como único heteroátomo de un ciclo.
- A61P11/00 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › Medicamentos para el tratamiento de trastornos del aparato respiratorio.
- A61P25/06 A61P […] › A61P 25/00 Medicamentos para el tratamiento de trastornos del sistema nervioso. › Agentes contra la migraña.
- C07D401/14 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07D COMPUESTOS HETEROCICLICOS (Compuestos macromoleculares C08). › C07D 401/00 Compuestos heterocíclicos que contienen dos o más heterociclos, que tienen átomos de nitrógeno como únicos heteroátomos del ciclo, siendo al menos un ciclo de seis miembros con solamente un átomo de nitrógeno. › que contienen tres o más heterociclos.
- C07D471/04 C07D […] › C07D 471/00 Compuestos heterocíclicos que contienen átomos de nitrógeno como únicos heteroátomos del sistema condensado, teniendo al menos un ciclo de seis miembros con un átomo de nitrógeno, no previstos en los grupos C07D 451/00 - C07D 463/00. › Sistemas condensados en orto.
PDF original: ES-2392779_T3.pdf
Fragmento de la descripción:
Derivados de piperidina como antagonistas del receptor de CGRP
Referencia cruzada a solicitudes relacionadas
La presente solicitud reivindica el beneficio de prioridad de la solicitud provisional de Estados Unidos número de serie 61/044198 presentada el 11 de abril de 2008.
Antecedentes de la invención
La divulgación se refiere en general a los nuevos compuestos de fórmula I, incluyendo sales farmacéuticamente aceptables, que son antagonistas del receptor de CGRP. La divulgación también se refiere a composiciones farmacéuticas y procedimientos para usar los compuestos en el tratamiento de trastornos relacionados con CGRP incluyendo migrañas, vasodilatación neurogénica, inflamación neurogénica, lesión térmica, choque circulatorio, sofocos asociados con la menopausia, enfermedades inflamatorias de las vías respiratorias tales como asma y enfermedad pulmonar obstructiva crónica (EPOC) .
El péptido relacionado con gen de calcitonina (CGRP) es un péptido de 37 aminoácidos de origen natural identificado por primera vez en 1982 (Amara, S. G. y col, Science 1982, 298, 240-244) . Se expresan dos formas del péptido (aCGRP y 1CGRP) que difieren en uno y tres aminoácidos en ratas y seres humanos, respectivamente. El péptido se distribuye ampliamente tanto en el sistema nervioso periférico (SNP) como en el central (SNC) , localizado principalmente en neuronas sensoriales aferentes y centrales, y presenta varios efectos biológicos, incluyendo vasodilatación.
Cuando se libera de la célula, el CGRP se une a receptores acoplados a proteína G de superficie celular específicos y ejerce su acción biológica predominantemente mediante activación de la adenilato ciclasa intracelular (Poyner, D.
R. y col, Br J Pharmacol 1992, 105, 441-7; Van Valen, F. y col, Neurosci Lett 1990, 119, 195-8.) . Se han propuesto dos clases de receptores de CGRP, CGRP1 y CGRP2, basándose en las propiedades antagonistas del fragmento peptídico CGRP (8-37) y la capacidad de análogos lineales de CGRP para activar receptores CGRP2 (Juaneda, C. y col. TiPS 2000, 21, 432-438) . Sin embargo, existe una falta de pruebas moleculares para el receptor CGRP2 (Brain,
S. D. y col, TiPS 2002, 23, 51-53) . El receptor CGRP1 tiene tres componentes: (i) un receptor de tipo receptor de calcitonina de 7 transmembranas (CRLR) ; (ii) la proteína modificadora de la actividad receptora transmembrana sencilla de tipo uno (RAMP1) ; y (iii) la proteína componente del receptor intracelular (RCP) (Evans B. N. y col., J Biol Chem. 2000, 275, 31438-43) . Se requiere RAMP1 para el transporte de CRLR a la membrana plasmática y para la unión del ligando con el receptor de CGRP (McLatchie, L. M. y col, Nature 1998, 393, 333-339) . Se requiere RCP para la transducción de señales (Evans B. N. y col., J Biol Chem. 2000, 275, 31438-43) . Hay diferencias específicas de especie conocidas en la unión de moléculas pequeñas antagonistas del receptor de CGRP viéndose normalmente mayor afinidad para el antagonismo del receptor humano que para otras especies (Brain, S. D. y col, TiPS 2002, 23, 51-53) . La secuencia de aminoácidos de RAMP1 determina la selectividad de especie, en particular, el resto de aminoácido Trp74 es responsable del fenotipo del receptor humano (Mallee y col. J Biol Chem 2002, 277, 14294-8) .
Se ha postulado que los inhibidores en el nivel del receptor para CGRP son útiles en afecciones patofisiológicas en las que se ha producido activación excesiva del receptor de CGRP. Algunas de estas incluyen vasodilatación neurogénica, inflamación neurogénica, migraña, cefalea histamínica y otras cefaleas, lesión térmica, choque circulatorio, sofocos de la menopausia y asma. La activación del receptor de CGRP se ha implicado en la patogenia de la migraña (Edvinsson L. CNS Drugs 2001; 15 (10) :745-53; Williamson, D. J. Microsc. Res. Tech. 2001, 53, 167178.; Grant, A. D. Brit. J. Pharmacol. 2002, 135, 356-362.) . Los niveles en suero de CGRP se elevan durante la migraña (Goadsby PJ, y col. Ann Neurol 1990; 28: 183-7) y el tratamiento con fármacos antimigrañosos devuelven los niveles de CGRP a los normales coincidiendo con un alivio de la cefalea (Gallai V. y col. Cephalalgia 1995; 15: 384-90) . Los que padecen migrañas muestran niveles basales de CGRP elevados en comparación con los controles (Ashina M, y col., Pain 2000, 86 (1-2) :133-8.2000) . La infusión de CGRP intravenoso produce cefalea duradera en los que padecen migrañas (Lassen LH, y col. Cephalalgia 2002 Feb; 22 (1) :54-61) . Los estudios preclínicos en perros y ratas indican que el bloqueo de CGRP sistémico con el antagonista peptídico CGRP (8-37) no altera la hemodinámica sistémica en reposo ni el flujo sanguíneo regional (Shen, Y-T. y col, J Pharmacol Exp Ther 2001, 298, 551-8) . Por lo tanto, los antagonistas del receptor de CGRP pueden presentar un nuevo tratamiento para la migraña que evita las desventajas cardiovasculares de vasoconstricción activa asociada con agonistas de 5-HT1B/1D no selectivos, “triptanos” (por ejemplo, sumatriptán) .
Los antagonistas de CGRP han mostrado eficacia en ensayos clínicos humanos. Véase Davis CD, Xu C. Curr Top Med Chem. 2008 8 (16) :1468-79; Benemei S, Nicoletti P, Capone JG, Geppetti P. Curr Opin Pharmacol. 2009 9 (1) :9
14. Epub 20 Ene 2009; Ho TW, Ferrari MD, Dodick DW, Galet V, Kost J, Fan X, Leibensperger H, Froman S, Assaid C, Lines C, Koppen H, Winner PK. Lancet. 2008 372:2115. Epub 25 Nov 2008; Ho TW, Mannix LK, Fan X, Assaid C, Furtek C, Jones CJ, Lines CR, Rapoport AM; Neurology 2008 70:1304. Epub 3 Oct 2007.
La invención proporciona ventajas técnicas, por ejemplo, los compuestos son nuevos e inhiben CGRP. Adicionalmente, los compuestos proporcionan ventajas para usos farmacéuticos, por ejemplo, con respecto a uno o
más de sus mecanismos de acción, unión, eficacia de inhibición, selectividad de diana, solubilidad, perfiles de seguridad o biodisponibilidad.
Se han desvelados antagonistas de receptor de CGRP en las publicaciones de PCT WO 2004/092166, WO 2004/092168, WO 2007/120590 y WO 2006/052378 así como en Medicinal Chemistr y Letters vol. 18, 2007, 755
758.
Breve descripción de las figuras
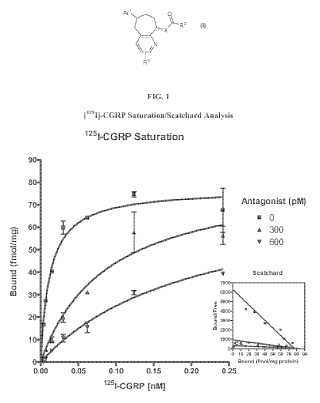
Figura 1. Análisis de Saturación de [125I]-CGRP/Scatchard. Saturación de [125I]-CGRP usando membranas de SK-N-MC en ausencia (cuadrados rellenos) y presencia (todos los demás) de antagonista de CGRP ejemplo 20. El inserto representa una representación de Scatchard de los mismos datos.
Figura 2. Análisis de Antagonismo Funcional/Schild. Respuesta a dosis de CGRP (producción de AMPc estimulada) en células SK-N-MC en ausencia (cuadrados abiertos) y presencia (todos los demás) de concentraciones crecientes (de izquierda a derecha, 0, 3 a 24 nM) del antagonista de CGRP ejemplo 20.
Figura 3. Validación Directa de Flujo Sanguíneo Facial como un Sustituto de Dilatación Arterial Intracraneal en la Rata. El suministro intravenoso de haCGRP i.v. induce aumentos porcentuales comparables (100-120 % de la línea basal) en el diámetro de la arteria meníngea media de la rata y flujo sanguíneo facial de la rata (barras rayadas izquierda y derecha, respectivamente) . El pretratamiento con el antagonista peptídico CGRP (8-37) produce una inhibición del 50 % de la administración de haCGRP i.v. posterior para ambas medidas (barras rellenas) . El diámetro de arterias intracraneales y el flujo sanguíneo facial se midieron simultáneamente en cada animal (n = 5 ratas) . Los datos son la media ± etm * p < 0, 05, ** p < 0, 01 frente a haCGRP correspondiente solamente.
Figura 4. Respuesta a Dosis para haCGRP del Flujo Sanguíneo Facial de Láser Doppler de Primate no Humano. El suministro de haCGRP (i.v.) induce el aumento dependiente de dosis del flujo sanguíneo facial de láser Doppler en primates no humanos (por ejemplo, tití común) . Los animales (n= 6) recibieron dosis crecientes de haCGRP a intervalos de 30 min. Los datos son el % de cambio máximo desde la línea basal ± etm, sirviendo cada animal como su propio control.
Descripción de la invención
La invención abarca una serie de compuestos antagonistas de CGRP incluyendo sales, composiciones farmacéuticamente aceptables, procedimientos para prepararlos y dichos compuestos para su uso en tratamiento terapéutico.
Un aspecto de la invención es un compuesto de fórmula I
en la que:
R1... [Seguir leyendo]
Reivindicaciones:
1. Un compuesto de fórmula I
en la que:
R1 es hidrógeno, ciano, halo, alquilo, haloalquilo, alcoxi, haloalcoxi, alquilSO2, amino, alquilamino, dialquilamino, azetidinilo, pirrolidinilo, piperidinilo, piperazinilo, N-alquilpiperazinilo o morfolinilo; R2 es N-piperidinilo y está sustituido en 4 con 1 sustituyente seleccionado del grupo constituido por
R3 es hidrógeno, halo, ciano, alquilo, haloalquilo, alcoxi o haloalcoxi; R4 es hidrógeno, halo, ciano, alquilo, haloalquilo, alcoxi o haloalcoxi; Ar1 es fenilo sustituido con 0-3 sustituyentes seleccionados del grupo constituido por ciano, halo, alquilo, haloalquilo, alcoxi, haloalcoxi y alquilSO2; X es O, CH2 o NH; y Y es un enlace, O, CH2 o NH;
o una sal farmacéuticamente aceptable del mismo.
2. Un compuesto de la reivindicación 1 con la estereoquímica designada.
3. Un compuesto de la reivindicación 2, en el que R1 es hidrógeno, halo, ciano, amino, alquilamino o dialquilamino; R2 es piperidinilo sustituido con 1 sustituyente seleccionado del grupo constituido por
R3 es hidrógeno o halo; R4 es hidrógeno o halo; Ar1 es fenilo con 0-2 sustituyentes halo; X es O, CH2 o NH; e Y es O;
o una sal farmacéuticamente aceptable del mismo.
4. Un compuesto de la reivindicación 3, en el que R1 es hidrógeno, cloro, ciano, amino, dimetilamino o t-butilamino; R2 es piperidinilo sustituido con 1 sustituyente seleccionado del grupo constituido por
Ar1 es fenilo o difluorofenilo; X es O, CH2, o NH; e Y es O; o una sal farmacéuticamente aceptable del mismo.
5. Un compuesto de la reivindicación 1, en el que R1 es hidrógeno, halo o ciano.
6. Un compuesto de la reivindicación 1, en el que el sustituyente es
7. Un compuesto de la reivindicación 1, en el que Ar1 es fenilo sustituido con 2 sustituyentes halo.
8. Un compuesto de la reivindicación 1, en el que Ar1 es 2, 3-difluorofenilo.
9. Un compuesto de la reivindicación 1, en el que X es O.
10. Un compuesto de la reivindicación 1, seleccionado del grupo constituido por
4. (2-oxo-4, 5-dihidro-1H-benzo[d] [1, 3]diazepin-3 (2H) -il) piperidin-1-carboxilato de (6, 9-trans) -6- (2, 3difluorofenil) -6, 7, 8, 9-tetrahidro-5H-ciclohepta[b]piridin-9-ilo; y
2-oxo-1, 2-dihidroespiro[benzo[d][1, 3]oxazina-4, 4’-piperidin]-1’-carboxilato de (6, 9-Trans) -6- (2, 3-difluorofenil) 6, 7, 8, 9-tetrahidro-5H-ciclohepta[b]piridin-9-ilo 4- (2-oxo-2, 3-dihidro-1H-imidazo[4, 5-b]piridin-1-il) piperidin-1-carboxilato de (6, 9-trans) -2-ciano-6- (2, 3difluorofenil) -6, 7, 8, 9-tetrahidro-5H-ciclohepta[b]piridin-9-ilo; 4- (2-oxo-2, 3-dihidro-1H-imidazo[4, 5-b]piridin-1-il) piperidin-1-carboxilato de (6R, 9R) -2-cloro-6- (2, 3-difluorofenil)
6, 7, 8, 9-tetrahidro-5H-ciclohepta[b]piridin-9-ilo; 4- (2-oxo-2, 3-dihidro-1H-imidazo[4, 5-b]piridin-1-il) piperidin-1-carboxilato de (6S, 9S) -2-cloro-6- (2, 3-difluorofenil)
6, 7, 8, 9-tetrahidro-5H-ciclohepta[b]piridin-9-ilo; 4- (2-oxo-2, 3-dihidro-1H-imidazo[4, 5-b]piridin-1-il) piperidin-1-carboxilato de (6, 9-trans) -6-fenil-6, 7, 8, 9-tetrahidro5H-ciclohepta[b]piridin-9-ilo; 4- (2-oxo-2, 3-dihidro-1H-imidazo[4, 5-b]piridin-1-il) piperidin-1-carboxilato de (6, 9-trans) -6- (2, 5-difluorofenil) 6, 7, 8, 9-tetrahidro-5H-ciclohepta[b]piridin-9-ilo; y 4- (2-oxo-2, 3-dihidro-1H-imidazo [4, 5-b] piridin-1-il) piperidin-1-carboxilato de (6, 9-trans) -6- (3, 4-Difluorofenil) 6, 7, 8, 9-tetrahidro-5H-ciclohepta[b]piridin-9-ilo; 1- (1- (2- (6, 9-Cis) -6- (2, 3-difluorofenil) -6, 7, 8, 9-tetrahidro-5H-ciclohepta[b]piridin-9-il) acetil) piperidin-4-il) -1Himidazo[4, 5-b]piridin-2 (3H) -ona; 1- (1- (2- (6R, 9S) -6- (2, 3-difluorofenil) -6, 7, 8, 9-tetrahidro-5H-ciclohepta[b]piridin-9-il) acetil) piperidin-4-il) -1Himidazo[4, 5-b]piridin-2 (3H) -ona; y 1- (1- (2- (6S, 9R) -6- (2, 3-difluorofenil) -6, 7, 8, 9-tetrahidro-5H-ciclohepta[b]piridin-9-il) acetil) piperidin-4-il) -1Himidazo[4, 5-b]piridin-2 (3H) -ona; N- ( (6R, 9R) -6- (2, 3-difluorofenil) -6, 7, 8, 9-tetrahidro-5H-ciclohepta[b]piridin-9-il) -4- (2-oxo-2, 3-dihidro-1H-imidazo [4, 5-b]piridin-1-il) piperidin-1-carboxamida; y N- ( (6S, 9S) -6- (2, 3-difluorofenil) -6, 7, 8, 9-tetrahidro-5H-ciclohepta[b]piridin-9-il) -4- (2-oxo-2, 3-dihidro-1H-imidazo [4, 5-b]piridin-1-il) piperidin-1-carboxamida; 4- (2-oxo-2, 3-dihidro-1H-imidazo[4, 5-b]piridin-1-il) piperidin-1-carboxilato de (6R, 9R) -2- (terc-butilamino) -6- (2, 3difluorofenil) -6, 7, 8, 9-tetrahidro-5H-ciclohepta[b]piridin-9-ilo; 4- (2-oxo-2, 3-dihidro-1H-imidazo[4, 5-b]piridin-1-il) piperidin-1-carboxilato de (6R, 9R) -2-amino-6- (2, 3difluorofenil) -6, 7, 8, 9-tetrahidro-5H-ciclohepta[b]piridin-9-ilo; 4- (2-oxo-2, 3-dihidro-1H-imidazo[4, 5-b]piridin-1-il) piperidin-1-carboxilato de (6R, 9R) -6- (2, 3-difluorofenil) -2dimetilamino-6, 7, 8, 9-tetrahidro-5H-ciclohepta[b]piridin-9-ilo; N- ( (6R, 9R) -3-amino-6- (2, 3-difluorofenil) -6, 7, 8, 9-tetrahidro-5H-ciclohepta[b]piridin-9-il) -4- (2-oxo-2, 3-dihidro-1Himidazo[4, 5-b]piridin-1-il) piperidin-1-carboxamida; y 4- (2-oxo-2, 3-dihidro-1H-imidazo[4, 5-b]piridin-1-il) piperidin-1-carboxilato de (6R, 9R) -6- (2, 3-difluorofenil) -3dimetilamino-6, 7, 8, 9-tetrahidro-5H-ciclohepta[b]piridin-9-ilo; y 4- (2-oxo-2, 3-dihidro-1H-imidazo[4, 5-b]piridin-1-il) piperidin-1-carboxilato de (6, 9-trans) -6- (2, 3-difluorofenil) 6, 7, 8, 9-tetrahidro-5H-ciclohepta[b]piridin-9-ilo; y 1- (1- ( ( (6R, 9R) -6- (2, 3-difluorofenil) -6, 7, 8, 9-tetrahidro-5H-ciclohepta[b]piridin-9-iloxi) carbonil) piperidin-4-il) -2-oxo1, 2-dihidroimidazo[4, 5-b]piridin-3-ida potásica;
o una sal farmacéuticamente aceptable de los mismos.
11. El compuesto de la reivindicación 1
o una sal farmacéuticamente aceptable del mismo.
12. Una composición que comprende un compuesto de una cualquiera de las reivindicaciones 1 a 11, o una sal farmacéuticamente aceptable del mismo, y un vehículo farmacéuticamente aceptable.
13. Un compuesto de una cualquiera de las reivindicaciones 1 a 11 o una sal farmacéuticamente aceptable del mismo para su uso en el tratamiento de una afección asociada con niveles aberrantes de CGRP seleccionada de migraña, cefaleas de migraña, vasodilatación neurogénica, inflamación neurogénica, lesión térmica, choque circulatorio, sofocos asociados con la menopausia, enfermedades inflamatorias de las vías respiratorias tales como asma y enfermedad pulmonar obstructiva crónica (EPOC) .
14. El compuesto para su uso de acuerdo con la reivindicación 13 en el que la afección es migraña.
15. Un compuesto seleccionado de entre: (6S, 9R) -6- (2, 3-difluorofenil) -9- (triisopropilsililoxi) -6, 7, 8, 9-tetrahidro-5H ciclohepta[b]piridin-5-ona de la fórmula
(R) -9- (triisopropilsililoxi) -6, 7, 8, 9-tetrahydro-5H-ciclohepta[b]piridin-5-ona de la fórmula
y (R) -9-hidroxi-6, 7, 8, 9-tetrahydro-5H-ciclohepta[b]piridin-5-ona de la fórmula
FIG. 1
Análisis de saturación de [125I]-CGRP/Scatchard
Saturación de 125I-CGRP
FIG. 2 Análisis de antagonismo funcional/Schild. Análisis de Schild.
FIG. 3
Validación directa de flujo sanguíneo facial como sustituto de la dilatación de arterias intracraneales en la rata.
intravital
FIG. 4
Respuesta a dosis para haCGRP en flujo sanguíneo facial de láser Doppler de primate no humano
Flujo sanguíneo facial de láser Doppler
Patentes similares o relacionadas:
Compuestos heterocíclicos que activan AMPK y métodos de uso de los mismos, del 29 de Julio de 2020, de RIGEL PHARMACEUTICALS, INC.: Un compuesto que es N-((cis)-1-(4-cianobencil)-3-fluoropiperidin-4-il)-6-(4-(4-metoxibenzoil)piperidin-1-carbonil)nicotinamida; N-((3S,4S)-1-(4-cianobencil)-3-fluoropiperidin-4-il)-6-(4-(4-metoxibenzoil)piperidin-1-carbonil)nicotinamida; […]
Derivados de piperidina 1,4 sustituidos, del 29 de Julio de 2020, de 89Bio Ltd: Un compuesto de acuerdo con la Fórmula I: **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en donde: A se selecciona de […]
Compuestos y procedimientos de uso, del 29 de Julio de 2020, de Medivation Technologies LLC: Un compuesto de fórmula (Aa-1): **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en la que: A representa H, halógeno, amino, […]
Ureas asimétricas p-sustituidas y usos médicos de las mismas, del 22 de Julio de 2020, de Helsinn Healthcare SA: Un compuesto de Fórmula I: **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en donde: una línea discontinua indica un enlace opcional; X es CH; […]
Ureas cíclicas como inhibidores de ROCK, del 22 de Julio de 2020, de BRISTOL-MYERS SQUIBB COMPANY: Un compuesto de acuerdo con la Fórmula (I): **(Ver fórmula)** o un enantiómero, un diastereómero, un estereoisómero, un tautómero, una sal farmacéuticamente aceptable […]
Inhibidores de Bcl-2/Bcl-xL y su uso en el tratamiento de cáncer, del 15 de Julio de 2020, de THE REGENTS OF THE UNIVERSITY OF MICHIGAN: Compuesto que tiene una estructura **(Ver fórmula)**
Derivado de dihidropiridazin-3,5-diona, del 15 de Julio de 2020, de CHUGAI SEIYAKU KABUSHIKI KAISHA: Un compuesto representado por la fórmula (I) o una sal del mismo, o un solvato del compuesto o la sal: **(Ver fórmula)** en donde R1, R4 y R5 se definen […]
Productos terapéuticos basados en la lantionina sintetasa 2 tipo C, del 15 de Julio de 2020, de LANDOS BIOPHARMA, INC: Un compuesto de la fórmula: **(Ver fórmula)** o una sal o éster farmacéuticamente aceptable de este, en donde: Q es piperazina-1,4-diilo; […]