Cristal de sal hidrocloruro de derivado de fenilalanina.
Un cristal de una sal de adición de ácido clorhídrico farmacéuticamente aceptable del compuesto representado por la fórmula (I) siguiente:**Fórmula**
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/JP2011/057798.
Solicitante: AJINOMOTO CO., INC..
Nacionalidad solicitante: Japón.
Dirección: 15-1, KYOBASHI 1-CHOME CHUO-KU TOKYO 104-8315 JAPON.
Inventor/es: KATAOKA, NORIYASU, TATARA,Akinori, KODAMA RIHO.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K31/517 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › condensadas en orto o en peri con sistemas carbocíclicos, p. ej. quinazolina, perimidina.
- A61P1/04 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › A61P 1/00 Medicamentos para el tratamiento de trastornos del tracto alimentario o del aparato digestivo. › para úlceras, gastritis o reflujo esofágico p.ej. antiácidos, inhibidores de la secreción ácida, protectores de la mucosa.
- A61P11/06 A61P […] › A61P 11/00 Medicamentos para el tratamiento de trastornos del aparato respiratorio. › Antiasmáticos.
- A61P17/06 A61P […] › A61P 17/00 Medicamentos para el tratamiento de problemas dermatológicos. › para el tratamiento de la psoriasis.
- A61P25/00 A61P […] › Medicamentos para el tratamiento de trastornos del sistema nervioso.
- A61P29/00 A61P […] › Agentes analgésicos, antipiréticos o antiinflamatorios que no actúan sobre el sistema nervioso central, p. ej. agentes antirreumáticos; Antiinflamatorios no esteroideos (AINEs).
- A61P3/10 A61P […] › A61P 3/00 Medicamentos para el tratamiento de trastornos del metabolismo (de la sangre o de fluido extracelular A61P 7/00). › para la hiperglucemia, p.ej. antidiabéticos.
- A61P35/00 A61P […] › Agentes antineoplásicos.
- A61P35/04 A61P […] › A61P 35/00 Agentes antineoplásicos. › específicos para la metástasis.
- A61P37/06 A61P […] › A61P 37/00 Medicamentos para el tratamiento de problemas inmunológicos o alérgicos. › Inmunosupresores, p. ej. medicamentos para el tratamiento del rechazo en injertos.
- A61P37/08 A61P 37/00 […] › Agentes antialérgicos (agentes antiasmáticos A61P 11/06; antialérgicos oftálmicos A61P 27/14).
- A61P43/00 A61P […] › Medicamentos para usos específicos, no previstos en los grupos A61P 1/00 - A61P 41/00.
- A61P9/00 A61P […] › Medicamentos para el tratamiento de trastornos en el aparato cardiovascular.
- A61P9/10 A61P […] › A61P 9/00 Medicamentos para el tratamiento de trastornos en el aparato cardiovascular. › para enfermedades isquémicas o ateroscleróticas, p.ej. medicamentos antianginosos, vasodilatadores coronarios,medicamentos para el tratamiento del infarto de miocardio, de la retinopatía, de la insuficiencia cerebrovascular, de la arterioesclerosis renal.
- C07D239/96 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07D COMPUESTOS HETEROCICLICOS (Compuestos macromoleculares C08). › C07D 239/00 Compuestos heterocíclicos que contienen ciclos de diazina-1,3 o diazina-1,3 hidrogenada. › Dos átomos de oxígeno.
PDF original: ES-2549768_T3.pdf



Fragmento de la descripción:
Cristal de sal hidrocloruro de derivado de fenilalanina Campo técnico
La presente invención se refiere a cristales de sales de un derivado de fenilalanina con una estructura específica, un 5 método para la preparación de la misma y el uso de la misma como medicina.
Antecedentes de la técnica
El compuesto representado por la fórmula química (I) como se especificará más tarde (al que se hace referencia de aquí en adelante como "el compuesto (I)" o una sal farmacéuticamente aceptable del mismo muestra una acción inhibidora de a-4-lntegrina in vivo, es un compuesto útil como agente terapéutico para el tratamiento, por ejemplo, de 10 enfermedades intestinales inflamatorias, y puede prepararse conforme a los métodos descritos en los documentos de patente 1 y 2, como se especificará más adelante. Además, se describe, en el documento de patente 3, un cristal de forma a o similar del compuesto (I) como una forma que es excelente en la estabilidad de almacenamiento y características de resistencia a la humedad. Además, el documento de patente 4 describe que la solubilidad del compuesto (I) puede mejorarse formando el compuesto (I), como un fármaco apenas soluble en agua, en una 15 dispersión de sólido, mientras se mantiene en su estado amorfo.
Por otra parte, también se ha conocido que si tal compuesto forma una sal, puede, por ejemplo, mejorarse su solubilidad y su biodisponibilidad, asi como la modificación de las características del compuesto o agente original (véase el documento 1 que no es una patente especificado más adelante). Sin embargo, todavía no se ha descrito ningún cristal de una sal farmacéuticamente aceptable del compuesto (I), y por lo tanto, se desea el desarrollo de 20 una sal cristalina del compuesto (I) con una excelente solubilidad en agua, mientras que mantiene una estabilidad suficiente para usar en la producción de preparaciones farmacéuticas que la contienen.
Bibliografía de la técnica anterior
Documento de patente
Documento de patente 1: panfleto de patente internacional abierta a consulta por el público N° 02/16329;
25 Documento de patente 2: panfleto de patente internacional abierta a consulta por el público N° 2004/074264; Documento de patente 3: panfleto de patente internacional abierta a consulta por el público N° 2005/051925; Documento de patente 4: panfleto de patente internacional abierta a consulta por el público N° 2005/046696; Documento que no es una patente
Documento que no es una patente 1: P. Heirich Stahl, Camille G. Wermuth (Eds.), "Handbook of Pharmaceutical 30 Salts", Wiley-VCH.
Descripción de la invención
Problemas que la invención ha de resolver
Es un objeto de la presente invención proporcionar un cristal de una sal del compuesto (I), que es excelente en su solubilidad en agua.
35 Medios para la solución de los problemas
Los inventores de esta invención han llevado a cabo diversos estudios para resolver los problemas anteriores asociados con las técnicas convencionales, y han encontrado que una sal del compuesto (I) con un ácido puede formar cristales con diversas formas cristalinas tratando el mismo en condiciones especificas, y que los problemas anteriores pueden resolverse con el uso de tal cristal, y de este modo han completado la presente invención.
40 Los detalles de la presente invención se darán a continuación:
(1) Un cristal de una sal de adición de ácido clorhídrico farmacéuticamente aceptable del compuesto representado por la fórmula (I) siguiente:
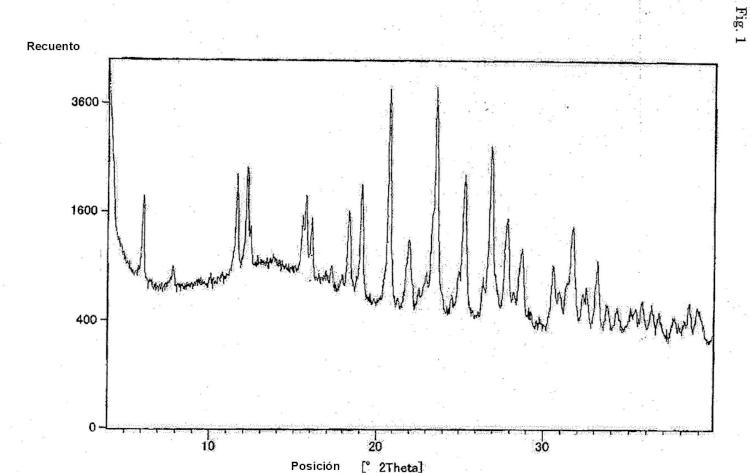
**(Ver fórmula)**(2) El cristal como se ha descrito en el punto (1) anterior, seleccionado de: cristal de forma Cl 1 caracterizado por los picos que aparecen en los ángulos (20) de difracción de 20,8, 23,6, 25,3 y 26,9 en el difractograma de rayos X en polvo; cristal de forma Cl 2 caracterizado por los picos que aparecen en los ángulos (20) de difracción de 5,24, 10,39, 21,04, y 21,41 en el difractograma de rayos X en polvo; cristal de forma Cl 3 caracterizado por los picos que aparecen en los ángulos (20) de difracción de 4,21, 10,13, 10,30 y 16,17 en el difractograma de rayos X en polvo; cristal de forma Cl 4 caracterizado por los picos que aparecen en los ángulos (20) de difracción de 4,07, 17,84, 23,83 y 24,87 en el difractograma de rayos X en polvo; cristal de forma Cl 5 caracterizado por los picos que aparecen en los ángulos (20) de difracción de 4,09, 22,12, 23,17 y 27,76 en el difractograma de rayos X en polvo; cristal de forma Cl 6 caracterizado por los picos que aparecen en los ángulos (20) de difracción de 22,32, 22,90, 26,43 y 26,77 en el difractograma de rayos X en polvo; o cristal de forma Cl 7 caracterizado por los picos que aparecen en los ángulos (20) de difracción de 16,65, 20,99, 22,61 y 24,70 en el difractograma de rayos X en polvo.
(3) Un cristal de una sal de adición de ácido clorhídrico farmacéuticamente aceptable como se ha descrito en el punto (2) anterior, que es un cristal de forma Cl 1 caracterizado por los picos que aparecen en los ángulos (20) de difracción de 20,8, 23,6, 25,3 y 26,9 en el difractograma de rayos X en polvo.
(4) Un cristal de una sal de adición de ácido clorhídrico farmacéuticamente aceptable como se ha descrito en el punto (2) anterior, que es un cristal de forma Cl 2 caracterizado por los picos que aparecen en los ángulos (20) de difracción de 5,24, 10,39, 21,04, y 21,41 en el difractograma de rayos X en polvo.
(5) Un cristal de una sal de adición de ácido clorhídrico farmacéuticamente aceptable como se ha descrito en el punto (2) anterior, que es un cristal de forma Cl 3 caracterizado por los picos que aparecen en los ángulos (20) de difracción de 4,21, 10,13, 10,30, 16,17 en el difractograma de rayos X en polvo.
(6) Un cristal de una sal de adición de ácido clorhídrico farmacéuticamente aceptable como se ha descrito en el punto (2) anterior, que es un cristal de forma Cl 4 caracterizado por los picos que aparecen en los ángulos (20) de difracción de 4,07, 17,84, 23,83 y 24,87 en el difractograma de rayos X en polvo.
(7) Un cristal de una sal de adición de ácido clorhídrico farmacéuticamente aceptable como se ha descrito en el punto (2) anterior, que es un cristal de forma Cl 5 caracterizado por los picos que aparecen en los ángulos (20) de difracción de 4,09, 22,12, 23,17 y 27,76 en el difractograma de rayos X en polvo.
(8) Un cristal de una sal de adición de ácido clorhídrico farmacéuticamente aceptable como se ha descrito en el punto (2) anterior, que es un cristal Cl 6 caracterizado por los picos que aparecen en los ángulos (20) de difracción de 22,32, 22,90, 26,43 y 26,77 en el difractograma de rayos X en polvo.
(9) Un cristal de una sal de adición de ácido clorhídrico farmacéuticamente aceptable como se ha descrito en el punto (2) anterior, que es un cristal de forma Cl 7 caracterizado por los picos que aparecen en los ángulos (20) de difracción de 16,65, 20,99, 22,61 y 24,70 en el difractograma de rayos X en polvo.
(10) Una composición farmacéutica que comprende un cristal como se ha descrito en uno cualquiera de los puntos anteriores (1) a (9).
(11) Un inhibidor de a-4-integrina que comprende un cristal como se ha descrito en uno cualquiera de los puntos anteriores (1) a (9).
(12) Un agente terapéutico o un agente profiláctico para tratar o prevenir una enfermedad inflamatoria, en el que el proceso de adhesión dependiente de a-4-integrina está implicado en la enfermedad, que comprende un cristal como se ha descrito en uno cualquiera de los puntos anteriores (1) a (9).
(13) Un agente terapéutico o un agente profiláctico para tratar o prevenir artritis reumatoide, enfermedades intestinales inflamatorias, lupus eritematoso diseminado, esclerosis diseminada o múltiple, síndrome de Sjógren, asma, soriasis, alergia, diabetes (mellitus), enfermedades cardiovasculares, arterieesclerosis, reestenosis, hiperplasia tumoral, metástasis tumoral y rechazo de trasplantes, caracterizado porque comprende un cristal como se ha descrito en uno cualquiera de los puntos anteriores (1) a (9).
Efecto de la invención
El cristal conforme a la presente invención puede manipularse fácilmente como un fármaco original para preparar un agente farmacéutico, y es excelente en, en particular, solubilidad, ya que está en forma cristalina. Además, posee preferiblemente una alta estabilidad en agua, suficiente para usar como un fármaco original de una preparación farmacéutica. Por lo tanto, el cristal conforme a la presente invención puede considerarse como un fármaco original para usar en la preparación de un agente farmacéutico o una preparación farmacéutica, que es excelente en la capacidad de absorción o biodisponibilidad y en... [Seguir leyendo]
Reivindicaciones:
1. Un cristal de una sal de adición de ácido clorhídrico farmacéuticamente aceptable del compuesto representado por la fórmula (I) siguiente:
[fórmula química 1]
**(Ver fórmula)**(I)
2. El cristal como se ha descrito en la reivindicación 1, seleccionado de: cristal de forma Cl 1 caracterizado por los picos que aparecen en los ángulos (20) de difracción de 20,8, 23,6, 25,3 y 26,9 en el difractograma de rayos X en polvo; cristal de forma Cl 2 caracterizado por los picos que aparecen en los ángulos (20) de difracción de 5,24, 10,39, 21,04, y 21,41 en el difractograma de rayos X en polvo; cristal de forma Cl 3 caracterizado por los picos que aparecen en los ángulos (20) de difracción de 4,21, 10,13, 10,30, 16,17 en el difractograma de rayos X en polvo; cristal de forma Cl 4 caracterizado por los picos que aparecen en los ángulos (20) de difracción de 4,07, 17,84, 23,83 y 24,87 en el difractograma de rayos X en polvo; cristal de forma Cl 5 caracterizado por los picos que aparecen en los ángulos (20) de difracción de 4,09, 22,12, 23,17 y 27,76 en el difractograma de rayos X en polvo; cristal Cl 6 caracterizado por los picos que aparecen en los ángulos (20) de difracción de 22,32, 22,90, 26,43 y 26,77 en el difractograma de rayos X en polvo; o cristal de forma Cl 7 caracterizado por los picos que aparecen en los ángulos (20) de difracción de 16,65, 20,99, 22,61 y 24,70 en el difractograma de rayos X en polvo.
3. Un cristal de una sal de adición de ácido clorhídrico farmacéuticamente aceptable conforme a la reivindicación 2, que es un cristal de forma Cl 1 caracterizado por los picos que aparecen en los ángulos (20) de difracción de 20,8, 23,6, 25,3 y 26,9 en el difractograma de rayos X en polvo.
4. Un cristal de una sal de adición de ácido clorhídrico farmacéuticamente aceptable conforme a la reivindicación 2, que es un cristal de forma Cl 2 caracterizado por los picos que aparecen en los ángulos (20) de difracción de 5,24, 10,39, 21,04, y 21,41 en el difractograma de rayos X en polvo.
5. Un cristal de una sal de adición de ácido clorhídrico farmacéuticamente aceptable conforme a la reivindicación 2, que es un cristal de forma Cl 3 caracterizado por los picos que aparecen en los ángulos (20) de difracción de 4,21, 10,13, 10,30, 16,17 en el difractograma de rayos X en polvo.
6. Un cristal de una sal de adición de ácido clorhídrico farmacéuticamente aceptable conforme a la reivindicación 2, que es un cristal de forma Cl 4 caracterizado por los picos que aparecen en los ángulos (20) de difracción de 4,07, 17,84, 23,83 y 24,87 en el difractograma de rayos X en polvo.
7. Un cristal de una sal de adición de ácido clorhídrico farmacéuticamente aceptable conforme a la
reivindicación 2, que es un cristal de forma Cl 5 caracterizado por los picos que aparecen en los ángulos (20) de difracción de 4,09, 22,12, 23,17 y 27,76 en el difractograma de rayos X en polvo.
8. Un cristal de una sal de adición de ácido clorhídrico farmacéuticamente aceptable conforme a la
reivindicación 2, que es un cristal 6 caracterizado por los picos que aparecen en los ángulos (23) de difracción de 22,32, 22,90, 26,43 y 26,77 en el difractograma de rayos X en polvo.
9. Un cristal de una sal de adición de ácido clorhídrico farmacéuticamente aceptable conforme a la
reivindicación 2, que es un cristal de forma Cl 7 caracterizado por los picos que aparecen en los ángulos (20) de difracción de 16,65, 20,99, 22,61 y 24,70 en el difractograma de rayos X en polvo.
10. Una composición farmacéutica que comprende un cristal como se ha descrito en una cualquiera de las reivindicaciones 1 a 9.
11. Un inhibidor de a-4-integrina que comprende un cristal como se ha descrito en una cualquiera de las reivindicaciones 1 a 9.
5 12. Un agente terapéutico o un agente profiláctico para tratar o prevenir una enfermedad inflamatoria, en el que
el proceso de adhesión dependiente de a-4-integrina está implicado en la enfermedad, que comprende un cristal como se ha descrito en una cualquiera de las reivindicaciones 1 a 9.
13. Un agente terapéutico o un agente profiláctico para tratar o prevenir artritis reumatoide, enfermedades intestinales inflamatorias, lupus eritematoso diseminado, esclerosis diseminada o múltiple, síndrome de Sjógren, 10 asma, soriasis, alergia, diabetes (mellitus), enfermedades cardiovasculares, arterieesclerosis, reestenosis, hiperplasia tumoral, metástasis tumoral y rechazo de trasplantes, caracterizado porque comprende un cristal como se ha descrito en una cualquiera de las reivindicaciones 1 a 9.
Patentes similares o relacionadas:
Compuestos y procedimientos de uso, del 29 de Julio de 2020, de Medivation Technologies LLC: Un compuesto de fórmula (Aa-1): **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en la que: A representa H, halógeno, amino, […]
Complejos de agentes terapéuticos de base vírica y poli(beta-amino-ésteres) modificados, del 29 de Julio de 2020, de Sagetis Biotech, SL: Un complejo de un agente terapéutico de base vírica con un polímero de fórmula I: **(Ver fórmula)** donde cada L1 y L2 están seleccionados […]
Compuestos de alquinilbenceno heterocíclicos, y composiciones médicas y usos de los mismos, del 29 de Julio de 2020, de Guangzhou Healthquest Pharma Co., Ltd: Un compuesto de alquinilbenceno heterocíclico que tiene la fórmula (I) y una sal farmacéuticamente aceptable, o estereoisómero del mismo, **(Ver […]
 Composiciones y métodos para el tratamiento de trastornos de células plasmáticas y trastornos prolinfocíticos de células b, del 29 de Julio de 2020, de Knopp Biosciences LLC: Una composición que comprende una cantidad terapéuticamente eficaz de dexpramipexol para su uso en el tratamiento de un trastorno de células B caracterizado por niveles elevados […]
Composiciones y métodos para el tratamiento de trastornos de células plasmáticas y trastornos prolinfocíticos de células b, del 29 de Julio de 2020, de Knopp Biosciences LLC: Una composición que comprende una cantidad terapéuticamente eficaz de dexpramipexol para su uso en el tratamiento de un trastorno de células B caracterizado por niveles elevados […]
Derivados de piperidina 1,4 sustituidos, del 29 de Julio de 2020, de 89Bio Ltd: Un compuesto de acuerdo con la Fórmula I: **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en donde: A se selecciona de […]
Profármacos de gemcitabina, del 29 de Julio de 2020, de NuCana plc: Una formulación farmacéutica que comprende gemcitabina-[fenil-benzoxi-L-alaninil)]-(S)-fosfato 3: **(Ver fórmula)** o una sal o solvato […]
Formas cristalinas de 6-((6,7-dimetoxiquinazolin-4-il)oxi)-N,2-dimetilbenzofuran-3-carboxamida, del 29 de Julio de 2020, de Hutchison Medipharma Limited: Forma I de 6-((6,7-dimetoxiquinazolin-4-il)oxi)-N,2-dimetilbenzofuran-3-carboxamida, en donde el difractograma de rayos X de polvo de la Forma […]
Derivado heteroarilo o sal farmacéuticamente aceptable del mismo, método de preparación del mismo y composición farmacéutica para prevenir o tratar enfermedades asociadas con PI3 quinasas, que contiene el mismo como principio activo, del 22 de Julio de 2020, de KOREA RESEARCH INSTITUTE OF CHEMICAL TECHNOLOGY: Un compuesto representado por la fórmula 1, un isómero óptico del mismo o una sal farmacéuticamente aceptable del mismo: **(Ver fórmula)** en la fórmula […]