Compuestos de GLP-1.
Un compuesto de GLP-1 que comprende un análogo de GLP-1 que comprende la secuencia de aminoácidos de fórmula I (SEC ID Nº:
5):
Xaa7-Gly-Xaa9-Xaa10-Xaa11-Xaa12-Xaa13-Xaa14-Xaa15-Xaa16-Xaa17-Xaa18-Xaa19-Xaa20-Xaa21-Xaa22-Cys-Xaa24- Xaa25-Xaa26-Xaa27Xaa28-Xaa29-Xaa30-Xaa31-Xaa32-Xaa33-Xaa34-Gly-Xaa36-Xaa37-Ser-Ser-Gly-Ala-Pro-Pro-Pro- Ser-C(O)-R1
en la que
R1 es OR2 o NR2R3;
R2 y R3 son independientemente hidrógeno o alquilo (C1-C8);
Xaa en la posición 7 es: L-histidina, D-histidina, desamino-histidina, 2-amino-histidina, 3-hidroxi-histidina, homohistidina, β-fluorometil-histidina o β-metil-histidina;
Xaa en la posición 9 es Glu, Asp o Lys;
Xaa en la posición 10 es Gly o His;
Xaa en la posición 11 es Thr, Ala, Gly, Ser, Leu, Ile, Val, Glu, Asp o Lys;
Xaa en la posición 12 es: His, Trp, Phe o Tyr;
Xaa en la posición 13 es Thr o Gly;
Xaa en la posición 14 es Ser, Ala, Gly, Thr, Leu, Ile, Val, Glu, Asp o Lys;
Xaa en la posición 15 es Asp o Glu;
Xaa en la posición 16 es Val, Ala, Gly, Ser, Thr, Leu, Ile, Tyr, Glu, Asp, Trp o Lys;
Xaa en la posición 17 es Ser, Ala, Gly, Thr, Leu, Ile, Val, Glu, Asp o Lys;
Xaa en la posición 18 es Ser, Ala, Gly, Thr, Leu, Ile, Val, Glu, Asp, Trp, Tyr, Lys, homolisina, ornitina, 4-carboxifenilalanina, ácido beta-glutámico, ácido beta-homoglutámico o ácido homoglutámico;
Xaa en la posición 19 es Tyr, Phe, Trp, Glu, Asp, Gln, Lys, homolisina, ornitina, 4-carboxi-fenilalanina, ácido beta-glutámico, ácido beta-homoglutámico o ácido homoglutámico;
Xaa en la posición 20 es Leu, Ala, Gly, Ser, Thr, Ile, Val, Glu, Asp, Met, Trp, Tyr, Lys, homolisina, ornitina, 4- carboxi-fenilalanina, ácido beta-glutámico o ácido homoglutámico;
Xaa en la posición 21 es Glu, Asp, Lys, homolisina, ornitina, 4-carboxi-fenilalanina, ácido beta-glutámico, ácido beta-homoglutámico o ácido homoglutámico;
Xaa en la posición 22 es Gly, Ala, Ser, Thr, Leu, Ile, Val, Glu, Asp, Lys, homolisina, ornitina, 4-carboxifenilalanina, ácido beta-glutámico, ácido beta-homoglutámico o ácido homoglutámico;
Xaa en la posición 24 es Ala, Gly, Ser, Thr, Leu, Ile, Val, Arg, Glu, Asp, Lys, homolisina, ornitina, 4-carboxifenilalanina, ácido beta-glutámico, ácido beta-homoglutámico o ácido homoglutámico;
Xaa en la posición 25 es Ala, Gly, Ser, Thr, Leu, Ile, Val, Glu, Asp, Lys, homolisina, ornitina, 4-carboxifenilalanina, ácido beta-glutámico, ácido beta-homoglutámico o ácido homoglutámico;
Xaa en la posición 26 es Lys, homolisina, Arg, Gln, Glu, Asp, His, ornitina, 4-carboxi-fenilalanina, ácido beta40 glutámico o ácido homoglutámico;
Xaa en la posición 27 es Leu, Glu, Asp, Lys, homolisina, ornitina, 4-carboxi-fenilalanina, ácido beta-glutámico, ácido beta-homoglutámico o ácido homoglutámico;
Xaa en la posición 28 es Phe, Trp, Asp, Glu, Lys, homolisina, ornitina, 4-carboxi-fenilalanina, ácido betaglutámico, ácido beta-homoglutámico o ácido homoglutámico;
Xaa en la posición 29 es Ile, Leu, Val, Ala, Phe, Asp, Glu, Lys, homolisina, ornitina, 4-carboxi-fenilalanina, ácido beta-glutámico, ácido beta-homoglutámico o ácido homoglutámico;
Xaa en la posición 30 es Ala, Gly, Ser, Thr, Leu, Ile, Val, Glu, Asp, Lys, homolisina, ornitina, 4-carboxifenilalanina, ácido beta-glutámico, ácido beta-homoglutámico o ácido homoglutámico;
Xaa en la posición 31 es Trp, Phe, Tyr, Glu, Asp o Lys;
Xaa en la posición 32 es Leu, Gly, Ala, Ser, Thr, Ile, Val, Glu, Asp o Lys;
Xaa33 es: Val o Lys;
Xaa34 es: Lys o Asn;
Xaa36 es: Arg o Gly;
Xaa37 es: Gly o Pro;
en la que el compuesto tiene una actividad de GLP-1, en la que dicha actividad de GLP-1 es actividad insulinotrópica.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2007/067150.
Solicitante: AMGEN INC..
Nacionalidad solicitante: Estados Unidos de América.
Dirección: ONE AMGEN CENTER DRIVE THOUSAND OAKS CA 91320 ESTADOS UNIDOS DE AMERICA.
Inventor/es: GEGG,COLIN VICTOR JR, MIRANDA,LESLIE PHILLIP, WINTERS,KATHERINE ANN, VENIANT-ELLISON,MURIELLE.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C07K14/60 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 14/00 Péptidos con más de 20 aminoácidos; Gastrinas; Somatostatinas; Melanotropinas; Sus derivados. › Factor de liberación de la hormona del crecimiento (GH-RF) (Somatoliberina).
PDF original: ES-2495741_T3.pdf
Fragmento de la descripción:
Compuestos de GLP-1 5 ANTECEDENTES
El péptido 1 similar al glucagón (GLP-1) y el glucagón peptídico relacionado se producen mediante procesamiento diferencial de proglucagón y tienen actividades biológicas opuestas. El proglucagón mismo se produce en células a del páncreas y en las células L enteroendocrinas, que están localizadas principalmente en el intestino delgado 1 distante y en el colon. En el páncreas, el glucagón se escinde selectivamente a partir de proglucagón. En el intestino, por el contrario, el proglucagón se procesa para formar GLP-1 y péptido 2 similar al glucagón (GLP-2), que corresponde con los residuos de aminoácidos 78-17 y 126-158 de proglucagón, respectivamente (véase, por ejemplo Irwin y Wong, 1995, Mol. Endocrinol. 9:267-277 y Bell y col., 1983, Nature 34:368-371). Por convención, la numeración de los aminoácidos de GLP-1 se basa en el GLP-1 (1-37) formado de la escisión de proglucagón. Las 15 formas biológicamente activas se generan a partir del procesamiento adicional de este péptido, que da GLP-1 (7- 37)-OH y GLP-1 (7-36)-NH2. El primer aminoácido de estos péptidos procesados es Hls7. Tanto GLP-1 (7-37)-OH (o simplemente GLP-1 (7-37)) como GLP-1 (7-36)-NH2 tienen las mismas actividades. Por conveniencia, el término GLP-1 se usa para referirse a ambas de estas formas.
El glucagón es secretado de las células a del páncreas en respuesta a baja glucosa en sangre, siendo el órgano diana principal para el glucagón el hígado. El glucagón estimula la descomposición de glicógeno e inhibe la biosíntesis de glicógeno. También inhibe la síntesis de ácidos grasos, pero mejora la gluconeogénesis. El resultado neto de estas acciones es aumentar significativamente la liberación de glucosa del hígado. Por el contrario, el GLP-1 disminuye la secreción de glucagón, mientras que se estimula la secreción de insulina, la captación de glucosa y la 25 formación de AMP cíclico (AMPc) en respuesta a la absorción de nutrientes por el Intestino. Vahos datos clínicos proporcionan pruebas de estas actividades. La administración de GLP-1, por ejemplo, en diabéticos tipo 2 malamente controlados normalizó sus niveles de glucosa en sangre en ayunas (véase, por ejemplo, Gutniak y col., 1992, New Eng. J. Med. 326:1316-1322).
El GLP-1 tiene varias actividades importantes. Por ejemplo, el GLP-1 también inhibe la motilidad gástrica y la secreción gástrica (véase, por ejemplo, Tolessa, 1998, J. Clin. Invest. 12:764-774). Este efecto, algunas veces referido como el efecto de freno ileal, produce una fase de retraso en la disponibilidad de nutrientes, reduciendo así significativamente la necesidad de respuesta rápida de insulina.
Los estudios también indican que GLP-1 puede promover la diferenciación y replicación celular, que a su vez ayuda en la conservación de células de islotes pancreáticos y un aumento en la masa de células (3 (véanse, por ejemplo, Andreasen y col., 1994, Digestión 55:221-228; Wang y col., 1997, J. Clin. Invest. 99:2883-2889; Mojsov, 1992, Int. J. Pep. Prot. Res. 4:333-343; y Xu y col., 1999, Diabetes 48:227-2276). Las pruebas también indican que GLP-1 puede aumentar la saciedad y disminuir la ingestión de alimento (véase, por ejemplo, Toft-Nielsen y col., 1999, 4 Diabetes Care 22:1137-1143; Flinty col., 1998, J. Clin. Invest. 11:515- 52; Gutswillery col., 1999 Gut 44:81-86).
Otra investigación indica que GLP-1 induce la expresión génica específica de células (3, incluyendo el transportador GLUT-1, receptor de insulina y hexocinasa-1 (véase, por ejemplo, Perfetti y Merkel, 2, Eur. J. Endocrinol. 143:717-725). Tal inducción podría invertirla intolerancia a glucosa frecuentemente asociada al envejecimiento.
Debido a que GLP-1 desempeña una función clave en la regulación de la homeostasis metabólica, es una diana atractiva para tratar una variedad de trastornos metabólicos, incluyendo diabetes, obesidad y síndrome metabólico. Los tratamientos actuales para diabetes incluyen inyección de insulina y administración de sulfonilureas, metformina y TZD. Sin embargo, estos enfoques tienen inconvenientes significativos. Las inyecciones de insulina, por ejemplo, 5 requieren consideraciones de dosificación complicada, y el tratamiento con sulfonilureas frecuentemente llega a ser ineficaz con el tiempo, la metformina puede inducir hipoglucemia y los TZD tienen efectos secundarios tales como aumento de peso corporal y edema. Las posibles ventajas de la terapia con GLP-1 incluyen: 1) aumento de la seguridad debido a que la secreción de insulina es dependiente de la hiperglucemia, 2) supresión de la secreción de glucagón que a su vez suprime la excesiva salida de glucosa, y 3) desaceleración del vaciado gástrico, que a su vez 55 desacelera la absorción de nutrientes y previene aumentos súbitos de glucosa.
Sin embargo, un obstáculo clave para el tratamiento eficaz con GLP-1 ha sido la semlvlda muy corta del péptido, que normalmente es sólo de algunos minutos (véase, por ejemplo, Holst, 1994, Gastroenterology 17:1848-1855). Se han desarrollado varios análogos con el objetivo de extender la semlvida de la molécula. Sin embargo, algunos de 6 éstos tienen efectos secundarios gastrointestinales significativos, Incluyendo vómitos y náuseas (véase, por ejemplo Agerso y col., 22, Dlabetologla 45:195-22).
Por consiguiente, así sigue existiendo una necesidad de moléculas mejoradas que tengan actividad tipo GLP-1, para uso en el tratamiento de varias enfermedades metabóllcas tal como diabetes, obesidad, síndrome de Intestino 65 Irritable y síndrome metabólico.
RESUMEN
En el presente documento se describen compuestos de GLP-1 que comprenden análogos de GLP-1 y tienen una 5 actividad de GLP-1 (por ejemplo, actividad insulinotrópica). También se proporcionan procedimientos de tratamiento de una variedad de enfermedades administrando una cantidad eficaz de las composiciones. Tales procedimientos pueden usarse para tratar, por ejemplo, diabetes, intolerancia a la glucosa, resistencia a la insulina, varios trastornos de lípidos, obesidad, enfermedades cardiovasculares y trastornos óseos.
Algunos de los compuestos de GLP-1 que se proporcionan en el presente documento, por ejemplo, comprenden un análogo de GLP-1 que comprende la secuencia de aminoácidos de la fórmula I (SEC ID N°: 5):
Xaa7-Gly-Xaa9-Xaaio-Xaaii-Xaai2-Xaai3-Xaai4-Xaai5-Xaai6-Xaai7-Xaai8-Xaai9-Xaa2o-Xaa2i-Xaa22-Cys-Xaa24- Xaa25-Xaa26-Xaa27-Xaa28-Xaa29-Xaa3-Xaa3i-Xaa32-Xaa33-Xaa34-Gly-Xaa36-Xaa37-Ser-Ser-Gly-Ala-Pro-Pro- 15 Pro-Ser-C(Oj-Ri (Fórmula I, SEC ID N°: 5)
en la que
Ri es OR2 o NR2R3;
R2 y R3 son independientemente hidrógeno o alquilo (Ci-Cs);
Xaa en la posición 7 es: L-histidina, D-histidina, desamino-histidina, 2-amino-histidina, 3-hidroxi-histidina, homohistidina, a-fluorometil-histidina o a-metil-histidina;
Xaa en la posición 9 es Glu, Asp o Lys;
Xaa en la posición 1 es Gly o His;
Xaa en la posición 11 es Thr, Ala, Gly, Ser, Leu, lie, Val, Glu, Asp o Lys;
Xaa en la posición 12 es: His, Trp, Phe o Tyr;
Xaa en la posición 13 es Thr o Gly;
Xaa en la posición 14 es Ser, Ala, Gly, Thr, Leu, lie, Val, Glu, Asp o Lys;
Xaa en la posición 15 es Asp o Glu;
Xaa en la posición 16 es Val, Ala, Gly, Ser, Thr, Leu, lie, Tyr, Glu, Asp, Trp o Lys;
Xaa en la posición 17 es Ser, Ala, Gly, Thr, Leu, lie, Val, Glu, Asp o Lys;
Xaa en la posición 18 es Ser, Ala, Gly, Thr, Leu, lie, Val, Glu, Asp, Trp, Tyr, Lys, homolisina, ornitina, 4-carboxi- fenilalanina, ácido beta-glutámico, ácido beta-homoglutámico o ácido homoglutámico;
Xaa en la posición 19 es Tyr, Phe, Trp, Glu, Asp, Gln, Lys, homolisina, ornitina, 4-carboxi-fenilalanina, ácido 35 beta-glutámico, ácido beta-homoglutámico o ácido homoglutámico;
Xaa en la posición 2 es Leu, Ala, Gly, Ser, Thr, lie, Val, Glu, Asp, Met, Trp, Tyr, Lys, homolisina, ornitina, 4- carboxi-fenilalanina, ácido beta-glutámico o ácido homoglutámico;
Xaa en la posición 21 es Glu, Asp, Lys, homolisina, ornitina, 4-carboxi-fenilalanina, ácido beta-glutámico, ácido beta-homoglutámico o ácido homoglutámico;
Xaa en la posición 22 es Gly, Ala, Ser, Thr, Leu, lie, Val, Glu, Asp, Lys, homolisina, ornitina, 4-carboxi- fenilalanina, ácido beta-glutámico, ácido beta-homoglutámico o ácido homoglutámico;
Xaa en la posición 24 es Ala, Gly, Ser, Thr, Leu, lie, Val, Arg, Glu, Asp, Lys, homolisina, ornitina, 4-carboxi- fenilalanina, ácido beta-glutámico, ácido beta-homoglutámico o ácido homoglutámico;
Xaa en la posición 25 es Ala, Gly, Ser, Thr, Leu, lie, Val, Glu, Asp, Lys, homolisina, ornitina, 4-carboxi- 45 fenilalanina, ácido beta-glutámico, ácido beta-homoglutámico... [Seguir leyendo]
Reivindicaciones:
1. Un compuesto de GLP-1 que comprende un análogo de GLP-1 que comprende la secuencia de aminoácidos de fórmula I (SEC ID N°: 5):
Xaa7-Gly-Xaa9-Xaaio-Xaaii-Xaai2-Xaai3-Xaai4-Xaai5-Xaai6-Xaai7-Xaai8-Xaai9-Xaa2o-Xaa2i-Xaa22-Cys-Xaa24-
Xaa25-Xaa26-Xaa27Xaa28-Xaa29-Xaa3o-Xaa3i-Xaa32-Xaa33-Xaa34-Gly-Xaa36-Xaa37-Ser-Ser-Gly-Ala-Pro-Pro-Pro-
Ser-C()-Ri
en la que
Ri es OR2 o NR2R3;
R2 y R3 son Independientemente hidrógeno o alquilo (Ci-C8);
Xaa en la posición 7 es: L-histidina, D-histidina, desamino-histidina, 2-amino-hlstldina, 3-hidroxi-histidina, 15 homohistldlna, a-fluorometil-histidina o a-metil-histidina;
Xaa en la posición 9 es Glu, Asp o Lys;
Xaa en la posición 1 es Gly o His;
Xaa en la posición 11 es Thr, Ala, Gly, Ser, Leu, lie, Val, Glu, Asp o Lys;
Xaa en la posición 12 es: His, Trp, Phe o Tyr;
Xaa en la posición 13 es Thr o Gly;
Xaa en la posición 14 es Ser, Ala, Gly, Thr, Leu, lie, Val, Glu, Asp o Lys;
Xaa en la posición 15 es Asp o Glu;
Xaa en la posición 16 es Val, Ala, Gly, Ser, Thr, Leu, lie, Tyr, Glu, Asp, Trp o Lys;
Xaa en la posición 17 es Ser, Ala, Gly, Thr, Leu, lie, Val, Glu, Asp o Lys;
Xaa en la posición 18 es Ser, Ala, Gly, Thr, Leu, lie, Val, Glu, Asp, Trp, Tyr, Lys, homolisina, ornitina, 4-carboxi- fenilalanina, ácido beta-glutámico, ácido beta-homoglutámlco o ácido homoglutámico;
Xaa en la posición 19 es Tyr, Phe, Trp, Glu, Asp, Gln, Lys, homolisina, ornitina, 4-carboxi-fenilalanina, ácido beta-glutámico, ácido beta-homoglutámico o ácido homoglutámico;
Xaa en la posición 2 es Leu, Ala, Gly, Ser, Thr, lie, Val, Glu, Asp, Met, Trp, Tyr, Lys, homolisina, ornitina, 4- 3 carboxi-femlalanina, ácido beta-glutámico o ácido homoglutámico;
Xaa en la posición 21 es Glu, Asp, Lys, homolisina, ornitina, 4-carboxi-fenilalanina, ácido beta-glutámico, ácido beta-homoglutámico o ácido homoglutámico;
Xaa en la posición 22 es Gly, Ala, Ser, Thr, Leu, lie, Val, Glu, Asp, Lys, homolisina, ornitina, 4-carboxi- fenilalanina, ácido beta-glutámico, ácido beta-homoglutámico o ácido homoglutámico;
Xaa en la posición 24 es Ala, Gly, Ser, Thr, Leu, lie, Val, Arg, Glu, Asp, Lys, homolisina, ornitina, 4-carboxi- fenilalanina, ácido beta-glutámico, ácido beta-homoglutámico o ácido homoglutámico;
Xaa en la posición 25 es Ala, Gly, Ser, Thr, Leu, lie, Val, Glu, Asp, Lys, homolisina, ornitina, 4-carboxi- fenilalanina, ácido beta-glutámico, ácido beta-homoglutámico o ácido homoglutámico;
Xaa en la posición 26 es Lys, homolisina, Arg, Gln, Glu, Asp, His, ornitina, 4-carboxi-fenilalanina, ácido beta- 4 glutámico o ácido homoglutámico;
Xaa en la posición 27 es Leu, Glu, Asp, Lys, homolisina, ornitina, 4-carboxi-fenilalanina, ácido beta-glutámico, ácido beta-homoglutámico o ácido homoglutámico;
Xaa en la posición 28 es Phe, Trp, Asp, Glu, Lys, homolisina, ornitina, 4-carboxi-fenilalanina, ácido beta- glutámico, ácido beta-homoglutámico o ácido homoglutámico;
Xaa en la posición 29 es lie, Leu, Val, Ala, Phe, Asp, Glu, Lys, homolisina, ornitina, 4-carboxi-fenilalanina, ácido beta-glutámico, ácido beta-homoglutámico o ácido homoglutámico;
Xaa en la posición 3 es Ala, Gly, Ser, Thr, Leu, lie, Val, Glu, Asp, Lys, homolisina, ornitina, 4-carboxi- fenilalanina, ácido beta-glutámico, ácido beta-homoglutámico o ácido homoglutámico;
Xaa en la posición 31 es Trp, Phe, Tyr, Glu, Asp o Lys;
Xaa en la posición 32 es Leu, Gly, Ala, Ser, Thr, lie, Val, Glu, Asp o Lys;
Xaa33 es: Val o Lys;
Xaa34 es: Lys o Asn;
Xaa36 es: Arg o Gly;
Xaa37 es: Gly o Pro;
en la que el compuesto tiene una actividad de GLP-1, en la que dicha actividad de GLP-1 es actividad insulinotrópica.
2. El compuesto de GLP-1 de la reivindicación 1, en la que el análogo de GLP-1 tiene la secuencia de aminoácidos 6 de cualquiera de SEC ID N°: 7 a 8 con no más de 5 sustituciones conservativas de aminoácidos, a condición de que las sustituciones conservativas de aminoácidos no estén en el aminoácido Xaas, Xaa23, y cualquiera de Xaa3s a Xaa45-
3. El compuesto de GLP-1 de la reivindicación 1, en el que el análogo de GLP-1 tiene la secuencia de aminoácidos 65 de cualquiera de SEC ID N°: 7 a 8.
4. El compuesto de GLP-1 de cualquiera de las reivindicaciones 1 a 3, que se modifica covalentemente con un polímero soluble en agua.
5. El compuesto de GLP-1 de la reivindicación 4, en el que el polímero soluble en agua se selecciona del grupo que 5 consiste en polletllenglicol, monometoxl-polietilengllcol, dextrano, celulosa, poli-(N-vinilpirrolidona)poMet¡lengMcol,
homopolímeros de propilenglicol, copolfmeros de poll(óxldo de propileno)/óxido de etlleno, polloles polioxietilados y alcohol polivlníllco.
6. El compuesto de GLP-1 de la reivindicación 4, en el que el polímero soluble en agua se selecciona del grupo que 1 consiste en polletllenglicol y dextrano.
7. El compuesto de GLP-1 de cualquiera de las reivindicaciones 1 a 3, en el que el análogo de GLP-1 está pegilado.
8. Una composición farmacéutica que comprende un vehículo farmacéuticamente aceptable y una cantidad eficaz 15 del compuesto de GLP-1 de cualquiera de las reivindicaciones 1 a 7.
9. Uso de un compuesto de GLP-1 de cualquiera de las reivindicaciones 1 a 3 para la preparación de una composición farmacéutica para tratar un sujeto con un trastorno metabólico, en el que el trastorno metabólico se selecciona del grupo de diabetes, obesidad y síndrome metabólico.
1. Un compuesto de GLP-1 de cualquiera de las reivindicaciones 1 a 3 para su uso en el tratamiento de un sujeto con un trastorno metabólico, en el que el trastorno metabólico se selecciona del grupo de diabetes, obesidad y síndrome metabólico.
11. Uso de un compuesto de GLP-1 de cualquiera de las reivindicaciones 1 a 3 para la preparación de una composición farmacéutica para potenciar la expresión de insulina o promover la secreción de insulina en un sujeto.
12. Un compuesto de GLP-1 de cualquiera de las reivindicaciones 1 a 3 para su uso en potenciar la expresión de insulina o promover la secreción de insulina en un sujeto.
Patentes similares o relacionadas:
Procedimiento para la síntesis de análogos de la grelina, del 24 de Enero de 2018, de Ipsen Manufacturing Ireland Limited: Un procedimiento para la síntesis de un péptido terapéutico mediante el uso de la química de Fmoc en fase sólida por etapas, que comprende las […]
GHRELINA-O-ACIL TRANSFERASA (GOAT) Y SUS USOS, del 1 de Junio de 2017, de UNIVERSIDAD DE CORDOBA: La presente invención se refiere al uso de los niveles obtenidos ex vivo a partir de una muestra biológica aislada de un sujeto de la cantidad o concentración […]
 Formulaciones farmacéuticas que comprenden insulina complejada con una dicetopiperazina, del 17 de Febrero de 2016, de MANNKIND CORPORATION: Una composicion que comprende microparticulas, que comprende insulina complejada a una dicetopiperazina, para su uso en medicina; en donde la composicion libera insulina […]
Formulaciones farmacéuticas que comprenden insulina complejada con una dicetopiperazina, del 17 de Febrero de 2016, de MANNKIND CORPORATION: Una composicion que comprende microparticulas, que comprende insulina complejada a una dicetopiperazina, para su uso en medicina; en donde la composicion libera insulina […]
Proteínas de fusión de albúmina, del 3 de Diciembre de 2014, de NOVOZYMES BIOPHARMA DK A/S: Una proteína de fusión de albúmina que comprende (i) factor IX, o un fragmento o una variante del factor IX, en la que la variante tiene al menos el 75 % de identidad […]
Proteínas de fusión de albúmina, del 4 de Junio de 2014, de NOVOZYMES BIOPHARMA DK A/S: Una proteína de fusión de albúmina que comprende (i) factor VII, o un fragmento o una variante del factor VII, fusionado con el extremo N-terminal de la (ii) […]
Compuestos análogos a secretagogos peptídicos de la hormona del crecimiento y preparaciones que los contienen, del 9 de Octubre de 2013, de CENTRO DE INGENIERIA GENETICA Y BIOTECNOLOGIA: Compuestos químicos peptídicos obtenidos por modelación molecularin silico, y cuya estructura les permite efectuar las mismas funciones que los secretagogos peptídicos de […]
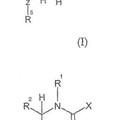 Secretagogos de la hormona del crecimiento, del 1 de Julio de 2013, de IPSEN PHARMA: Un compuesto de la fórmula (I) **Fórmula**
en la que
X es **Fórmula**
Y es H o NR12R13;
Z es -C(O)- o -SO2-
n es, independientemente […]
Secretagogos de la hormona del crecimiento, del 1 de Julio de 2013, de IPSEN PHARMA: Un compuesto de la fórmula (I) **Fórmula**
en la que
X es **Fórmula**
Y es H o NR12R13;
Z es -C(O)- o -SO2-
n es, independientemente […]
ANÁLOGOS DE LA GRELINA, del 22 de Junio de 2011, de IPSEN PHARMA: Un compuesto según la fórmula (I): (R2R3)-A1-A2-A3-A4-A5-A6-A7-A8-A9-A10-A11-A12-A13-A14-A15-A16-A17-A18-A19-A20-A21-A22-A23-A24-A25-A26-A27-A28-R1 (I), […]