COMPUESTOS DE ARN DE DOBLE HEBRA ESPECIFICOS DE VGLUT.
Moléculas de ARNsi específicas de VGLUT con una secuencia seleccionada entre **Fórmula**
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2005/001970.
Solicitante: GRUNENTHAL GMBH.
Nacionalidad solicitante: Alemania.
Dirección: ZIEGLERSTRASSE 6, 52078 AACHEN.
Inventor/es: GILLEN, CLEMENS, DR., CHRISTOPH, THOMAS, WEIHE,EBERHARD, BAHRENBERG,GREGOR, SCHAFER,K.-H.,MARTIN, BENDER,FLORIAN.
Fecha de Publicación: .
Fecha Concesión Europea: 16 de Junio de 2010.
Clasificación Internacional de Patentes:
- C12N15/113E
Clasificación PCT:
- A61K31/7088 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › Compuestos que tienen al menos tres nucleósidos o nucleótidos.
- C12N15/11 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 15/00 Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K). › Fragmentos de ADN o de ARN; sus formas modificadas (ADN o ARN no empleado en tecnología de recombinación C07H 21/00).
- C12Q1/68 C12 […] › C12Q PROCESOS DE MEDIDA, INVESTIGACION O ANALISIS EN LOS QUE INTERVIENEN ENZIMAS, ÁCIDOS NUCLEICOS O MICROORGANISMOS (ensayos inmunológicos G01N 33/53 ); COMPOSICIONES O PAPELES REACTIVOS PARA ESTE FIN; PROCESOS PARA PREPARAR ESTAS COMPOSICIONES; PROCESOS DE CONTROL SENSIBLES A LAS CONDICIONES DEL MEDIO EN LOS PROCESOS MICROBIOLOGICOS O ENZIMOLOGICOS. › C12Q 1/00 Procesos de medida, investigación o análisis en los que intervienen enzimas, ácidos nucleicos o microorganismos (aparatos de medida, investigación o análisis con medios de medida o detección de las condiciones del medio, p. ej. contadores de colonias, C12M 1/34 ); Composiciones para este fin; Procesos para preparar estas composiciones. › en los que intervienen ácidos nucleicos.
Clasificación antigua:
- A61K31/7088 A61K 31/00 […] › Compuestos que tienen al menos tres nucleósidos o nucleótidos.
- C12N15/11 C12N 15/00 […] › Fragmentos de ADN o de ARN; sus formas modificadas (ADN o ARN no empleado en tecnología de recombinación C07H 21/00).
- C12Q1/68 C12Q 1/00 […] › en los que intervienen ácidos nucleicos.
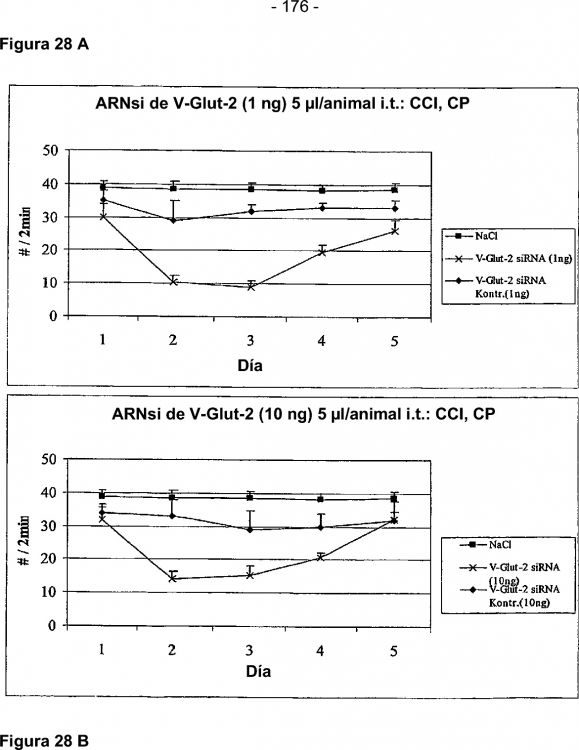
Fragmento de la descripción:
La invención se refiere a moléculas de ARN de doble hebra (ARNds) pequeñas, en particular a moléculas desencadenantes de interferencia dirigidas contra miembros de la familia de los VGLUT, y a células huésped que contienen el ARNds según la invención. Los ARNds según la invención y las células huésped correspondientes son adecuados como medicamentos o para la producción de medicamentos, en particular para el tratamiento del dolor y de otros estados patológicos relacionados con miembros de la familia de los VGLUT o con la expresión no fisiológica de éstos.
De acuerdo con la definición de la Asociación Internacional para el Estudio del Dolor (IASP), el dolor es una “experiencia sensorial y emocional desagradable, asociada con una lesión aguda o potencial de un tejido o descrita en términos de este tipo de lesiones” (Wall y Melzack, 1999). El organismo reacciona frente a un estímulo doloroso (nociceptivo) con una reacción compleja en la que intervienen componentes discriminadores sensoriales, cognitivos, afectivos, autónomos y motores. Mientras que el dolor agudo constituye una reacción protectora fisiológica y tiene una importancia vital para la supervivencia del individuo, el dolor crónico no tiene ninguna función biológica clara. El dolor nociceptivo se desencadena a través de estímulos nóxicos, como calor, estimulación mecánica, protones o frío, en órganos sensoriales de umbral alto especializados, los nociceptores, y es transmitido en forma de actividad eléctrica al asta posterior de la médula espinal a través de fibras C no mielinizadas o fibras A poco mielinizadas. Para ello, los nociceptores están dotados de receptores específicos y canales de iones (Scholz y Woolf, 2002).
El tejido herido o lesionado, las inflamaciones o las células tumorales pueden ser señales para los nociceptores, conduciendo a la liberación de mediadores químicos de células inflamatorias, vasos sanguíneos y terminales aferentes, que bien producen por sí mismos una activación de los nociceptores (por ejemplo a través de la bradiquinina), bien modifican el comportamiento estímulo-respuesta de las fibras nerviosas aferentes, por ejemplo mediante la reducción del umbral de activación (por ejemplo a través de prostaglandinas, interleuquinas, NGF), provocando así una sensibilización de los nociceptores (Scholz y Woolf, 2002).
La intensidad del dolor viene determinada por la cantidad de impulsos por unidad de tiempo. En caso de una estimulación nociceptiva periférica, los componentes de respuesta sináptica rápida (5 - 20 mseg) y las respuestas reflejas monosinápticas están mediados principalmente por los receptores de AMPA y cainato, mientras que los receptores de NMDA y de glutamato metabotrópicos intervienen de forma especial en los componentes de respuesta tardíos más persistentes (20 - 150 mseg) y con mediación polisináptica (Tölle, 1997).
La liberación de glutamato en el asta posterior de la médula espinal desempeña un papel decisivo en el origen de dolores crónicos (Baranauskas y Nitri, 1998; Zhuo, 2001). La liberación de glutamato conduce a la activación de los receptores de glutamato (AMPA, cainato, mGlu-R, NMDA). Por consiguiente, las proteínas que intervienen en la liberación de glutamato son un objetivo interesante para la investigación del dolor.
El glutamato es uno de los neurotransmisores excitatorios más importantes del sistema nervioso de los vertebrados. El aminoácido no esencial glutamato no puede superar la barrera hematoencefálica y, por ello, se sintetiza en el cerebro a partir de glucosa y muchos otros precursores.
La enzima glutaminasa activada por fosfato (PAG) cataliza la formación de glutamato en las terminaciones nerviosas excitatorias a partir de glutamina. El transportador vesicular de glutamato (VGLUT) empaqueta el glutamato en vesículas y, después de la llegada de un potencial de acción despolarizadora por la afluencia de calcio, libera el glutamato de las vesículas en la fisura sináptica. Desde la fisura sináptica, el glutamato es transportado en parte a través de un transportador de membrana plasmática para aminoácidos excitatorios (EAATs) de vuelta a los terminales excitatorios, donde de nuevo es empaquetado en vesículas.
Por consiguiente, en el transporte de glutamato intervienen proteínas transportadoras de 2 superfamilias: transportadores de membrana plasmática y el transportador vesicular de membrana (Disbrow y col., 1982; Shioi y col., 1989; Tabb y col., 1992).
Se han identificado tres transportadores vesiculares de glutamato, el VGLUT1 (SLC17A6), el VGLUT2 (SLC17A7) y el VGLUT3 (SLC17A8) como miembros de la familia de los transportadores SLC-17 (transportadores vesiculares de glutamato/fosfato de tipo I), que median en el transporte de aniones orgánicos y que en primer lugar se identificaron como transportadores de fosfato dependientes de Na+). El VGLUT1, el VGLUT2 y el VGLUT3 se denominan en conjunto como VGLUT. Las proteínas de la familia SLV17 consisten en proteínas transmembrana de varios intervalos con 6 a 12 dominios transmembrana hipotéticos, apareciendo los tres transportadores de glutamato arriba mencionados como subfamlia de la familia SLC17. Las secuencias de aminoácidos de los tres VGLUT arriba mencionados presentan una altísima homología entre sí (Takamori y col., 2002). La secuencia de ADNc del VGLUT2 humano se encuentra en los bancos de datos bajo el número de acceso de banco de genes NM_020346. La secuencia de aminoácidos del VGLUT2 humano se encuentra en los bancos de datos bajo el número de acceso NP_065079. La secuencia de ADNc del VGLUT2 de rata se encuentra en los bancos de datos bajo el número de acceso NM_053427. La secuencia de aminoácidos de VGLUT2 de rata se encuentra en los bancos de datos bajo el número de acceso NP_445879. La secuencia de ADNc del VGLUT2 de ratón se encuentra en los bancos de datos bajo el número de acceso BC038375. La secuencia de aminoácidos de VGLUT2 de ratón se encuentra en los bancos de datos bajo el número de acceso AAH38375.
Las capas corticales del cerebro presentan un fuerte nivel de expresión de ARNm de VGLUT1, mientras que el ARNm de VGLUT2 se puede detectar principalmente en la capa IV de la corteza. La expresión de VGLUT3 se localiza, por ejemplo, en las células inhibidoras en la capa II de la corteza parietal o en las interneuronas GAD-positivas del estrato radiado de CA1-CA3 del hipocampo. Además, VGLUT1 y VGLUT2 sólo se han podido detectar en las terminaciones nerviosas, mientras que VGLUT3 no sólo se ha detectado en las vesículas sinápticas, sino también en estructuras vesiculares de astrocitos y dendritas neuronales (Fremeau y col., 2002).
El VGLUT1 y el VGLUT2 se expresan en dos poblaciones independientes en el ganglio espinal, presentando una tercera subpoblación una coexpresión de VGLUT1 y VGLUT2. El ARNm de VGLUT2 es expresado principalmente por neuronas DRG pequeñas y medianas. En cambio, el ARNm de VGLUT1 es expresado principalmente por neuronas DRG medianas y grandes (ganglio de la raíz dorsal). Esporádicamente también se encuentran neuronas que expresan ARNm de VGLUT3 en el ganglio espinal (Oliveira y col., 2003; Tood y col., 2003).
Tanto el VGLUT1 como el VGLUT2 se pueden detectar a nivel proteínico en la sustancia gris de la médula espinal (Varoqui y col., 2002). La dominancia del VGLUT2 en el asta posterior superficial indica un papel destacado en la transmisión del dolor. La dominancia de VGLUT1 en el asta posterior profunda indica un papel en la propiocepción. Por consiguiente, principalmente el VGLUT2, pero también el VGLUT1, constituyen un objetivo para la investigación del dolor (Varoqui y col., 2002).
El tratamiento eficaz del dolor es uno de los grandes retos de la medicina molecular. El dolor agudo y transitorio es una importante señal del cuerpo para preservar a las personas contra daños graves producidos por el entorno o por sobrecarga del cuerpo. En cambio, el dolor crónico, que dura más que la causa del dolor y que el tiempo previsible de curación, no tiene ninguna función biológica conocida y afecta a cientos de millones de personas en todo el mundo. Sólo en Alemania, alrededor de 7,5 millones de personas padecen dolor crónico. Por desgracia, el tratamiento farmacológico del dolor crónico todavía es insatisfactorio y, en consecuencia, sigue siendo un reto para la investigación médica actual. A menudo, los analgésicos existentes en la actualidad no son suficientemente eficaces y, en parte, tienen graves efectos secundarios.
Debido a su función y su perfil de expresión, las proteínas de VGLUT en general...
Reivindicaciones:
1. Moléculas de ARNsi específicas de VGLUT con una secuencia seleccionada entre
2. Célula aislada que contiene al menos una molécula de ARNsi según la reivindicación 1, a excepción de células madre embrionarias humanas.
3. Medicamento que contiene al menos una molécula de ARNsi según la
**(Ver fórmula)**
5
reivindicación 1 y/o al menos una célula según la reivindicación 2 y en 10 caso dado también sustancias auxiliares y/o aditivos adecuados.
4. Sistema de diagnóstico que contiene al menos una molécula de ARNsi según la reivindicación 1 y/o al menos una célula según la reivindicación 2 y en caso dado también aditivos adecuados.
5. Utilización de al menos una molécula de ARN-si según la reivindicación 1
15 y/o al menos una célula según la reivindicación 2 para la producción de un medicamento o un analgésico para el tratamiento del dolor, en particular del dolor crónico, alodinia táctil, dolor provocado térmicamente y/o dolor inflamatorio.
6. Utilización de al menos una molécula de ARNsi según la reivindicación 1 20 y/o al menos una célula según la reivindicación 2 para la producción de un medicamento para el tratamiento de la incontinencia urinaria, síntomas neurógenos de la vejiga, prurito, tumores, inflamaciones, asma.
7. Molécula de ARNsi según la reivindicación 1 y/o célula según la
reivindicación 2 para su utilización en la terapia genética, preferentemente 5 en la terapia genética in vivo o in vitro.
8. Procedimiento in vitro para la inhibición de la expresión de al menos un miembro de la familia de los VGLUT en una célula, caracterizado porque se introduce una molécula de ARNsi según la reivindicación 1 en dicha célula.
10 9. Procedimiento según la reivindicación 8, caracterizado porque la molécula de ARNsi se incluye en estructuras micelares, preferentemente liposomas.
10. Procedimiento según una de las reivindicaciones 8 ó 9, caracterizado porque la molécula de ARNsi se incluye en cápsides virales naturales o
15 en cápsides producidas por métodos químicos o enzimáticos o en estructuras derivadas de éstas.
Patentes similares o relacionadas:
INHIBIDORES SELECTIVOS DE LA EXPRESIÓN Y/O LA ACTIVIDAD DEL RECEPTOR CB2 PARA EL TRATAMIENTO DE LA OBESIDAD Y LOS TRASTORNOS RELACIONADOS CON LA OBESIDAD, del 13 de Febrero de 2012, de INSTITUT NATIONAL DE LA SANTE ET DE LA RECHERCHE MEDICALE (INSERM): Inhibidor selectivo de la expresión del receptor CB2 seleccionado de entre el grupo constituido por moléculas de ADN o ARN antisentido, ARN inhibidores pequeños (ARNip) […]
CARBOHIDRATO U OLIGONUCLEOTIDOS MODIFICADOS EN POSICIÓN 2' QUE TIENEN ENLACES INTERNUCLEOSIDICOS ALTERNOS, del 7 de Diciembre de 2011, de ISIS PHARMACEUTICALS, INC.: Un compuesto que comprende una pluralidad de nucleósidos modificados en posición 2' unidos covalentemente que tienen la fórmula: en la que : cada […]
SIRNA Y SHRNA PARA LA ELABORACION DE MEDICAMENTOS FRENTE A LA PRESIONINTRAOCULAR ELEVADA, del 20 de Junio de 2011, de UNIVERSIDAD COMPLUTENSE DE MADRID: siRNA y shRNA para la elaboración de medicamentos frente a la presión intraocular elevada. La presente invención proporciona moléculas de siRNA y de shRNA para […]
 OLIGORRIBONUCLEÓTIDOS PARA INFLUIR EN EL CRECIMIENTO DEL CABELLO, del 11 de Mayo de 2011, de BEIERSDORF AG: Oligorribonucleótidos, que inducen la degradación del mRNA de estructuras, que influyen de forma estimuladora en el ciclo del cabello, dichas estructuras forman parte […]
OLIGORRIBONUCLEÓTIDOS PARA INFLUIR EN EL CRECIMIENTO DEL CABELLO, del 11 de Mayo de 2011, de BEIERSDORF AG: Oligorribonucleótidos, que inducen la degradación del mRNA de estructuras, que influyen de forma estimuladora en el ciclo del cabello, dichas estructuras forman parte […]
 MODULACIÓN DE NIVELES DE EXPRESIÓN DE TRPV, del 11 de Mayo de 2011, de SYLENTIS S.A.U: Uso de una dosis farmacéuticamente eficaz de ANsi dirigido frente a TRPV1 en la preparación de un fármaco para su uso en el tratamiento de un estado ocular caracterizado […]
MODULACIÓN DE NIVELES DE EXPRESIÓN DE TRPV, del 11 de Mayo de 2011, de SYLENTIS S.A.U: Uso de una dosis farmacéuticamente eficaz de ANsi dirigido frente a TRPV1 en la preparación de un fármaco para su uso en el tratamiento de un estado ocular caracterizado […]
COMPOSICIONES Y METODOS PARA INHIBICION DE ANGIOGENESIS POR ARN-SI, del 10 de Junio de 2010, de THE TRUSTEES OF THE UNIVERSITY OF PENNSYLVANIA: Un ácido ribonucleico de interferencia corto aislado (ARNsi) que comprende una cadena de ARN sentido de aproximadamente 19 a aproximadamente 25 nucleótidos […]
 ENZIMAS DE ADN ACTIVAS Y ESTABLES, del 24 de Mayo de 2010, de GRUNENTHAL GMBH: Enzima de ADN de tipo 10-23 que incluye, desde el extremo 5'' hacia el extremo 3'', un primer brazo de reconocimiento de sustrato ("sección I"), una […]
ENZIMAS DE ADN ACTIVAS Y ESTABLES, del 24 de Mayo de 2010, de GRUNENTHAL GMBH: Enzima de ADN de tipo 10-23 que incluye, desde el extremo 5'' hacia el extremo 3'', un primer brazo de reconocimiento de sustrato ("sección I"), una […]
Método para analizar ácido nucleico molde, método para analizar sustancia objetivo, kit de análisis para ácido nucleico molde o sustancia objetivo y analizador para ácido nucleico molde o sustancia objetivo, del 29 de Julio de 2020, de Kabushiki Kaisha DNAFORM: Un método para analizar un ácido nucleico molde, que comprende las etapas de: fraccionar una muestra que comprende un ácido nucleico molde […]