Composiciones de proteínas de células cutáneas fetales para el tratamiento de afecciones, trastornos o enfermedades de la piel y métodos para prepararlas y usarlas.
Una composición para usar en el tratamiento de la vulvodinia que comprende una o más proteínas de célulascutáneas fetales y un vehículo aceptable,
en la que dichas células cutáneas fetales se obtienen de una o máscélulas fibroblastos fetales humanas después de lisis, en la que la una o más células fibroblastos fetales humanas sehan obtenido a las 12-16 semanas de gestación.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/IB2005/004182.
Solicitante: Neogyn, Inc.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 101 West Big Beaver Road, Suite 845, Columbia Center II Troy, MI 48084 ESTADOS UNIDOS DE AMERICA.
Inventor/es: LAURENT-APPLEGATE,LEO, HOHLFELD,PATRICK.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K35/36 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 35/00 Preparaciones medicinales que contienen sustancias de constitución indeterminada o sus productos de reacción. › Piel; Sistema piloso; Uñas; Glándulas sebáceas; Cerumen; Epidermis; Células epiteliales; Queratinocitos; Células de Langerhans; Células del ectodermo (islotes de Langerhans A61K 35/39).
PDF original: ES-2400576_T3.pdf
Fragmento de la descripción:
Composiciones de proteínas de células cutáneas fetales para el tratamiento de afecciones, trastornos o enfermedades de la piel y métodos para prepararlas y usarlas Campo de la invención La presente invención se refiere a composiciones para usar en el tratamiento de la vulvodinia. Las composiciones contienen proteínas de células cutáneas fetales obtenidas de células fibroblastos fetales humanas después de lisis celular inducida, en las que las células fibroblastos fetales humanas se han obtenido a las 12-16 semanas de gestación.
Antecedentes de la invención Hasta una determinada edad gestacional, la piel fetal cura sin formación de cicatriz o solo con cicatriz muy pequeña (llamado también reparación sin cicatriz o curación sin cicatriz) después de herida (Dang C. et al., Clin. Plast. Surg. 2003: 30, 13-23) , que indica una orquestación (regulación) óptima (equilibrada) de una respuesta celular coordinada en la piel fetal durante un periodo de tiempo de gestación específico. Sin embargo, la piel de los recién nacidos, jóvenes y adultos (que corresponde a piel no fetal) cura con formación de cicatrices después de sufrir una herida, lo que indica que la respuesta celular coordinada en la piel no fetal es menos óptima o menos equilibrada que en la piel fetal.
En animales grandes y seres humanos, la reparación sin cicatriz después de sufrir una herida se produce hasta mitad de gestación al principio del tercer trimestre. Alrededor de este periodo de tiempo, la curación de heridas fetales pasa de producirse sin cicatriz a la curación con formación de cicatriz tras herida de la piel fetal. En la piel, la reparación sin cicatriz en el feto se caracteriza por la regeneración de una dermis organizada con apéndices normales (folículo piloso, glándula sebácea, glándula apocrina) . Se cree que la curación sin cicatriz es, al menos en parte, el resultado de una falta relativa de inflamación, lo que corresponde a una respuesta pro- y antiinflamatoria equilibrada (óptima) después de sufrir una herida.
La capacidad para curar sin formación de cicatriz parece que es intrínseca de la piel fetal y probablemente es el resultado de la interacción orquestada de muchas proteínas reguladoras incluyendo citoquinas. Esto se ilustra a continuación.
Las heridas fetales sin cicatriz curan con poca inflamación, y el inicio de la cicatrización durante la reparación fetal se correlaciona con la presencia de un infiltrado inflamatorio agudo (G. P. Yang et al. Wound Rep. Reg. 2003; 11: 411418) . Además, la introducción de inflamación en heridas que normalmente curan sin cicatriz produce un aumento de la deposición de colágeno y cicatrización. Esto sugiere una función importante de la inflamación durante la formación de cicatriz. Cuando el sistema inmunitario se desarrolla y aumenta su respuesta inflamatoria resultante, se produce la formación de cicatriz en el sitio de la reparación. La síntesis y remodelado de la matriz extracelular (ECM) por los fibroblastos de la herida es probablemente el determinante principal de la arquitectura dérmica después de reparación. Las diferencias entre la cicatrización y la arquitectura de colágeno sin cicatriz se pueden explicar parcialmente por diferencias fenotípicas entre los fibroblastos adultos y fetales.
Los fibroblastos fetales y adultos presentan diferencias en las tasas sintéticas de colágeno, ácido hialurónico (HA) y otros componentes de la ECM. In vitro, los fibroblastos fetales sintetizan más colágeno de tipo III y IV que sus homólogos adultos. Los fibroblastos fetales pueden proliferar (o multiplicarse) y sintetizar colágeno simultáneamente. Los fibroblastos fetales tienen una mayor capacidad para migrar en los geles de colágeno que los fibroblastos de adultos. El aumento de la densidad celular disminuye la producción de HA en el adulto, pero no afecta a la síntesis de HA de los fibroblastos fetales.
Las isoformas del factor de crecimiento transformante (TGF) TGF-beta 1 y TGF-beta 2 (ambas isoformas son factores de crecimiento; los factores de crecimiento pertenecen a la familia de las proteínas citoquinas) tienen funciones profibróticas (inducen fibrosis) y promueven la formación de cicatriz. Su expresión es mayor en la curación de heridas normal, y la administración exógena de este factor de crecimiento a las heridas de adultos aumenta la acumulación de colágeno, proteoglicanos y células inflamatorias. El TGF-beta-1 también disminuye las metaloproteasas de la matriz y aumenta los inhibidores endógenos de la expresión de metaloproteasas de la matriz, lo cual puede favorecer la acumulación de colágeno y cicatrización. Además, el tratamiento de heridas en ratas adultas con anticuerpos neutralizantes contra TGF-beta 1 y TGF-beta 2 reduce la formación de cicatriz. También se ha descrito que el tratamiento con fibromodulina, un modulador de TGF-beta reduce la cicatrización postnatal.
Además, parece que la proporción relativa de isoformas de TGF-beta y no la cantidad absoluta de una cualquiera de las isoformas, determina el resultado de la reparación de la herida. En las heridas fetales sin cicatriz, la expresión del TGF-beta 3 (isoforma de TGF-beta) es mayor, mientras que la expresión de TGF-beta-1 no cambia. A la inversa, la expresión de TGF-beta-1 es mayor y la de TGF-beta 3 es menor en las heridas fetales que cicatrizan. El tratamiento de heridas en ratas adultas con TGF-beta 3 exógeno reduce la formación de cicatriz. Estos datos sugieren que la relación de TGF-beta 3 a TGF-beta 1 puede determinar si la arquitectura de la piel se restablece o forma cicatriz después de la herida.
Las interleuquinas (pertenecientes a la familia de proteínas citoquinas) regulan la quimiotaxia y activación de las células inflamatorias. La interleuquina-6 (IL-6) estimula la quimiotaxia de monocitos y la activación de macrófagos mientras que la interleuquina-8 (IL-8) atrae neutrófilos y estimula la neovascularización. La herida estimula un aumento rápido de IL-6 e IL-8, que persiste en el adulto pero desaparece rápidamente en el feto. El factor de crecimiento derivado de plaquetas (PDGF, factor de crecimiento que pertenece a la familia de proteínas citoquinas) induce la producción de IL-6 de los fibroblastos de adulto. A su vez, la adición de IL-6 a heridas fetales produce la cicatrización temprana. En los fibroblastos fetales, comparados con los de adultos, la expresión de IL-6 e IL-8 de los fibroblastos es más baja en el valor inicial y después de estimulación con PDGF. La interleuquina-10 (IL-10) tiene una función antiinflamatoria al disminuir la producción de IL-6 e IL-8. Por ejemplo, se ha mostrado en el ratón adulto, que las heridas tratadas con un vector adenovírico que expresa en exceso IL-10 presentan menor inflamación y curación sin cicatriz.
El PDGF y la familia de factores de crecimiento de fibroblastos (FGF) son citoquinas profibróticas adicionales. El PDGF, un mitógeno potente y quimioactractor para fibroblastos, tiene una expresión prolongada durante la formación de cicatriz, pero desaparece rápidamente en las heridas fetales. Por ejemplo, se ha mostrado que el tratamiento de heridas en conejos fetales con PDGF induce un notable aumento de la inflamación aguda, reclutamiento de fibroblastos, y deposición de colágeno. La familia de FGF de citoquinas, incluyendo el factor de crecimiento de queratinocitos-1 y 2 (factores de crecimiento que pertenecen a la familia de proteínas citoquinas) tiene una mayor expresión con el aumento de la edad gestacional en la piel fetal y durante la formación de heridas en el adulto.
En cambio, un mitógeno para células endoteliales, el factor de crecimiento endotelial vascular (VEGF, factor de crecimiento que pertenece a la familia de proteínas citoquinas) , aumenta al doble en heridas sin cicatriz, mientras que su expresión no cambia en heridas fetales que cicatrizan. Por lo tanto, un mayor estímulo de la angiogénesis y la permeabilidad vascular puede ayudar a la rápida curación de las heridas fetales.
Los mecanismos exactos de la curación sin cicatriz siguen siendo desconocidos, a pesar del gran aumento del conocimiento adquirido en la última década. La reparación de heridas fetales sin cicatriz es un procedimiento estrechamente regulado (orquestado) que implica diferentes mediadores celulares tales como citoquinas y otras proteínas.
Las terapias actuales no proporcionan un mecanismo para la curación sin cicatriz. Por lo tanto, un objeto de la presente invención es proporcionar composiciones y métodos para usar las composiciones descritas para tratar sujetos que padecen una afección, trastorno o enfermedad de la piel, y que necesiten una curación sin cicatriz y/o necesiten una respuesta equilibrada para la inflamación cutánea.... [Seguir leyendo]
Reivindicaciones:
1. Una composición para usar en el tratamiento de la vulvodinia que comprende una o más proteínas de células cutáneas fetales y un vehículo aceptable, en la que dichas células cutáneas fetales se obtienen de una o más células fibroblastos fetales humanas después de lisis, en la que la una o más células fibroblastos fetales humanas se han obtenido a las 12-16 semanas de gestación.
2. Uso de una composición de la reivindicación 1, en la fabricación de un medicamento para tratar la vulvodinia.
3. La composición para usar según la reivindicación 1 o el uso de la reivindicación 2, en la que dichos uno o más fibroblastos fetales se han obtenido a partir de tejido cutáneo fetal entero o fragmentos de tejido cutáneo fetal.
4. La composición para usar según la reivindicación 1 o el uso de la reivindicación 2, en la que dichos uno o más fibroblastos fetales se inmortalizan.
5. La composición para usar según la reivindicación 1 o el uso de la reivindicación 2, en la que dichos uno o más fibroblastos fetales se obtienen de un banco de células o de una línea celular.
6. La composición para usar según la reivindicación 1 o el uso de la reivindicación 2, en la que dichas una o más proteínas de fibroblastos fetales se purifican.
7. La composición para usar según la reivindicación 1 o el uso de la reivindicación 2, en la que dicho lisato comprende uno o más componentes celulares.
8. La composición para usar según la reivindicación 1 o el uso de la reivindicación 2, en la que dichas una o más proteínas de fibroblastos fetales comprenden una o más citoquinas, enzimas, hormonas, proteínas estructurales de la matriz extracelular, neuropéptidos o antagonistas de neuropéptidos.
9. La composición para usar según el uso de la reivindicación 8, en la que dichas citoquinas comprenden factores de crecimiento, interleuquinas, linfoquinas, monoquinas, interferones, factores estimuladores de colonias o quimioquinas o combinaciones y mezclas de los mismos.
10. La composición para usar según la reivindicación 1 o el uso de la reivindicación 2, que además comprende analgésicos, anestésicos, agentes antiinflamatorios, agentes antihistamínicos, antioxidantes, antiirritantes, agentes antimicrobianos, agentes antibacterianos, agentes antifúngicos, conservantes, agentes estabilizantes de proteínas, inhibidores de proteasa, agentes protectores de la piel, protectores solares o combinaciones y mezclas de los mismos.
11. La composición para usar según la reivindicación 1 o el uso de la reivindicación 2, en la que dicha composición es adecuada para la administración tópica, en mucosa o vaginal.
12. La composición para usar según la reivindicación 1 o el uso de la reivindicación 2, en la que dicha composición es una pomada, loción, crema, espuma, mousse, pulverizador, aerosol, emulsión, nanoemulsión, máscara, microemulsión, gel, hidrogel, disolución, esponja o dispersión.
13. La composición para usar según la reivindicación 1 o el uso de la reivindicación 2, en la que dicha composición es una emulsión de agua en aceite o de aceite en agua o la composición es una crema basada en emulsión de agua en aceite o de aceite en agua.
14. La composición para usar según la reivindicación 1 o el uso de la reivindicación 2, en la que dichas una o más proteínas de fibroblastos fetales se incorporan en dicha composición en una concentración entre 0, 001 y 95%, preferiblemente entre 0, 01% y 5%, más preferiblemente entre 0, 05% y 0, 25%.
15. La composición para usar según la reivindicación 1, en la que dicha lisis celular es inducida y no es espontánea.
16. La composición para usar según la reivindicación 1, en la que dicha lisis celular se lleva a cabo de forma mecánica, física o química, o se lleva a cabo mediante uno o más ciclos de congelación-descongelación.
17. La composición para usar según la reivindicación 1, en la que dicha lisis celular se lleva a cabo con entre 100 y
60.000.000 fibroblastos fetales suspendidos en 1 ml de un sistema acuoso, preferiblemente entre 10.000.000 y
20.000.00 células cutáneas fetales suspendidas en 1 ml de un sistema acuoso.
18. La composición para usar según la reivindicación 17, en la que dicho sistema acuoso es un sistema de tampón fisiológico o un sistema de disolución salina tamponada con fosfato.
19. La composición para usar según la reivindicación 17, en la que dicho sistema acuoso comprende además uno o más compuestos químicos estabilizantes de proteínas, inhibidores de proteasa, agentes antimicrobianos, agentes antibacterianos, antioxidantes, conservantes o combinaciones y mezclas de los mismos.
20. La composición para usar según la reivindicación 1 o el uso de la reivindicación 2, en la que dicha vulvodinia es la vestibulitis vulvar o el síndrome de vestibulitis vulvar.
21. La composición para usar o el uso según la reivindicación 20, en la que el tratamiento de la vulvodinia comprende además el uso de corticoesteroides, estrógeno, progesterona, lidocaína, hidrocloruro de pramoxina, capsaicina, isotretinoina, interferón-a, interferón-1, interferón-y, dapsona, aciclovir, antidepresivos tricíclicos o combinaciones o mezclas de los mismos.
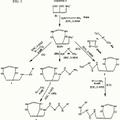
Figura 1 Figura 2 Figura 3 Figura 4
ANTES DESPUÉS
Figura 5
ANTES DESPUÉS
Figura 6
ANTES DESPUÉS
Figura 7 7
ANTES DESPUÉS
Figura 8
ANTES DESPUÉS
Figura 9
Patentes similares o relacionadas:
Una terapia de combinación para un injerto estable y a largo plazo usando protocolos específicos para el agotamiento de los linfocitos T/B, del 20 de Mayo de 2020, de YEDA RESEARCH AND DEVELOPMENT CO. LTD.: Una dosis de células hematopoyéticas inmaduras de linfocitos T agotados, en donde dichas células hematopoyéticas inmaduras de linfocitos T agotados comprenden menos de 5 x 105 […]
Complejo proteomelánico bioasimilable, preparación y usos, del 11 de Septiembre de 2019, de Carlini, Rosanna: Complejo proteomelánico bioasimilable, que comprende al menos un extracto proteico, soluble o parcialmente soluble y melanina, siendo dicho complejo proteomelánico bioactivo […]
Terapia combinada para el tratamiento de pacientes con trastornos neurológicos e infarto cerebral, del 11 de Septiembre de 2019, de Moleac Pte Ltd: Una composición para uso en el tratamiento de infarto cerebral, infarto cardiaco, una enfermedad neurodegenerativa, traumatismo cerebral y traumatismo del sistema nervioso, […]
Dispositivo de preparación de suspensión celular, del 7 de Agosto de 2019, de Avita Medical Ltd: Un aparato para desarrollar de forma perioperatoria a un paciente una suspensión celular de una muestra de tejido de piel, y para aplicar inmediatamente […]
Composición farmacéutica que comprende una suspensión de células totales obtenida de folículo piloso y factores de crecimiento derivados de plasma para tratar la alopecia, del 7 de Agosto de 2019, de GORROCHATEGUI BARRUETA, ALBERTO: Método de obtención de una composición que comprende una suspensión celular que comprende células progenitoras del pelo (HPC) de un sujeto humano y factores de crecimiento […]
 Armazones de colágeno estabilizados y esterilizados con aditivos activos unidos, del 31 de Julio de 2019, de Synovis Orthopedic and Woundcare, Inc: Un proceso para fabricar un bioimplante esterilizado químicamente que comprende un tejido biológico y heparina, en el que la heparina se conjuga covalentemente […]
Armazones de colágeno estabilizados y esterilizados con aditivos activos unidos, del 31 de Julio de 2019, de Synovis Orthopedic and Woundcare, Inc: Un proceso para fabricar un bioimplante esterilizado químicamente que comprende un tejido biológico y heparina, en el que la heparina se conjuga covalentemente […]
Composición para regeneración de tejidos, del 17 de Julio de 2019, de ACELL, INC.: Una composición desvitalizada regenerativa de tejido, que comprende membrana basal epitelial intacta, y al menos la porción subyacente […]
Método de esterilización de dermis, del 15 de Mayo de 2019, de LIFECELL CORPORATION: Un procedimiento para descelularizar un tejido, que comprende: aplicar una presión de al menos 200 MPa a un líquido que contiene una muestra de tejido que comprende […]