COMPOSICIONES Y MÉTODOS PARA LA UTILIZACIÓN TERAPÉUTICA DE UNA SECUENCIA ASOCIADA CON EL GEN ATONAL.
Una secuencia de aminoácidos o una secuencia de ácido nucleico asociada con atonal para estimular el crecimiento terapéutico de las células mecanorreceptoras del oído interno en un animal,
donde dicha secuencia de aminoácidos asociada con atonal tiene, o dicha secuencia de ácido nucleico asociada con atonal codifica, un polipéptido que tiene al menos un 80% de identidad con la secuencia AANARERRRMHGLNHAFDQLR
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2000/015410.
Solicitante: BAYLOR COLLEGE OF MEDICINE.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: ONE BAYLOR PLAZA HOUSTON, TX 77030 ESTADOS UNIDOS DE AMERICA.
Inventor/es: ZOGHBI,Huda,Y. , BELLEN,Hugo , BIRMINGHAM,Nessan , HASSAN,Bassem , BEN-ARIE,Nissim,Dept. of Cell and Animal Biology.
Fecha de Publicación: .
Fecha Solicitud PCT: 1 de Junio de 2000.
Clasificación PCT:
- A61K38/00 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00).
Clasificación antigua:
- G01N FISICA. › G01 METROLOGIA; ENSAYOS. › INVESTIGACION O ANALISIS DE MATERIALES POR DETERMINACION DE SUS PROPIEDADES QUIMICAS O FISICAS (procedimientos de medida, de investigación o de análisis diferentes de los ensayos inmunológicos, en los que intervienen enzimas o microorganismos C12M, C12Q).
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Eslovenia, Finlandia, Rumania, Chipre, Lituania, Letonia, Ex República Yugoslava de Macedonia, Albania.
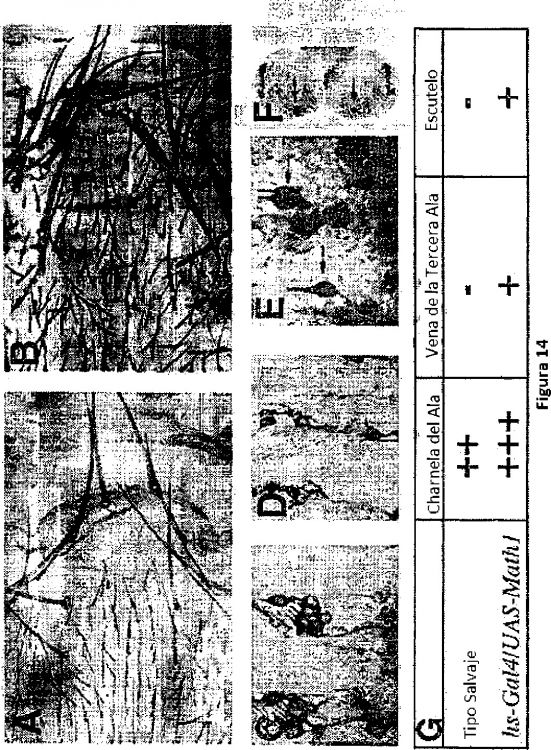
Fragmento de la descripción:
Composiciones y métodos para la utilización terapéutica de una secuencia asociada con el gen atonal.
Campo de la invención
La presente invención se refiere de manera general al campo del diagnóstico genético y de la terapia génica y, más particularmente, a la caracterización y utilización de una secuencia de ácido nucleico o de aminoácidos asociada a atonal.
Antecedentes de la invención
Un intrincado patrón de interacciones en y entre las células dirige el desarrollo secuencial de las neuronas desde la división de las células progenitoras neuroepiteliales. Múltiples señales extracelular e intracelulares modelan este proceso. Entre las señales intracelulares clave están los factores de transcripción, los cuales inducen la expresión de una cascada de genes. Una subclase de factores de transcripción, perteneciente a la familia de proteínas con un motivo hélice-bucle-hélice básico (bHLH), es expresada muy temprano cuando se toma la decisión de proliferar o de diferenciarse. Esta función es particularmente crucial, ya que mutaciones en estos genes al principio del desarrollo pueden eliminar estructuras neurales completas.
En Drosophila, el gen atonal (ato), que es homólogo a Math1, Math2, Hath1 y Hath2, codifica una proteína bHLH esencial para el desarrollo de los órganos cordotonales (órganos sensoriales encontrados en la pared corporal, en las articulaciones y en las antenas que funcionan en la propriocepción, en el equilibrio y en la audición) (Eberl, 1999; McIver, 1985; van Staaden y Römer, 1998). Los CHOs pueblan el sistema nervioso periférico (SNP) de la pared corporal y las articulaciones (tórax, abdomen, esternón, alas, patas) y de las antenas (Moulins, 1976), proporcionando a la mosca una información sensorial muy similar a la que proporcionan el tacto y los mecanorreceptores en los vertebrados (McIver, 1985; Moulins, 1976). Boyan (Boyan, 1993) propuso que, en el curso de la evolución, diferentes CHOs se especializan para oír en diferentes insectos. Esta hipótesis fue confirmada recientemente por van Staaden y Römer (1998). En Drosophila, los CHOs del órgano de Johnston, situados en el segundo segmento de las antenas, funcionan en la audición de campo cercano (Dreller y Kirschner, 1993; Eberl, 1999) y en la geotaxis negativa.
Durante el desarrollo, ato se expresa en un grupo de células progenitoras a partir de las cuales son seleccionadas las células fundadoras de los CHO (Jarman y col., 1993). Probablemente el mismo funciona regulando la expresión de los genes necesarios para la especificación y el desarrollo del linaje de los CHO, ya que codifica una proteína con un motivo hélice-bucle-hélice básico (bHLH) que forma dímeros con la proteína "Daughterless" y se une a secuencias "E-box", activando de este modo los genes (Jarman y col., 1993). La especificidad de los CHO está codificada por el dominio básico de ato, el cual se requiere para la unión al ADN en las proteínas con bHLH (Chien y col., 1996; Davis y col., 1990; Jarman y Ahmed, 1998; Vaessin y col., 1990). El ato es necesario y suficiente para la generación de CHOs en la mosca: la pérdida de la función ato da lugar a la pérdida de CHOs, mientras que la expresión ectópica de ato produce la formación de CHOs ectópicos (Jarman y col., 1993). Las moscas adultas que carecen de la función atonal no coordinan, no vuelan y tienen una audición deficiente. La sobreexpresión del gen atonal de la mosca puede generar nuevas neuronas cordotonales, indicando que el gen atonal es esencial y suficiente para el desarrollo de esta población neuronal.
En los vertebrados, durante la miogénesis y la neurogénesis, la especificación del destino celular requiere factores de transcripción con un motivo hélice-bucle-hélice básico (bHLH). Math1 (homólogo 1 del atonal de ratón, "mouse atonal homolog-1") es uno de tales factores, y se expresa en el cerebro posterior, en la médula espinal dorsal, en la capa germinal externa del cerebelo, en el intestino, en las articulaciones, en el oído y en las células de Merkel de la piel (que funcionan como mecanorreceptores) (Akazawa y col., 1995; Ben-Arie y col., 1996; Ben-Arie y col., 1997). Los ratones heterozigotos para una deleción dirigida de Math1 (Math+/-) son viables y tienen un aspecto normal, pero los ratones carentes (nulos) de Math1 (Math-/-) mueren poco después de nacer y carecen de neuronas granulares cerebelosas.
Math1 es uno de los homólogos de ato más próximo conocidos, con un 82% de similitud de aminoácidos en el dominio bHLH y un 100% de conservación del dominio básico que determina la especificidad de reconocimiento de la diana (Ben-Arie y col., 1996; Chien y col., 1996). Math1 se expresa de manera transitoria en el SNC comenzando el día 9 embrionario (E9) en la porción dorsal del tubo neural. Math1 se expresa también en el labio rómbico del cuarto ventrículo del cerebro, donde nacen los precursores de las células granulares cerebelosas en E13-15 (Alder y col., 1996). Después de la proliferación y la diferenciación, estas células progenitoras migran para formar la capa granular externa (EGL) del primordio cerebeloso (Hatten y Heintz, 1995). Las células de la EGL proliferantes continúan expresando Math1 durante las tres primeras semanas post-natales, hasta poco antes de migrar a su destino adulto final para generar la capa granular interna (IGL) del cerebelo (Akazawa y col., 1995; Ben-Arie y col., 1996). Otro grupo de células, una pequeña población de precursores neuronales de la médula espinal dorsal, expresan Math1 durante E10-E14 (Akazawa y col., 1995; Ben-Arie y col., 1996). Estas células precursoras expresan también las proteínas con el homeodominio LIM (LH2A y LH2B), marcadores de la clase D1 de las interneuronas comisurales (Lee y col., 1998). Helms y Johnson (1998) informaron que la expresión de lacZ bajo el control de elementos reguladores de Math1 reproducía los patrones de expresión de Math1 en el cerebelo y en la médula espinal en desarrollo, y demostraron que Math1 se expresaba en precursores que dan lugar a una subpoblación de interneuronas comisurales dorsales.
Con el fin de determinar la función in vivo de Math1, los inventores generaron ratones (Math1-/-) que carecían de la proteína MATH1. Esta mutación anulativa produce anormalidades cerebelosas importantes: la falta de proliferación y migración de las células granulares desde el labio rómbico en E14,5, y la ausencia de la EGL completa al nacimiento (Ben-Arie y col., 1997). No está claro si la agénesis de las neuronas granulares cerebelosas es debida un fallo de la especificación de los progenitores o a la incapacidad de las células para proliferar y/o diferenciarse. Los neonatos no pueden respirar y mueren poco después del nacimiento, pero no existen defectos macroscópicos en ninguno de los nervios craneales ni en los núcleos del tronco cerebral que puedan explicar el fallo respiratorio.
El hecho de que Math1 se exprese en el oído interno sugiere que la expresión de Math1 es necesaria para el desarrollo de los órganos auditivos o del equilibrio. El oído interno se forma inicialmente como un engrosamiento del ectodermo, denominado placoda ótica, entre los rombómeros 5 y 6 del cerebro posterior. La placoda ótica da lugar a neuronas del VIIIº nervio craneal y se invagina para dar lugar al otocisto, a partir del cual se desarrollará el oído interno. El oído interno maduro de los mamíferos contiene un órgano auditivo, la cóclea, y cinco órganos vestibulares: el utrículo, el sáculo y tres canales semicirculares. Los epitelios sensoriales de estos órganos constan de células pilosas mecanorreceptoras, células de soporte y terminaciones nerviosas. Las células pilosas sirven como mecanorreceptores para transformar las ondas sonoras y el movimiento de la cabeza en información auditiva y posicional. Las células pilosas y las células de soporte proceden ambas de una célula progenitora común y proliferan y se diferencian dentro del epitelio sensorial, con un número máximo de mitosis entre los días embrionarios 13 y 18 (E13-18) en los ratones. Aunque varios genes han sido implicados en el desarrollo del oído interno, tales como int2 (Mansour y col., 1993), pax2 (Torres y col., 1996) y Hmx3 (Wang y col., 1998), no se ha demostrado que se requiera ninguno de...
Reivindicaciones:
1. Una secuencia de aminoácidos o una secuencia de ácido nucleico asociada con atonal para estimular el crecimiento terapéutico de las células mecanorreceptoras del oído interno en un animal, donde dicha secuencia de aminoácidos asociada con atonal tiene, o dicha secuencia de ácido nucleico asociada con atonal codifica, un polipéptido que tiene al menos un 80% de identidad con la secuencia AANARERRRMHGLNHAFDQLR.
2. Una secuencia de aminoácidos o una secuencia de ácido nucleico asociada con atonal para la generación terapéutica de células pilosas del oído interno, donde dicha secuencia de aminoácidos asociada con atonal tiene, o dicha secuencia de ácido nucleico asociada con atonal codifica, un polipéptido que tiene al menos un 80% de identidad con la secuencia AANARERRRMHGLNHAFDQLR.
3. Una secuencia de aminoácidos o una secuencia de ácido nucleico asociada con atonal para el tratamiento de un animal con deterioro auditivo, donde dicha secuencia de aminoácidos asociada con atonal tiene, o dicha secuencia de ácido nucleico asociada con atonal codifica, un polipéptido que tiene al menos un 80% de identidad con la secuencia AANARERRRMHGLNHAFDQLR.
4. La secuencia de aminoácidos o de ácido nucleico de la reivindicación 2 ó 3 que es formulada para inyección en el oído de dicho animal.
5. Una secuencia de aminoácidos o una secuencia de ácido nucleico asociada con atonal para el tratamiento de un animal con un trastorno del equilibrio, donde dicha secuencia de aminoácidos asociada con atonal tiene, o dicha secuencia de ácido nucleico asociada con atonal codifica, un polipéptido que tiene al menos un 80% de identidad con la secuencia AANARERRRMHGLNHAFDQLR.
6. Una secuencia de aminoácidos o una secuencia de ácido nucleico asociada con atonal para el tratamiento de un animal con una enfermedad de las articulaciones, donde dicha secuencia de aminoácidos asociada con atonal tiene, o dicha secuencia de ácido nucleico asociada con atonal codifica, un polipéptido que tiene al menos un 80% de identidad con la secuencia AANARERRRMHGLNHAFDQLR.
7. La secuencia de aminoácidos o de ácido nucleico de la reivindicación 6 en la que dicha enfermedad de las articulaciones es osteoartritis.
8. La secuencia de aminoácidos o de ácido nucleico de cualquiera de las reivindicaciones 1 a 7, que es formulada para ser administrada mediante un vehículo para la administración.
9. La secuencia de aminoácidos o de ácido nucleico de la reivindicación 8, donde dicho vehículo para la administración es seleccionado de un vector adenovírico, un vector retrovírico, un vector vírico adenoasociado, un plásmido, un liposoma, un ácido nucleico, un péptido, un lípido, un carbohidrato y una combinación de los mismos.
10. La secuencia de aminoácidos o de ácido nucleico de la reivindicación 8, en la que dicho vehículo para la administración es un vector vírico o un vector no vírico.
11. La secuencia de aminoácidos o de ácido nucleico de la reivindicación 8, en la que dicho vehículo para la administración es una célula.
12. La secuencia de aminoácidos o de ácido nucleico de cualquiera de las reivindicaciones 1 a 11, que es la secuencia de aminoácidos o la secuencia de ácido nucleico de Math1 o Hath1.
13. La secuencia de aminoácidos o de ácido nucleico de cualquiera de las reivindicaciones 1 a 12, donde dicho animal es un humano.
14. La secuencia de aminoácidos o de ácido nucleico de cualquiera de las reivindicaciones 1 a 13, la cual está destinada para ser administrada después, antes o al mismo tiempo que la administración de una segunda secuencia de ácido nucleico que codifica otro producto génico terapéutico.
15. Una composición que contiene una secuencia de aminoácidos o una secuencia de ácido nucleico asociada con atonal en combinación con un vector vírico como vehículo para la administración, donde dicho vehículo para la administración tiene como resultado la administración de una cantidad terapéuticamente eficaz de dicha secuencia de aminoácidos asociada con atonal o de dicha secuencia de ácido nucleico asociada con atonal a una célula, y donde dicha secuencia de aminoácidos asociada con atonal es, o dicha secuencia de ácido nucleico asociada con atonal codifica, un polipéptido que contiene al menos un 80% de identidad con la secuencia AANARERRRMH- GLNHAFDQLR.
16. La composición de la reivindicación 15, en la que dicho vehículo para la administración es seleccionado de un vector adenovírico, un vector retrovírico, un vector adenoasociado o una combinación de los mismos.
17. Una composición que contiene:
18. La composición de la reivindicación 17, en la que una secuencia de ácido nucleico que codifica dicha secuencia de aminoácidos asociada con atonal está unida operativamente a una secuencia de ácido nucleico que codifica un dominio de unión al receptor de una toxina bacteriana.
19. La composición de la reivindicación 17, en la que una secuencia de ácido nucleico que codifica dicha secuencia de aminoácidos asociada con atonal está unida operativamente a una secuencia de ácido nucleico que codifica un dominio de transducción de una proteína.
20. Una proteína de fusión que comprende una secuencia de aminoácidos asociada con atonal o un fragmento de la misma y una secuencia de aminoácidos deseada, donde dicha secuencia de aminoácidos asociada con atonal es una secuencia de aminoácidos que tiene al menos un 80% de identidad con la secuencia AANARERRRMHGLNHAFDQLR.
21. Una secuencia de ácido nucleico que codifica la proteína de fusión de la reivindicación 20.
22. Utilización de una secuencia de aminoácidos o de una secuencia de ácido nucleico asociada con atonal para la fabricación de un medicamento para estimular el crecimiento terapéutico de las células mecanorreceptoras del oído interno de un animal, donde dicha secuencia de aminoácidos asociada con atonal tiene, o dicha secuencia de ácido nucleico asociada con atonal codifica, un polipéptido que tiene al menos un 80% de identidad con la secuencia AANARERRRMHGLNHAFDQLR.
23. Utilización de una secuencia de aminoácidos o de una secuencia de ácido nucleico asociada con atonal para la fabricación de un medicamento para la generación terapéutica de células pilosas del oído interno, donde dicha secuencia de aminoácidos asociada con atonal tiene, o dicha secuencia de ácido nucleico asociada con atonal codifica, un polipéptido que tiene al menos un 80% de identidad con la secuencia AANARERRRMHGLNHAFDQLR.
24. Utilización de una secuencia de aminoácidos o de una secuencia de ácido nucleico asociada con atonal para la fabricación de un medicamento para tratar a un animal del deterioro auditivo, donde dicha secuencia de aminoácidos asociada con atonal tiene, o dicha secuencia de ácido nucleico asociada con atonal codifica, un polipéptido que tiene al menos un 80% de identidad con la secuencia AANARERRRMHGLNHAFDQLR.
25. Utilización de una secuencia de aminoácidos o de una secuencia de ácido nucleico asociada con atonal para la fabricación de un medicamento para tratar a un animal de un trastorno del equilibrio, donde dicha secuencia de aminoácidos asociada con atonal tiene, o dicha secuencia de ácido nucleico asociada con atonal codifica, un polipéptido que tiene al menos un 80% de identidad con la secuencia AANARERRRMHGLNHAFDQLR.
26. Utilización de una secuencia de aminoácidos o de una secuencia de ácido nucleico asociada con atonal para la fabricación de un medicamento para tratar a un animal de una enfermedad de las articulaciones, donde dicha secuencia de aminoácidos asociada con atonal tiene, o dicha secuencia de ácido nucleico asociada con atonal codifica, un polipéptido que tiene al menos un 80% de identidad con la secuencia AANARERRRMHGLNHAFDQLR.
Patentes similares o relacionadas:
NANOPARTÍCULAS MULTIFUNCIONALES PARA TERAGNOSIS, del 30 de Julio de 2020, de UNIVERSIDAD DE GRANADA: Nanopartículas multifuncionales para teragnosis. La presente invención se refiere al campo de la medicina, en particular a nanopartículas (NP) […]
Modificación de FVIII dirigida al sitio, del 15 de Julio de 2020, de BAYER HEALTHCARE LLC: Un conjugado que tiene actividad procoagulante del factor VIII que comprende un factor VIII polipeptídico funcional con el dominio B eliminado que está mutado […]
Anticuerpos del OPGL, del 15 de Julio de 2020, de AMGEN FREMONT INC.: Un anticuerpo, que comprende una cadena pesada y una cadena ligera, donde: a) la cadena pesada comprende: 1) una secuencia de aminoácidos recogida […]
Formulaciones estables que contienen anticuerpos anti-PCSK9, del 15 de Julio de 2020, de AMGEN INC.: Una formulación estable que comprende un anticuerpo monoclonal que se une específicamente a PCSK9, en donde PCSK9 comprende los aminoácidos de la SEQ ID NO: […]
Polipéptidos de unión a IL-17A, del 15 de Julio de 2020, de AFFIBODY AB: Polipéptido de unión a IL-17A, que comprende un motivo de unión BM a IL-17A, cuyo motivo consiste en una secuencia de aminoácidos seleccionada […]
Composición a base de hidroxiapatita en polvo para el tratamiento del linfoma B o T, del 1 de Julio de 2020, de URODELIA: Composición para uso como autovacuna antitumoral para el tratamiento de linfomas B o T en un sujeto, que comprende un polvo de hidroxiapatita y/o de […]
Tratamiento de disfunción eréctil y otras indicaciones, del 1 de Julio de 2020, de STRATEGIC SCIENCE & TECHNOLOGIES, LLC: Una composición para su uso en un método de tratamiento de la disfunción sexual en un sujeto, preferiblemente un sujeto humano, comprendiendo la composición: […]
Péptido con eficacia antiobesidad y antidiabética y uso del mismo, del 17 de Junio de 2020, de CAREGEN CO., LTD: Un péptido que consiste en la secuencia de aminoácidos de SEQ ID NO: 1 o SEQ ID NO: 2.