COMPOSICIONES Y METODOS PARA INMUNIDAD MEJORADA DE CELULAS NEOPLASICAS IN VIVO.
ESTA INVENCION PROPORCIONA UN METODO DE PREVENCION O REDUCCION DE LA SEVERIDAD DE UN CANCER EN UN SUJETO POR MEDIO DE LA ESTIMULACION DE LA RESPUESTA INMUNOLOGICA DEL SUJETO CONTRA EL CANCER.
LA INVENCION PROPORCIONA, POR EJEMPLO, UN METODO DE ESTIMULACION DE LA RESPUESTA INMUNOLOGICA EN UN SUJETO POR MEDIO DE LA ADMINISTRACION AL SUJETO DE CELULAS TUMOROSAS QUE SON ESENCIALMENTE SIMILARES A LAS CELULAS CANCEROSAS DEL SUJETO Y QUE ESTAN MODIFICADAS GENETICAMENTE PARA REDUCIR O INHIBIR LA EXPRESION DE UNO O MAS AGENTES INMUNORREDUCTORES. ADEMAS, LA INVENCION PROPORCIONA UN METODO DE PREVENCION O REDUCCION DE LA SEVERIDAD DE UN CANCER EN UN SUJETO POR MEDIO DE LA ESTIMULACION DE LA RESPUESTA INMUNOLOGICA DEL INDIVIDUO CONTRA EL CANCER POR MEDIO DE LA ADMINISTRACION AL SUJETO DE CELULAS TUMOROSAS QUE SON ESENCIALMENTE SIMILARES A LAS CELULAS CANCEROSAS DEL SUJETO Y QUE ESTAN MODIFICADAS GENETICAMENTE PARA EVITAR LA EXPRESION DE UN AGENTE INMUNORREDUCTOR Y, EN COMBINACION CON LAS CELULAS TUMOROSAS MODIFICADAS GENETICAMENTE, UN AGENTE INMUNOESTIMULADOR. LA INVENCION, ADEMAS, PROPORCIONA UNAS COMPOSICIONES UTILES PARA LA PUESTA EN PRACTICA DE ESTOS METODOS RECLAMADOS
Tipo: Resumen de patente/invención. Número de Solicitud: W9509198US.
Solicitante: SIDNEY KIMMEL CANCER CENTER.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: SUITE 200, 3099 SCIENCE PARK ROAD,SAN DIEGO, CA 92121.
Inventor/es: SOBOL, ROBERT, E., FAKHRAI, HABIB, DORIGO,OLIVER.
Fecha de Publicación: .
Fecha Concesión Europea: 9 de Septiembre de 2009.
Clasificación Internacional de Patentes:
- A61K39/00D6
- C07K14/495 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 14/00 Péptidos con más de 20 aminoácidos; Gastrinas; Somatostatinas; Melanotropinas; Sus derivados. › Factor de crecimiento transformante (TGF).
- C12N15/113C
Clasificación PCT:
- A01N63/00 NECESIDADES CORRIENTES DE LA VIDA. › A01 AGRICULTURA; SILVICULTURA; CRIA; CAZA; CAPTURA; PESCA. › A01N CONSERVACION DE CUERPOS HUMANOS O ANIMALES O DE VEGETALES O DE PARTES DE ELLOS (conservación de alimentos o productos alimenticios A23 ); BIOCIDAS, p. ej. EN TANTO QUE SEAN DESINFECTANTES, PESTICIDAS O HERBICIDAS (preparaciones de uso médico, dental o para el aseo que eliminan o previenen el crecimiento o la proliferación de organismos no deseados A61K ); PRODUCTOS QUE ATRAEN O REPELEN A LOS ANIMALES; REGULADORES DEL CRECIMIENTO DE LOS VEGETALES. › Biocidas, productos que repelen o atraen a los animales perjudiciales, o reguladores del crecimiento de los vegetales, que contienen microorganismos, virus, hongos microscópicos, animales, o sustancias producidas por, u obtenidas a partir de microorganismos, virus, hongos microscópicos o animales, p. ej. encimas o productos de fermentación (que contienen compuestos de constitución determinada A01N 27/00 - A01N 59/00; algas unicelulares A01N 65/03).
- A61K39/00 A […] › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › Preparaciones medicinales que contienen antígenos o anticuerpos (materiales para ensayos inmunológicos G01N 33/53).
- C12N15/00 C […] › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K).
Clasificación antigua:
- A01N63/00 A01N […] › Biocidas, productos que repelen o atraen a los animales perjudiciales, o reguladores del crecimiento de los vegetales, que contienen microorganismos, virus, hongos microscópicos, animales, o sustancias producidas por, u obtenidas a partir de microorganismos, virus, hongos microscópicos o animales, p. ej. encimas o productos de fermentación (que contienen compuestos de constitución determinada A01N 27/00 - A01N 59/00; algas unicelulares A01N 65/03).
- C12N15/00 C12N […] › Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K).
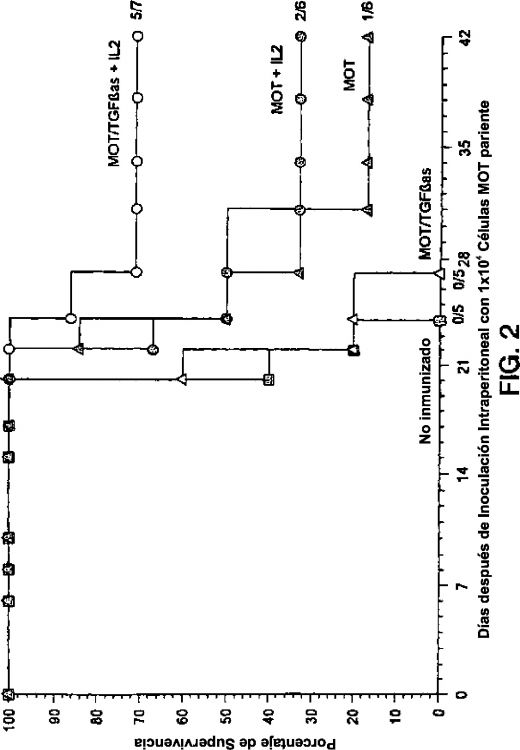
Fragmento de la descripción:
Composiciones y métodos para inmunidad mejorada de células neoplásicas in vivo.
Antecedente de la invención
La presente invención se relaciona generalmente con vacunas antineoplásicas y, más particularmente, con el uso de terapia de gen para aumentar las funciones inmunológicas en respuesta a vacunas antineoplásicas.
Avances recientes en nuestro entendimiento de la biología del sistema inmune han conducido a la identificación de citoquinas como modulares importantes de respuestas inmunes. Las citoquinas producidas por linfocitos se denominan linfoquinas. Estos agentes median muchas de las respuestas inmunes a los tumores. Varias citoquinas han sido producidas por metodología de ADN recombinante y se evalúan por sus efectos antineoplásicos.
La administración de linfoquinas e inmunomodulares relacionados ha producido algunas respuestas positivas en pacientes con varios tipos de neoplasmas. Sin embargo, la administración de citoquina actual se asocia frecuentemente con efectos tóxicos que limitan el valor terapéutico de estos agentes. Por ejemplo, la interleuquina-2 (IL-2) es una linfoquina importante en la generación de inmunidad antineoplásica. En respuesta a antígenos neoplásicos, un subconjunto de linfocitos, células T auxiliares, secretan una pequeña cantidad de IL-2, que actúa localmente en el sitio de estimulación de antígeno de tumor para activar las células T citotóxicas y linfocitos citolíticos naturales que median la destrucción de la célula neoplásica sistémica.
En adición a los agentes inmunoestimuladores tal como citoquinas, que regulan positivamente las funciones efectoras inmunes, también existen moléculas que exhiben actividad inmunosupresora. Estos agentes inmunosupresores, si se regulan aberrantemente, pueden tener efectos perjudiciales en la inducción de inmunidad sistémica. Por ejemplo, una o más isoformas de factor ß de crecimiento transformante (TGFß) pueden ser un agente inmunosupresor que se secreta por muchos tipos de tumor. Los sobrenadanates de cultivo de células neoplásicas que secretan una forma inmunosupresora de TGFß pueden reducir la citotoxicidad específica de tumor in vitro. En estos ensayos de citotoxicidad in vitro, la inhibición de la actividad TGFß mediante la expresión de TGFß anticodificante puede mejorar la citotoxicidad de célula neoplásica.
Debido, en parte, a concentraciones endógenas de agentes inmunosupresores en un sujeto que tiene un cáncer, no se puede predecir si inhibir la secreción de un agente inmunosupresor por la célula neoplásica hará a la célula neoplásica inmunogénica in vivo. Por ejemplo, el TGFß secretado por células de cáncer puede circular a través de un paciente con cáncer y generalmente el paciente inmunocomprometido. Como un resultado, la administración de células neoplásicas que son sustancialmente similares a las células de cáncer del paciente y que se modifican genéticamente para evitar la expresión de un agente inmunosupresor no necesariamente se esperaría estimular la respuesta inmune del paciente contra la células de cáncer. De forma similar, los resultados de modelos in vitro de respuestas inmunes antineoplásicas no predicen confiablemente el resultado de manipulaciones del sistema inmune relacionadas in vivo.
Se ha intentado la modulación de concentraciones de citoquina como un medio para mejorar una respuesta inmune del paciente con cáncer hacia células de cáncer objetivo. Por ejemplo, la administración intravenosa, intralinfática o intralesional de IL-2 ha producido respuestas clínicamente significativas en algunos pacientes con cáncer. Sin embargo, efectos tóxicos severos tal como hipotensión y edema limitan la dosis y eficacia de la administración IL-2 intravenosa e intralinfática. La toxicidad de linfoquinas administradas sistémicamente no es sorprendente cuando estos agentes median las interacciones celulares locales y normalmente se secretan solo en cantidades muy pequeñas. Adicionalmente, la administración intralesional de IL-2 puede ser difícil de llevar a cabo y puede originar morbilidad significativa del paciente.
Para evitar la toxicidad de la administración de citoquina sistémica, un método alternativo involucra la transferencia del gen citoquina en células neoplásicas que han producido respuestas inmunes antineoplásicas en varios modelos de tumor de animal. En estos estudios, la expresión de citoquinas luego que el gen citoquina se transfiere en células neoplásicas resulta en una reducción en tumorogenicidad de las células neoplásicas que secretan citoquina cuando se implantan en anfitriones singeneicos. La reducción en la tumorogenicidad ocurre utilizando IL-2, interferón-gama o interleuquina-4. En estudios que emplean la transferencia del gen IL-2, los animales tratados también desarrollan inmunidad antineoplásica sistémica y se protegen contra exposiciones a células neoplásicas posteriores con células neoplásicas de los padres no modificadas. La inhibición similar del crecimiento de tumor y la inmunidad protectora también se demuestra cuando se desarrollan inmunizaciones con una mezcla de células neoplásicas de padres no modificadas y células neoplásicas que se modifican genéticamente para expresar IL-2. La no toxicidad se asocia con la expresión transgen de linfoquina localizada en estos estudios de animal.
Las citoquinas también se han expresado en tipos celulares heterólogos tal como fibroblastos, que se coinyectan en un paciente con cáncer con las células de cáncer de los propios pacientes. La coinyección de células que expresan citoquina produce una inducción similar de inmunidad antineoplásica sistémica cuando se produce por células neoplásicas que expresan citoquina. No obstante, aunque estos procedimientos de transferencia de gen pueden proporcionar inmunidad antineoplásica significativa comparado con otros métodos, una fracción significativa de los pacientes no responde óptimamente a tal terapia. Así, existe una necesidad de proporcionar métodos más efectivos para evitar o reducir la severidad de un cáncer en un paciente. La presente invención satisface esta necesidad y proporciona ventajas muy bien relacionadas.
Resumen de la invención
La presente invención se relaciona con un método para evitar o reducir la severidad de un cáncer en un sujeto al estimular la respuesta inmune del sujeto contra el cáncer. Por ejemplo, un paciente con cáncer se puede inmunizar con células neoplásicas que son sustancialmente similares a las células de cáncer del sujeto pero que se modifican genéticamente para evitar la expresión de por lo menos un agente inmunosupresor.
La invención proporciona el uso de células neoplásicas que son sustancialmente similares a las células de cáncer del sujeto pero que se modifican genéticamente para evitar la expresión de por lo menos un agente inmunosupresor y se seleccionan del grupo que consiste de fibronectina TGFß, tenascina, p15E y el factor inhibidor de blastogenia de linfocito, opcionalmente, para expresar por lo menos un agente inmunoestimulador tal como una citoquina o un antígeno neoplásico conocido para la preparación de una composición farmacéutica para estimular una respuesta inmune del sujeto contra un cáncer. La invención proporciona adicionalmente el uso de dichas células neoplásicas en combinación con un agente inmunoestimulador tal como un adyuvante, una citoquina o células que expresan citoquina (células CE), que son células que se modifican genéticamente para expresar una citoquina para la preparación de una composición farmacéutica para estimular una respuesta inmune del paciente con cáncer contra el cáncer.
La invención también proporciona composiciones útiles para evitar o reducir la severidad de un cáncer en un sujeto al estimular la respuesta inmune del sujeto contra el cáncer. Una composición de la invención puede contener células neoplásicas que son sustancialmente similares a las células de cáncer del sujeto y que se modifican genéticamente para evitar la expresión de por lo menos un agente inmunosupresor que se selecciona del grupo que consiste de TGFß, fibronectina, tenascina, p15E y el factor inhibidor de blastogenia de linfocito. Adicionalmente, si se desea, las células neoplásicas modificadas genéticamente se pueden modificar adicionalmente para expresar un agente inmunoestimulador tal como una citoquina o un antígeno neoplásico conocido. Una composición de la invención también puede contener un agente inmunoestimulador tal como un adyuvante,...
Reivindicaciones:
1. Uso de células neoplásicas alogénicas modificadas genéticamente para la preparación de una composición farmacéutica para estimular una respuesta inmune contra un cáncer, en donde dichas células neoplásicas se modifican genéticamente para reducir o inhibir la expresión de por lo menos un agente inmunosupresor, en donde dicho agente inmunosupresor se selecciona del grupo que consiste de TGFß, fibronectina, tenascina, p15E y el factor inhibidor de blastogenia de linfocito.
2. El uso de la reivindicación 1, en donde dicho agente inmunosupresor es TGFß2.
3. El uso de la reivindicación 1 o 2, en donde dichas células neoplásicas alogénicas se derivan de un sujeto a ser tratado.
4. El uso de la reivindicación 1 o 2, en donde dichas células neoplásicas alogénicas son células neoplásicas de donante.
5. El uso de las reivindicaciones 1 a 4, en donde dichas células neoplásicas alogénicas son células carcinoma, células glioma, células sarcoma, células linfoma, células melanoma o células de leucemia.
6. El uso de las reivindicaciones 1 a 5, en donde dicha modificación genética para reducir o inhibir la expresión de un agente inmunosupresor se lleva a cabo por recombinación homóloga del gen mutante de un gen que codifica dicho agente inmunosupresor en dicha célula neoplásica alogénica.
7. El uso de las reivindicaciones 1 a 5, en donde dicha modificación genética para reducir o inhibir la expresión de un agente inmunosupresor se lleva a cabo al proporcionar en dicha célula neoplásica alogénica una secuencia de ácido nucleico codificante que hibrida a una molécula de ácido nucleico que codifica dicho agente inmunosupresor.
8. El uso de las reivindicaciones 1 a 5, en donde dicha modificación genética para reducir o inhibir la expresión de un agente inmunosupresor se lleva a cabo al proporcionar en dicha célula neoplásica alogénica una secuencia de ácido nucleico que codifica una ribozima que reconoce e inactiva dicho agente inmunosupresor.
9. El uso de las reivindicaciones 1 a 8, en donde dicha composición farmacéutica comprende adicionalmente un agente inmunoestimulador, en donde dicho agente inmunoestimulador es una citoquina o una célula que expresa citoquina, y en donde dicha citoquina se selecciona del grupo que consiste de interleuquina-1, interleuquina-2, interleuquina-3, interleuquina-4, interleuquina-5, interleuquina-6, interleuquina-7 interleuquina-12, interleuquina-15, interferón-gama, factor de necrosis de tumor, factor que estimula la colonia de granulocito o factor que estimula la colonia de granulocito-macrófago.
10. El uso de las reivindicaciones 1 a 8, en donde dichas células neoplásicas alogénicas adicionalmente se modifican genéticamente para expresar por lo menos un agente inmunoestimulador, en donde dicho agente inmunoestimulador es la molécula B7 coestimuladora, una molécula MHC clase I, una molécula MHC clase II, un antígeno neoplásico conocido o una citoquina seleccionada del grupo que consiste de interleuquina-1, interleuquina-2, interleuquina-3, interleuquina-4, interleuquina-5, interleuquina-6, interleuquina-7, interleuquina-12, interleuquina-15, gama-interferón, factor de necrosis de tumor, factor que estimula la colonia de granulocito y factor que estimula la colonia de granulocito-macrófago.
11. Una composición para estimular una respuesta inmune a un cáncer, en donde dicha composición comprende células neoplásicas alogénicas que se modifican genéticamente para reducir o inhibir la expresión de por lo menos un agente inmunosupresor, en donde dicho agente inmunosupresor se selecciona del grupo que consiste de TGFß, fibronectina, tenascina, p15E y el factor inhibidor de blastogenia de linfocito.
12. La composición de la reivindicación 11, en donde dicho agente inmunosupresor es TGFß2.
13. La composición de la reivindicación 11 o 12, en donde dichas células neoplásicas alogénicas se derivan de un sujeto a ser tratado.
14. La composición de la reivindicación 11 o 12, en donde dichas células neoplásicas alogénicas son células neoplásicas de donante.
15. La composición de las reivindicaciones 11 a 14, en donde dichas células neoplásicas alogénicas son células carcinoma, células glioma, células sarcoma, células linfoma, células melanoma o células de leucemia.
16. La composición de las reivindicaciones 11 a 15, en donde dichas células neoplásicas alogénicas modificadas genéticamente contienen un gen inactivado que codifica dicho agente inmunosupresor.
17. La composición de las reivindicaciones 11 a 15, en donde dichas células neoplásicas alogénicas modificadas genéticamente contienen una secuencia de ácido nucleico codificante que hibrida a una molécula de ácido nucleico que codifica dicho agente inmunosupresor.
18. La composición de las reivindicaciones 11 a 15, en donde dichas células neoplásicas alogénicas modificadas genéticamente contienen una secuencia de ácido nucleico que codifica una ribozima que reconoce e inactiva dicho agente inmunosupresor.
19. La composición de las reivindicaciones 11 a 18, en donde dicha composición comprende adicionalmente un agente inmunoestimulador, en donde dicho agente inmunoestimulador es una citoquina o una célula que expresa citoquina, y en donde dicha citoquina se selecciona del grupo que consiste de interleuquina-1, interleuquina-2, interleuquina-3, interleuquina-4, interleuquina-5, interleuquina-6, interleuquina-7 interleuquina-12, interleuquina-15, interferón-gama, factor de necrosis de tumor, factor que estimula la colonia de granulocito o factor que estimula la colonia de granulocito-macrófago.
20. La composición de las reivindicaciones 11 a 18, en donde dichas células neoplásicas alogénicas adicionalmente se modifican genéticamente para expresar un agente inmunoestimulador, en donde dicho agente inmunoestimulador es la molécula B7 coestimuladora, una molécula MHC clase I, una molécula MHC clase II, un antígeno neoplásico conocido o una citoquina seleccionada del grupo que consiste de interleuquina-1, interleuquina-2, interleuquina-3, interleuquina-4, interleuquina-5, interleuquina-6, interleuquina-7, interleuquina-12, interleuquina-15, gama-interferón, factor de necrosis de tumor, factor que estimula la colonia de granulocito y factor que estimula la colonia de granulocito-macrófago.
Patentes similares o relacionadas:
Péptido que muestra actividad que promueve la generación de melanina y uso del mismo, del 8 de Abril de 2020, de CAREGEN CO., LTD: Un péptido que consiste en la secuencia de aminoácidos de la SEQ ID NO: 1.
Proceso para la preparación de mezclas de alta pureza de factores proteínicos procedentes de calostro bovino, del 13 de Noviembre de 2019, de Tenagro S.r.l: Proceso para la preparación de una mezcla de factores proteínicos procedentes de calostro bovino que comprende las siguientes etapas: […]
Anticuerpos anti-TGF-beta modificados genéticamente y fragmentos de unión a antígeno, del 22 de Mayo de 2019, de GENZYME CORPORATION: Un anticuerpo humano aislado o fragmento de unión a antígeno del mismo que se une a y neutraliza TGFβ1, TGFβ1 y TGFβ3 humanos, […]
Proteínas de fusión dirigidas/inmunomoduladoras y métodos de preparación de las mismas, del 30 de Mayo de 2018, de BIOCON LIMITED: Una proteína de fusión quimérica que consiste en un resto de direccionamiento para dirigir a una célula cancerosa, un resto inmunomodulador que contrarresta […]
Procedimientos de tratamiento del cáncer colorrectal, del 9 de Mayo de 2018, de Nogra Pharma Limited: Un oligonucleótido antisentido SMAD7 para su uso en un procedimiento de tratamiento del cáncer colorrectal en un paciente, en el que el oligonucleótido […]
Composiciones y métodos para incrementar la mineralización de la substancia ósea, del 14 de Junio de 2017, de UCB PHARMA, S.A.: Un anticuerpo o fragmento del mismo que se unen a una proteína codificada por el SEQ ID NO: 1.
Composiciones y métodos para anticuerpos y proteínas de fusión inmunomoduladores dirigidos contra dianas, del 3 de Mayo de 2017, de THE JOHNS HOPKINS UNIVERSITY: Una composición que comprende una molécula de fusión bifuncional dirigida contra dianas, en la que dicha molécula comprende un resto seleccionador de dianas y un resto […]
Supresión del cáncer, del 29 de Marzo de 2017, de Ipsen Bioinnovation Limited: Un polipéptido, para uso en la supresión o tratamiento del cáncer mediante la inhibición de la secreción autocrina de una célula cancerosa en un paciente, […]