COMPOSICIONES PARA INHIBIR LA PROTEINCINASA C-ALFA PARA EL TRATAMIENTO DE DIABETES MELLITUS.
Uso de inhibidores de la actividad de la proteincinasa C-α
(PKC-α) para la preparación de una composición farmacéutica para el tratamiento y/o la prevención de retinopatía diabética, neuropatía diabética y nefropatía diabética
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/DE2003/003165.
Solicitante: PHENOS GMBH.
Nacionalidad solicitante: Alemania.
Dirección: FEODOR-LYNEN-STR. 5 30625 HANNOVER ALEMANIA.
Inventor/es: MENNE,JAN,C/O PHENOMIQUES GMBH, HALLER,HERMANN,MEDIZINISCHE HOCHSCHULE HANNOVER.
Fecha de Publicación: .
Fecha Solicitud PCT: 23 de Septiembre de 2003.
Fecha Concesión Europea: 28 de Julio de 2010.
Clasificación Internacional de Patentes:
- A61K31/235 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › que tienen un núcleo aromático unido a un grupo carboxilo.
- A61K31/355 A61K 31/00 […] › Tocoferoles, p. ej. vitamina E.
- A61K31/7088 A61K 31/00 […] › Compuestos que tienen al menos tres nucleósidos o nucleótidos.
- A61K38/13 A61K […] › A61K 38/00 Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00). › Ciclosporinas.
- A61K38/45 A61K 38/00 […] › Transferasas (2).
Clasificación PCT:
- A61K31/235 A61K 31/00 […] › que tienen un núcleo aromático unido a un grupo carboxilo.
- A61K31/355 A61K 31/00 […] › Tocoferoles, p. ej. vitamina E.
- A61K31/7088 A61K 31/00 […] › Compuestos que tienen al menos tres nucleósidos o nucleótidos.
- A61K38/13 A61K 38/00 […] › Ciclosporinas.
- A61K38/45 A61K 38/00 […] › Transferasas (2).
- A61K39/395 A61K […] › A61K 39/00 Preparaciones medicinales que contienen antígenos o anticuerpos (materiales para ensayos inmunológicos G01N 33/53). › Anticuerpos (aglutininas A61K 38/36 ); Inmunoglobulinas; Inmunosuero, p. ej. suero antilinfocitario.
- A61P5/48 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › A61P 5/00 Medicamentos para el tratamiento de trastornos del sistema endocrino. › de las hormonas pancreáticas.
Clasificación antigua:
- A61K31/235 A61K 31/00 […] › que tienen un núcleo aromático unido a un grupo carboxilo.
- A61K31/355 A61K 31/00 […] › Tocoferoles, p. ej. vitamina E.
- A61K31/7088 A61K 31/00 […] › Compuestos que tienen al menos tres nucleósidos o nucleótidos.
- A61K38/13 A61K 38/00 […] › Ciclosporinas.
- A61K38/45 A61K 38/00 […] › Transferasas (2).
- A61K39/395 A61K 39/00 […] › Anticuerpos (aglutininas A61K 38/36 ); Inmunoglobulinas; Inmunosuero, p. ej. suero antilinfocitario.
- A61P5/48 A61P 5/00 […] › de las hormonas pancreáticas.
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Eslovenia, Finlandia, Rumania, Chipre, Lituania, Letonia, Ex República Yugoslava de Macedonia, Albania.
PDF original: ES-2356286_T3.pdf

Fragmento de la descripción:
La presente invención se refiere al uso de inhibidores de la actividad de la proteincinasa C-α (PKC-α) para la preparación de una composición farmacéutica para el tratamiento y/o la prevención de retinopatía diabética, neuropatía diabética y nefropatía diabética.
La diabetes mellitus es una de las enfermedades más frecuentes en el mundo occidental que afecta a aproximadamente el 5% de la población. La diabetes mellitus se clasifica en una diabetes de tipo I, que generalmente ya aparece durante la adolescencia, y en la diabetes de tipo II también denominada diabetes de aparición en adultos. Debido a un trastorno del metabolismo de la glucosa, en ambas formas de diabetes se producen valores de glucosa permanentemente elevados en la sangre, lo que en el caso de los pacientes afectados conduce después de varios años a diferentes complicaciones. Las complicaciones más frecuentes y al mismo tiempo las más temidas son la retinopatía diabética que causa ceguera, la neuropatía diabética que puede traer consigo la amputación de los pies o de las piernas y la nefropatía diabética.
Una nefropatía diabética se desarrolla en aproximadamente el 40% de todos los pacientes con diabetes y es mundialmente la causa más frecuente de insuficiencia renal crónica y de un tratamiento de diálisis. Aproximadamente del 30 al 40% de todos los nuevos pacientes de diálisis presentan una nefropatía diabética. Como la lesión renal diabética sólo se desarrolla lentamente, es de gran importancia clínica identificar ya prematuramente pacientes que tienen un alto riesgo de desarrollar una insuficiencia renal para empezar etapas terapéuticas adecuadas. Uno de los primeros signos clínicos de una lesión renal incipiente es la aparición de una llamada microalbuminuria. A este respecto se produce una excreción de 30-300 mg de albúmina en la orina recogida en 24 horas. En el caso normal se excretan menos de 30 mg de albúmina por día. Una microalbuminuria aparece bajo las condiciones terapéuticas presentes en aproximadamente el 25% de los diabéticos con diabetes de tipo I o de tipo II (Alzaid, Diabetes Care, 19 (1996), 79-89; Klein y col., Diabetes Care, 22 (1999), 743-751; Valmadrid y col., Arch. Intern. Med., 160 (2000), 1093-1100). El riesgo de desarrollar una insuficiencia renal es en pacientes con microalbuminuria aproximadamente 10 veces más alto que en pacientes con excreción de albúmina normal. Una nefropatía diabética que se caracteriza por una proteinuria de más de 300 mg/día y/o una función renal limitada se desarrolla en aproximadamente del 5 al 10% de todos los pacientes con diabetes y microalbuminuria por año. El riesgo de desarrollar una retinopatía diabética también es considerablemente elevado en diabéticos con microalbuminuria en comparación con diabéticos sin microalbuminuria (Vigstrup y Mogensen, Acta Ophthalmol. (Copenh), 63 (1985), 530-534).
Como mostraron estudios a largo plazo con más de diez años de seguimiento, la mortalidad cardiovascular ya aumenta aproximadamente el doble en diabéticos de tipo II y de tipo I en el estadio de microalbuminuria en comparación con diabéticos sin microalbuminuria, también después de ajustarse para los factores de riesgo convencionales como colesterol e hipertensión (Rossing y col., Bmj, 313 (1996), 779-784; Gerstein y col., Diabetes Care, 23 (2000), supl. 2: B35-39; Valmadrid y col., 2000). También puede detectarse una elevada mortalidad cardiovascular en pacientes con microalbuminuria sin diabetes mellitus (Gerstein y col., Jama, 286 (2001), 421-426).
Hay distintas hipótesis sobre por qué la microalbuminuria es un marcador extremadamente importante para la aparición de complicaciones en pacientes con diabetes. Según la llamada “hipótesis de Steno” (Deckert, Feldt-Rasmussen y col., Diabetologia, 32 (1989), 219-226), la pérdida de moléculas negativamente cargadas, es decir aniónicas, en la matriz extracelular es responsable de la aparición de albuminuria, retinopatía diabética y complicaciones cardiovasculares, por ejemplo, cardiopatía coronaria. Esta hipótesis está respaldada por datos adquiridos tanto en seres humanos como también en sistemas de modelos animales y se ha confirmado en los últimos años por resultados de otros grupos de trabajo.
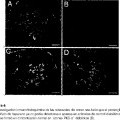
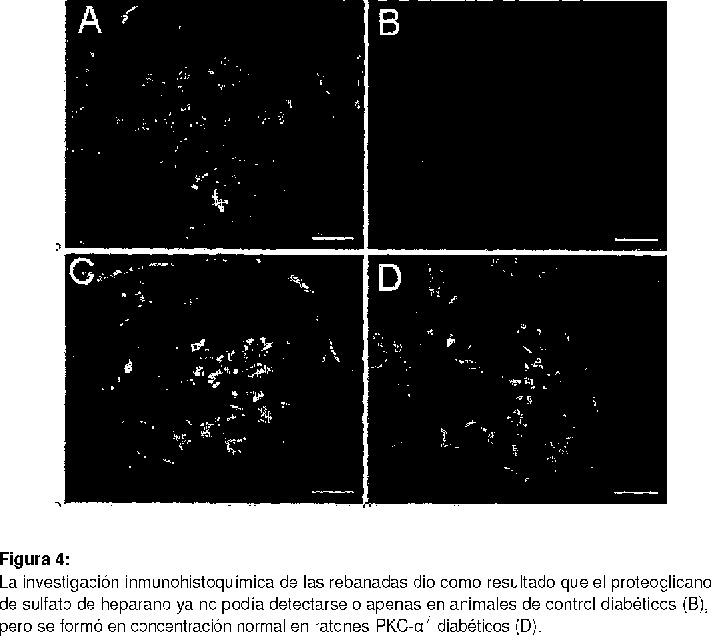
En el riñón, la orina es secretada en los corpúsculos renales, los llamados glomérulos. Para evitar el paso de proteínas, por ejemplo, albúmina, el lado de la sangre está separado del lado de la orina por un membrana llamada la membrana basal. La membrana basal presenta poros pequeños que hacen posible el paso de moléculas más pequeñas por la membrana basal, mientras que las moléculas de proteína no pueden pasar por la membrana debido a su tamaño. No obstante, en pacientes con microalbuminuria se produce el paso de pequeñas proteínas como albúmina aunque el tamaño de poro no aumenta inicialmente. Como explicación para este fenómeno pudo mostrarse que en los poros o en el borde de los poros están presentes moléculas de carga negativa que repelen las proteínas también negativamente cargadas (Kverneland, Feldt- Rasmussen y col., Diabetologia, 29 (1986), 634-639; Deckert, Feldt-Rasmussen y col., Kidney Int., 33 (1988), 100-106; Kverneland, Welinder y col., Diabetologia, 31 (1988), 708-710). En el caso de estas moléculas con cargas negativas se trata de proteoglicanos. Los proteoglicanos son macromoléculas complejas que están constituidas por proteínas a las que están covalentemente asociadas cadenas de polisacáridos. Las cadenas de polisacáridos están constituidas principalmente por sulfato de heparano y están muy negativamente cargadas. El proteoglicano que está más frecuentemente presente en el cuerpo es perlecan. El perlecan es una proteína de 460 kd de tamaño y tiene varias cadenas laterales de polisacáridos (Murdoch e Iozzo, Virchows Arch. A. Pathol. Anato. Histopathol., 423 (1993), 237-242; Iozzo, Cohen y col., Biochem. J., 302 (1994), 625-639; Murdoch, Liu y col., J. Histochem. Cytochem., 42 (1994), 239-249). En pacientes con diabetes y microalbuminuria, el sulfato de heparano apenas está presente en la membrana basal glomerular. En pacientes con nefropatía diabética avanzada ya no puede detectarse sulfato de heparano en la membrana
45
55
basal, aunque las cadenas de proteína todavía estén presentes. Este efecto se explica mediante una síntesis de sulfato de heparano reducida bajo condiciones hiperglucémicas como las que se presentan en diabéticos (Parthasarathy y Spiro, Diabetes, 31 (1982), 738-741; Deckert, Feldt-Rasmussen y col., 1988; Nakamura y Myers, Diabetes, 37 (1988), 1202-1211; Nerlich y Schleicher, Am. J. Pathol., 139 (1991), 889-899; Makino, Ikeda y col., Nephron, 61 (1992), 415-421; Scandling y Myers, Kidney Int., 41 (1992), 840-846; Vernier, Steffes y col., Kidney Int., 41 (1992), 1070-1080; Tamsma, van den Born y col., Diabetologia, 37 (1994), 313-320; Iozzo y San Antoniom, J. Clin. Invest., 108 (2001), 349-355). Además, pudo mostrarse que los proteoglicanos de sulfato de heparano no sólo evitan la filtración glomerular de albúmina por la carga negativa, sino que probablemente también son responsables de la integridad del tamaño de poro dentro de la membrana basal (Deckert, Kofoed-Enevoldsen y col., Diabetologia, 36 (1993), 244-251). Así, a medida que avanza la insuficiencia renal, la pérdida de proteoglicanos de sulfato de heparano conduce a una destrucción de la microestructura de la membrana basal. Estos cambios podrían explicar por qué durante el transcurso de la nefropatía diabética se produce una gran proteinuria no selectiva con pérdida de proteínas más grandes como inmunoglobulina. Los proteoglicanos de sulfato de heparano también son fuertes inhibidores de la expansión mesangial en los corpúsculos renales. Esto es de gran interés ya que en el caso de pacientes con diabetes se produce clásicamente una expansión del tejido conjuntivo mesangial. Por tanto, no es sorprendente que la pérdida de proteoglicanos de sulfato de heparano en pacientes con diabetes sea culpable de una causa importante de la expansión mesangial.
Sin embargo, la pérdida de sulfato de heparano se produce en diabéticos no sólo en el riñón, sino en casi todos los otros órganos. Así se produce una clara reducción de sulfato de heparano en el tejido conjuntivo de la retina, del músculo esquelético, de las paredes de las arterias y de la piel, así como de los glóbulos rojos. Las células endoteliales también presentan una síntesis reducida de sulfato de heparano (Yokoyama, Hoyer, y col., Diabetes, 46 (1997), 1875-1880; van der Pijl, Daha y col., Diabetologia, 41 (1998), 791-798). Como los proteoglicanos... [Seguir leyendo]
Reivindicaciones:
1. Uso de inhibidores de la actividad de la proteincinasa C-α (PKC-α) para la preparación de una
composición farmacéutica para el tratamiento y/o la prevención de retinopatía diabética, neuropatía diabética y
nefropatía diabética.
2. Uso según la reivindicación 1, en el que el inhibidor de la actividad de la proteincinasa C-α es un anticuerpo que reacciona con la proteincinasa C-α, especialmente un anticuerpo monoclonal o policlonal, como un anticuerpo humanizado, o en el que el inhibidor cambia el estado de fosforilación de la proteincinasa C-α.
3. Uso según una de las reivindicaciones 1 ó 2, en el que el inhibidor de la actividad de la proteincinasa C-α es al mismo tiempo un inhibidor de la actividad de la proteincinasa C-β.
10 4. Uso según una de las reivindicaciones 1 a 3, en el que el inhibidor de la actividad de la proteincinasa C-α se utiliza en combinación con un inhibidor de la actividad de la proteincinasa C-β.
5. Uso según la reivindicación 4, en el que el inhibidor es un anticuerpo que reacciona con la
proteincinasa C-β, especialmente un anticuerpo monoclonal o policlonal, preferiblemente un anticuerpo
humanizado.
15 6. Uso según la reivindicación 5, en el que el inhibidor cambia el estado de fosforilación de la teincinasa C-β.
Patentes similares o relacionadas:
Composición oftálmica para el tratamiento de la enfermedad del ojo seco, del 10 de Junio de 2020, de NOVALIQ GMBH: Una composición farmacéutica para usarse en el tratamiento tópico de la enfermedad de ojo seco en un sujeto que padece enfermedad del ojo seco, en donde la composición […]
Procedimiento para la fabricación de emulsiones oftálmicas de tipo aceite en agua, del 15 de Abril de 2020, de Santen SAS: Procedimiento para la fabricación de un preconcentrado de una emulsión oftálmica de tipo aceite en agua, comprendiendo dicho procedimiento una […]
Combinación de canrenoato y exenatida, del 8 de Abril de 2020, de Genesis Pharma SA: Una combinación que comprende un modulador de insulina, en donde el modulador de insulina es exenatida o una sal farmacéuticamente aceptable de la misma, y […]
Nanoportadores sintéticos tolerogénicos para reducir las respuestas de anticuerpos, del 1 de Abril de 2020, de Selecta Biosciences, Inc: Una composición para usar en un método que promueve una respuesta inmunitaria tolerogénica a un antígeno que de otro modo causaría una respuesta inmunitaria […]
Cannabidiol para la prevención y el tratamiento de la enfermedad de injerto contra huésped, del 19 de Febrero de 2020, de MOR RESEARCH APPLICATIONS LTD.: Una composición que comprende un cannabidiol para usar en la prevención y el tratamiento de la enfermedad de injerto contra huésped GVHD en un sujeto que la […]
Micropartículas cargadas con ciclosporina de liberación sostenida, del 29 de Enero de 2020, de Midatech Pharma (Wales) Limited: Una formulación farmacéutica de liberación controlada, que comprende micropartículas cargadas con ciclosporina de un polímero biorreabsorbible, que comprende poli(D,L-lactida), […]
Composiciones que comprenden agentes farmacéuticos poco solubles en agua y agentes antimicrobianos, del 15 de Enero de 2020, de ABRAXIS BIOSCIENCE, LLC: Una composición que comprende (a) nanopartículas que comprenden un agente farmacéutico poco soluble en agua y albúmina, (b) un edetato y citrato, […]
Composición oftálmica que comprende ciclosporina y trehalosa, del 8 de Enero de 2020, de Huons Co., Ltd: Una composición oftálmica que comprende ciclosporina y trehalosa como ingredientes activos, donde una relación de peso de ciclosporina:trehalosa es de 1:20 - 200 y la ciclosporina […]