COMPOSICIONES FARMACAUTICAS Y PROCEDIMIENTOS DE TRATAMIENTO CON INSULINA.
Una composición farmacéutica en una forma adecuada para suministro nasal a un paciente que comprende:
una cantidad eficaz terapéuticamente de insulina, un potenciador de permeación, y un vehículo líquido; estando dicha composición a un pH ácido, pero no mayor de un pH de 4,5, y siendo dicho potenciador de permeación un potenciador Hsieh que tiene la estructura siguiente: **(Ver fórmula)**en la que X e Y son oxígeno, azufre o un grupo imino de la estructura **(Ver fórmula)**o =N-R, con la condición de que cuando Y es el grupo imino, X es es un grupo imino, y cuando Y es azufre, X es azufre o un grupo imino, A es un grupo que tiene la estructura **(Ver fórmula)**en la que X e Y son tal como se han definido anteriormente, m y n son números enteros que tienen un valor de desde 1 hasta 20 y la suma de m+n no es mayor de 25, p es un número entero que tiene un valor de 0 ó 1, q es un número entero que tiene un valor de 0 ó 1, r es un número entero que tiene un valor de 0 ó 1, y cada R, R1, R2, R3, R4, R5 y R6 es independientemente hidrógeno o un grupo alquilo que tiene desde 1 hasta 6 átomos de carbono los cuales pueden ser de cadena recta o ramificada, con la condición de que solamente uno de R1 a R6 puede ser un grupo alquilo, con la condición de que cuando p, q y r tienen un valor de 0 e Y es oxígeno, m+n es al menos 11, y con la condición adicional de que cuando X es un grupo imino, q es igual a 1, Y es oxígeno, y p y r son 0, en cuyo caso m+n es al menos 11
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2004/040313.
Solicitante: CPEX PHARMACEUTICALS, INC.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 2 HOLLAND WAY EXETER, NH 03833 ESTADOS UNIDOS DE AMERICA.
Inventor/es: GYURIK, ROBERT, J., REPPUCCI,CARL.
Fecha de Publicación: .
Fecha Solicitud PCT: 2 de Diciembre de 2004.
Fecha Concesión Europea: 21 de Julio de 2010.
Clasificación Internacional de Patentes:
- A61K38/28 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 38/00 Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00). › Insulinas.
- A61K47/10 A61K […] › A61K 47/00 Preparaciones medicinales caracterizadas por los ingredientes no activos utilizados, p. ej. portadores o aditivos inertes; Agentes de direccionamiento o agentes modificadores enlazados químicamente al ingrediente activo. › Alcoholes; Fenoles; Sus sales, p. ej. glicerol; Polietilenglicoles [PEG]; Poloxámeros; Éteres alquílicos PEG/POE.
- A61K47/14 A61K 47/00 […] › Esteres de ácidos carboxílicos, p. ej. monoglicéridos de ácidos grasos, triglicéridos de cadenas medianas, parabenos o ésteres de ácidos grasos y de polietilenglicol (PEG).
- A61K47/26 A61K 47/00 […] › Hidratos de carbono, p. ej. alcoholes de azúcares, amino azúcares, ácidos nucleicos, mono-, di- u oligo-sacáridos; Sus derivados, p. ej. polisorbatos, ésteres de ácidos grasos sorbitano o glicirricina.
- A61K47/34 A61K 47/00 […] › Compuestos macromoleculares obtenidos por reacciones distintas a aquellas en las que intervienen solamente enlaces insaturados carbono-carbono, p. ej. poliésteres, poly(amino ácidos), polisiloxanos, polifosfacinas, copolímeros de polialquilenglicol o poloxámeros (A61K 47/10 tiene prioridad).
- A61K47/44 A61K 47/00 […] › Aceites, grasas o ceras previstas en dos o más grupos de A61K 47/02 - A61K 47/42; Aceites naturales o aceites naturales modificados, grasas o ceras, p. ej. aceite de ricino, aceite de ricino polietoxilado, cera Montana, lignito, goma laca, colofonía, cera de abeja o lanolina (glicéridos sintéticos, p. ej. triglicéridos de cadena mediana, A61K 47/14).
- A61K9/00M14
- A61K9/00M5
- A61K9/107D
Clasificación PCT:
- A61K38/28 A61K 38/00 […] › Insulinas.
- A61K47/22 A61K 47/00 […] › Compuestos heterocíclicos, p. ej. ácido ascórbico, tocoferol o pirrolidonas.
- A61K9/00 A61K […] › Preparaciones medicinales caracterizadas por un aspecto particular.
- A61K9/107 A61K […] › A61K 9/00 Preparaciones medicinales caracterizadas por un aspecto particular. › Emulsiones.
- A61P3/10 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › A61P 3/00 Medicamentos para el tratamiento de trastornos del metabolismo (de la sangre o de fluido extracelular A61P 7/00). › para la hiperglucemia, p.ej. antidiabéticos.
Clasificación antigua:
- A61K38/00 A61K […] › Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00).
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Eslovenia, Finlandia, Rumania, Chipre, Lituania, Letonia, Ex República Yugoslava de Macedonia, Albania.
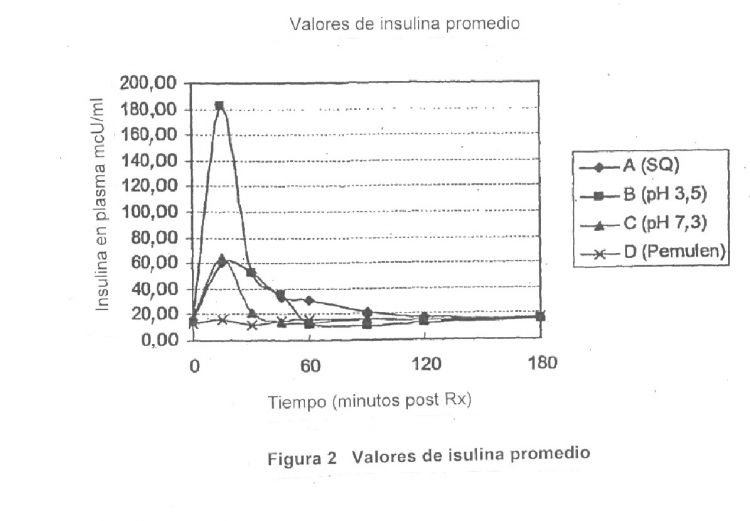
Fragmento de la descripción:
La presente invención se refiere a composiciones y procedimientos para el suministro de insulina, y más particularmente para el suministro de insulina distinto de mediante inyección, a través de la piel, a membranas de diversas membranas nasales.
La insulina se usa generalmente para tratar pacientes que sufren de diabetes. En general, la insulina se suministra a un paciente mediante inyección.
La Patente de EE.UU. 5.023.252 describe una composición para suministro de insulina mediante una vía distinta de mediante inyección. Más particularmente, dicha patente describe el uso de composiciones que incluyen potenciadores de permeación para el suministro de insulina a través de la piel y membranas de cavidades del cuerpo sin requerir una inyección.
La presente invención está dirigida a una mejora en dichas composiciones y al uso de las mismas.
De acuerdo con la invención, se proporciona una composición farmacéutica para suministro nasal que comprende: (A) insulina; (B) un potenciador de permeación tal como se describe más adelante; y (C) un vehículo líquido en el que la composición está en un pH ácido.
El solicitante ha encontrado que cuando se usa una composición que contiene una combinación de insulina y potenciador de permeación, se obtienen resultados mejorados cuando la composición está en un pH ácido.
Se propone tratar un paciente que necesite de insulina con una combinación de insulina, un potenciador de permeación, y un vehículo líquido; conteniendo la combinación un pH ácido no mayor de 4,5. Preferiblemente, el pH de la composición no es mayor de 4 ni por debajo de 2. El pH es preferiblemente al menos de 2.
En general, el pH de la composición es al menos de 2 y no mayor de 4,5. En una realización preferida, el pH no es mayor de 4. Un intervalo preferido de pH es desde 2,5 hasta 3,8. En una realización preferida, el pH es aproximadamente de 3.
El pH de la composición puede mantenerse mediante el uso de un tampón adecuado. La selección de un tampón para mantener el pH deseado se considera que está dentro del ámbito de los expertos en la técnica en base a las directrices establecidas en la presente memoria. Como ejemplos representativos de tampones adecuados pueden mencionarse el tampón de ácido cítrico, tampón de fosfato, y similares, tal como es en el uso común y también adecuado para formulaciones médicas.
En general, el potenciador de permeación que se usa es uno que potencia la permeación de la composición de insulina a través de la mucosa nasal.
En una composición que contiene una cantidad eficaz de insulina, el potenciador de
permeación es un compuesto de la estructura:
**(Ver fórmula)**
en la que X e Y son oxígeno, azufre o un grupo imino de la estructura
**(Ver fórmula)**
o =N-R, con la condición de que cuando Y es el grupo imino, X es es un grupo imino, y cuando Y es azufre, X es azufre o un grupo imino, A es un grupo que tiene la estructura
**(Ver fórmula)**
en la que X e Y son tal como se han definido anteriormente, m y n son números enteros que tienen un valor de desde 1 hasta 20 y la suma de m+n no es mayor de 25, p es un número entero que tiene un valor de 0 ó 1, q es un número entero que tiene un valor de 0 ó 1, r es un número entero que tiene un valor de 0 ó 1, y cada R, R1, R2, R3, R4, R5 y R6 es independientemente hidrógeno o un grupo alquilo que tiene desde 1 hasta 6 átomos de carbono los cuales pueden ser de cadena recta o ramificada, con la condición de que solamente uno de R1 a R6 puede ser un grupo alquilo, con la condición de que cuando p, q y r tienen un valor de 0 e Y es oxígeno, m+n es al menos 11, y con la condición adicional de que cuando X es un grupo imino, q es igual a 1, Y es oxígeno, y p y r son 0, en cuyo caso m+n es al menos 11, y dicho compuesto potenciará la velocidad de paso del fármaco a través de membranas del cuerpo. En adelante, en la presente memoria a estos compuestos se hará referencia como potenciadores. Cuando R, R1, R2, R3, R4, R5 o R6 es alquilo, este puede ser metilo, etilo, propilo, isopropilo, butilo, isobutilo, sec-butilo, amilo, hexilo, y similares. Dichos potenciadores de permeación se describen en la Patente de EE.UU. 5.023.252 y la Patente de EE.UU. 5.731.303.
Preferiblemente, los compuestos de esta invención son las lactonas cíclicas (compuestos en los que tanto X como Y son oxígeno, q es 1 y r es 0), los diésteres cíclicos (los compuestos en los que tanto X como Y son oxígeno, y tanto q como r son 1), y las cetonas cíclicas (los compuestos en los que tanto q como r son 0 e Y es oxígeno). En los diésteres cíclicos m+n es preferiblemente al menos 3. En las cetonas cíclicas m+n es preferiblemente desde 11 hasta 15 y p es preferiblemente 0.
A los potenciadores de la fórmula estructural anterior se hace referencia a los mismos en la presente memoria como “potenciadores Hsieh” y se encuentran descritos, por ejemplo, en las Patentes de EE.UU. No. 5.023.252 y 5.731.303 anteriormente mencionadas (denominados en la presente memoria más adelante como “Patentes Hsieh”). Dichos potenciadores son lipofílicos y son “compatibles con membranas”, lo que significa que no causan daño a la membrana sobre la cual se aplica la composición de la presente invención (denominada en adelante en la presente memoria como “membrana diana”). Dichos potenciadores producen igualmente un bajo nivel de irritabilidad o no irritabilidad a la membrana diana y, de hecho, sirven como un emoliente.
Los potenciadores preferidos para uso en la presente invención son potenciadores macrocíclicos. El término “macrocíclico” se usa en la presente memoria para referirse a compuestos cíclicos que tienen al menos 12 carbonos en el anillo. Los ejemplos de potenciadores macrocíclicos preferidos para uso en la presente invención incluyen: (A) cetonas macrocíclicas, por ejemplo, 3-metilciclopentadecanona (muscona), 9-cicloheptadecen-1-ona (civetona), ciclohexadecanona, y ciclopentadecanona (normuscona); y (B) ésteres macrocíclicos, por ejemplo, pentadecalactonas tales como oxaciclohexadecan-2-ona (ciclopentadecanolida, ω-pentadecalactona).
La oxaciclohexadecan-2-ona y ciclopentadecanona son especialmente preferidas.
El potenciador está presente en la composición en una concentración eficaz para potenciar la penetración de la insulina, a ser suministrada, a través de la membrana. Deberían tenerse en cuenta diversas consideraciones en la determinación de la cantidad de potenciador a usar. Dichas consideraciones incluyen, por ejemplo, la cantidad de flujo (velocidad de paso a través de la membrana) logrado y la estabilidad y compatibilidad de los componentes en las formulaciones. Generalmente, el potenciador se usa en una cantidad de aproximadamente 0,01 hasta aproximadamente 25% en peso de la composición, más generalmente en una cantidad de aproximadamente 0,1 hasta aproximadamente 15% en peso de la composición, y en realizaciones preferidas en una cantidad de aproximadamente 0,5 hasta aproximadamente 15% en peso de la composición.
El vehículo líquido está presente en la composición en una concentración eficaz para servir como un vehículo adecuado para las composiciones de la presente invención. En general, el vehículo se usa en una cantidad de aproximadamente 40 hasta aproximadamente 98% en peso de la composición y en realizaciones preferidas en una cantidad de aproximadamente 50 hasta aproximadamente 98% en peso de la composición.
Las composiciones de insulina de la presente invención se suministran preferiblemente como un espray nasal. En una realización de este tipo, el vehículo líquido preferido es agua, estando la insulina dispersada o disuelta en el agua en una cantidad eficaz terapéuticamente.
En una realización preferida, el potenciador de permeación está emulsificado en la fase acuosa que contiene la insulina. La emulsificación puede llevarse a cabo mediante el uso de uno o más tensioactivos adecuados. La selección de un tensioactivo adecuado se considera que entra dentro del ámbito de los expertos en la práctica de la presente invención en base a las directrices de la presente memoria. Esencialmente, puede usarse cualquier tensioactivo o mezcla de tensioactivos adecuado en la práctica de la presente invención, incluyendo, por ejemplo, tensioactivos aniónicos, catiónicos, y no iónicos. Los tensioactivos preferidos son tensioactivos no...
Reivindicaciones:
1. Una composición farmacéutica en una forma adecuada para suministro nasal a un paciente que comprende: una cantidad eficaz terapéuticamente de insulina, un potenciador de permeación, y un vehículo líquido; estando dicha composición a un pH ácido, pero no mayor de un pH de 4,5, y siendo dicho potenciador de permeación un potenciador Hsieh que tiene la estructura siguiente:
**(Ver fórmula)**
en la que X e Y son oxígeno, azufre o un grupo imino de la estructura
**(Ver fórmula)**
o =N-R, con la condición de que cuando Y es el grupo imino, X es es un grupo imino, y cuando Y es azufre, X es azufre o un grupo imino, A es un grupo que tiene la estructura
**(Ver fórmula)**
en la que X e Y son tal como se han definido anteriormente, m y n son números enteros que tienen un valor de desde 1 hasta 20 y la suma de m+n no es mayor de 25, p es un número entero que tiene un valor de 0 ó 1, q es un número entero que tiene un valor de 0 ó 1, r es un número entero que tiene un valor de 0 ó 1, y cada R, R1, R2, R3, R4, R5 y R6 es independientemente hidrógeno o un grupo alquilo que tiene desde 1 hasta 6 átomos de carbono los cuales pueden ser de cadena recta o ramificada, con la condición de que solamente uno de R1 a R6 puede ser un grupo alquilo, con la condición de que cuando p, q y r tienen un valor de 0 e Y es oxígeno, m+n es al menos 11, y con la condición adicional de que cuando X es un grupo imino, q es igual a 1, Y es oxígeno, y p y r son 0, en cuyo caso m+n es al menos 11.
2. La composición farmacéutica de la reivindicación 1, en la que dicho pH ácido es desde 2 hasta 4.
3. La composición farmacéutica de cualquiera de las reivindicaciones precedentes, que comprende además un inhibidor de la cristalización.
4. La composición farmacéutica de cualquiera de las reivindicaciones precedentes, en la que dicha composición está en la forma de una emulsión en la que el potenciador Hsieh está emulsificado en una fase acuosa que incluye la insulina.
5. La composición farmacéutica de cualquiera de las reivindicaciones precedentes, en la 5 que dicho potenciador Hsieh es un potenciador de permeación macrocíclico.
6. La composición farmacéutica de cualquiera de las reivindicaciones precedentes, en la que dicho potenciador Hsieh es ciclopentadecalactona o ciclohexadecanona.
7. La composición farmacéutica de cualquiera de las reivindicaciones precedentes, en la
que dicho potenciador de permeación está emulsificado dentro de dicha fase acuosa mediante 10 un tensioactivo que tiene un HLB de desde 7 hasta 14.
8. La composición farmacéutica de cualquiera de las reivindicaciones precedentes, que comprende además un inhibidor de la cristalización capaz de rebajar la temperatura de cristalización de dicho potenciador de permeación por debajo de 25ºC.
9. La composición farmacéutica de la reivindicación 8, en la que dicho inhibidor de la cristalización es capaz de rebajar la temperatura de cristalización de dicho potenciador de permeación por debajo de 5ºC.
10. La composición farmacéutica de la reivindicación 9, en la que dicho inhibidor de la cristalización está seleccionado entre el grupo constituido por aceites naturales, substancias oleosas, ceras, ésteres, e hidrocarburos.
11. Una composición farmacéutica de acuerdo cualquiera de las reivindicaciones 1-10, para uso en el tratamiento de un paciente con insulina.
12. Un producto que comprende un aplicador de espray nasal, dispositivo de dosificación de espray intra-nasal, o atomizador que incluye una composición farmacéutica de una cualquiera de las reivindicaciones precedentes.
Patentes similares o relacionadas:
 CD52 soluble para su uso en el tratamiento o la prevención de la esclerosis múltiple o de la artritis reumatoide, del 29 de Julio de 2020, de THE WALTER AND ELIZA HALL INSTITUTE OF MEDICAL RESEARCH: Uno cualquiera o más de:
i) glucoproteína CD52 soluble, ii) una proteína de fusión que comprende la glucoproteína CD52 soluble como una primera proteína, y una segunda proteína;
[…]
CD52 soluble para su uso en el tratamiento o la prevención de la esclerosis múltiple o de la artritis reumatoide, del 29 de Julio de 2020, de THE WALTER AND ELIZA HALL INSTITUTE OF MEDICAL RESEARCH: Uno cualquiera o más de:
i) glucoproteína CD52 soluble, ii) una proteína de fusión que comprende la glucoproteína CD52 soluble como una primera proteína, y una segunda proteína;
[…]
Preparaciones ácidas de insulina con estabilidad mejorada, del 15 de Julio de 2020, de SANOFI-AVENTIS DEUTSCHLAND GMBH: Formulación farmacéutica que contiene insulina humana Gly(A21),Arg(B31),Arg(B32) y un tensioactivo, elegido de un grupo que contiene Tween 20® y Tween 80®; siendo […]
Formulaciones de inulina y de acetato de inulina, del 5 de Junio de 2020, de SOUTH DAKOTA STATE UNIVERSITY (100.0%): Una composición que comprende micropartículas o nanopartículas de acetato de inulina (InAc) y una molécula de carga, en la que la molécula de carga está encapsulada […]
Terapia para la diabetes, del 13 de Mayo de 2020, de BOEHRINGER INGELHEIM INTERNATIONAL GMBH: Un inhibidor de DPP-4, que es linagliptina, para uso terapéutico por administración subcutánea.
Formulaciones farmacéuticas estabilizadas de análogos de insulina y/o derivados de insulina, del 29 de Abril de 2020, de SANOFI: Una formulación farmacéutica que comprende (a) al menos un análogo y/o derivado de insulina, en donde dicho análogo de insulina se selecciona del grupo que […]
Dispositivo, composición y método para el diagnóstico basado en tejidos, del 29 de Abril de 2020, de THE REGENTS OF THE UNIVERSITY OF CALIFORNIA: Un dispositivo para licuar al menos parcialmente un tejido de un sujeto vivo, que comprende: un depósito que se configura para acoplar operativamente […]
Dispositivo tragable para la administración de fármacos, del 22 de Abril de 2020, de Rani Therapeutics, LLC: Un dispositivo ingerible para la administración de un agente terapéutico hacia el interior de una pared luminal del tubo gastrointestinal de un paciente, […]
Preparación farmacéutica que contiene insulina en forma cristalina así como también solubilizada, del 18 de Marzo de 2020, de NOVO NORDISK A/S: Una formulación farmacéutica que comprende insulina humana AspB28, protamina, Zn++, un tampón, un agente de isotonicidad, un compuesto fenólico que es una mezcla de fenol y […]