Composición de liberación sostenida que contiene SDF-1.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/JP2008/003204.
Solicitante: ONO PHARMACEUTICAL CO., LTD..
Nacionalidad solicitante: Japón.
Dirección: 1-5, DOSHOMACHI 2-CHOME CHUO-KU OSAKA 541-0045 JAPON.
Inventor/es: TABATA,Yasuhiko.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K38/22 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 38/00 Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00). › Hormonas (derivados de pro-opiomelanocortina, pro-encefalina o pro-dinorfina A61K 38/33, p. ej. corticotropina A61K 38/35).
- A61K47/42 A61K […] › A61K 47/00 Preparaciones medicinales caracterizadas por los ingredientes no activos utilizados, p. ej. portadores o aditivos inertes; Agentes de direccionamiento o agentes modificadores enlazados químicamente al ingrediente activo. › Proteínas; Polipéptidos; Sus productos de degradación; Sus derivados, p. ej. albúmina, gelatina or zeína (oligopéptidos que contienen hasta cinco aminoácidos A61K 47/18; poliaminoácidos A61K 47/34).
- A61K9/06 A61K […] › A61K 9/00 Preparaciones medicinales caracterizadas por un aspecto particular. › Ungüentos; Excipientes para éstos (aparatos para su fabricación A61J 3/04).
- A61K9/50 A61K 9/00 […] › Microcápsulas (A61K 9/52 tiene prioridad).
- A61P19/08 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › A61P 19/00 Medicamentos para el tratamiento de problemas del esqueleto. › para las enfermedades óseas, p.ej. raquitismo, enfermedad de Paget.
- A61P9/10 A61P […] › A61P 9/00 Medicamentos para el tratamiento de trastornos en el aparato cardiovascular. › para enfermedades isquémicas o ateroscleróticas, p.ej. medicamentos antianginosos, vasodilatadores coronarios,medicamentos para el tratamiento del infarto de miocardio, de la retinopatía, de la insuficiencia cerebrovascular, de la arterioesclerosis renal.
PDF original: ES-2378918_T3.pdf
Fragmento de la descripción:
Composición de liberación sostenida que contiene SDF-1
5 Campo técnico
La presente invención se refiere a una composición de liberación sostenida que contiene SDF-1 que es un tipo de quimoquina. Más específicamente, la presente invención se refiere a una composición de liberación sostenida que contiene SDF-1 y un hidrogel de gelatina succinada o un hidrogel de gelatina sulfoacetilada.
Antecedentes de la técnica
El SDF-1 (factor-1 obtenido de células estromales) es una proteína que pertenece a una familia de quimoquina CXC que contiene 4 restos de cisteína conservados y se reconoce que tiene una pluralidad de isoformas incluyendo a, β y γ. Desde 1993 hasta 1994, se descubrió SDF-1 como una proteína secretora novedosa producida por células estromales de la médula ósea y adicionalmente como una proteína que tiene una función promotora del crecimiento de clones de células progenitoras linfoides-B. A partir de entonces en 1996, se reveló que SDF-1 es una proteína que inhibe un receptor necesario para la invasión del virus de inmunodeficiencia humano (VIH) en una célula hospedadora.
Se ha sabido que ratones sin SDF-1 mueren inmediatamente después del nacimiento y presentan anormalidades en la hematopoyesis en la médula ósea, formación del tabique interventricular o formación de tejido neural. Adicionalmente, se ha revelado que el receptor del SDF-1 es CXCR4 y que el primer SDF-1 entre las quimoquinas forma una relación de ligando-receptor junto con CXRC4.
Una de las acciones fisiológicas del SDF-1 es una acción de inducción de la angiogénesis. La acción de inducción de la angiogénesis de SDF-1 se basa en una acción de reclutamiento de células progenitoras vasculares a un sitio isquémico y ha atraído la atención ya que es un mecanismo diferente de la actividad inductora de angiogénesis debido a factores del crecimiento que tienen una actividad inductora de la angiogénesis intrínseca tal como factor del crecimiento de fibroblastos básico (FGFb) o factor del crecimiento endotelial vascular (VEGF) .
Hasta la fecha, los documentos que vinculan SDF-1 con la angiogénesis han informado que la producción de SDF-1 está inducida por el factor 1 inducible por hipoxia (HIF-1) producido en el sitio isquémico usando modelos animales de elevación de piel dorsal y por consiguiente se provoca la acumulación de células progenitoras vasculares en el sitio isquémico (por ejemplo, véase Nature Medicine, volumen 10 (8) , páginas 858-864 (2004) ) . Adicionalmente, se ha informado que el trasplante de fibroblastos que se han modificado genéticamente para producir SDF-1 en sitios de infarto de miocardio acumula células progenitoras vasculares obtenidas de la médula ósea en los sitios de infarto y adicionalmente mejora la función cardíaca (por ejemplo, véase Lancet (volumen 362, páginas 697-703 (2003) ) . También se ha informado que la administración de genes de SDF-1 a sitios de isquemia de extremidades inferiores ha dado como resultado la observación de angiogénesis y un aumento del volumen del flujo sanguíneo (por ejemplo, refiérase a Circulation, volumen 109, páginas 2454-2461, (2004) ) .
Los ejemplos de composiciones de liberación sostenida que contienen factores de crecimiento que tienen una actividad de angiogénesis incluyen una formulación que combina FGFb con un gel de gelatina reticulado (por 45 ejemplo, véase la Publicación Internacional Nº WO 94/27630) o una formulación que combina un factor de crecimiento de hepatocitos (HGF) con un hidrogel de gelatina (por ejemplo, véase la Publicación Internacional Nº WO 2003/007982) .
Sin embargo, ambas de las técnicas anteriores no muestran la administración externa continua de SDF-1 y no ha existido ninguna composición de liberación sostenida segura que posibilite la manifestación eficaz de una acción farmacológica de SDF-1 y que se pueda administrar a un organismo viviente.
Divulgación de la invención
55 Problemas a solucionar por la invención
En general, cuando se administra una proteína a un organismo viviente en una forma de solución acuosa, se puede obtener un efecto biológico no deseado debido a que la proteína se degrada rápidamente. Con el fin de resolver un problema de este tipo, se han investigado diversas técnicas de liberación sostenida en los últimos años y se ha informado de varias composiciones de liberación sostenida que contienen sustancias fisiológicamente activas. Sin embargo, debido a las estructuras diversas y a las acciones farmacológicas diversas de las proteínas, es extremadamente difícil diseñar preparaciones que puedan impartir eficazmente únicamente una acción farmacológica específica de una proteína determinada a un organismo viviente. Debido a que el mecanismo de trabajo de SDF-1 difiere de factores de crecimiento conocidos previamente que tienen una actividad de angiogénesis 65 y no existe ejemplo de administración externa continua a un organismo viviente, no está para nada claro con respecto a qué concentración local (o concentración en sangre) durante qué duración de acción induciría un efecto farmacológico deseable para un organismo viviente o qué vehículo de liberación sostenida se podría usar con el fin de estabilizar SDF-1 in vivo.
Es decir, un objeto de la presente invención es proporcionar una composición de liberación sostenida que contenga 5 SDF-1, adecuada para inducir una acción fisiológica local y posibilitar la administración segura a un organismo viviente.
Medios para resolver los problemas
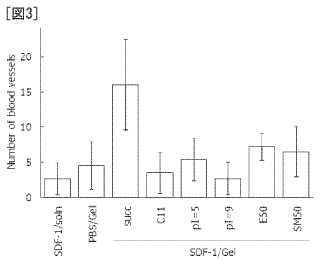
En base a las investigaciones diligentes que usan numerosos vehículos de liberación sostenida, los presentes inventores han observado que un hidrogel de gelatina succinada o un hidrogel de gelatina sulfoacetilada muestra excelentes efectos de liberación sostenida de SDF-1 y que cuando cada hidrogel se administra a un organismo viviente junto con SDF-1, se obtiene un efecto inductor de la angiogénesis visiblemente excelente que no se observa cuando se usan otros vehículos de liberación sostenida. Los presentes inventores condujeron investigaciones adicionales basándose en la apreciación anterior y de esta manera completaron la presente invención.
Por tanto, la presente invención proporciona:
[1] Una composición de liberación sostenida que contiene (1) SDF-1 y (2) un hidrogel que contiene gelatina modificada que tiene un grupo carboxilo y/o un grupo sulfo;
[2] La composición de liberación sostenida de acuerdo con [1], en la que el hidrogel que contiene gelatina modificada que tiene un grupo carboxilo y/o un grupo sulfo es un hidrogel de gelatina succinada, un hidrogel de gelatina sulfoacetilada o una mezcla de los mismos en una proporción arbitraria;
[3] La composición de liberación sostenida de acuerdo con [2], en la que el hidrogel de gelatina succinada, el hidrogel de gelatina sulfoacetilada o la mezcla de los mismos en una proporción arbitraria se produce reticulando gelatina succinada, gelatina sulfoacetilada o una mezcla de las mismas en una proporción arbitraria al punto isoeléctrico de aproximadamente 4, 5 a aproximadamente 5, 0 usando un agente de reticulación;
[4] La composición de liberación sostenida de acuerdo con [2], en la que el hidrogel de gelatina succinada, el hidrogel de gelatina sulfoacetilada o la mezcla de los mismos en una proporción arbitraria se produce reticulando gelatina succinada, gelatina sulfoacetilada o una mezcla de las mismas en una proporción arbitraria a la proporción de modificación de aproximadamente el 15% a aproximadamente el 30% usando un agente de reticulación;
[5] La composición de liberación sostenida de acuerdo con [2], en la que el hidrogel de gelatina succinada, el hidrogel de gelatina sulfoacetilada o la mezcla de los mismos en una proporción arbitraria se produce reticulando gelatina succinada, gelatina sulfoacetilada o una mezcla de las mismas en una proporción arbitraria que tiene un peso molecular promedio de aproximadamente 90.000 a aproximadamente 110.000 usando un agente de reticulación;
[6] La composición de liberación sostenida de acuerdo con [1], en la que SDF-1 es SDF-1α, SDF-1β o una mezcla de los mismos en una proporción arbitraria;
[7] La composición de liberación sostenida de acuerdo con [1] para inyección, administración transnasal, administración transdérmica, administración rectal o implante;
[8] La composición de liberación sostenida de acuerdo con [7] para implante;
... [Seguir leyendo]
Reivindicaciones:
1. Una composición de liberación sostenida que contiene (1) SDF-1 y (2) un hidrogel que contiene gelatina modificada que tiene un grupo carboxilo y/o un grupo sulfo. 5
2. La composición de liberación sostenida de acuerdo con la reivindicación 1, en la que el hidrogel que contiene gelatina modificada que tiene un grupo carboxilo y/o un grupo sulfo es un hidrogel de gelatina succinada, un hidrogel de gelatina sulfoacetilada o una mezcla de los mismos en una proporción arbitraria.
5. La composición de liberación sostenida de acuerdo con la reivindicación 2, en la que el hidrogel de gelatina succinada, el hidrogel de gelatina sulfoacetilada o la mezcla de los mismos en una proporción arbitraria se produce reticulando gelatina succinada, gelatina sulfoacetilada o una mezcla de las mismas en una proporción arbitraria que tiene un peso molecular promedio de aproximadamente 90.000 a aproximadamente 110.000 usando un agente de reticulación. 6. La composición de liberación sostenida de acuerdo con la reivindicación 1, en la que SDF-1 es SDF-1α, SDF-1β o una mezcla de los mismos en una proporción arbitraria. 8. La composición de liberación sostenida de acuerdo con la reivindicación 7 para uso en implante. 10. La composición de liberación sostenida de acuerdo con la reivindicación 8, en la que SDF-1 se libera durante al menos 1 semana. 40 11. La composición de liberación sostenida de acuerdo con la reivindicación 10, en la que SDF-1 se libera durante aproximadamente 1 mes hasta aproximadamente 2 meses. 12. La composición de liberación sostenida de acuerdo con la reivindicación 7, en la que la inyección es inyección de 45 microesfera subcutánea. 13. La composición de liberación sostenida de acuerdo con la reivindicación 1 para su uso en el tratamiento y/o supresión de progresión de síntomas de enfermedad isquémica o enfermedad ósea. 50 14. Una preparación farmacéutica que comprende la composición de liberación sostenida de acuerdo con la reivindicación 1. 15. La preparación farmacéutica de acuerdo con la reivindicación 14 para su uso en el tratamiento y/o supresión de progresión de síntomas de enfermedad isquémica o enfermedad ósea. 55 10 3. La composición de liberación sostenida de acuerdo con la reivindicación 2, en la que el hidrogel de gelatina succinada, el hidrogel de gelatina sulfoacetilada o la mezcla de los mismos en una proporción arbitraria se produce reticulando gelatina succinada, gelatina sulfoacetilada o una mezcla de las mismas en una proporción arbitraria al punto isoeléctrico de aproximadamente 4, 5 a aproximadamente 5, 0 usando un agente de reticulación.
15 4. La composición de liberación sostenida de acuerdo con la reivindicación 2, en la que el hidrogel de gelatina succinada, el hidrogel de gelatina sulfoacetilada o la mezcla de los mismos en una proporción arbitraria se produce reticulando gelatina succinada, gelatina sulfoacetilada o una mezcla de las mismas en una proporción arbitraria a la proporción de modificación de aproximadamente el 15% hasta aproximadamente el 30% usando un agente de reticulación.
30 7. La composición de liberación sostenida de acuerdo con la reivindicación 1 para su uso en una inyección, administración transnasal, administración transdérmica, administración rectal o implante.
35 9. La composición de liberación sostenida de acuerdo con la reivindicación 8, que tiene una proporción de contenido de agua de desde aproximadamente el 95% hasta aproximadamente el 98%.
Patentes similares o relacionadas:
Microesferas o micropartículas biodegradables o bioerosionables de liberación con el tiempo en suspensión en una formulación de fármaco inyectable de formación de depósito solidificante, del 8 de Julio de 2020, de ALLERGAN, INC.: Material compuesto para la administración de fármacos, que comprende: una pluralidad de micropartículas dispersas en una composición de medios; en el que las micropartículas […]
Composiciones tópicas que comprenden un corticosteroide y un retinoide para tratar la psoriasis, del 1 de Julio de 2020, de Bausch Health Ireland Limited: Una composición farmacéutica tópica para usar en el tratamiento de la psoriasis, la composición que comprende: (a) propionato de halobetasol […]
Método para tratar enfermedades recurrentes de la piel y la membrana mucosa provocadas por HSV-1 y HSV-2, del 24 de Junio de 2020, de Tets, Viktor Veniaminovich: Una preparación que incluye una base que contiene 0.5% ó 1% de sal de (2,6-diclorofenil)amida del ácido carbopentoxisulfanílico de fórmula general: **(Ver […]
Composición para uso en el tratamiento de paroniquia, del 24 de Junio de 2020, de Veloce BioPharma LLC: Una composición para uso en el tratamiento de una infección fúngica, micótica, viral y/o bacteriana, en donde la infección es paroniquia, cuya composición comprende: […]
Composiciones biodegradables adecuadas para liberación controlada, del 24 de Junio de 2020, de Ingell Technologies Holding B.V: Composición que comprende un copolímero de bloques triples según la fórmula 1 B-A-B en la que A representa un bloque de poli-(etilenglicol) lineal […]
Emulsión de aceite en agua de monetasona y propilenglicol, del 24 de Junio de 2020, de Galenica AB: Un método para preparar una emulsión de aceite en agua que comprende furoato de mometasona, comprendiendo el método a) preparar una fase oleosa mezclando […]
El ácido glicólico mejora la motilidad del esperma, del 10 de Junio de 2020, de Pan-Montojo, Francisco: Ácido glicólico o una sal o éster farmacéuticamente aceptable del mismo para su uso en el tratamiento o la prevención de la infertilidad masculina mediante […]
Formulación farmacéutica basada en minoxidil para uso tópico y kit de la misma, del 3 de Junio de 2020, de Farmalabor S.r.l: Una disolución viscosa o formulación de gel para el tratamiento tópico de la alopecia androgenética, que comprende: - minoxidil como principio activo a una concentración […]