Un complejo de tomoxiprol amorfo y ciclodextrina con una rápida velocidad de disolución y procedimiento para su preparación.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2012/061261.
Solicitante: Fondazione Istituto Insubrico di Ricerca per la Vita.
Nacionalidad solicitante: Italia.
Dirección: Via Roberto Lepetit, 34 21040 Gerenzano (VA) ITALIA.
Inventor/es: MILANESE, ALBERTO, NEBULONI, MARINO, CARRANO,LUCIA.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K31/4184 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › condensados con carbociclos, p. ej. bencimidazoles.
- A61K47/48
- A61P29/00 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › Agentes analgésicos, antipiréticos o antiinflamatorios que no actúan sobre el sistema nervioso central, p. ej. agentes antirreumáticos; Antiinflamatorios no esteroideos (AINEs).
PDF original: ES-2547920_T3.pdf





Fragmento de la descripción:
Un complejo de tomoxiprol amorfo y ciclodextrina con una rápida velocidad de disolución y procedimiento para su preparación Antecedentes tecnológicos El tomoxiprol, 2- (4-metoxifenil) -3- (1-metiletil) -3H-naft[1, 2-d]imidazol (anteriormente indicado como MDL 035) es un compuesto que pertenece a la clase de los inhibidores de la ciclooxigenasa 2, con actividad analgésica, antiinflamatoria, antiartritis. La eficacia del tomoxiprol contra dichos trastornos se ha demostrado en estudios con animales. En contraste con la mayoría de los fármacos utilizados clínicamente, las dosis activas del compuesto están desprovistas de actividad ulcerogénica (P. Schiatti et al. Arzneim -. Forsch / Drug Res 1986, 36, 102-109; Véase también el documento EP 0 012 866 A1)
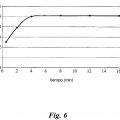
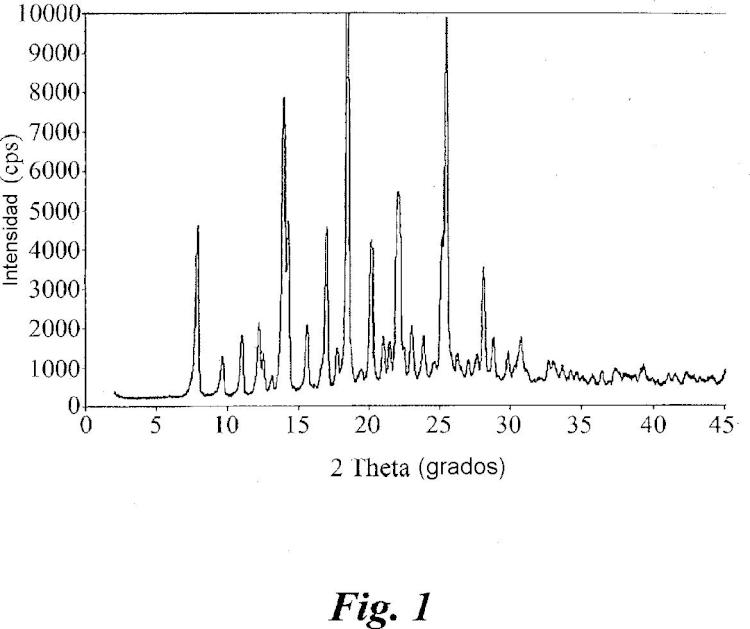
Los estudios farmacocinéticos han demostrado que un porcentaje substancial del tomoxiprol administrado por vía oral se absorbe y da concentraciones adecuadas en la sangre que duran varias horas. Sin embargo, la absorción es lenta, alcanzando la concentración máxima de la substancia en la sangre más de una hora después de la administración (A. Bernareggi et al. J. Liquid Chromatography 1984, 7, 2093-2101) . Debido a su alta lipofilia el tomoxiprol a menos que se ionice es prácticamente insoluble en agua. Es una base débil: a valores de pH inferiores a 2 se ioniza parcialmente y es moderadamente soluble en agua. La velocidad de disolución es lenta, debido a las propiedades físicas de la forma cristalina (Forma I) en la que el compuesto se ha obtenido hasta ahora. La XRPD de los cristales se muestra en la Fig.1.
Dado que la molécula presenta buenas características de penetración de la membrana, su lenta velocidad de disolución en los fluidos gástricos parece ser responsable de su lenta absorción y, en consecuencia de un inicio retrasado de la acción.
El principal uso previsto del tomoxiprol es como analgésico, para el tratamiento de enfermedades como el dolor dental, dolor post-traumático, dolor de cabeza y dismenorrea. Un rápido inicio de la acción terapéutica con el consiguiente alivio del dolor es un aspecto importante del tratamiento médico de dichas enfermedades.
La presente invención se refiere a diferentes enfoques para obtener una velocidad de disolución más rápida de la molécula en condiciones que simulan jugo gástrico, y por consiguiente una más rápida absorción del fármaco.
Primer enfoque: forma amoría o nuevas formas cristalinas.
La lenta velocidad de disolución de los cristales de la Forma I de tomoxiprol (ilustrada en la Fig. 2) es debida a sus características físicas: baja humectabilidad superficial (ángulo de contracto con agua 81º a cualquier pH) y una alta estabilidad de la red cristalina, como se demuestra por el punto de fusión (165ºC) . Los intentos de obtener diferentes formas cristalinas que consisten en disolver la muestra en un disolvente e inducir la precipitación enfriando o concentrando la disolución fracasaron. Se usaron varios disolventes, tales como acetona, etanol anhidro, cloruro de metileno. En todos los casos se observó la Forma I cristalina, punto de fusión 165ºC (determinado por DSC, véase el gráfico dado en la Fig. 5) .
Sorprendentemente, mientras que en etanol anhidro cristalizó la Forma I, en etanol 96% se obtuvo un sólido que consiste principalmente en una nueva forma (Forma II) . Se prepararon cristales puros de la nueva forma disolviendo la muestra en metanol, añadiendo agua para precipitar el compuesto y retirando metanol a vacío. La Forma II en DSC se caracteriza por un punto de fusión de 155ºC, seguido de recristalización a Forma I y subsecuente fusión a 165ºC. Como se predice por los resultados de DSC, la Forma II es inestable e incluso a temperatura ambiente se transforma lentamente en Forma I.
Es sabido que la forma amoría de un producto tiene una velocidad de disolución mucho más rápida que la de la estructura cristalina. Esto es debido al hecho de que las formas amorías tienen mayor superficie específica y su energía de red es mucho más débil que en los cristales. Dichos factores influyen en la velocidad de disolución pero no en la solubilidad absoluta de las diferentes estructuras físicas, que depende de otros factores, principalmente del grado de ionización de la substancia.
Se realizaron intentos de preparar la forma amoría disolviendo la muestra en un disolvente y obteniendo una rápida precipitación por adición lenta de un disolvente en el que el tomoxiprol no es soluble. Por adicción de agua a disoluciones de etanol o acetona, o de éter de petróleo a disoluciones de cloroformo o diclorometano, se produjeron siempre cristales de la Forma I. Disolviendo tomoxiprol en metanol y por adición de agua se obtuvieron los anteriormente descritos cristales de la Forma II.
El único resultado positivo, formación de una forma amoría, se obtuvo por medio de una técnica diferente, que consiste en la evaporación instantánea de una disolución de tomoxiprol. Una disolución de tomoxiprol en etanol se evaporó instantáneamente por secado por pulverización. Se obtuvo una capa amoría vítrea de tomoxiprol. Sin embargo, la substancia era muy inestable y en corto tiempo se transformaba en cristales de Forma I. Por consiguiente parece que la forma amoría del compuesto es intrínsecamente inestable.
Segundo enfoque: complejos de tomoxiprol con ciclodextrinas La bibliografía científica y las patentes informan de muchos ejemplos de incrementar la solubilidad en agua de fármacos formando complejos o aductos de compuestos con ciclodextrinas. Sin embargo, en general, se obtiene solubilidad significativamente mejorada solo con altas relaciones molares de ciclodextrina/substancia activa. En muchos ejemplos, se usan disoluciones de más de 10% (peso/vol) de ciclodextrina para obtener una solubilidad significativa del fármaco (T. Loftsson et al. J. Pharm. Sc. 1996, 85, 1097-1025) . Dichas relaciones fármaco/ciclodextrina son apropiadas para la administración parenteral o para gotas acuosas para los ojos pero la alta cantidad relativa de ciclodextrina con respecto a fármaco las hacen técnicamente inapropiadas para la preparación de comprimidos o cápsulas para administración oral.
En la práctica farmacéutica industrial y en el uso comercial, incluyendo la conformidad de los pacientes, se imponen límites para el tamaño de los dispositivos de suministro oralmente. En general, el contenido total de ingredientes activos de un comprimido o cápsula, preferentemente, no debe exceder del peso de un gramo.
Otra propiedad publicada de los complejos fármaco/ciclodextrina es la estabilización de las formas en estado sólido amorfo o cristalino de producto activo.
Sin embargo, el estado de la técnica muestra que en la mayoría de los casos la estabilización de una forma amoría de una substancia se obtiene con una relación molar de ciclodextrina/substancia mayor de 2. Como ejemplo en el documento US 2006/0135473 se informa de que el complejo beta-ciclodextrina/piroxicam con relación molar 2, 5:1 muestra el mejor rendimiento de estabilización y velocidad de disolución.
Otra enseñanza derivable del estado de la técnica es que en varios casos no es posible obtener aductos substancia/ciclodextrina en los que la substancia esté totalmente presente en forma amoría (M.N. Reddy et al. AAPS
J. 2004, 6, 68-86; S. Rawat et al. Eur. J. Pha.r Biopharm. 2004, 57, 263-267) . Por ejemplo, en dichos documentos se muestra que varios métodos diferentes de preparar un complejo de celecoxib/beta-ciclodextrina dieron solo mezclas de celecoxib cristalino y aductos amorfos. Además, no siempre la formación de un complejo de substancia activa/ciclodextrina estabiliza la forma amoría de la substancia activa (F. Hirayama et al. Pharm. Res. 1994, 11, 1776-70, PubMed 7899242) . En este documento se describe que el complejo de nifedipina/2-hidroxipropil-betaciclodextrina, en lugar de estabilizar la substancia en su forma amoría, acelera su conversión a una forma cristalina. El documento EP 1219306 A describe composiciones que comprenden ciclodextrinas y fármacos de desprendimiento de NO en los que el fármaco está unido a un radical no desprendimiento de NO.
Aunque el tomoxiprol se menciona entre un grupo extremadamente grande de compuestos que se pueden unir a un radical de desprendimiento de NO y a continuación combinar con ciclodextrina, este documento no contiene ninguna descripción de un complejo y método para su preparación en el que la relación molar entre la substancia activa y ciclodextrina tiene un valor predeterminado y no proporciona ninguna indicación o pista o sugerencia para preparar un complejo estable en el que el tomoxiprol esté contenido en una relación molar de casi 1:1 con 2-hidroxipropilbeta-ciclodextrina.... [Seguir leyendo]
Reivindicaciones:
1. Un complejo de tomoxiprol con 2-hidroxipropil beta-ciclodextrina en el que el tomoxiprol está estabilizado en la forma amoría y la relación molar entre tomoxiprol amorfo y 2-hidroxipropil-beta-ciclodextrina varía de 0, 9:1 y 1:1.
2. Un complejo según la reivindicación 1, que es un complejo de tomoxiprol con 2-hidroxipropil-betaciclodextrina en el que el tomoxiprol está estabilizado en la forma amoría y el contenido de tomoxiprol varía de 17 a 18, 5% en peso.
3. Un complejo según una cualquiera de las reivindicaciones 1 y 2 que muestra los siguientes picos de absorción de IR (cm-1) 3343, 2927, 1609, 1526, 1457, 1370, 1250, 1150, 1081, 1020, 947, 838, 801, 752, 700, 575,
521.
4. Un método para producir un complejo de tomoxiprol amorfo con 2-hidroxipropil-beta-ciclodextrina según una cualquiera de las reivindicaciones 1, 2 y 3, que comprende disolver tomoxiprol y 2-hidroxipropil-beta-ciclodextrina en proporción molar de 1:1 a 1:1, 5 en etanol, calentar la mezcla .
3. 40ºC para obtener una disolución transparente, evaporar rápidamente la mezcla de reacción a presión atmosférica bajo una corriente de aire caliente .
4. 50ºC hasta que se forma un residuo sólido, secar el residuo a vacío y, opcionalmente, lavar el polvo amorfo obtenido con etanol frío.
5. Un complejo de tomoxiprol amorfo con 2-hidroxipropil-beta-ciclodextrina según una cualquiera de las reivindicaciones 1, 2 y 3 para su uso como un medicamento.
6. Un complejo para su uso según la reivindicación 5 en el que el medicamento es un agente analgésico, antiinflamatorio y antiartrítico.
7. Una composición farmacéutica que contiene como ingrediente activo un complejo de tomoxiprol amorfo con 2-hidroxipropil-beta-ciclodextrina según una cualquiera de las reivindicaciones 1, 2 y 3.
8. Una composición farmacéutica según la reivindicación 7, que es una forma de dosificación farmacéutica oral.
9. Una forma de dosificación farmacéutica oral según la reivindicación 8 que es un comprimido o cápsula.
10. Un comprimido o una cápsula según la reivindicación 9 que tiene un contenido del complejo de tomoxiprol amorfo con 2-hidroxipropil-beta-ciclodextrina según una cualquiera de las reivindicaciones 1, 2 y 3 que corresponde a de 50 a 150 miligramos de tomoxiprol.
11. Un complejo de tomoxiprol amorfo con 2-hidroxipropil-beta-ciclodextrina según una cualquiera de las reivindicaciones 1, 2 y 3 para su uso como un medicamento para tratar el dolor.
12. Un complejo de tomoxiprol amorfo con 2-hidroxipropil-beta-ciclodextrina para uso según la reivindicación 11, en el que se necesita una rápida absorción de tomoxiprol y rápido inicio de la acción terapéutica.
Patentes similares o relacionadas:
Derivativos del ácido siálico para la derivatización y conjugación de proteínas, del 20 de Diciembre de 2019, de LIPOXEN TECHNOLOGIES LIMITED: Un procedimiento de producción de un derivativo aldehído de un ácido siálico en el que un material de partida que tiene una unidad de ácido siálico en el […]
GELES DE QUITOSANO(A) CONTENIENDO NANOPARTICULAS METALICAS DE COBRE, PLATA Y ANTIBIOTICOS (CIPROFLOXACINO, CEFOTAXIME, GENTAMICINA Y CLOXACILINA), del 12 de Diciembre de 2019, de CARDENAS Y CIA LTDA: En la presente invención se describen geles de quitosano (poli-beta-glucosamina) con propiedades bactericidas y fungicidas en mezcla con nanopartículas […]
Compuestos de polímero de polialquileno y usos de los mismos, del 20 de Noviembre de 2019, de Biogen MA Inc: Una composición farmacéutica que comprende un conjugado y un vehículo, adyuvante, diluyente, conservante y/o solubilizante farmacéuticamente […]
Composiciones y métodos para la liberación dirigida de fármacos in vitro e in vivo a células de mamíferos mediante minicélulas intactas derivadas de bacterias, del 23 de Octubre de 2019, de ENGENEIC MOLECULAR DELIVERY PTY LTD: Una composición que comprende: (a) una pluralidad de minicélulas intactas derivadas de bacterias que tienen paredes celulares intactas, en donde la pluralidad […]
Moléculas con semividas prolongadas, composiciones y usos de las mismas, del 16 de Octubre de 2019, de MEDIMMUNE, LLC: Una molécula modificada que comprende una proteína o agente no de proteína y un dominio constante de IgG, en la que el dominio constante de IgG comprende un dominio CH3 humano […]
Método para la preparación de oligo etilenglicol monodisperso, del 19 de Junio de 2019, de NEKTAR THERAPEUTICS: Un método para preparar un oligo (etilenglicol) monodisperso, comprendiendo dicho método: (i) hacer reaccionar un oligo (etilenglicol) terminado […]
Construcciones de moléculas MHC y sus usos para el diagnóstico y terapia, del 29 de Mayo de 2019, de DAKO DENMARK A/S: Una construcción de moléculas MHC en forma soluble en un medio de solubilización o inmovilizada en un soporte sólido o semi-sólido, comprendiendo dicha construcción de moléculas […]
Usos terapéuticos de anticuerpos monoclonales frente al receptor de la angiotensina II tipo 1, del 17 de Mayo de 2019, de QUEEN MARY AND WESTFIELD COLLEGE: Un anticuerpo monoclonal o un fragmento del mismo que se une al péptido que consiste en la secuencia EDGIKRIQDD para su uso en el tratamiento de la proliferación […]