Células iniciadoras de tumores y procedimientos de uso de las mismas.
Una población de células iniciadoras de tumores aislada, derivada de una población de células tumorales,
comprendiendo la población de células iniciadoras de tumores aislada al menos el 90% de células iniciadoras detumores, en el que las células iniciadoras de tumores (i) expresan 5T4 a un nivel que es al menos 2 veces mayorque el de las células no tumorigénicas del mismo origen, (ii) son tumorigénicas, (iii) son capaces de migración, (iv)son capaces de autorrenovación y (v) generan tumores que comprenden células no tumorigénicas.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2010/028926.
Solicitante: WYETH LLC.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: FIVE GIRALDA FARMS MADISON, NJ 07940 ESTADOS UNIDOS DE AMERICA.
Inventor/es: DAMELIN,MARC ISAAC, GELES,KENNETH G, GOLAS,JONATHON P, BOGHAERT,ERWIN, ZHOU,BIN-BING S.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C12N5/095 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 5/00 Células no diferenciadas humanas, animales o vegetales, p. ej. líneas celulares; Tejidos; Su cultivo o conservación; Medios de cultivo para este fin (reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00). › Células madre; Células progenitoras.
PDF original: ES-2405605_T3.pdf
Fragmento de la descripción:
Células iniciadoras de tumores y procedimientos de uso de las mismas Solicitud relacionada Se reivindica prioridad respecto de la Solicitud Provisional de Estados Unidos Nº 61/164.272, presentada el 27 de marzo del 2009, que se incorpora en el presente documento por referencia en su totalidad.
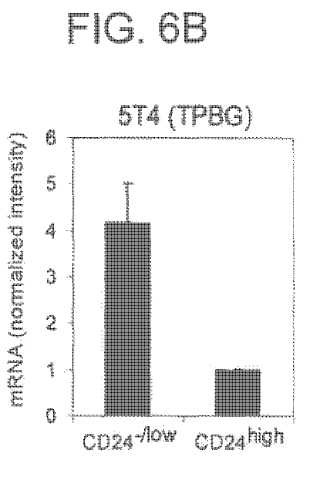
Campo de la invención La presente invención se refiere, en general, a células altamente tumorigénicas, denominadas también células madre cancerosas o células iniciadoras de tumores, a procedimientos para aislarlas y a marcadores de células iniciadoras de tumores para su uso en dichos procedimientos. Más particularmente, la presente invención se refiere a células iniciadoras de tumores que tienen altos niveles de expresión de 5T4 (5T4alto) , opcionalmente con niveles bajos o sin expresión de CD24 (CD24-/bajo) y con expresión de CD44 (CD44+) . Las poblaciones de células iniciadoras de tumores desveladas son útiles para la identificación de nuevos fármacos y dianas para la terapia contra el cáncer y para ensayar la eficacia de fármacos existentes contra el cáncer.
Antecedentes de la invención Las rutas señalizadoras que regulan la autorrenovación y diferenciación contribuyen a la heterogeneidad celular dentro de los tumores. Los diversos estados de autorrenovación y diferenciación se ponen de manifiesto en las subpoblaciones tumorales y células tumorales individuales que presentan niveles dispares de tumorigenicidad in vivo y clonogenicidad in vitro. Véase Lobo y col., Annu. Rev. Cell Dev. Biol., 2007 23: 675-699; Reya y col, Nature, 2001,
414: 105-111. El desarrollo de nuevos modelos tumorales ha comenzado a permitir la caracterización de la heterogeneidad tumoral a niveles celulares. Implantes de tumores sólidos en ratones inmunocomprometidos presentan una rica arquitectura que refleja la histología de la muestra original pero que no está recapitulada en xenoinjertos de líneas celulares cultivadas en suero. El cultivo de células cancerosas en medio asérico definido y/o en matrices tridimensionales conserva las características fisiológicas de las células más que el cultivo en medio con suero (Lee y col., Cancer Cell, 2006, 9: 391-403) . La separación de células activadas por fluorescencia (FACS) de células de tumores, xenoinjertos y líneas celulares ha facilitado la caracterización molecular de subpoblaciones tumorales específicas.
En muchos tumores, las células definidas por marcadores de superficie específicos forman tumores más eficazmente que otras células en el mismo tumor. Estas células se denominan como alternativa células iniciadoras de tumores multipotentes, células madre cancerosas, células iniciadoras de tumores y células iniciadoras de cáncer. Las células iniciadoras de tumores se identificaron en primer lugar en el sistema hematopoyético (Bonnet y Dick, Nat. Med., 1997, 3 (7) : 730-737) y desde entonces se han identificado en tumores sólidos, incluyendo tumores cerebrales, de mama, colon, cabeza y cuello, pulmón, melanoma, páncreas y próstata. Véase Visvader y Lindeman, Nat. Rev. Cancer, 2008, 8: 755-768 y referencias citadas en la misma. En un tipo de tumor particular, puede usarse el mismo conjunto de marcadores de superficie celular para aislar células iniciadoras de tumores de muestras de tumores recientes, xenoinjertos y líneas celulares. Véase por ejemplo, Al-Hajj y col., Proc. Natl. Acad. Sci. USA, 2003, 100: 3983-3988: Filmore y Kuperwasser, Breast Cancer Res., 2008, 10: R25; Hermann y col., Cell Stem Cell, 2007, 1: 313-323; Matsui y col., Blood, 2004, 103: 2332-2336. Se ha mostrado recientemente que CD44, un marcador de células iniciadoras de tumores en diversos tipos de tumores, tiene un papel directo en la tumorigénesis y están reprimidas por p53 (Godar y col., Cell, 2008, 134: 62-73) .
Las células iniciadoras de tumores presentan resistencia a terapias convencionales. Por ejemplo, en muestras de pacientes con cáncer de mama que habían recibido quimioterapia había una gran riqueza de células iniciadoras de tumores, lo que sugiere una explicación para la reincidencia de la enfermedad después del tratamiento (Yu y col., Cell, 2007, 131: 1109-1123) . De manera similar, células iniciadoras de tumor CD133+ en glioblastoma eran resistentes a radiación lo cual erradicaba las células CD133 - más frecuentes (Bao y col., Cancer Res., 2006, 68: 6043-6048) . Por tanto, en el contexto de terapia, la eliminación de células iniciadoras de tumor podría requerir mecanismos diana distintos de los usados para dirigirse al volumen del tumor.
Para desarrollar tratamientos que aumentan significativamente la supervivencia del paciente prolongada en cáncer, las células iniciadoras de tumores responsables de la recurrencia tumoral y metástasis representan una importante diana terapéutica para esta enfermedad. Para acometer dicha necesidad, la presente invención proporciona poblaciones aisladas y enriquecidas de células iniciadoras de tumores que pueden usarse para ensayar la eficacia de nuevos y existentes fármacos contra el cáncer.
Sumario de la invención La presente invención proporciona poblaciones de células iniciadoras de tumor aisladas y enriquecidas. En un aspecto de la invención, una población de células iniciadoras de tumores aislada deriva de una población de células tumorales, comprendiendo la población de células iniciadoras de tumor aislada al menos un 90% de células iniciadoras de tumores, en el que las células iniciadoras de tumores (i) expresan 5T4 a un nivel que es al menos dos
veces superior al de las células no tumorigénicas del mismo origen, (ii) son tumorigénicas, (iii) pueden migrar, (iv) pueden autorrenovarse y (v) generan tumores que comprenden células no tumorigénicas. En otro aspecto de la invención, se proporciona una población de células iniciadoras de tumores enriquecida, que deriva de una población de células tumorales que comprende células iniciadoras de tumores y células no tumorigénicas, y en el que las células iniciadoras de tumores (i) expresan 5T4 a un nivel que es al menos 2 veces superior al de las células no tumorigénicas del mismo origen, (ii) son tumorigénicas, (iii) pueden migrar, (iv) pueden autorrenovarse, (v) generan tumores que comprenden células no tumorigénicas y (vi) están enriquecidas al menos 2 veces en comparación con la población de células tumorales. Las poblaciones de células iniciadoras de tumores aisladas o enriquecidas también pueden expresar CD24 a un nivel que es al menos 2 veces inferior al de las células no tumorigénicas del mismo origen y/o expresar CD44.
También se proporcionan procedimientos de preparación de poblaciones de células iniciadoras de tumores aisladas y enriquecidas. Por ejemplo, un procedimiento representativo de aislamiento o enriquecimiento de una población de células iniciadoras de tumores incluye las etapas de (a) proporcionar células tumorales disociadas, en el que una mayoría de las células exprese 5T4 a un nivel bajo y una minoría de las células exprese 5T4 a un nivel alto; (b) poner en contacto las células tumorales disociadas con un agente que se una específicamente a 5T4; y (c) seleccionar células que se unan específicamente al agente de (b) a un grado que presente un nivel alto de expresión de 5T4 que sea al menos aproximadamente 2 veces mayor que el nivel bajo; mediante lo cual una población de células iniciadoras de tumores se aísla o enriquece. Opcionalmente, los procedimientos para preparar una población de células iniciadoras de tumor que expresen 5T4 aisladas o enriquecidas incluye las etapas adicionales de poner en contacto las células tumorales disociadas con un agente que se une específicamente a CD44; y seleccionar células que se unen específicamente al agente para un nivel que presente expresión de CD44. Opcionalmente, los procedimientos para la preparación de una población de células iniciadoras de tumor que expresen 5T4 aislada o enriquecida también pueden incluir las etapas de poner en contacto las células tumorales disociadas con un agente que se una específicamente a CD24; y seleccionar células que se unan específicamente al agente a un grado que presente un nivel bajo de expresión de CD24 que sea al menos aproximadamente 5 veces inferior al de las células no tumorigénicas del mismo origen. Como alternativa, la población de células iniciadoras de tumores puede enriquecerse cultivando las células tumorales primarias en condiciones aséricas. En otro procedimiento representativo adicional de la invención, el aislamiento o enriquecimiento de una población de células iniciadoras de tumores que expresen 5T4 puede incluir poner en contacto las células tumorales disociadas con un agente que se una específicamente a CD24; y agotar las células que se unan específicamente al agente a... [Seguir leyendo]
Reivindicaciones:
1. Una población de células iniciadoras de tumores aislada, derivada de una población de células tumorales, comprendiendo la población de células iniciadoras de tumores aislada al menos el 90% de células iniciadoras de tumores, en el que las células iniciadoras de tumores (i) expresan 5T4 a un nivel que es al menos 2 veces mayor que el de las células no tumorigénicas del mismo origen, (ii) son tumorigénicas, (iii) son capaces de migración, (iv) son capaces de autorrenovación y (v) generan tumores que comprenden células no tumorigénicas.
2. La población de células iniciadoras de tumores aislada de la reivindicación 1, que comprende al menos el 95% de células iniciadoras de tumores.
3. La población de células iniciadoras de tumores aislada de la reivindicación 1, en la que las células iniciadoras de tumores comprenden menos de aproximadamente el 50% de la población de células tumorales a partir de la cual deriva, tal como menos de aproximadamente el 33%, menos de aproximadamente el 25%, menos de aproximadamente el 15% o menos de aproximadamente 10% de la población de células de tumores de la cual deriva.
4. Una población de células iniciadoras de tumores enriquecida derivada de una población de células de tumores que comprende células iniciadoras de tumores y células no tumorigénicas, en la que las células iniciadoras de tumores (i) expresan 5T4 a un nivel que es al menos 2 veces mayor que el de las células no tumorigénicas del mismo origen, (ii) son tumorigénicas, (iii) son capaces de migración, (iv) son capaces de autorrenovación y (v) generan tumores que comprenden células no tumorigénicas y (vi) están enriquecidas al menos 2 veces en comparación con la población de células tumorales.
5. La población de células iniciadoras de tumores enriquecida de la reivindicación 4, en la que las células iniciadoras de tumores están enriquecidas al menos 5 veces en comparación con la población de células tumorales, tal como al menos 10 veces, al menos 50 veces, o al menos 100 veces en comparación con la población de células tumorales.
6. La población de células iniciadoras de tumores aislada de la reivindicación 1 o la población de células iniciadoras de tumores enriquecidas de la reivindicación 4, que expresa 5T4 a un nivel que es al menos 5 veces mayor que el de las células no tumorigénicas del mismo origen, tal como al menos 10 veces mayor que el de las células no tumorigénicas del mismo origen.
7. La población de células iniciadoras de tumores aislada de la reivindicación 1 o la población de células iniciadoras de tumores enriquecidas de la reivindicación 4, que adicionalmente expresa CD24 a un nivel que es al menos 5 veces inferior al de las células no tumorigénicas del mismo origen, y/o que expresan adicionalmente CD44.
8. La población de células iniciadoras de tumores aislada de la reivindicación 1 o la población de células iniciadoras de tumores enriquecidas de la reivindicación 4, que deriva de un tumor pulmonar.
9. La población de células iniciadoras de tumores aislada de la reivindicación 1 o la población de células iniciadoras de tumores enriquecidas de la reivindicación 4, en la que una subpoblación de aproximadamente 10 células o menor de la población de células iniciadoras de tumores aislada tiene la capacidad de formar un tumor palpable.
10. Un procedimiento para aislar o enriquecer una población de células iniciadoras de tumores que comprende:
(a) proporcionar células tumorales disociadas, en el que una mayoría de las células expresan 5T4 a un nivel bajo y una minoría de las células expresa 5T4 a un nivel alto;
(b) poner en contacto las células tumorales disociadas con un agente que se una específicamente a 5T4, tal como un anticuerpo anti-5T4; y
(c) seleccionar células que se unen específicamente al agente de (b) a un grado que presente un nivel alto de expresión de 5T4 que sea al menos aproximadamente 2 veces mayor que el nivel bajo; mediante el cual una población de células iniciadoras de tumores es aislada o es enriquecida.
11. El procedimiento de la reivindicación 10, en el que la población de células iniciadoras de tumores aislada o enriquecida comprende al menos el 95% de células iniciadoras de tumores.
12. El procedimiento de la reivindicación 10, mediante el cual la población de células iniciadoras de tumores está enriquecida en células iniciadoras de tumores al menos 2 veces en comparación con las células tumorales disociadas, tal como al menos 5 veces o al menos 10 veces en comparación con las células tumorales disociadas.
13. El procedimiento de la reivindicación 11, en el que las células tumorales disociadas son células cancerosas pulmonares.
14. El procedimiento de la reivindicación 10, en el que la selección de células se realiza mediante citometría de flujo, selección de células activada por fluorescencia, inmunopurificación, separación en columnas por afinidad o selección magnética.
15. El procedimiento de la reivindicación 10, que comprende adicionalmente (d) poner en contacto las células
tumorales disociadas con un agente que se una específicamente a CD44, tal como un anticuerpo anti-CD44; y (e) seleccionar células que se unen específicamente al agente de (d) en una medida que presente expresión de CD44.
16. El procedimiento de la reivindicación 10 o 15, que comprende adicionalmente:
(d) poner en contacto las células tumorales disociadas con un agente que se una específicamente a CD24, tal como un anticuerpo anti-CD24; y
(e) seleccionar células que se unen específicamente al agente de (d) en una medida que presente un bajo nivel de expresión de CD24 que sea al menos aproximadamente 5 veces inferior al de las células no tumorigénicas del mismo origen.
17. El procedimiento de la reivindicación 10 o 15, que comprende adicionalmente:
(d) poner en contacto las células tumorales disociadas con un agente que se una específicamente a CD24, tal como un anticuerpo anti-CD24; y
(e) empobrecer células que se unen específicamente al agente de (d) en una medida que muestre un alto nivel de expresión de CD24 que sea al menos aproximadamente 5 veces mayor que el de las células no tumorigénicas del mismo origen.
18. El procedimiento de la reivindicación 10, que adicionalmente comprende:
(d) poner en contacto las células tumorales disociadas con uno o más agentes que se unan específicamente a un marcador de diferenciación expresado por las células tumorales; y
(e) empobrecer la población de células iniciadoras de tumores de células que se unan específicamente a uno o más agentes de (d) .
19. Una población de células iniciadoras de tumores aislada o enriquecida preparada de acuerdo con el procedimiento de una cualquiera de las reivindicaciones 10-18.
20. Un procedimiento para ensayar la eficacia de un fármaco contra el cáncer o un fármaco candidato contra el cáncer que comprende:
(a) proporcionar una población de células iniciadoras de tumores aislada o enriquecida de acuerdo con una cualquiera de las reivindicaciones 1-9 o 19;
(b) poner en contacto las células iniciadoras de tumores con un fármaco contra el cáncer o un fármaco candidato contra el cáncer; y
(c) observar un cambio en el potencial tumorigénico de las células iniciadoras de tumores después de poner en contacto las células iniciadoras de tumores con el fármaco contra el cáncer o fármaco candidato contra el cáncer.
Patentes similares o relacionadas:
Método de producción de citoblastos pluripotentes que tienen un gen receptor de linfocitos T específico de antígenos, del 11 de Marzo de 2020, de Kawamoto, Hiroshi: Un método in vitro de inducir linfocitos T para una inmunoterapia basada en células, que comprende las etapas de: proporcionar citoblastos pluripotentes […]
Método para el aislamiento de células madre de mamíferos y usos de las mismas, del 11 de Marzo de 2020, de Hyperstem SA: Un método para producir una población aislada de células madre tumorales de mamíferos enriquecidas en células madre cancerosas (CMC) o células […]
Preparaciones farmacéuticas de células EPR humanas y usos de las mismas, del 5 de Junio de 2019, de Astellas Institute for Regenerative Medicine: Una composición farmacéutica que comprende: una pluralidad de células epiteliales pigmentarias de la retina (EPR); y un vehículo farmacéuticamente aceptable; […]
Selección como diana de un nicho de células madre de cáncer quiescentes, del 3 de Abril de 2019, de THE REGENTS OF THE UNIVERSITY OF CALIFORNIA: Método para predecir la capacidad farmacológica de una célula madre de leucemia (LSC), comprendiendo el método: (i) detectar y cuantificar en al menos una o una pluralidad […]
Métodos y materiales para la diferenciación hematoendotelial de células madre pluripotentes humanas en condiciones definidas, del 6 de Marzo de 2019, de WISCONSIN ALUMNI RESEARCH FOUNDATION: Un medio de cultivo celular sin xenógenos y sin albúmina adecuado para la diferenciación hematoendotelial de células madre pluripotentes humanas, en donde el […]
Procedimiento para el cultivo de una subpoblación de células tumorales epiteliales circulantes de un líquido corporal, del 14 de Marzo de 2018, de Pachmann, Ulrich: Procedimiento para el cultivo de células tumorales epiteliales circulantes de un líquido corporal de un ser humano o un animal que padece […]
Ensayos de detección para identificación y validación de agentes que se direccionan a células madre de cáncer, del 26 de Julio de 2017, de MCMASTER UNIVERSITY: Un método para identificar y validar un agente de prueba como un agente selectivo de células madre anticáncer, comprendiendo el método: […]
Método para aislar una célula cancerosa resistente a agentes quimioterapéuticos con propiedades de célula madre, del 12 de Abril de 2017, de THE ROGOSIN INSTITUTE, INC: Un método para determinar el pronóstico de un sujeto que padece cáncer, que comprende: i) encapsular una muestra de células cancerosas tomadas de dicho sujeto en […]