ANTICUERPOS MONOCLONALES PARA EL FACTOR DE CRECIMIENTO DE HEPATOCITOS.
Anticuerpo monoclonal humanizado o quimérico (mAb) que compite con el anticuerpo L2G7 producido por el hibridoma nº de ATCC:
PTA-5162 para la unión al factor de crecimiento de hepatocitos (HFG), y que neutraliza el HGF e inhibe el crecimiento de un xenoinjerto de tumor humano en un ratón como un agente único
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2004/026565.
Solicitante: GALAXY BIOTECH, LLC.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 22830 SAN JUAN ROAD,CUPERTINO CA 95014.
Inventor/es: KIM, KYUNG, JIN, SU,YI-CHI.
Fecha de Publicación: .
Fecha Concesión Europea: 14 de Julio de 2010.
Clasificación Internacional de Patentes:
- C07K16/22 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 16/00 Inmunoglobulinas, p. ej. anticuerpos mono o policlonales. › contra factores de crecimiento.
Clasificación PCT:
- A61K39/395 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 39/00 Preparaciones medicinales que contienen antígenos o anticuerpos (materiales para ensayos inmunológicos G01N 33/53). › Anticuerpos (aglutininas A61K 38/36 ); Inmunoglobulinas; Inmunosuero, p. ej. suero antilinfocitario.
- A61P35/00 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › Agentes antineoplásicos.
- C07K16/22 C07K 16/00 […] › contra factores de crecimiento.
- C07K16/30 C07K 16/00 […] › de células tumorales.
- C12N5/20 C […] › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 5/00 Células no diferenciadas humanas, animales o vegetales, p. ej. líneas celulares; Tejidos; Su cultivo o conservación; Medios de cultivo para este fin (reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00). › siendo uno de los integrantes de la fusión un linfocito B.
Clasificación antigua:
- A61K39/395 A61K 39/00 […] › Anticuerpos (aglutininas A61K 38/36 ); Inmunoglobulinas; Inmunosuero, p. ej. suero antilinfocitario.
- C07K16/22 C07K 16/00 […] › contra factores de crecimiento.
- C12N5/20 C12N 5/00 […] › siendo uno de los integrantes de la fusión un linfocito B.
- G01N33/53 FISICA. › G01 METROLOGIA; ENSAYOS. › G01N INVESTIGACION O ANALISIS DE MATERIALES POR DETERMINACION DE SUS PROPIEDADES QUIMICAS O FISICAS (procedimientos de medida, de investigación o de análisis diferentes de los ensayos inmunológicos, en los que intervienen enzimas o microorganismos C12M, C12Q). › G01N 33/00 Investigación o análisis de materiales por métodos específicos no cubiertos por los grupos G01N 1/00 - G01N 31/00. › Ensayos inmunológicos; Ensayos en los que interviene la formación de uniones bioespecíficas; Materiales a este efecto.
- G01N33/563 G01N 33/00 […] › en los que interviene fragmentos de anticuerpos.
- G01N33/574 G01N 33/00 […] › para el cáncer.
- G01N33/577 G01N 33/00 […] › en los que interviene anticuerpos monoclonados.
Fragmento de la descripción:
Anticuerpos monoclonales para el factor de crecimiento de hepatocitos.
Campo de la invención
La presente invención se refiere en general a la combinación de anticuerpo monoclonal (mAb) y tecnologías de ADN recombinante para desarrollar nuevos compuestos biológicos y más particularmente, por ejemplo a la producción de anticuerpos monoclonales que se enlazan a y neutralizan el factor de crecimiento de hepatocito.
Antecedentes de la invención
El factor de crecimiento de hepatocito humano (HGF) es un polipéptido heterodimérico multifuncional producido por células mesenquimales. Se ha demostrado que el HGF estimula la angiogénesis, morfogénesis y mitogenesis, así como el crecimiento y dispersión de varios tipos de células (Bussolino et al., J. Cell. Biol. 119:629, 1992; Zarnegar and Michalopoulos, J. Cell. Biol. 129:1177, 1995; Matsumoto et al., Ciba. Found. Symp. 212:198, 1997; Birchmeier y Gherardi, Trends Cell. Biol. 8:404, 1998; Xin et al. Am. J. Pathol. 158:1111, 2001). Las actividades pleiotrópicas de HGF son mediadas por medio de su receptor, una tirosina quinasa de transmembrana codificada por el protooncogén cMet. Además de regular una variedad de funciones celulares normales el HGF y su receptor c-Met han demostrado estar involucrados en el inicio, la invasión y la metástasis de tumores (Jeffers et al., J. Mol. Med. 74:505, 1996; Comoglio y Trusolino, J. Clin. Invest. 109:857, 2002). HGF/cMet son coexpresados, frecuentemente sobreexpresados sobre varios tumores sólidos humanos en los que se incluyen tumores derivado de pulmón, colon, recto, estómago, riñón, ovario, piel, mieloma múltiple y tejido tiroides (Prat et al., Int. J. Cancer 49:323, 1991; Chan et al., Oncogen 2:593, 1988, Weidner et al., Am. J. Respir. Cell. Mol. Biol. 8:229, 1993; Derksen et al., Blood 99:1405, 2002). HGF actúa como un factor de crecimiento autocrino (Rong et al., Proc. Nacional. Acad. Sci. USA 91:4731, 1994; Koochekpour et al., Cancer Res. 57:5391; 1997) y paracrino (Weidner et al., Am. J. Respir. Cell. Mol. Biol. 8:229, 1993) y regulador antiapoptótico (Gao et al., J. Biol. Chem. 276:47257, 2001) para estos tumores.
HGF es una proteína de 102 kDa con secuencia y similaridad estructural al plasminógeno y otras enzimas de la coagulación de la sangre (Nakamura et al., Nature 342:440, 1989; Weidner et al., Am. J. Respir. Cell. Mol. Biol. 8:229, 1993, cada una de las cuales es incorporada a la presente memoria como referencia) (Figura 1). El HGF humano es sintetizado como un precursor de 728 aminoácidos (preproHGF), que sufre escisión intracelular a una forma de una sola cadena inactiva (proHGF) (Nakamura et al., Nature 342:440, 1989; Rosen et al., J. Cell. Biol. 127:1783, 1994). En la secreción extracelular, el proHGF es escindido para producir la molécula heterodimérica disulfuro-enlazada biológicamente activa compuesta de una a-subunidad y ß-subunidad (Nakamura et al., Nature 342:440, 1989; Naldini et al., EMBO J. 11:4825, 1992). La a-subunidad contiene 440 residuos (69 kDa con glicosilación), constituida por el dominio de horquilla N-terminal y cuatro dominios kringle. La ß-subunidad contiene 234 residuos (34 kDa) y tiene un dominio semejante a serina proteasa, que carece de actividad proteolítica. La escisión de HGF es requerida para la activación del receptor, pero no para el enlace del receptor (Hartmann et al., Proc. Natl. Acad. Sci. USA 89:11574, 1992; Lokker et al., J. Biol. Chem. 268:17145, 1992). HGF contiene 4 sitios de N-glicosilación supuestos, 1 en la a-subunidad y 3 en la ß-subunidad. El HGF presenta 2 sitios de enlace específico de célula únicos: un sitio de enlace de alta afinidad (Kd = 2 x 10-10 M) para el receptor cMet y un sitio de enlace de baja afinidad (Kd = 10-9 M) para proteoglicanos de sulfato heparina (HSPG), que están presentes sobre la superficie celular y la matriz extracelular (Naldini et al., Oncogene 6:501, 1991; Bardelli et al., J. Biotechnol. 37:109, 1994; Sakata et al., J. Biol. Chem., 272:9457, 1997). La NK2 (una proteína que comprende el N-término y los primeros dos dominios kringle de la a-subunidad) es suficiente para el enlace a cMet y activación de la cascada de señal para mobilidad, sin embargo la proteína de plena longitud es requerida para la respuesta mitogénica (Weidner et al., Am. J. Respir. Cell. Mol. Biol. 8:229, 1993). HSPG se enlaza al HGF al interactuar con el término N de HGF (Aoyama, et al., Biochem. 36:10286, 1997; Sakata, et al., J. Biol. Chem. 272:9457, 1997). Las funciones postuladas para la interacción HSPG-HGF incluyen la mejora de la biodisponibilidad de HGF, actividad biológica y oligomerización (Bardelli, et al., J. Biotechnol. 37:109,1994; Zioncheck et al., J. Biol. Chem. 270:16871, 1995).
El cMet es un elemento de la familia de receptor de proteína tirosina quinasa clase IV. El gen cMet de plena longitud fue clonado e identificado como el protooncógeno cMet (Cooper, et al., Nature 311:29, 1984; Park et al., Proc. Natl. Acad. Sci. USA 84:6379, 1987). El receptor cMet es sintetizado inicialmente como un precursor de una sola cadena, parcialmente glicosilado, p170(MET) (figura 1)(Park et al., Proc. Natl. Acad. Sci. USA 84:6379, 1987; Giordano et al., Nature 339:155, 1989; Giordano et al., Oncogene 4:1383, 1989; Bardelli et al., J. Biotechnol. 37:109, 1994). Después de la glicosilación adicional, la proteína es escindida proteolíticamente a una proteína madura de 190 kDa heterodimérica (1.385 aminoácidos), constituida por la a-subunidad de 50 kDa (residuos 1-307) y la ß-subunidad de 145 kDa. El dominio de tirosina quinasa citoplásmica de la ß-subunidad está involucrado en la transducción de señal.
Varios procedimientos diferentes han sido investigados para obtener una molécula antagónica de la interacción HGF/cMet: proteínas HGF truncadas tales como NK1 (dominio N terminal más dominio kringle 1; Lokker et al., J. Biol. Chem. 268:17145, 1993), NK2 (dominio N terminal más dominios kringle 1 y 2; Chan et al., Science 254:1382, 1991) y NK4 (dominio N-terminal más cuatro dominios kringle; Kuba et al., Cancer Res. 60:6737, 2000), mAbs anti-cMet (Dodge, Master's Thesis, San Francisco State University, 1998) y mAbs anti-HGF (Cao et al., Proc. Natl. Acad. Sci. USA 98:7443, 2001, que es incorporado a la presente memoria como referencia).
NK1 y NK2 pueden competir efectivamente con el enlace de HGF a su receptor, pero han demostrado tener actividades agonistas parciales in vitro (Cioce et al., J. Biol. Chem. 271:13110, 1996; Schwall et al., J. Cell. Biol. 133:709, 1996), en lugar de actividades puramente antagonistas como se desea. Más recientemente, Kuba et al., Cancer Res. 60:6737, 2000, demostraron que NK4 podría inhibir parcialmente el crecimiento primario (figura 2) y la metástasis de tumor de pulmón murino LLC en un modelo de ratón desnudo mediante infusión continua de NK4. El hecho de que NK4 se deba administrar continuamente para obtener una inhibición de crecimiento parcial de tumores primarios indica una vida media potencialmente corta de la molécula NK4 y/o carencia de potencia. En comparación con NK4, la utilización de anticuerpos se beneficiará de su farmacocinética favorable y la posibilidad de obtener anticuerpos con potencia mucho más alta.
Como otro enfoque, Dodge (Master's Thesis, San Francisco State University, 1998) generó anticuerpos (mAbs) monoclonales anti-cMet antagónicos. Un mAb, 5D5, exhibió fuerte actividad antagónica en ELISA, pero indujo una respuesta proliferativa de cMet que expresa células BAF-3, supuestamente debido a la dimerización de los receptores de membrana. Prat et al., J. Cell. Sci. 111:237, 1998, también se informó de dichas actividades agonistas de mAbs anti-cMet. Zaccolo et al., Eur. J. Immunol 27:618, 1997, usaron métodos de exhibición de fago para desarrollar fragmentos de Fab humanos contra factor de crecimiento de hepatocitos de ratón y humano. Estos fragmentos Fab no tuvieron ningún efecto sobre la actividad de HGF cuando se usaron solos. Cuando uno de los fragmentos de Fab HGF anti-humano fue combinado con un anticuerpo que se enlazó al fragmento Fab por sí mismo, mejoró realmente la actividad de HGF en un análisis biológico.
Cao et al., Proc. Natl. Acad. Sci. USA 98:7443, 2001 demostraron que la administración de un cóctel de tres mAbs anti-HGF, los cuales fueron seleccionados sobre la base de su capacidad para inhibir la actividad...
Reivindicaciones:
1. Anticuerpo monoclonal humanizado o quimérico (mAb) que compite con el anticuerpo L2G7 producido por el hibridoma nº de ATCC: PTA-5162 para la unión al factor de crecimiento de hepatocitos (HFG), y que neutraliza el HGF e inhibe el crecimiento de un xenoinjerto de tumor humano en un ratón como un agente único.
2. mAb según la reivindicación 1 que es un fragmento Fab o F(ab')2 o un anticuerpo de cadena única.
3. mAb según cualquiera de las reivindicaciones anteriores, que inhibe la unión del HFG al cMet por lo menos 50%.
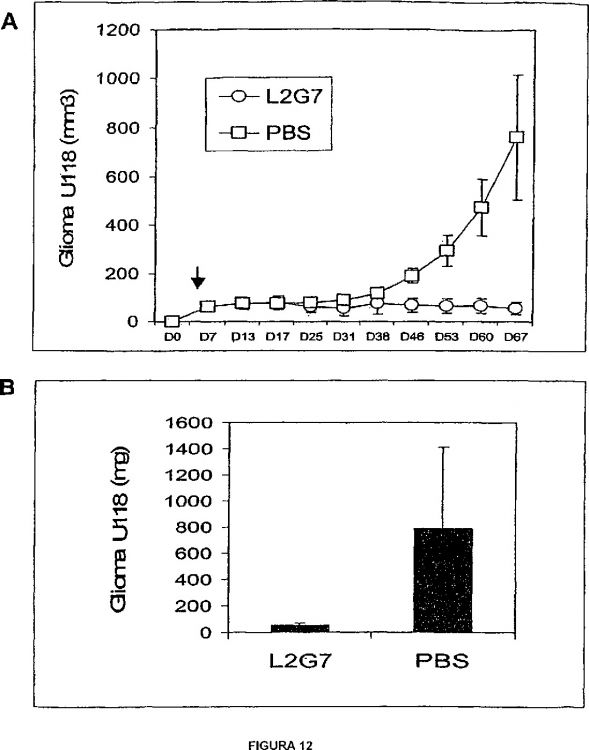
4. mAb según cualquiera de las reivindicaciones anteriores, que inhibe el crecimiento de un xenoinjerto de tumor de glioblastoma humano U118 en un ratón.
5. mAb según cualquiera de las reivindicaciones anteriores que inhibe la angiogénesis inducida por el HGF.
6. mAb según cualquiera de las reivindicaciones anteriores que se une específicamente a HGF con una afinidad de unión de por lo menos 108 M-1.
7. mAb según la reivindicación 1, que es un mAb L2G7 quimérico o humanizado.
8. Línea celular que produce un mAb según cualquiera de las reivindicaciones anteriores.
9. Composición farmacéutica que comprende un anticuerpo monoclonal (mAb) a una concentración de 1 a 100 mg/ml en un portador fisiológicamente aceptable, en la que el mAb compite con un anticuerpo producido por el hibridoma nº de ATCC: PTA-5162 para la unión del factor de crecimiento de hepatocitos (HGF), y que neutraliza el HGF e inhibe el crecimiento de un xenoinjerto de tumor de glioblastoma humano U118 en un ratón como agente único.
10. Composición farmacéutica según la reivindicación 9, en la que el mAb es un mAb según cualquiera de las reivindicaciones 1 a 8.
11. Anticuerpo monoclonal (mAb) que compite con el anticuerpo producido por el hibridoma nº de ATCC: PTA-5162 para la unión al factor de crecimiento de hepatocitos (HGF), y que neutraliza el HGF e inhibe el crecimiento de un xenoinjerto de tumor de glioblastoma humano U1118 en un ratón como agente único, para la utilización en el tratamiento del cáncer en un paciente a una dosis de 0,1 a 5 mg/kg o hasta 10, 15 ó 20 mg/kg.
Patentes similares o relacionadas:
 Métodos para producir proteínas bicatenarias en bacterias, del 29 de Julio de 2020, de GENENTECH, INC.: Un método para producir un receptor de linfocitos T monoclonal de movilización inmunitaria contra el cáncer (ImmTAC) que comprende una cadena alfa del receptor de linfocitos […]
Métodos para producir proteínas bicatenarias en bacterias, del 29 de Julio de 2020, de GENENTECH, INC.: Un método para producir un receptor de linfocitos T monoclonal de movilización inmunitaria contra el cáncer (ImmTAC) que comprende una cadena alfa del receptor de linfocitos […]
Método para el tratamiento de la osteoporosis, del 22 de Julio de 2020, de AMGEN INC.: Un anticuerpo antiesclerostina que comprende una CDR-H1 de la SEQ ID NO: 245, una CDR-H2 de la SEQ ID NO: 246, una CDR-H3 de la SEQ ID NO: 247, […]
Anticuerpo anti-FGF23 y composición farmacéutica que comprende el mismo, del 15 de Julio de 2020, de Kyowa Kirin Co., Ltd: Anticuerpo o fragmento funcional del mismo que se une a la totalidad o a una parte del epítopo de FGF23 humano, al que se une un anticuerpo producido […]
Anticuerpos scFv que pasan las capas epitelial y/o endotelial, del 1 de Julio de 2020, de ESBATech, an Alcon Biomedical Research Unit LLC: Un anticuerpo monocatenario (scFv) que comprende: (a) un dominio variable de la cadena ligera (VL) que tiene tres regiones CDR de VL no […]
 Tratamiento del cáncer usando inhibidores de TGF-beta y PD-1, del 24 de Junio de 2020, de XOMA TECHNOLOGY LTD.: Un inhibidor del factor de crecimiento transformante beta (TGFβ) y un inhibidor de la proteina de muerte celular programada 1 (PD-1) para usar en un metodo […]
Tratamiento del cáncer usando inhibidores de TGF-beta y PD-1, del 24 de Junio de 2020, de XOMA TECHNOLOGY LTD.: Un inhibidor del factor de crecimiento transformante beta (TGFβ) y un inhibidor de la proteina de muerte celular programada 1 (PD-1) para usar en un metodo […]
Métodos para el tratamiento de la enfermedad ocular en sujetos humanos, del 10 de Junio de 2020, de Clearside Biomedical, Inc: Una formulación farmacéutica que comprende un fármaco para su uso en un método de tratamiento de un trastorno ocular posterior en un sujeto humano que […]
Método para tratar la pérdida de hueso alveolar mediante el uso de anticuerpos antiesclerostina, del 3 de Junio de 2020, de AMGEN INC.: Un anticuerpo antiesclerostina para su uso en un método para aumentar la altura del hueso alveolar en un sujeto que padece pérdida de hueso alveolar, donde […]
Proteínas de captura de la superficie celular recombinantes, del 13 de Mayo de 2020, de REGENERON PHARMACEUTICALS, INC.: Un método para detectar y aislar células que producen altos niveles de una proteína heterodimérica que tiene una primera subunidad y una segunda subunidad, […]