ANTICUERPOS CONTRA EL RECEPTOR DEL FACTOR I DE CRECIMIENTO SIMILAR A INSULINA Y USOS DE LOS MISMOS.
Anticuerpo ligante de IGF-1R humano, caracterizado porque comprende:
a) una cadena pesada de anticuerpo que comprende como CDRs, la CDR1 de aminoácidos 31 a 35, la CDR2 de aminoácidos 50 a 66, y la CDR3 de aminoácidos 99 a 107 de secuencia SEC ID nº 1, y una cadena ligera de anticuerpo que comprende como CDRs, la CDR1 de aminoácidos 24 a 34, la CDR2 de aminoácidos 50 a 56 y la CDR3 de aminoácidos 89 a 98 de secuencia SEC ID nº 2, o b) una cadena pesada de anticuerpo que comprende como CDRs, la CDR1 de aminoácidos 31 a 35, la CDR2 de aminoácidos 50 a 66, y la CDR3 de aminoácidos 99 a 107 de secuencia SEC ID nº 3, y una cadena ligera de anticuerpo que comprende como CDRs, la CDR1 de aminoácidos 24 a 34, la CDR2 de aminoácidos 50 a 56 y la CDR3 de aminoácidos 89 a 98 de secuencia SEC ID nº 4
Tipo: Patente Europea. Resumen de patente/invención. Número de Solicitud: E08007731.
Solicitante: F. HOFFMANN-LA ROCHE AG.
Nacionalidad solicitante: Suiza.
Dirección: GRENZACHERSTRASSE 124 4070 BASEL SUIZA.
Inventor/es: MUNDIGL, OLAF, KOPETZKI, ERHARD, SCHUMACHER, RALF, KUENKELE,KLAUS-PETER, PARREN,PAUL, REBERS,FRANK, VAN DE WINKEL,JAN, VAN VUGT,MARTINE, Graus,Yvo.
Fecha de Publicación: .
Fecha Solicitud PCT: 9 de Julio de 2004.
Clasificación Internacional de Patentes:
- C07K16/28G
- C07K16/28Z
Clasificación PCT:
- A61K39/395 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 39/00 Preparaciones medicinales que contienen antígenos o anticuerpos (materiales para ensayos inmunológicos G01N 33/53). › Anticuerpos (aglutininas A61K 38/36 ); Inmunoglobulinas; Inmunosuero, p. ej. suero antilinfocitario.
- C07K16/28 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 16/00 Inmunoglobulinas, p. ej. anticuerpos mono o policlonales. › contra receptores, antígenos celulares de superficie o determinantes celulares de superficie.
- C12N15/13 C […] › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 15/00 Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K). › Inmunoglobulinas.
- C12N5/16 C12N […] › C12N 5/00 Células no diferenciadas humanas, animales o vegetales, p. ej. líneas celulares; Tejidos; Su cultivo o conservación; Medios de cultivo para este fin (reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00). › Células animales.
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Eslovenia, Finlandia, Rumania, Chipre, Lituania, Letonia.
PDF original: ES-2360454_T3.pdf




Fragmento de la descripción:
La presente invención se refiere a anticuerpos contra el receptor del factor I similar a insulina (IGF-1R), a métodos para su producción, a composiciones farmacéuticas que contienen dichos anticuerpos y a usos de los mismos.
El factor I de crecimiento similar a la insulina (IGF-1R, EC 2.7.112, antígeno CD221) pertenece a la familia de las proteínas tirosina quinasa transmembranales (LeiRoith D. et al., Endocrin. Rev. 16:143-163, 1995, y Adams T.E. et al., Cell. Mol. Life Sci. 57 (2000) 1050-1063). El IGF-1R se une a IGF-1 con elevada afinidad e inicia la respuesta fisiológica frente a dicho ligando in vivo. IGF-1R también se une a IGF-2, sin embargo con una afinidad ligeramente inferior.La sobreexpresión de IGF-1R estimula la transformación neoplásica de las células y existe evidencia de que IGF-1R se encuentra implicado en la transformación maligna de las células y por lo tanto de que es una diana útil para el desarrollo de agentes terapéuticos para el tratamiento del cáncer (Adams et al., Cell Mol. Life Sci. 57:1050-1093, 2000). 57 (2000) 1050-1063).
Los anticuerpos contra IGF-1R son bien conocidos del estado de la técnica y han sido investigados por sus efectos antitumorales in vitro e in vivo (Benini S. et al., Clin. Cancer Res. 7:1790-1797, 2001; Scotlandi K. et al., Cancer Gene Ther. 9:296-307, 2002; Scotlandi K. et al., Int. J. Cancer 101:11-16, 2002; Brunetti A. et al., Biochem. Biophys. Res. Commun. 165:212-218, 1989; Prigent S.A. et al., J. Biol. Chem. 265:9970-9977, 1990 Li S.L. et al., Cancer Immunol. Immu¬nother. 49:243-252, 2000; Pessino A. et al., Biochem. Biophys. Res. Commun. 162:1236-1243, 1989; Surinya
K.H. et al., J. Biol. Chem. 277:16718-16725, 2002; Soos M.A. et al., J. Biol. Chem. 267:12955-12963, 1992; Soos M.A. et al., Proc. Natl. Acad. Sci. USA 86:5217-5221, 1989; O'Brien R.M. et al., EMBO J. 6:4003-4010, 1987; Taylor R. et al., Biochem. J. 242:123-129, 1987; Soos M.A. et al., Biochem. J. 235:199-208, 1986; Li S.L. et al., Biochem. Biophys. Res. Commun. 196:92-98, 1993; Delafontaine P. et al., J. Mol. Cell. Cardiol. 26:1659-1673, 1994; Kull F.C. Jr. et al. J. Biol. Chem. 258:6561-6566, 1983; Morgan D.O. y Roth R.A., Biochemistry 25:1364-1371, 1986; Forsayeth J.R. et al., Proc. Natl. Acad. Sci. USA 84:3448-3451, 1987; Schaefer E.M. et al., J. Biol. Chem. 265:13248-13253, 1990; Gustafson T.A. y Rutter W.J., J. Biol. Chem. 265:18663-18667, 1990; Hoyne P.A. et al., FEBS Lett. 469:57-60, 2000; Tulloch P.A. et al., J. Struct. Biol. 125:11-18, 1999; Rohlik Q.T. et al., Biochem. Biophys. Res. Comm. 149:276-281, 149; y Kalebic T. et al., Cancer Res. 54:5531-5534, 1994; Adams T.E. et al., Cell. Mol. Life Sci. 57:1050-1063, 2000; Dricu A. et al., Glycobiology 9:571-579, 1999; Kanter-Lewensohn L. et al., Melanoma Res. 8:389-397, 1998; Li S.L. et al., Cancer Immunol. Immunother. 49:243-252, 2000). Los anticuerpos contra IGF-1R también se describen en gran cantidad de publicaciones adicionales, por ejemplo Arteaga C.L. et al., Breast Cancer Res. Treatment 22:101-106, 1992; y Hailey J. et al., Mol. Cancer Ther. 1:1349-1353, 2002.
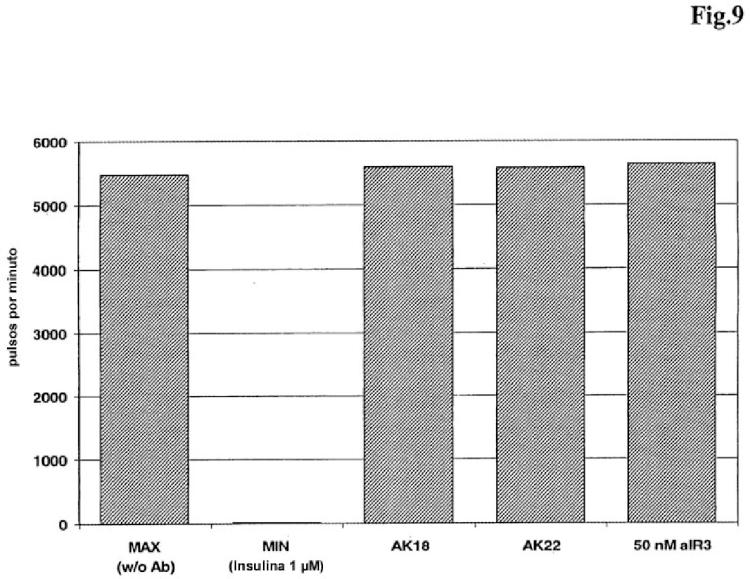
En particular, el anticuerpo monoclonal contra IGF-1R denominado αIR3 se utiliza ampliamente en la investigación de los procesos mediados por IGF-1R y de las enfermedades mediadas por IGF-1R tales como el cáncer. Alfa-IR3 también ha sido descrito por Kull F.C., J. Biol. Chem. 258:6561-6566, 258. Desde entonces se han publicado aproximadamente cien publicaciones referidas a la investigación y al uso terapéutico de αIR3 con respecto a su efecto antitumoral, solo o conjuntamente con agentes citostáticos tales como la doxorrubicina y la vincristina. αIR3 es un anticuerpo monoclonal murino que es conocido que inhibe la unión de IGF-1 al receptor de IGF pero no la unión de IGF-2 a IGF-1R. αIR3 estimula a concentraciones elevadas la proliferación de las células tumorales y la fosforilación de IGF-1R (Bergmann U. et al., Cancer Res. 55:2007-2011, 1995; Kato H. et al., J. Mol. Biol. 268:2655-2661, 1993). Existen otros anticuerpos (por ejemplo 1H7, Li S.L. et al., Cancer Immunol. Immunother. 49:243-252, 2000) que inhiben la unión de IGF-2 a IGF-1R más potentemente que la unión de IGF-1. Un resumen del estado de la técnica de los anticuerpos y de sus propiedades y características se describe en Adams T.E. et al., Cell. Mol. Life Sci. 57:1050-1063, 2000.
La mayoría de los anticuerpos descritos en el estado de la técnica se obtiene del ratón. Dichos anticuerpos no resultan útiles, tal como es bien conocido del estado de la técnica, para la terapia de pacientes humanos sin alteraciones adicionales tales como la quimerización o la humanización Basándose en estas desventajas, los anticuerpos humanos resultan claramente preferentes como agentes terapéuticos en el tratamiento de los pacientes humanos. Los anticuerpos humanos son bien conocidos en el estado de la técnica (van Dijk M.A. y van de Winkel J.G., Curr. Opin. Pharmacol. 5:368-374, 2001). Basándose en dicha tecnología, pueden producirse anticuerpos humanos contra una gran diversidad de dianas. Se describen ejemplos de anticuerpos humanos contra IGF-1R en la patente WO nº 02/053596, que muestran, sin embargo, actividad agonista.
Sin embargo, todavía existe una necesidad de anticuerpos contra IGF-1R con beneficios convincentes para los pacientes que necesitan terapia antitumoral. El beneficio relevante para el paciente es, en términos sencillos, la reducción del crecimiento tumoral y una prolongación significativa del tiempo hasta la progresión causada por el tratamiento con el agente antitumorigénico.
Descripción resumida de la invención
La invención proporciona anticuerpos que se unen al IGF-1R humano que comprenden como agentes determinantes de complementariedad (CDRs) las secuencias siguientes: a) una cadena pesada de anticuerpo que comprende como 5 CDRs, la CDR1 de aminoácidos 31 a 35, la CDR2 de aminoácidos 50 a 66 y la CDR3 de aminoácidos 99 a 107 de la secuencia SEC ID nº 1, y una cadena ligera de anticuerpo que comprende como CDRs, la CDR1 de aminoácidos 24 a 34, la CDR2 de aminoácidos 50 a 56 y la CDR3 de aminoácidos 89 a 98 de la secuencia SEC ID nº 2, o b) una cadena pesada de anticuerpo que comprende como CDRs, la CDR1 de aminoácidos 31 a 35, la CDR2 de aminoácidos 50 a 66 y la CDR3 de aminoácidos 99 a 107 de la secuencia SEC ID nº 3, y una cadena ligera de anticuerpo que comprende como CDRs, la CDR1 de aminoácidos 24 a 34, la CDR2 de aminoácidos 50 a 56 y la CDR3 de aminoácidos 89 a 98 de la secuencia SEC ID nº 4.
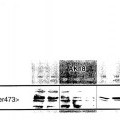
Un anticuerpo según la invención se une a IGF-1R, inhibiendo la unión de IGF-1 e IGF-2 a IGF-1R, es del isotipo IgG1, muestra una proporción entre los valores de IC50 de inhibición de la unión de IGF-1 a IGF-1R y de inhibición de la unión 15 de IGF-2 a IGF-1R, de entre 1:3 y 3:1, inhibe por lo menos 80%, preferentemente por lo menos 90%, a una concentración de 5 nM, la fosforilación de IGF-1R en un ensayo celular de fosforilación con células HT29 en un medio que contiene 0,5% de suero de feto bovino inactivado por calor (FCS) en comparación con dicho ensayo sin dicho anticuerpo, y no muestra actividad estimuladora de IGF-1R medida como fosforilación de PKB a una concentración de 10 µM en un ensayo celular de fosforilación con células 3T3 que proporciona entre 400.000 y 600.000 moléculas de IGF-1R por célula en un medio que contiene 0,5% de suero de feto bovino (FCS) inactivado por calor en comparación con dicho ensayo sin dicho anticuerpo.
Los anticuerpos según la invención muestran ventajas para los pacientes que necesitan terapia antitumoral y proporcionan una reducción del crecimiento tumoral y una prolongación significativa del tiempo hasta la progresión. Los 25 anticuerpos según la invención presentan nuevas propiedades inventivas que causan un beneficio para un paciente que sufre una enfermedad asociada a una desregulación de IGF, especialmente una enfermedad tumoral. Los anticuerpos según la invención se caracterizan por las propiedades anteriormente indicadas. Por lo tanto, las propiedades son especialmente la unión específica a IGF-1R, la inhibición de la unión de IGF-1 e IGF-2 a IGF-1R en la proporción anteriormente indicada, siendo del isotipo IgG1, y la no activación de la señalización de IGF-1R incluso en células que sobreexpresaban IGF-1R a una concentración de 200 veces su valor de IC50. Los anticuerpos que no presentan "actividad mimética de IGF-1" proporcionan una fuerte ventaja al utilizarse como agente terapéutico.
Preferentemente, un anticuerpo según la invención induce, además, la muerte celular de 20% o más de las células de una preparación... [Seguir leyendo]
Reivindicaciones:
1. Anticuerpo ligante de IGF-1R humano, caracterizado porque comprende:
a) una cadena pesada de anticuerpo que comprende como CDRs, la CDR1 de aminoácidos 31 a 35, la CDR2 de aminoácidos 50 a 66, y la CDR3 de aminoácidos 99 a 107 de secuencia SEC ID nº 1, y una cadena ligera de anticuerpo que comprende como CDRs, la CDR1 de aminoácidos 24 a 34, la CDR2 de aminoácidos 50 a 56 y la CDR3 de aminoácidos 89 a 98 de secuencia SEC ID nº 2, o
b) una cadena pesada de anticuerpo que comprende como CDRs, la CDR1 de aminoácidos 31 a 35, la CDR2 de aminoácidos 50 a 66, y la CDR3 de aminoácidos 99 a 107 de secuencia SEC ID nº 3, y una cadena ligera de anticuerpo que comprende como CDRs, la CDR1 de aminoácidos 24 a 34, la CDR2 de aminoácidos 50 a 56 y la CDR3 de aminoácidos 89 a 98 de secuencia SEC ID nº 4.
2. Anticuerpo según la reivindicación 1, caracterizado porque es un anticuerpo humano o humanizado.
3. Anticuerpo según la reivindicación 1 ó 2, caracterizado por una afinidad de entre aproximadamente 10-13 y 10-9 M (KD).
4. Anticuerpo según la reivindicación 1, obtenible a partir de la línea celular de hibridoma <IGF-1R> HUMAB clon 18 (DSM nº ACC 2587) o <IGF-1R> HUMAB clon 22 (DSM nº ACC 2594).
5. Utilización de un anticuerpo según las reivindicaciones 1 a 4 para la preparación de una composición farmacéutica.
6. Composición farmacéutica que contiene un anticuerpo según las reivindicaciones 1 a 4.
7. Líneas celulares de hibridoma <IGF-1R> HUMAB clon 18 (DSM nº ACC 2587) y <IGF-1R> HUMAB clon 22 (DSM nº ACC 2594).
8. Método para la preparación de una composición farmacéutica que comprende un anticuerpo según las reivindicaciones 1 a 4.
9. Ácido nucleico codificante de un anticuerpo ligante de IGF-1R humano, caracterizado porque comprende:
a) una cadena pesada de anticuerpo que comprende como CDRs, la CDR1 de aminoácidos 31 a 35, la CDR2 de aminoácidos 50 a 66, y la CDR3 de aminoácidos 99 a 107 de secuencia SEC ID nº 1, y una cadena ligera de anticuerpo que comprende como CDRs, la CDR1 de aminoácidos 24 a 34, la CDR2 de aminoácidos 50 a 56 y la CDR3 de aminoácidos 89 a 98 de secuencia SEC ID nº 2, o
b) una cadena pesada de anticuerpo que comprende como CDRs, la CDR1 de aminoácidos 31 a 35, la CDR2 de aminoácidos 50 a 66 y la CDR3 de aminoácidos 99 a 107 de secuencia SEC ID nº 3, y una cadena ligera de anticuerpo que comprende como CDRs, la CDR1 de aminoácidos 24 a 34, la CDR2 de aminoácidos 50 a 56 y la CDR3 de aminoácidos 89 a 98 de secuencia SEC ID nº 4.
10. Vector de expresión que comprende un ácido nucleico según la reivindicación 9, capaz de expresar dicho ácido nucleico en una célula huésped procariótica o en una célula huésped CHO, NS0, SP210, H3K293, COS o de levadura.
11. Célula huésped procariótica o célula huésped CHO, NS0, SP210, H3K293, COS o levadura que comprende el vector según la reivindicación 10.
12. Método para la producción de un polipéptido ligante del IGF-1R humano, caracterizado por la expresión de un ácido nucleico codificante de una cadena pesada de anticuerpo y un ácido nucleico codificante de una cadena ligera de anticuerpo según la reivindicación 9 en una célula huésped procariótica o en una célula huésped CHO, NS0, SP210, H3K293, COS o levadura y la recuperación de dicho polipéptido a partir de dicha célula.
13. Anticuerpo según las reivindicaciones 1 a 4 para la utilización como medicamento destinado al tratamiento de un paciente que necesita terapia antitumoral.
14. Anticuerpo para la utilización como medicamento según la reivindicación 13, caracterizado porque el anticuerpo se administra en combinación con un agente citotóxico, un profármaco del mismo o una radioterapia citotóxica.
Patentes similares o relacionadas:
AGENTE INMUNOTERAPÉUTICO PARA CD37 Y COMBINACIÓN CON UN AGENTE QUIMIOTERAPÉUTICO BIFUNCIONAL DEL MISMO, del 21 de Noviembre de 2011, de Emergent Product Development Seattle, LLC: Una molécula de unión específica a CD37, que comprende una secuencia de aminoácidos como se muestra en el SEQ ID NO. 253
BLOQUEO DE LA MIGRACIÓN DE LEUCOCITOS Y DE LA INFLAMACIÓN POR INTERFERENCIA CON CD99/HEC2, del 17 de Noviembre de 2011, de CORNELL RESEARCH FOUNDATION, INC.: Un anticuerpo anti-CD99 que inhibe la migración transendotelial (MTE) de leucocitos mediada por CD99, para uso en un procedimiento para el tratamiento de una estado […]
ENSAYOS Y MÉTODOS USANDO BIOMARCADORES, del 21 de Septiembre de 2011, de GENENTECH, INC.: Un procedimiento para predecir la sensibilidad de una muestra de tejido o de células de mamífero a un anticuerpo agonista de DR4 o anticuerpo agonista de DR5, […]
FRAGMENTO DE ANTICUERPO CAPAZ DE MODULAR LA MULTIRRESISTENCIA Y COMPOSICIONES Y KITS Y MÉTODOS QUE UTILIZAN EL MISMO, del 2 de Septiembre de 2011, de TECHNION RESEARCH AND DEVELOPMENT FOUNDATION, LTD.: Un anticuerpo Fv monocatenario que comprende una región de fijación de antígeno capaz de fijar una porción extracelular de una glicoproteína P, en donde el anticuerpo […]
PREVENTIVO O REMEDIO PARA ENFERMEDADES INFLAMATORIAS DEL INTESTINO QUE CONTIENE ANTICUERPO ANTI-CD81 COMO PRINCIPIO ACTIVO, del 16 de Agosto de 2011, de DAINIPPON SUMITOMO PHARMA CO., LTD.: Uso de anticuerpo anti-CD81 para la preparación de una composición farmacéutica para prevenir, mejorar o tratar enfermedad inflamatoria del intestino (EII)
 UTILIZACIÓN DE UN ANTICUERPO ANTI-CD151 PARA EL TRATAMIENTO DEL CÁNCER, del 21 de Junio de 2011, de PIERRE FABRE MEDICAMENT: Uso de al menos un anticuerpo o uno de sus fragmentos funcionales, capaz de unirse a la proteína CD151 y de inhibir así el crecimiento tumoral para la preparación […]
UTILIZACIÓN DE UN ANTICUERPO ANTI-CD151 PARA EL TRATAMIENTO DEL CÁNCER, del 21 de Junio de 2011, de PIERRE FABRE MEDICAMENT: Uso de al menos un anticuerpo o uno de sus fragmentos funcionales, capaz de unirse a la proteína CD151 y de inhibir así el crecimiento tumoral para la preparación […]
COMPOSICIONES FARMACÉUTICAS DE ANTICUERPOS PARA ENFERMEDADES CAUSADAS POR VIRUS, del 3 de Junio de 2011, de THERANOR SPRL: Una composición farmacéutica para usar en el tratamiento de una enfermedad causada por virus de la gripe en seres humanos, conteniendo dicha composición una […]
PROCEDIMIENTO PARA CLONACIÓN DE ANTICUERPOS ANÁLOGOS, del 9 de Diciembre de 2011, de SYMPHOGEN A/S: Un procedimiento para producir una biblioteca de pares análogos que comprenden secuencias que codifican para la región variable enlazada, comprendiendo dicho procedimiento: a) […]