ANTIBIÓTICOS GLICOPEPTÍDICOS SUBSTANCIALMENTE PUROS AC-98-1, AC-98-2, AC-98-3, AC-98-4 Y AC-98-5.
Una composición farmacéutica que comprende un compuesto sustancialmente puro que tiene la estructura o una sal farmacéuticamente aceptable del mismo,
en combinación con un vehículo farmacéuticamente aceptable
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2002/013073.
Solicitante: WYETH HOLDINGS CORPORATION.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: FIVE GIRALDA FARMS MADISON, NJ 07940-0874 ESTADOS UNIDOS DE AMERICA.
Inventor/es: CARTER, GUY THOMAS, HE,HAIYIN.
Fecha de Publicación: .
Fecha Solicitud PCT: 25 de Abril de 2002.
Clasificación Internacional de Patentes:
- A61K31/395 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › que tienen el nitrógeno como heteroátomo de un ciclo, p. ej. guanetidina o rifamicina.
- C07H15/203 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07H AZUCARES; SUS DERIVADOS; NUCLEOSIDOS; NUCLEOTIDOS; ACIDOS NUCLEICOS (derivados de ácidos aldónicos o sacáricos C07C, C07D; ácidos aldónicos, ácidos sacáricos C07C 59/105, C07C 59/285; cianohidrinas C07C 255/16; glicales C07D; compuestos de constitución indeterminada C07G; polisacáridos, sus derivados C08B; ADN o ARN concerniente a la ingeniería genética, vectores, p. ej. plásmidos o su aislamiento, preparación o purificación C12N 15/00; industria del azúcar C13). › C07H 15/00 Compuestos que contienen radicales hidrocarbonados o hidrocarbonados sustituidos, unidos directamente a los heteroátomos de los radicales sacárido. › Carbociclos monocíclicos distintos de los ciclos ciclohexano; Sistemas carbocíclicos bicíclicos.
- C07H19/04 C07H […] › C07H 19/00 Compuestos que contienen un heterociclo que comparten un heteroátomo del ciclo con un radical sacárido; Nucleósidos; Mononucleótidos; Sus anhidro-derivados. › Radicales heterocíclicos que contienen solamente nitrógeno como heteroátomo del ciclo.
- C07K9/00F2
Clasificación PCT:
- A61K38/12 A61K […] › A61K 38/00 Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00). › Péptidos cíclicos.
- A61K38/14 A61K 38/00 […] › Péptidos que contienen radicales sacárido; Sus derivados.
Clasificación antigua:
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Eslovenia, Finlandia, Rumania, Chipre, Lituania, Letonia, Ex República Yugoslava de Macedonia, Albania.
Fragmento de la descripción:
ANTECEDENTES DE LA INVENCIÓN
1. Campo de la invención
La presente invención se refiere a nuevos antibióticos glicopeptídicos substancialmente puros, designados como AC–98–3, AC–98–4 y AC–98–5, o sales farmacéuticamente aceptables de los mismos, a procedimientos para la 5 preparación y aislamiento de tales antibióticos, a procedimientos de utilización de tales antibióticos para tratar infecciones bacterianas y a composiciones farmacéuticas que contienen tales antibióticos.
2. Descripción de la técnica anterior
La patente de Estados Unidos nº 3.495.004 divulga un organismo productor Streptomyces hygroscopicus NRRL 3085, y las condiciones de producción para preparar una mezcla compleja de antibióticos AC–98. No se divulgan 10 detalles de las estructuras de los antibióticos individuales. Como se describe en la patente de los Estados Unidos 3.495.004, la mezcla de antibióticos AC–98 no podría ser separada en los componentes individuales mediante intercambio iónico (IRC–50), filtración en gel (CM–sephadex), o cromatografía de fase normal (gel de sílice desactivado).
BREVE DESCRIPCIÓN DE LOS DIBUJOS 15
La figura 1 muestra el espectro de absorción infrarroja del AC–98–1.
La figura 2 muestra el espectro de absorción infrarroja del AC–98–2.
La figura 3 muestra el espectro de absorción infrarroja del AC–98–3.
La figura 4 muestra el espectro de absorción infrarroja del AC–98–4.
La figura 5 muestra el espectro de absorción infrarroja del AC–98–5. 20
La figura 6 muestra el espectro de resonancia magnética nuclear de protones del AC–98–1.
La figura 7 muestra el espectro de resonancia magnética nuclear de protones del AC–98–2.
La figura 8 muestra el espectro de resonancia magnética nuclear de protones del AC–98–3.
La figura 9 muestra el espectro de resonancia magnética nuclear de protones del AC–98–4.
La figura 10 muestra el espectro de resonancia magnética nuclear de protones del AC–98–5. 25
La figura 11 muestra el espectro de resonancia magnética nuclear de carbono 13 del AC–98–1.
La figura 12 muestra el espectro de resonancia magnética nuclear de carbono 13 del AC–98–2.
La figura 13 muestra el espectro de resonancia magnética nuclear de carbono 13 del AC–98–3.
La figura 14 muestra el espectro de resonancia magnética nuclear de carbono 13 del AC–98–4.
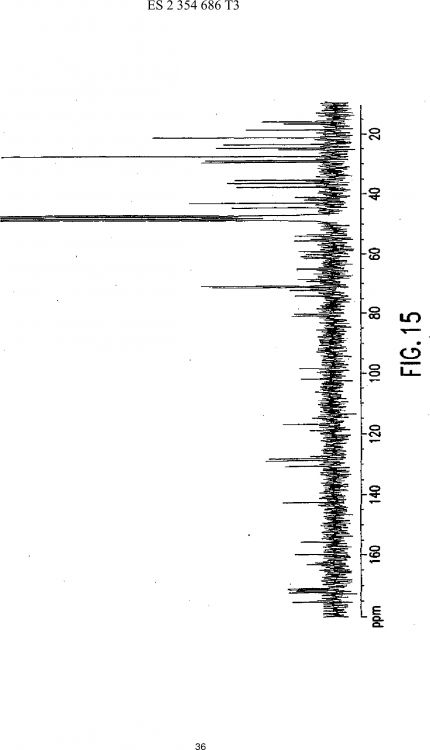
La figura 15 muestra el espectro de resonancia magnética nuclear de carbono 13 del AC–98–5. 30
SUMARIO DE LA INVENCIÓN
Ahora se han descubierto nuevos antibióticos glicopeptídicos substancialmente puros, designados como AC–98–1, AC–98–2, AC–98–3, AC–98–4 y AC–98–5, o sales farmacéuticamente aceptables de los mismos.
La estructura del AC–98–1 es:
Las características fisicoquímicas del AC–98–1 son como sigue:
a) Fórmula molecular aparente: C54H78N12O25
b) Peso molecular: ES (IEP) [M+2H]2+ = M/Z 648 (p. m. = 1292) EMBARAR (Espectro de Masas Bombardeo por Átomos Rápidos de Alta Resolución) calculado para C54H78N12O25Na = M/Z 1317.5099 EMBARAR observado = 5 M/Z 1317,5164 mmu = 6,5
c) Espectro de Absorción Ultravioleta: max nm MeOH = 280, 273, 201;
d) Espectro de Absorción Infrarrojo: como se muestra en la FIG. 1 (disco de KBr): 3374, 3277, 1681, 1634, 1554, 1510 cm–1;
e) Espectro de Resonancia Magnética de Protón: como se muestra en la FIG. 6 (300 MHz, CD3OD/D2O 1:1) 10
f) Espectro de Resonancia Magnética Nuclear de Carbono 13: como se muestra en la FIG. 11 (75 MHz, CD3OD/D2O 1:1), los picos significativos se listan a continuación ( en TMS);
174,4, 173,9, 173,5, 173,5, 173,2, 173,0, 161,9, 161,7, 157,8, 144,8, 133,1, 133,0, 131,3, 130,5, 129,8, 119,4, 104,3, 100,8, 83,5, 82,7, 76,6, 76,4, 74,9, 74,1, 73,7, 73,5, 73,5, 73,3, 72,2, 72,0, 71,3, 69,5, 67,6, 63,8, 63,8, 63,8, 63,5, 62,7, 61,8, 58,3, 58,3, 57,8, 56,8, 56,1, 45,0, 44,8, 44,6, 15 44,1, 38,7, 19,9.
La estructura de AC–98–2 es:
Las características fisicoquímicas del AC–98–2 son como sigue:
a) Fórmula molecular aparente: C42H58N12O15
b) Peso molecular: ES (IEP) [M+2H]2+ = M/Z 486 (p. m. = 970) EMBARAR calculado para C42H58N12O15Na = M/Z 992,4077 EMBARAR observado = M/Z 993,4042 mmu = 3,5 5
c) Espectro de Absorción Ultravioleta: max nm MeOH = 280, 273, 201;
d) Espectro de Absorción Infrarrojo: como se muestra en la FIG. 2 (disco de KBr): 3374, 3277, 1681, 1634, 1554, 1510 cm–1;
e) Espectro de Resonancia Magnética de Protón: como se muestra en la FIG. 7 (300 MHz, CD3OD/D2O 1:1)
f) Espectro de Resonancia Magnética Nuclear de Carbono 13: como se muestra en la FIG.12 (75 MHz, CD3OD/D2O 10 1:1), los picos significativos se listan a continuación ( en TMS);
174,3, 173,9, 173,5, 173,6, 173,2, 173,0, 162,0, 161,7, 158,2, 144,7, 133,1, 130,0, 131,3, 130,5, 129,8, 117,8, 83,5, 82,8, 73,7, 72,2, 71,9, 71,3, 67,6, 63,8, 63,8, 62,8, 61,8, 58,3, 58,3, 57,8, 56,8, 56,1, 45,1, 44,8, 44,5, 44,2, 38,7, 19,7.
La estructura de AC–98–3 es: 15
Las características fisicoquímicas del AC–98–3 son como sigue:
a) Fórmula molecular aparente: C58H96N12O26
b) Peso molecular: ES (IEP) [M+2H]2+ = M/Z 690 (p. m. = 1378) EMBARAR calculado para C59H87N12O26= M/Z 1379,5854 EMBARAR observado = M/Z 1379,5861 mmu = 0,5 5
c) Espectro de Absorción Ultravioleta: max nm MeOH = 280, 273, 201;
d) Espectro de Absorción Infrarrojo: como se muestra en la FIG. 3 (disco de KBr): 3374, 3277, 1681, 1634., 1554, 1510 cm–1;
e) Espectro de Resonancia Magnética de Protón: como se muestra en la FIG. 8 (300 MHz, CD3OD/D2O 1:1)
f) Espectro de Resonancia Magnética Nuclear de Carbono 13: como se muestra en la FIG.13 (75 MHz, CD3OD/D2O 10 1:1), los picos significativos se listan a continuación ( en TMS);
177,3, 174,4, 173,9, 173,5, 173,5, 173,2, 173,0, 161,9, 161,7, 157,8, 144,8, 133,2, 133,1, 131,2, 130,5, 129,8, 119,4, 101,2, 100,8, 83,5, 82,8, 76,7, 75,2, 74,8, 73,9, 73,7, 73,6, 71,7, 76,4, 72,2, 72,0, 71,3, 69,9, 67,6, 63,9,63,8, 63,8, 63,5, 62,7, 61,8, 58,4,58,3, 57,8, 56,8, 56,1, 45,0, 44,8, 44,6, 44,1, 38,7, 19,7, 45,6, 28,2, 24,27, 24,24. 15
La estructura de AC–98–4 es:
Las características fisicoquímicas del AC–98–4 son como sigue:
a) Fórmula molecular aparente: C59H86N12O26
b) Peso molecular: ES (IEP) [M+2H]2+ = M/Z 690 (p. m. = 1378) EMBARAR calculado para C59H87N12O26 = M/Z 1379,5854 EMBARAR observado = M/Z 1379,5879 mmu = 2,5 5
c) Espectro de Absorción Ultravioleta: max nm MeOH = 280, 273, 201;
d) Espectro de Absorción Infrarrojo: como se muestra en la FIG. 4 (disco de KBr): 3374, 3277, 1681, 1634, 1554, 511 cm–1;
e) Espectro de Resonancia Magnética de Protón: como se muestra en la FIG. 9 (300 MHz, CD3OD/D2O 1:1)
f) Espectro de Resonancia Magnética Nuclear de Carbono 13: como se muestra en la FIG.14 (75 MHz, CD3OD/D2O 10 1:1), los picos significativos se listan a continuación ( en TMS);
174,4, 173,9, 173,5, 173,6, 173,2, 173,0, 161,8, 161,8, 158,0, 144,9, 133,2, 133,1, 131,2, 130,5, 129,8, 119,5, 104,1, 101,1, 83,7, 82,8, 76,6, 76,9, 75,0, 74,2, 73,8, 73,6, 76,4, 71,4, 72,1, 72,1, 71,4, 67,0, 67,6, 63,8, 63,8, 63,9, 63,7, 62,7, 61,8, 58,4, 58,4,...
Reivindicaciones:
1. Una composición farmacéutica que comprende un compuesto sustancialmente puro que tiene la estructura
o una sal farmacéuticamente aceptable del mismo, en combinación con un vehículo farmacéuticamente aceptable.
2. Una composición farmacéutica según la reivindicación 1 en la que el compuesto sustancialmente puro tiene 5 la estructura
3. Una composición farmacéutica que comprende un compuesto sustancialmente puro que tiene la estructura
o una sal farmacéuticamente aceptable del mismo, en combinación con un vehículo farmacéuticamente aceptable.
4. Una composición farmacéutica según la reivindicación 3 en la que el compuesto sustancialmente puro tiene la estructura
5
5. Una composición farmacéutica que comprende un compuesto sustancialmente puro que tiene la estructura
o una sal farmacéuticamente aceptable del mismo, en combinación con un vehículo farmacéuticamente aceptable.
6. Una composición farmacéutica según la reivindicación 5 en la que el compuesto sustancialmente puro tiene la estructura
5
7. Uso de un compuesto sustancialmente puro como se describe en una cualquiera de las reivindicaciones 1 a 6 o una sal farmacéuticamente aceptable del mismo, o una composición como se describe en una cualquiera de las reivindicaciones 1 a 6, en la preparación de un medicamento para el tratamiento de infecciones bacterianas en un animal de sangre caliente.
Patentes similares o relacionadas:
Inhibidores de la replicación del virus de la inmunodeficiencia humana, del 13 de Mayo de 2020, de VIIV Healthcare UK (No.5) Limited: Un compuesto de fórmula I, incluyendo las sales farmacéuticamente aceptables del mismo: **(Ver fórmula)** en la que: cada uno de R1a y R1b se selecciona independientemente […]
Combinaciones y modos de administración de agentes terapéuticos y terapia combinada, del 8 de Abril de 2020, de ABRAXIS BIOSCIENCE, LLC: Una composición que comprende nanopartículas que comprenden paclitaxel y una albúmina, para uso en un método para el tratamiento de cáncer de pulmón en un individuo, en […]
Politerapia para el tratamiento de infecciones por VHB, del 25 de Marzo de 2020, de Novira Therapeutics Inc: rn inhibidor del ensamblaje de la cápside y peginterferón alfa-2a, siendo el inhibidor del ensamblaje de la cápside un compuesto de fórmula IVc: **(Ver fórmula)** o […]
Inhibidores de MCL1 macrocíclicos para tratar el cáncer, del 19 de Febrero de 2020, de ASTRAZENECA AB: Un compuesto que es acido 17-cloro-5,13,14,22-tetrametil-28-oxa-2,9-ditia-5,6,12,13,22- pentaazaheptaciclo[27.7.1.14,7.011,15.016,21.020,24.030,35]octatriaconta-1 ,4 ,6,11,14,16,18,20,23,29,31,33,35-tridecaeno- […]
Compuestos que comprenden restos de heteroarilo unidos y su uso como nuevos modificadores del sabor umami, saborizantes y potenciadores del sabor para composiciones comestibles, del 18 de Diciembre de 2019, de Firmenich Incorporated: Un compuesto de la Fórmula (IA), **(Ver fórmula)** o una sal comestiblemente aceptable del mismo; y en el que i) n' es cero, uno, dos o tres, y cada R20 se […]
Procedimientos de tratamiento de encefalopatía hepática, del 11 de Diciembre de 2019, de Salix Pharmaceuticals, Ltd: Rifaximina para su uso en la disminución del riesgo de un sujeto de episodios importantes de encefalopatía hepática (EH) en un sujeto que padece EH o en un sujeto con […]
Compuestos terapéuticamente activos y sus métodos de utilización, del 20 de Noviembre de 2019, de Agios Pharmaceuticals, Inc: Compuesto que presenta la fórmula Ia o una sal o hidrato farmacéuticamente aceptable del mismo, en el que: **(Ver fórmula)** el anillo A se selecciona de fenilo, […]
Uso de plerixafor para tratar y/o prevenir exacerbaciones agudas de la enfermedad pulmonar obstructiva crónica, del 9 de Octubre de 2019, de Université de Bordeaux: Una composición para su uso en un método para tratar y/o prevenir las EAEPOC, que comprende una cantidad terapéuticamente eficaz de plerixafor […]