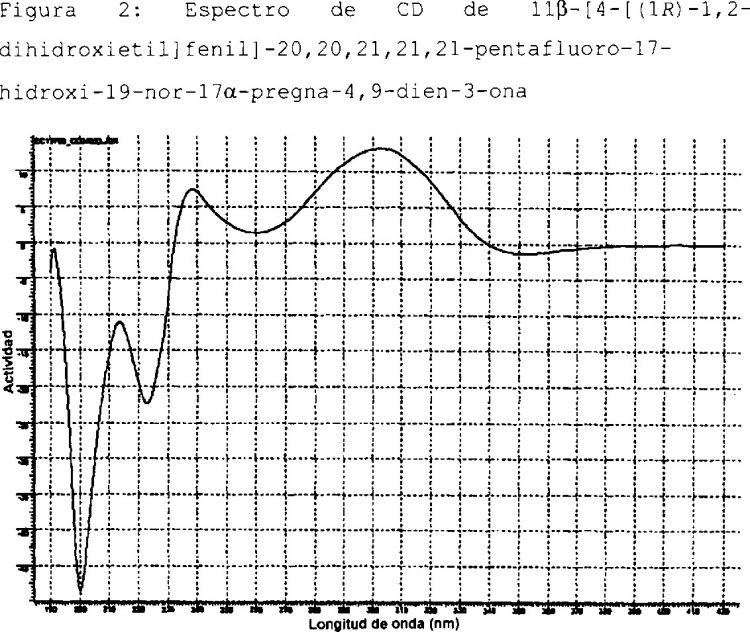
ANTAGONISTAS DEL RECEPTOR DE PROGESTERONA.
Un antagonista del receptor de progesterona de fórmula general I:
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2007/009997.
Solicitante: BAYER SCHERING PHARMA AKTIENGESELLSCHAFT.
Nacionalidad solicitante: Alemania.
Dirección: MULLERSTRASSE 178,13353 BERLIN.
Inventor/es: FUHRMANN, ULRIKE, PETROV, ORLIN, CLEVE, ARWED, SCHMIDT,ANJA, GARKE,GUNNAR, PRUEHS,STEFAN, BRUDNY-KLOEPPEL,MARGARETE, ROTTMANN,ANTJE, HASSELMANN,RAINER, SCHULTZE-MOSGAU,MARCUS, MOELLER,CARSTEN.
Fecha de Publicación: .
Fecha Concesión Europea: 21 de Abril de 2010.
Clasificación Internacional de Patentes:
- C07J1/00C5
- C07J21/00C1
- C07J51/00 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07J ESTEROIDES (seco-steroides C07C). › Esteroides normales con la estructura del ciclopenta [a] hidrofenantreno no modificada no previstos en los grupos C07J 1/00 - C07J 43/00.
Clasificación PCT:
- A61K31/567 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › sustituidos en posición 17 alfa, p. ej. mestranol, noretandrolona.
- A61P5/36 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › A61P 5/00 Medicamentos para el tratamiento de trastornos del sistema endocrino. › Antiprogestágenos.
- C07J1/00 C07J […] › Esteroides normales que contienen carbono, hidrógeno, halógeno u oxígeno no sustituidos en posición 17 beta por un átomo de carbono, p. ej. estrano, androstano.
- C07J21/00 C07J […] › Esteroides normales que contienen carbono, hidrógeno, halógeno u oxígeno, teniendo un heterociclo que contiene oxígeno condensado en espiro con la estructura del ciclopenta [a] hidrofenantreno.
- C07J51/00 C07J […] › Esteroides normales con la estructura del ciclopenta [a] hidrofenantreno no modificada no previstos en los grupos C07J 1/00 - C07J 43/00.
Fragmento de la descripción:
Antagonistas del receptor de progesterona.
La presente invención se refiere a antagonistas del receptor de progesterona de fórmula general I:

en la que R1 puede ser un átomo de hidrógeno, y R2 es un grupo hidroxilo, o R1 y R2 pueden ser juntos un grupo oxo; a fármacos (composiciones farmacéuticas) que los contienen; y a su uso en la fabricación de medicamentos.
La invención se refiere en particular a los antagonistas del receptor de progesterona
- 11ß-[4-(1,2-dihidroxietil)fenil]-20,20,21,21,21-pentafluoro-17-hidroxi-19-nor-17a-pregna-4,9-dien-3-ona y sus epímeros individuales
- 11ß-[4-[(1R)-1,2-dihidroxietil]fenil]-20,20,21,21,21-pentafluoro-17-hidroxi-19-nor-17a-pregna-4,9-dien-3-ona, y
- 11ß-[4-[(1S)-1,2-dihidroxietil]fenil]-20,20,21,21,21-pentafluoro-17-hidroxi-19-nor-17a-pregna-4,9-dien-3-ona, y
- 20,20,21,21,21-pentafluoro-17-hidroxi-11ß-[4-(hidroxiacetil)fenil]-19-nor-17a-pregna-4,9-dien-3-ona,
y a fármacos que los contienen, y a su uso en la fabricación de medicamentos.
Un compuesto preferido de esta invención es 20,20,21,21,21-pentafluoro-17-hidroxi-11ß-[4-(hidroxiacetil)fenil]-19-nor-17a-pregna-4,9-dien-3-ona.
Los compuestos con actividad antigestágena (antagonistas competitivos del receptor de progesterona) se conocieron por primera vez en 1982 (documentos RU 486; EP 57115), y desde entonces se han descrito muy bien. Los esteroides con actividad antigestágena, que son diferentes de las sustancias según la invención, y que tienen una cadena lateral 17a fluorada, se publicaron en el documento WO 98/34947 y en Fuhrmann et al., J. Med. Chem. 43, 5010-5016 (2000). La clase de compuestos descrita en el documento WO 98/34947 permitió una gran variedad de sustituyentes en la posición 11 del núcleo esteroideo, pero no se extendió a grupos alquilfenílicos disustituidos. El documento EP 57115 permitió un intervalo de sustituyentes en la posición 11 del núcleo esteroideo, pero requirió que tales sustituyentes contuviesen un átomo de nitrógeno, de fósforo o de silicio. Por lo tanto, no hay ninguna sugerencia de que los esteroides que contienen un sustituyente que contiene flúor en la posición 17 y un sustituyente alquilfenílico disustituido en la posición 11 del núcleo esteroideo pudiesen tener propiedades deseables.
Las sustancias reivindicadas aquí son al menos parcialmente metabolitos de una sustancia reivindicada en el documento WO 98/34947.
El objeto de la presente invención es proporcionar nuevos antagonistas competitivos del receptor de progesterona y fármacos que los contienen, y por tanto crear vías alternativas para tratar enfermedades ginecológicas.
El objeto se ha logrado mediante la síntesis de 11ß-[4-(1,2-dihidroxietil)fenil]-20,20,21,21,21-pentafluoro-17-hidroxi-19-nor-17a-pregna-4,9-dien-3-ona y 20,20,21,21,21-pentafluoro-17-hidroxi-11ß-[4-(hidroxiacetil)fenil]-19-nor-17a-pregna-4,9-dien-3-ona. Los epímeros de 11ß-[4-(1,2-dihidroxietil)fenil]-20,20,21,21,21-pentafluoro-17-hidroxi-19-nor-17a-pregna-4,9-dien-3-ona se pueden preparar específicamente por medio de separación cromatográfica en una columna Chiracel OD-H con hexano/etanol 90:10 (v/v) como fase móvil, o partiendo de entidades estructurales quirales tales como (R)- o (S)-1-(4-bromofenil)-1,2-etanodiol.
Los compuestos de esta invención son por lo tanto aquellos favorables que se han preparado mediante procedimientos químicos.
Convenientemente, la invención proporciona un dihidroxicompuesto de esta invención sustancialmente libre de su isómero, que está al menos 90%, más apropiadamente al menos 95%, preferiblemente al menos 98%, y lo más preferible 100% libre del isómero correspondiente.
Puesto que los compuestos de la invención se van a usar en composiciones farmacéuticas, es mejor proporcionarlos en forma aislada, por ejemplo como un sólido, convenientemente como un sólido sustancialmente puro, por ejemplo sustancialmente libre de otros compuestos esteroideos u otros agentes biológicamente activos.
Las sustancias de fórmula general I son ingredientes activos farmacéuticos valiosos. Se pueden usar, entre otros, para la fabricación de preparaciones farmacéuticas para el tratamiento de miomas o endometriosis, para anticoncepción femenina, para el control de la fertilidad postcoital, para provocar la menstruación, para inducir el parto, para la terapia de sustitución hormonal, para el tratamiento de síntomas asociados con dismenorrea, para el tratamiento de irregularidades hormonales, y para el tratamiento de tumores dependientes de hormonas, por ejemplo un carcinoma de mama positivo al receptor de progesterona. Su eficacia como antagonistas del receptor de progesterona se ha identificado en el ensayo de aborto en la rata, y mediante la determinación del índice de McPhail en el conejo.
Las sustancias de fórmula general I muestran una estabilidad metabólica en microsomas hepáticos humanos (HLM) mayor que el antagonista del receptor de progesterona 11ß-(4-acetilfenil)-20,20,21,21,21-pentafluoro-17-hidroxi-19-nor-17a-pregna-4,9-dien-3-ona descrito en el documento WO 98/34947. Esto es indicativo de la biodisponibilidad oral potenciada de los compuestos de esta invención, de forma que se pueden usar en composiciones farmacéuticas adaptadas para la administración oral.
Los fármacos (composiciones farmacéuticas) según la invención se pueden adaptar para la administración sistémica o local. Generalmente se prefiere adaptar los fármacos para la administración sistémica, por ejemplo mediante inyección o mediante administración oral. Si se contemplan las formas inyectables, éstas se pueden preparar mediante métodos convencionales conocidos en la técnica para formular esteroides. Si se contemplan formas administrables oralmente, éstas también se pueden preparar mediante métodos convencionales conocidos en las técnicas farmacéuticas para formular esteroides.
Las formas preferidas de los fármacos comprenderán un compuesto de fórmula 1 y un vehículo farmacéuticamente aceptable para ellos.
La composición farmacéutica de la invención se puede proporcionar en una forma adecuada para la administración sistémica o local, de la cual la más conveniente es generalmente una forma administrable sistémicamente. La forma administrable sistémicamente se puede adaptar para administración mediante inyección, por ejemplo como una forma estéril, por ejemplo una emulsión. La forma administrable sistémicamente se puede adaptar para administración oral, y tales formas generalmente son muy adecuadas. Tales formas generalmente serán una forma de dosificación unitaria que contiene una cantidad predeterminada del compuesto de la invención. Las formas adecuadas incluyen comprimidos, cápsulas, polvos, granulados, y similares, de los cuales se prefieren generalmente los comprimidos. Tales formas de dosificación se pueden fabricar de manera convencional, y el vehículo farmacéuticamente aceptable puede ser cualquier vehículo adecuado, especialmente un vehículo que se sabe que está en uso en medicamentos esteroideos de formulación.
La forma de dosificación unitaria puede contener 0,01-100 mg de las sustancias reivindicadas.
Los Ejemplos que siguen sirven para ilustrar la invención sin que impliquen de ninguna forma una limitación.
Ejemplo 1
Síntesis de 11ß-[4-(1,2-dihidroxietil)fenil]-20,20,21,21,21-pentafluoro-17-hidroxi-19-nor-17a-pregna-4,9-dien-3-ona
a) Cetal 3-(2,2-dimetilpropano-1,3-diílico) de la 11ß-(4-etenilfenil)-5-hidroxi-5a-estr-9-en-3,17-diona
Se colocan 3,3 g de limaduras de magnesio en 14 ml de tetrahidrofurano absoluto en gas inerte, y se añade una gota de 1,2-dibromoetano. Después de que la reacción ha comenzado, se añade lentamente gota a gota una disolución de 25 g de 4-bromoestireno en 137 ml de tetrahidrofurano absoluto, de manera que la temperatura interna permanece en el intervalo desde 40 hasta 45ºC. La mezcla de reacción se agita posteriormente durante una hora hasta que el magnesio ha reaccionado completamente. Entonces se añaden a la mezcla 2,26 g de cloruro de cobre (I). Se añade lentamente gota a gota una disolución de 8,5 g de cetal 3-(2,2-dimetilpropano-1,3-diílico) de la 5,10-epoxi-5a,10a-estr-9(11)-en-3,17-diona (para su preparación, véase Tetrahedron Lett. 26, 2069-2072 (1985)) en 137 ml de tetrahidrofurano absoluto. La mezcla de...
Reivindicaciones:
1. Un antagonista del receptor de progesterona de fórmula general I:
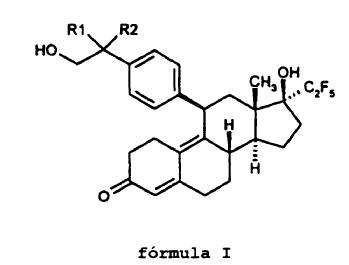
en la que R1 puede ser un átomo de hidrógeno y R2 un grupo hidroxilo, o R1 y R2 pueden ser juntos un grupo oxo.
2. Un compuesto según la reivindicación 1, que es 11ß-[4-(1,2-dihidroxietil)fenil]-20,20,21,21,21-pentafluoro-17-hidroxi-19-nor-17a-pregna-4,9-dien-3-ona.
3. Un compuesto según la reivindicación 1, que es 11ß-[4-[(1R)-1,2-dihidroxietil]fenil]-20,20,21,21,21-pentafluoro-17-hidroxi-19-nor-17a-pregna-4,9-dien-3-ona.
4. Un compuesto según la reivindicación 1, que es 11ß-[4-[(1S)-1,2-dihidroxietil]fenil]-20,20,21,21,21-pentafluoro-17-hidroxi-19-nor-17a-pregna-4,9-dien-3-ona.
5. Un compuesto según la reivindicación 1, que es 20,20,21,21,21-pentafluoro-17-hidroxi-11ß-[4-(hidroxiacetil)fenil]-19-nor-17a-pregna-4,9-dien-3-ona.
6. Un fármaco que contiene antagonistas del receptor de progesterona como se reivindica en la reivindicación 1.
7. El fármaco según la reivindicación 6, que contiene 11ß-[4-(1,2-dihidroxietil)fenil]-20,20,21,21,21-pentafluoro-17-hidroxi-19-nor-17a-pregna-4,9-dien-3-ona.
8. El fármaco según la reivindicación 7, que contiene 11ß-[4-[(1R)-1,2-dihidroxietil]fenil]-20,20,21,21,21-pentafluoro-17-hidroxi-19-nor-17a-pregna-4,9-dien-3-ona.
9. El fármaco según la reivindicación 7, que contiene 11ß-[4-[(1S)-1,2-dihidroxietil]fenil]-20,20,21,21,21-pentafluoro-17-hidroxi-19-nor-17a-pregna-4,9-dien-3-ona.
10. El fármaco según la reivindicación 6, que contiene 20,20,21,21,21-pentafluoro-17-hidroxi-11ß-[4-(hidroxiace- til)fenil]-19-nor-17a-pregna-4,9-dien-3-ona.
11. Uso de antagonistas del receptor de progesterona según la reivindicación 1 para la preparación de un medicamento para el tratamiento de endometriosis, miomas, o tumores dependientes de hormonas, especialmente carcinoma de mama, y de preparaciones farmacéuticas para la anticoncepción femenina.
12. Uso según la reivindicación 11, que contiene 11ß-[4-(1,2-dihidroxietil)-fenil]-17ß-hidroxi-17a-(1,1,2,2,2-pentafluoroetil)estra-4,9-dien-3-ona.
13. Uso según la reivindicación 12, que contiene 11ß-[4-[(1R)-1,2-dihidroxietil]-fenil]-20,20,21,21,21-pentafluoro-17-hidroxi-19-nor-17a-pregna-4,9-dien-3-ona.
14. Uso según la reivindicación 12, que contiene 11ß-[4-[(1S)-1,2-dihidroxietil]fenil]-20,20,21,21,21-pentafluoro-17-hidroxi-19-nor-17a-pregna-4,9-dien-3-ona.
15. Uso según la reivindicación 11, que contiene 20,20,21,21,21-pentafluoro-17-hidroxi-11ß-[4-(hidroxiacetil)fenil]-19-nor-17a-pregna-4,9-dien-3-ona.
16. Cetal 2,2-dimetilpropano-1,3-diílico de la 11ß-(4-etenilfenil)-20,20,21,21,21-pentafluoro-5,17-dihidroxi-19-nor-5a,17a-pregn-9-en-3-ona como intermedio en la preparación del antagonista del receptor de progesterona de fórmula general I.
17. Cetal 2,2-dimetilpropano-1,3-diílico de la 11ß-[4-(1,2-dihidroxietil)fenil]-20,20,21,21,21-pentafluoro-5,17-dihidroxi-19-nor-5a,17a-pregn-9-en-3-ona como intermedio en la preparación del antagonista del receptor de progesterona de fórmula general I.
18. Cetal 2,2-dimetilpropano-1,3-diílico de la 11ß-{4-[(4R)-2,2-dimetil-1,3-dioxolan-4-il]fenil}-20,20,21,21,21-pentafluoro-5,17-dihidroxi-19-nor-5a,17a-pregn-9-en-3-ona como intermedio en la preparación del antagonista del receptor de progesterona de fórmula general I.
19. Cetal 2,2-dimetilpropano-1,3-diílico de la 11ß-[4-[2-[[[(1,1-dimetiletil)dimetilsilil]oxi]metil]-1,3-dioxolan-2-il]fenil]-20,20,21,21,21-pentafluoro-5,17-dihidroxi-19-nor-5a,17a-pregn-9-en-3-ona como intermedio en la preparación del antagonista del receptor de progesterona 20,20,21,21,21-pentafluoro-17-hidroxi-11ß-[4-(hidroxiacetil)fenil]-19-nor-17a-pregna-4,9-dien-3-ona.
20. Cetal 2,2-dimetilpropano-1,3-diílico de la 20,20,21,21,21-pentafluoro-5,17-dihidroxi-11ß[4-[4-[2-(hidroxime- til)-1,3-dioxolan-2-il]fenil]-19-nor-5a,17a-pregn-9-en-3-ona como intermedio en la preparación del antagonista del receptor de progesterona 20,20,21,21,21-pentafluoro-17-hidroxi-11ß-[4-(hidroxiacetil)fenil]-19-nor-17a-pregna-4,9-dien-3-ona.
21. Un compuesto según cualquiera de las reivindicaciones 1 a 7 en forma aislada, preferiblemente en forma sólida.
22. Un compuesto según cualquiera de las reivindicaciones 3 ó 4 cuando está sustancialmente libre del otro compuesto de las reivindicaciones 3 ó 4, en el que la expresión "sustancialmente libre" significa que el compuesto de la reivindicación 3 ó 4 está al menos 90% libre del isómero correspondiente, que es el otro compuesto de la reivindicación 3 ó 4.
23. Un fármaco según cualquiera de las reivindicaciones 6 a 10 adaptado para administración oral, preferiblemente como una forma de dosificación unitaria.
24. Un fármaco según cualquiera de las reivindicaciones 6 a 10 u 11, que contiene de 0,01 mg a 100 mg del compuesto de la reivindicación 1.
Patentes similares o relacionadas:
Derivados de ácidos biliares como agonistas FXR/TGR5, del 1 de Julio de 2020, de ENANTA PHARMACEUTICALS, INC: Un compuesto representado por la Formula I, o una sal o ester aceptable farmaceuticamente de este: **(Ver fórmula)** en donde: Ra es hidrogeno o -C1-C8 alquilo […]
Procedimiento industrial para la síntesis de acetato de ulipristal y su análogo 4-acetilo, del 21 de Mayo de 2019, de RICHTER GEDEON NYRT: Un procedimiento para la síntesis del compuesto de fórmula (I)**Fórmula** en el que el significado de R es un grupo dimetilamino o acetilo, caracterizado porque a) […]
Compuestos que comprenden uno o más dominios hidrófobos y un dominio hidrófilo que comprende restos de PEG, útiles para unir células, del 9 de Abril de 2019, de F. HOFFMANN-LA ROCHE AG: Un compuesto que comprende, preferentemente que consiste en, uno o más dominios hidrófobos y un dominio hidrófilo, en el que el uno o más dominios […]
Antagonistas de progesterona, del 26 de Octubre de 2018, de Evestra, Inc: Un compuesto que tiene la estructura:**Fórmula** en donde R7 es (E)-CH≥CH-CF3, -CH2-CF≥CF2 o -CF2-CH≥CH2
Procedimiento de producción de derivados de 21-metoxi-11-beta-fenil-19-nor-pregna-4,9-dieno-3,20-diona, del 24 de Septiembre de 2018, de RICHTER GEDEON NYRT: Procedimiento de síntesis de un compuesto de fórmula (I)**Fórmula** en la que el significado de R es un grupo dimetilamino o acetilo, caracterizado por […]
Derivados de testosterona con una sustitución carboxialquilo en la posición 3 y sus utilizaciones para la producción de los esteroides marcados para la determinación de la concentración de testosterona en una muestra biológica, del 23 de Agosto de 2017, de BIOMERIEUX: Derivado de testosterona de fórmula general (I) siguiente:**Fórmula** en la que n es un número entero comprendido entre 1 y 10 e Y representa un grupo […]
Un procedimiento para la producción de 19-norpregn-4-en-3,20-diona-17?-ol (gestonorona) y productos intermedios correspondientes, del 26 de Octubre de 2016, de RICHTER GEDEON NYRT: Un procedimiento para la síntesis de (17α)-17-acetil-17-hidroxi-estr-4-en-3-ona de fórmula (I)**Fórmula** caracterizado por hacer reaccionar el compuesto […]
Proceso para la producción de intermediarios de estetrol, del 6 de Abril de 2016, de Estetra S.P.R.L: Proceso para la preparacion de un compuesto de fórmula **Fórmula** dicho proceso comprendiendo las etapas de: a) reaccionar un compuesto de formula , con […]