Análogos sintéticos de péptidos de regeneración neuronal.
Un compuesto de péptido de regeneración neuronal (PRN) sintético que comprende un dominio de péptidomodificado APGR y/o un dominio de péptido modificado RAGG,
en el que el compuesto PRN se selecciona delgrupo que consiste en la SEC ID Nº: 4, SEC ID N º: 5 y SEC ID Nº: 6.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2008/011951.
Solicitante: Curonz Holdings Company Limited.
Nacionalidad solicitante: Nueva Zelanda.
Dirección: Level 1, 29 Nugent Street Auckland NUEVA ZELANDA.
Inventor/es: BRIMBLE,MARGARET,ANNE, HARRIS,PAUL WILLIAM RICHARD, SIEG,FRANK.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C07K14/435 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 14/00 Péptidos con más de 20 aminoácidos; Gastrinas; Somatostatinas; Melanotropinas; Sus derivados. › de animales; de humanos.
- C07K14/475 C07K 14/00 […] › Factores de crecimiento; Reguladores de crecimiento.
PDF original: ES-2433568_T3.pdf
Fragmento de la descripción:
Análogos sintéticos de péptidos de regeneración neuronal
Campo de la invención La presente invención se refiere a análogos sintéticos de péptidos de acuerdo con las reivindicaciones que tienen propiedades de regeneración neuronal, migración, proliferación, diferenciación y/o crecimiento axonal. Estos péptidos se denominan “Péptidos de Regeneración Neuronal” o “PRN.” En particular, la presente invención se refiere a análogos de péptidos relativamente cortos de acuerdo con las reivindicaciones que tienen una o más propiedades biológicas de los PRN.
Antecedentes Los péptidos de regeneración neuronal (PRN) son una clase de péptidos que se ha demostrado que presentan propiedades deseables para promover la función neuronal en mamíferos. Estas funciones incluyen supervivencia neuronal, proliferación neuronal, crecimiento neuronal, migración neuronal y diferenciación neuronal. Anteriormente se han descrito diversos PRN, e incluyen los desvelados en las Solicitudes de Patente de Estados Unidos Nos 10/225.838 y 10/976.699, PCT/US02/026782, PCT/US2004/036203, PCT/US2006017534 (WO 2006/121926) y PCT/US2006026994.
Resumen Los PRN descritos hasta ahora tienen propiedades farmacodinámicas deseables y promueven la regeneración neuronal, migración, proliferación, diferenciación y/o crecimiento axonal. Recientemente se han descubierto análogos de PRN sintéticos que también tienen propiedades farmacocinéticas mejoradas. Existe una necesidad en la técnica de moléculas sintéticas o péptidos modificados que tengan propiedades farmacodinámicas deseables similares a las de los PRN pero que también tengan propiedades farmacocinéticas mejoradas y/o sean químicamente estables.
Determinados aspectos de la presente incluyen nuevas moléculas de análogos de PRN sintéticos que pueden usarse para tratar trastornos del sistema nervioso central u otros sistemas en los que los PRN son eficaces. Otro aspecto es proporcionar terapias para trastornos de degeneración y muerte celular, incluyendo determinados trastornos del sistema nervioso. En algunos aspectos, los análogos de PRN sintéticos pueden usarse para tratar
efectos adversos de esclerosis lateral amiotrófica (ELA) , esclerosis múltiple (EM) , estrés oxidativo (por ejemplo, enfermedad de Huntington) o neuropatía periférica (NP) . Un aspecto adicional de la presente invención es la producción de análogos de PRN con estabilidad mejorada.
Debe entenderse que las expresiones “compuesto PRN”, “análogo de PRN”, “SEC ID Nº:” y otras expresiones de este tipo, para simplificar, se usan para identificar las moléculas de la invención y no para proporcionar su completa caracterización. Por tanto, en el presente documento, un “análogo de PRN” puede caracterizarse por tener una secuencia de aminoácidos particular, una representación de la estructura bidimensional particular, pero se entiende que la molécula en sí reivindicada tiene otras características, incluyendo estructura 3-dimensional, movilidad sobre determinados enlaces y otras propiedades de la molécula en su conjunto. Las moléculas en sí mismas y sus 45 propiedades son, en general, los objetos de la presente invención.
También debe entenderse que la denominación de un péptido como un “PRN” no significa que este tenga exclusivamente efectos neuronales. Más bien, la expresión PRN pretende incluir péptidos que tengan componentes estructurales similares, como se describe en las solicitudes de patente anteriores, aunque puedan tener efectos sobre otros tipos de células, tejidos y/u órganos. En determinadas realizaciones, se proporcionan análogos de PRN relativamente cortos que pueden tener mayor estabilidad, debido, al menos en parte, a una menor degradación enzimática. En otras realizaciones, se proporcionan análogos de PRN que tienen aminoácidos modificados. En otras realizaciones adicionales, se proporcionan análogos de PRN que tienen sustituyentes no aminoacídicos que reemplazan aminoácidos.
Breve descripción de las figuras La presente invención se describirá con referencia a sus realizaciones específicas. Otras características y aspectos de la presente invención pueden apreciarse por referencia a las Figuras, en las que:
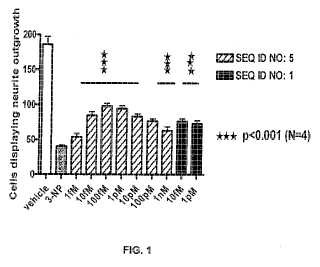
La Figura 1 representa un gráfico de efectos neuroprotectores de dos PRN, la SEC ID Nº 5 de la presente invención y la SEC ID Nº 1 en cultivos celulares expuestos a la neurotoxina 3-NP.
La Figura 2 representa un gráfico de resultados de estudios de efectos neuroprotectores de la SEC ID Nº 1 en el que el péptido se conservó - 20 C y a - 4 ºC.
La Figura 3 representa un gráfico de resultados de estudios de efectos neuroprotectores de la SEC ID Nº 5 de la presente invención en el que el péptido se conservó a -20 °C o - 4 °C.
La Figura 4 representa un gráfico de resultados de un estudio ampliado de efectos neuroprotectores de la SEC ID Nº 5 de la presente invención y de la SEC ID Nº 1 en cultivos celulares tratados con la neurotoxina 3-NP, similares a los mostrados en la Figura 1.
La Figura 5 representa un gráfico que muestra efectos significativos a largo plazo de la secuencia
REGRRDAPGRAGG (SEC ID Nº 12) de la presente descripción disminuyendo la gravedad de disfunción motora en animales con EAE, cuando el PRN sintético se administró en el punto máximo de la enfermedad. La puntuación 1 es la puntuación más baja y solo implica una cola flácida, mientras que las puntuaciones más altas implican debilidad (puntuación 2) o parálisis completa de las patas traseras (puntuación 3) . Para el análisis estadístico se utilizó el ensayo de Kruskal-Wallis; ** p < 0, 01 frente puntuación del día 1 de tratamiento (datos expresados como media ± ETM) . La Figura 6 representa un gráfico de resultados de puntuaciones de marcha en barra de equilibrio (beam walking) de ratas con neuropatía periférica inducida por piridoxina (800 mg/kg/día) y tratadas con vehículo o con la SEC ID Nº 5 de la presente invención a dos dosis diferentes. La Figura 7 representa un gráfico de resultados de puntuaciones de marcha en barra de equilibrio de ratas con neuropatía periférica inducida por piridoxina (1.200 mg/kg) y tratadas con vehículo o con la SEC ID Nº 5 de la presente invención. La Figura 8 representa gráficos de resultados de estudios de longevidad de ratones con un modelo murino de esclerosis lateral amiotrófica (ELA) y los efectos de dos dosis diferentes de un PRN sintético de la presente invención, SEC ID Nº 5.
Descripción detallada En la presente descripción, se proporcionan compuestos PRN que tiene una secuencia de un péptido nativo. Por ejemplo, un PRN de este tipo es un péptido que tiene una longitud de 11 aminoácidos (11 unidades) con la siguiente estructura.
NH2-G1RRAAPGRAGG11-NH2SEC ID Nº 1
Debe apreciarse que los compuestos sintéticos o análogos de los PRN pueden tener extremos C amidados o pueden tener restos hidroxilo (OH) C terminales. También debe apreciarse que las expresiones “compuesto PRN”, “análogo de PRN” y expresiones similares se refieren a compuestos de la presente invención o a péptidos PRN o a proteínas PRN previamente descritos.
Análogos sintéticos de los PRN
La presente invención proporciona análogos sintéticos de los PRN que pueden tener uno o más de los siguientes tipos de modificaciones: (1) estabilización de giros β, (2) reemplazo de restos de glicina, (3) reemplazo del resto de glicina N terminal y/o (4) ciclado.
1. Estabilización de giros
Las probabilidades de Chou y Fasman para la predicción de giros β revelan que en la SEC ID Nº 1 pueden encontrarse giros β probables en los dominios APGR (SEC ID Nº 2) y RAGG (SEC ID Nº 3) , como se indica a continuación en negrita:
SEC ID Nº 1. NH2. G1RRAAPGRAGG11-NH2 SEC ID Nº 1
Los giros β pueden estabilizarse introduciendo impedimentos estéricos tales como aminoácidos alquilados. Entre los aminoácidos fáciles de conseguir que pueden usarse se incluyen el ácido aminoisobutírico (Aib, α-H en alanina 50 reemplazada con metilo) que puede usarse como un reemplazo para cualquiera o ambos restos de alanina y glicina.
A. Modificación del dominio APGR
En la secuencia APGR (SEC ID Nº 2) , la alanina o la glicina pueden reemplazarse con ácido aminoisobutírico 55 (Aib) . La sustitución de la alanina con Aib produce el siguiente análogo de la invención: NH2-G1 RRA-Aib-PGRAGG11 -NH2 SEC ID Nº 4
B. Modificación del dominio RAGG
En otra secuencia de giro β probable, RAGG (SEC ID Nº 3) , la alanina puede reemplazarse con ácido aminoisobutírico... [Seguir leyendo]
Reivindicaciones:
1. Un compuesto de péptido de regeneración neuronal (PRN) sintético que comprende un dominio de péptido modificado APGR y/o un dominio de péptido modificado RAGG, en el que el compuesto PRN se selecciona del 5 grupo que consiste en la SEC ID Nº: 4, SEC ID Nº: 5 y SEC ID Nº: 6.
2. El compuesto PRN sintético de la reivindicación 1 que consiste en la SEC ID Nº 5.
3. El compuesto PRN sintético de la reivindicación 1 que consiste en la SEC ID Nº 4. 10
4. Una composición farmacéutica que comprende el compuesto PRN sintético de una cualquiera de las reivindicaciones 1 a 3 y un excipiente farmacéuticamente aceptable.
5. El compuesto PRN sintético de una cualquiera de las reivindicaciones 1 a 3 o la composición farmacéutica de la 15 reivindicación 4 para su uso en terapia.
6. El compuesto PRN sintético de una cualquiera de las reivindicaciones 1 a 3 o la composición farmacéutica de la reivindicación 4 para su uso en un procedimiento de tratamiento de un trastorno neurológico en un mamífero, que comprende administrar al mamífero una cantidad farmacéuticamente eficaz del compuesto PRN sintético o de la composición farmacéutica.
7. El compuesto PRN sintético o la composición farmacéutica de la reivindicación 6, en donde el trastorno neurológico es esclerosis lateral amiotrófica, lesión neurotóxica, lesión oxidativa, esclerosis múltiple, neuropatía periférica, hipoxia/isquemia, lesión craneal traumática o cirugía de injerto de derivación de la arteria coronaria,
preferentemente neuropatía periférica diabética.
Patentes similares o relacionadas:
 Proteínas de dominio de fibronectina tipo III con solubilidad mejorada, del 24 de Junio de 2020, de BRISTOL-MYERS SQUIBB COMPANY: Un polipéptido que comprende restos de armazones a base de fibronectina que comprenden un 10º dominio de fibronectina tipo III (10Fn3) modificado, […]
Proteínas de dominio de fibronectina tipo III con solubilidad mejorada, del 24 de Junio de 2020, de BRISTOL-MYERS SQUIBB COMPANY: Un polipéptido que comprende restos de armazones a base de fibronectina que comprenden un 10º dominio de fibronectina tipo III (10Fn3) modificado, […]
Material basado en polímero con secuencias peptídicas unidas mediante enlace covalente, degradables por vía enzimática, del 17 de Junio de 2020, de TissueGUARD GmbH: Material basado en polímero con secuencias peptídicas unidas mediante enlace covalente, degradables por vía enzimática, que presentan al menos un punto disociable […]
Moléculas de ácido nucleico de Nucampholin para controlar plagas de insectos coleópteros, del 17 de Junio de 2020, de FRAUNHOFER-GESELLSCHAFT ZUR FORDERUNG DER ANGEWANDTEN FORSCHUNG E.V.: Una molécula de ácido nucleico aislada que comprende un polinucleótido que codifica una molécula de ácido ribonucleico de horquilla (hpARN) con una estructura […]
PÉPTIDO DE MITICINA Y SU USO EN REGENERACIÓN CELULAR, del 4 de Junio de 2020, de CONSEJO SUPERIOR DE INVESTIGACIONES CIENTIFICAS: La presente invención se refiere a unos péptidos derivados de la micitina C y sus usos terapéuticos, más concretamente en la regeneración celular y/o […]
Péptido de miticina y su uso en regeneración celular, del 28 de Mayo de 2020, de CONSEJO SUPERIOR DE INVESTIGACIONES CIENTIFICAS: Péptido de miticina y su uso en regeneración celular. La presente invención se refiere a unos péptidos derivados de la micitina C y sus usos terapéuticos, más concretamente […]
Proteínas recombinantes y sus usos terapéuticos, del 27 de Mayo de 2020, de Bioven 3 Limited: Una proteína recombinante, que comprende: una secuencia polipeptídica inmunogénica que incluye la subunidad B de la toxina del cólera (CT-B) o la subunidad […]
Procedimiento de purificación de G-CSF, del 27 de Mayo de 2020, de MYLAN PHARMACEUTICALS, INC: Procedimiento de purificación de factor recombinante estimulador de colonias de granulocitos (G-CSF), que comprende al menos una cromatografía de intercambio […]
Enzimas con actividad ácido clorogénico esterasa y actividad feruloil esterasa, del 27 de Mayo de 2020, de SternEnzym GmbH & Co. KG: Una enzima con actividad ácido clorogénico esterasa y actividad feruloil esterasa que comprende una secuencia que tiene al menos 85 % de identidad de aminoácidos […]