3,5-DIHIDROXI-2,2-DIMETIL-VALERONITRILOS PARA LA SINTESIS DE EPOTILONES Y SUS DERIVADOS Y PROCEDIMIENTO PARA LA PREPARACION Y LA UTILIZACION.
Compuestos de la fórmula general I **(Ver fórmula)** en la que R1 y R2 pueden ser iguales o diferentes y representan,
independientemente uno de otro, un grupo protector de alcohol o, en el caso de que R1 y R2 estén puenteados, representan un grupo protector de cetal
Tipo: Resumen de patente/invención. Número de Solicitud: W0208730EP.
Solicitante: BAYER SCHERING PHARMA AKTIENGESELLSCHAFT.
Nacionalidad solicitante: Alemania.
Dirección: MULLERSTRASSE 178,13353 BERLIN.
Inventor/es: PLATZEK, JOHANNES, DR., PETROV, ORLIN, WESTERMANN, JURGEN.
Fecha de Publicación: .
Fecha Concesión Europea: 30 de Septiembre de 2009.
Clasificación Internacional de Patentes:
- C07C253/30 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07C COMPUESTOS ACICLICOS O CARBOCICLICOS (compuestos macromoleculares C08; producción de compuestos orgánicos por electrolisiso electroforesis C25B 3/00, C25B 7/00). › C07C 253/00 Preparación de nitrilos de ácidos carboxílicos (de cianógeno o sus compuestos C01C 3/00). › por reacciones que no implican la formación de grupos ciano.
- C07C255/12 C07C […] › C07C 255/00 Nitrilos de ácidos carboxílicos (cianógeno o sus compuestos C01C 3/00). › que contienen grupos ciano y grupos hidroxi unidos a la estructura carbonada.
- C07C255/13 C07C 255/00 […] › que contienen grupos ciano y grupos hidroxi eterificados unidos a la estructura carbonada.
- C07C255/20 C07C 255/00 […] › estando la estructura carbonada sustituida además por átomos de oxígeno unidos por enlaces sencillos.
- C07D319/06 C07 […] › C07D COMPUESTOS HETEROCICLICOS (Compuestos macromoleculares C08). › C07D 319/00 Compuestos heterocíclicos que contienen ciclos de seis miembros que tienen dos átomos de oxígeno como únicos heteroátomos del ciclo. › no condensados con otros ciclos.
- C12P13/00B
- C12P41/00C2
Clasificación PCT:
- C07C253/30 C07C 253/00 […] › por reacciones que no implican la formación de grupos ciano.
- C07C255/12 C07C 255/00 […] › que contienen grupos ciano y grupos hidroxi unidos a la estructura carbonada.
- C07C255/13 C07C 255/00 […] › que contienen grupos ciano y grupos hidroxi eterificados unidos a la estructura carbonada.
- C07C255/20 C07C 255/00 […] › estando la estructura carbonada sustituida además por átomos de oxígeno unidos por enlaces sencillos.
- C07D319/06 C07D 319/00 […] › no condensados con otros ciclos.
Clasificación antigua:
- C07C253/30 C07C 253/00 […] › por reacciones que no implican la formación de grupos ciano.
- C07C255/16 C07C 255/00 […] › que contienen grupos ciano y átomos de oxígeno unidos por enlaces sencillos, unidos al mismo átomo de carbono de una estructura carbonada acíclica.
- C07D301/02 C07D […] › C07D 301/00 Preparación de oxiranos. › Síntesis del ciclo de oxirano.
- C07D319/06 C07D 319/00 […] › no condensados con otros ciclos.
- C07F7/18 C07 […] › C07F COMPUESTOS ACICLICOS, CARBOCICLICOS O HETEROCICLICOS QUE CONTIENEN ELEMENTOS DISTINTOS DEL CARBONO, HIDROGENO, HALOGENOS, OXIGENO, NITROGENO, AZUFRE, SELENIO O TELURO (porfirinas que contienen metal C07D 487/22; compuestos macromoleculares C08). › C07F 7/00 Compuestos que contienen elementos de los grupos 4 o 14 del sistema periódico. › Compuestos que tienen uno o más enlaces C— Si así como uno o más enlaces C— O— Si.
Fragmento de la descripción:
3,5-dihidroxi-2,2-dimetil-valeronitrilos para la síntesis de epotilones y sus derivados y procedimiento para la preparación y la utilización.
El invento se refiere al objeto caracterizado en las reivindicaciones, es decir a unos nuevos productos intermedios y procedimientos nuevos para su preparación, y a su utilización. El procedimiento para la preparación de nuevos productos intermedios parte de unos baratos materiales de partida, proporciona los productos intermedios en altas purezas en cuanto a enantiómeros, en una alta pureza química, así como en buenos rendimientos y permite la preparación a gran escala técnica.
El invento se utiliza en la síntesis del eslabón A de epotilones naturales y modificados por síntesis o de derivados de éstos. Los epotilones son unos anillos del tipo de macrólidos de 16 miembros, que se aislaron a partir de cultivos de la mixobacteria Sorangium Cellosum y son representantes de una clase de unos muy prometedores agentes antitumorales, que habían sido ensayados como eficaces contra una serie de linajes de cáncer. Una recopilación acerca de las síntesis ha sido descrita por J. Mulzer y colaboradores en J. Org. Chem. 2000, 65, 7.456-7.467.
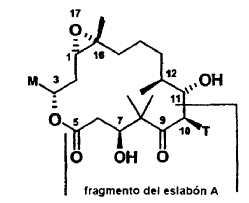
En la bibliografía, junto a los epotilones naturales, se ha descrito un gran número de derivados sintéticos de epotilones, que varían en su mayor parte dentro de los radicales M y T. M representa aquí en la mayoría de los casos un radical heterocíclico. La mayoría de las síntesis de los epotilones naturales y de los derivados sintéticos de epotilones utilizan el fragmento del eslabón A, que representa a los átomos de carbono C5 - C10 en el macrólido. Dentro de este eslabón A (véase más adelante) el C1 es el C5 en el macrólido y el C6 es el C10 en el macrólido, etc.
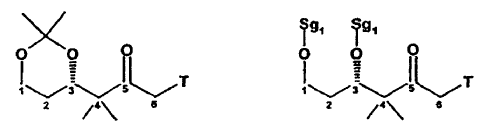
En este caso, T representa un alquilo de C1-C4 o un radical alquenilo, Sg1 y Sg2 representan unos grupos protectores que son habituales para un experto en la especialidad, tales como, por ejemplo, el grupo TBDMS.
Una posible preparación del eslabón A se describe, por ejemplo, en el documento de solicitud de patente internacional WO 00/58254. En él se divulga una síntesis a base de ß-cetoésteres, que se pueden transformar en el eslabón A en unas secuencias de varias etapas. La quiralidad es introducida por medio de una hidrogenación asimétrica de un ß-cetoéster de acuerdo con Noyori:

La transformación del grupo éster en una cetona se puede realizar en este caso solamente mediante una secuencia de varias etapas. En este caso, después de realizar una protección de los grupos 1- y 3-hidroxi, se reduce el grupo éster (átomo C-5) para formar el alcohol, y se lleva a cabo la oxidación para formar el aldehído, la reacción por adición de Grignard de un radical alquilo con un compuesto de alquil-magnesio o respectivamente de alquil-litio proporciona un alcohol secundario, que se oxida a continuación. Con el fin de acceder a partir del éster a la cetona, son necesarias en total 8 etapas. La reacción directa de un éster no es selectiva, puesto que el producto preparado de manera intermedia reacciona ulteriormente. El siguiente esquema muestra la vía total de síntesis:
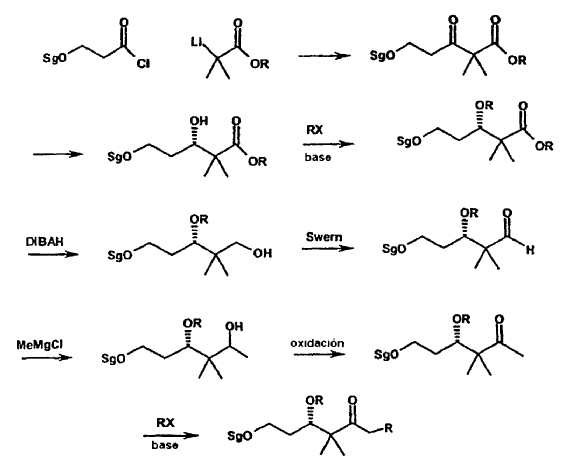
B. Paniker y colaboradores, en Tetrahedron 2000, 56, 78-59-7.868, han descrito un método para la síntesis del eslabón A. Allí se describe que la reacción aldólica con un eslabón quiral proporciona una reacción poco selectiva. A través del rodeo que pasa por una N-metil-tioacetil-oxazolidona se describe la síntesis del átomo C3 quiral en una secuencia de varias etapas con una diastereoselectividad mejorada por medio de un borenolato. Para conseguir unas diastereoselectividades útiles, es necesaria una sustitución del grupo metil-tio; el tioéter se separa después de la reacción aldólica.
Además, a partir del estado de la técnica (R. E. Taylor, Y. Chen, Org, Lett. (2001), 3(14), 2.221-2.224) se puede deducir una secuencia, en la que se utiliza un éster fenílico para la reacción de Grignard. El rendimiento conseguido en este caso se indica como de 77%. En el ejemplo descrito por A. Fürstner, en Chem. Comm. 2001, 1.057-1.059 se consigue un rendimiento de 67%. Estos rendimientos de la reacción de Grignard a partir del estado de la técnica son manifiestamente más bajos que los del presente invento.
En J. Org. Chem. 2000, 65, 7.456-7.467 se describe adicionalmente una síntesis asimétrica de un ß-cetoéster, llevándose a cabo una variante en una forma asimétrica como una reacción aldólica. Como catalizador, en este método se utiliza D-Ts-valina, que se puede preparar a partir del caro aminoácido D-valina. Este método proporciona un valor del ee (exceso enantiomérico) de 90%. Otro ejemplo acerca de esto es descrito por R. E. Taylor, Y. Chen, Org. Lett (2001), 3(14), 2.221-2.224, como una reacción aldólica asimétrica, en la que el rendimiento es de 71%.
Un método adicional para la preparación de un eslabón A de etil-cetona, protegido doblemente con TBDMS, es descrito finalmente por Nicolaou en Chem. Eur. J. 2000, 6, 2.783-2.800.
El presente invento comprende la misión de poder preparar un compuesto intermedio de partida de la fórmula general I, empleable universalmente, así como de los antípodas ópticamente puros de las fórmulas generales Ia y Ib.
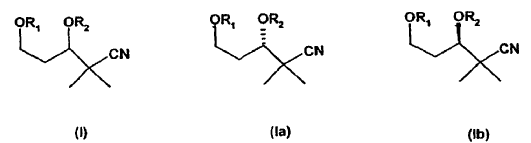
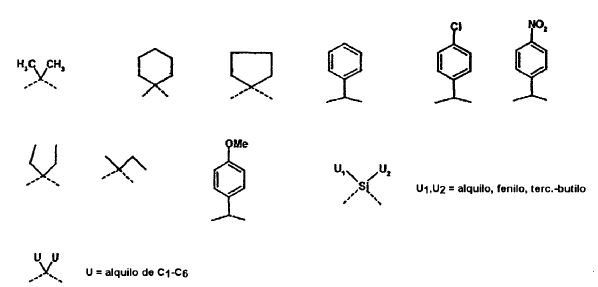
en las que los R1 y R2 pueden ser iguales o diferentes y representan, independientemente uno de otro, un grupo protector de alcohol habitual para un experto en la especialidad, por ejemplo, bencilo, 4-metoxi-bencilo, 3,4-dimetoxi-bencilo, THP, TBDMS, TMS, TES, TIP, TBDPS, MEM, MOM, alilo, tritilo,
o en el caso de que R1 y R2 estén puenteados, representan un grupo protector de cetal, tal como p.ej.
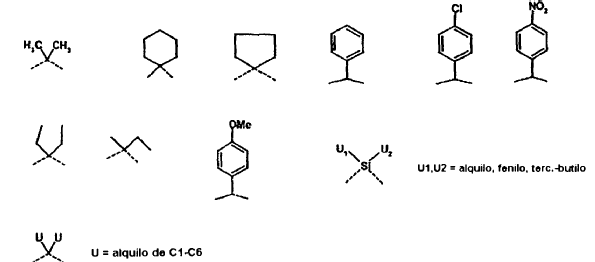
a fin de preparar fragmentos del eslabón A para unas síntesis totales de epotilones.
A este fin, se hacen reaccionar unos compuestos de la fórmula general I tal como se describe a continuación:

Las reacciones de compuestos de la fórmula general I, así como de sus antípodas Ia y Ib para formar las cetonas AK se efectúan con metil-litio o con compuestos metílicos de Grignard según procedimientos clásicos conocidos para un experto en la especialidad, el tratamiento acuoso proporciona entonces la cetona. La subsiguiente alquilación con un halogenuro de alquilo o de alquenilo de la fórmula T-Hal (Hal = Cl, Br, J, o tosilato, mesilato, triflato, etc.) mediando adición de una base, proporciona los fragmentos del eslabón A.
Sin embargo, también se puede acceder directamente al A, haciendo reaccionar las amidas de la fórmula general I directamente con compuestos orgánicos metálicos tales como p.ej. el compuesto de litio Li-CH2-T y tratando a continuación con agua. Las reacciones químicas arriba descritas transcurren por lo general sin problemas y proporcionan los eslabones A en altos rendimientos.
Por lo tanto, subsistía la necesidad de un procedimiento realizable a gran escala técnica, que permita poner a disposición un compuesto intermedio empleable universalmente para la preparación del eslabón A al realizar la síntesis total de epotilones.
Junto a los altos rendimientos al realizar la transformación en los eslabones A, se ha de resaltar la accesibilidad relativamente fácil de los compuestos de la fórmula general I a partir de unos materiales de partida relativamente baratos. Además de esto, los compuestos conformes al invento, al contrario que los ésteres y las cetonas que se conocen a partir de la bibliografía, son estables en almacenamiento y pueden hacerse reaccionar, según sea necesario, durante una campaña de síntesis en curso. Los compuestos de la fórmula general I son en su mayor parte unos materiales sólidos cristalinos y pueden ser purificados mediante...
Reivindicaciones:
1. Compuestos de la fórmula general I
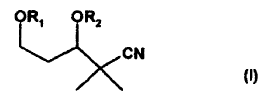
en la que
R1 y R2
pueden ser iguales o diferentes y representan, independientemente uno de otro, un grupo protector de alcohol o, en el caso de que R1 y R2 estén puenteados, representan un grupo protector de cetal.
2. Compuestos de la fórmula general Ia de acuerdo con la reivindicación 1,
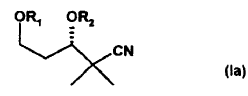
en la que
R1 y R2
pueden ser iguales o diferentes y representan, independientemente uno de otro, un grupo protector de alcohol o, en el caso de que R1 y R2 estén puenteados, representan un grupo protector de cetal.
3. Compuestos de la fórmula general Ib de acuerdo con la reivindicación 1,
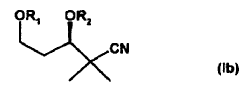
en la que
R1 y R2
pueden ser iguales o diferentes y representan, independientemente uno de otro, un grupo protector de alcohol o, en el caso de que R1 y R2 estén puenteados, representan un grupo protector de cetal.
4. Compuestos de acuerdo con las reivindicaciones 1, 2, 3, caracterizados porque R1 y R2 pueden ser iguales o diferentes y representan, independientemente uno de otro, un grupo protector de alcohol, tal como bencilo, 4-metoxi-bencilo, 3,4-dimetoxi-bencilo, THP, TBDMS, TMS, TES, TIP, TBDPS, MEM, MOM, alilo, tritilo, o en el caso de que R1 y R2 estén puenteados, representan un grupo protector de cetal


5. Compuestos de la fórmula general Ia de acuerdo con la reivindicación 2 escogidos entre la lista formada por
3(S)-3,5-acetona-dimetil-cetal-2,2-dimetil-pentano-nitrilo

3(S)-3,5-ciclohexanona-cetal-2,2-dimetil-pentano-nitrilo
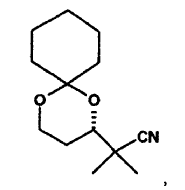
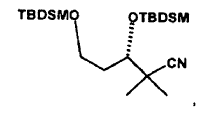
3(S)-3,5-di-terc.-butil-dimetil-sililoxi-2,2-dimetil-pentano-nitrilo
3,5-benzaldehído-acetal-2,2-dimetil-pentano-nitrilo
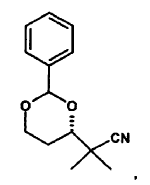
3,5-difenil-silano-2,2-dimetil-pentano-nitrilo

6. Compuestos de la fórmula II,
2,2-dimetil-3,5-dihidroxi-valeronitrilo y sus isómeros

7. Compuestos de acuerdo con la reivindicación 6, caracterizados porque la configuración junto al átomo de C del alcohol secundario es S.
8. Compuestos de acuerdo con la reivindicación 6, caracterizados porque la configuración junto al átomo de C del alcohol secundario es R.
9. Compuestos de la fórmula general III
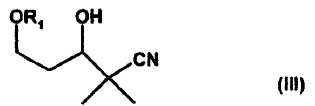
en la que
R1 representa un grupo protector de alcohol.
10. Compuestos de acuerdo con la reivindicación 9, caracterizados porque el grupo protector de alcohol R1 representa bencilo, 4-metoxi-bencilo, 3,4-dimetoxi-bencilo, THP, TBDMS, TMS, TES, TIP, TBDPS, MEM, MOM, alilo, tritilo.
11. Compuestos de acuerdo con la reivindicación 9 o 10, caracterizados porque la configuración junto al átomo de C del alcohol secundario es S.
12. Compuestos de acuerdo con la reivindicación 9 o 10, caracterizados porque la configuración junto al átomo de C del alcohol secundario es R.
13. Compuesto de acuerdo con la reivindicación 11, 5-benciloxi-2,2-dimetil-3(S)-hidroxi-pentano-nitrilo.
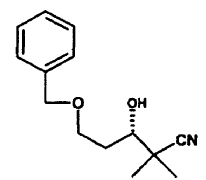
14. Compuestos de la fórmula general XII
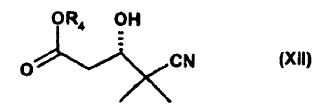
en la que
R4 representa un grupo alquilo de C1-C6, metilo, etilo, terc.-butilo, fenilo o bencilo.
15. Compuestos de acuerdo con la reivindicación 14, caracterizados porque la configuración junto al átomo de C del alcohol secundario es R.
16. Utilización de los compuestos de acuerdo con por lo menos una de las reivindicaciones 1 a 15 para la síntesis de epotilones naturales y sintéticos o de derivados de epotilones.
17. Procedimiento para la preparación de compuestos de acuerdo con las reivindicaciones 1 a 4, caracterizado porque, partiendo de los compuestos de acuerdo con las reivindicaciones 6 a 8, se protegen los grupos de alcohol con los grupos protectores R1 y R2.
18. Procedimiento de acuerdo con la reivindicación 17, caracterizado porque los grupos protectores R1 y R2 representan el grupo cetal de acetona y el grupo TBDMS.
19. Procedimiento para la preparación de compuestos ópticamente activos de la fórmula general IIIa
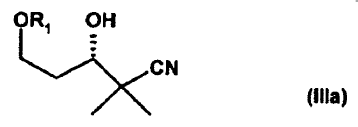
caracterizado porque se saponifica enantioselectivamente mediante una saponificación enzimática un éster racémico de la fórmula general VI
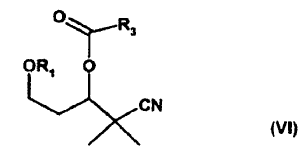
en la que
R1 representa un grupo protector de alcohol y
R3 representa un grupo alquilo de C1-C6 o un grupo alilo, fenilo o bencilo.
20. Procedimiento de acuerdo con la reivindicación 19, caracterizado porque la enzima utilizada para la saponificación es la lipasa Amano AY.
21. Procedimiento para la preparación de compuestos ópticamente activos de la fórmula general IIIa.
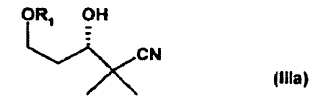
en la que
R1 representa un grupo protector de alcohol, caracterizado porque partiendo de los compuestos de la fórmula general VII
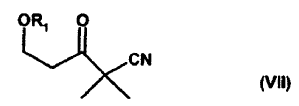
se lleva a cabo una reducción quiral del grupo ceto.
22. Procedimiento de acuerdo con la reivindicación 19 o 21, caracterizado porque el grupo protector de alcohol R1 representa bencilo, 4-metoxi-bencilo, 3,4-dimetoxi-bencilo, THP, TBDMS, TMS, TES, TIP, TBDPS, MEM, MOM, alilo, tritilo.
23. Procedimiento de acuerdo con la reivindicación 21, caracterizado porque la reducción quiral del grupo ceto se lleva a cabo mediante una hidrogenación catalítica con un catalizador del tipo de Noyori.
24. Procedimiento de acuerdo con la reivindicación 21, caracterizado porque la reducción quiral del grupo ceto se lleva a cabo mediante una reducción enzimática.
25. Procedimiento para la preparación de compuestos de la fórmula general XIII
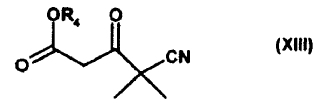
en la que
R4 representa un grupo alquilo de C1-C6, metilo, etilo, terc.-butilo, fenilo o bencilo,
caracterizado porque se hacen reaccionar unos compuestos de la fórmula general XIV

en la que
R4 representa un grupo alquilo de C1-C6, metilo, etilo, terc.-butilo, fenilo o bencilo.
Nu representa un grupo lábil tal como Cl, Br, imidazol, -OPh, -O-C6H4NO2, -O-alquilo de C1-C4
con un compuesto de la fórmula general V
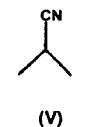
26. Procedimiento para la preparación de cetonas de la fórmula general A
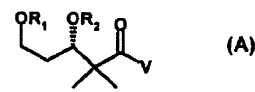
en la que R1 y R2 pueden ser iguales o diferentes y representan, independientemente uno de otro, un grupo protector de alcohol o, en el caso de que R1 y R2 estén puenteados, representan un grupo protector de cetal y V representa un radical alquilo de C1-C5 o un radical alquenilo,
caracterizado porque se hacen reaccionar unos compuestos de la fórmula general Ia
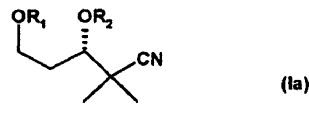
con unos compuestos de la fórmula general B
en la que M representa Li ó MgCl, MgBr o MgJ
y a continuación se tratan mediando una hidrólisis acuosa.
27. Procedimiento de acuerdo con la reivindicación 26, caracterizado porque R1 y R2 pueden ser iguales o diferentes y representan, independientemente uno de otro, un grupo protector de alcohol, tal como bencilo, 4-metoxi-bencilo, 3,4-dimetoxi-bencilo, THP, TBDMS, TMS, TES, TIP, TBDPS, MEM, MOM, alilo, tritilo o, en el caso de que R1 y R2 estén puenteados, representan un grupo protector de cetal.
28. Procedimiento de acuerdo con la reivindicación 26 o 27, caracterizado porque los compuestos de la fórmula general M-V representan MeLi, EtLi, propil-Li, BuLi, CH2=CH-CH2CH2-Li.
Patentes similares o relacionadas:
Compuestos que presentan actividad antioxidante contra radicales libres y actividad anti-inflamatoria, y las correspondientes composiciones farmacéuticas o cosméticas para cuidado de la piel, del 8 de Julio de 2020, de GIULIANI S.P.A.: Un compuesto que tiene la fórmula general (I): **(Ver fórmula)** donde R = H, CH2-OH, CH2-O-CO-CH3, CH2-O-CO-Ph (Ph = fenilo) R' = H, CH2-O-CO-CH3, […]
Procedimiento para la producción de monómeros a partir de mezclas de isómeros, del 22 de Enero de 2020, de Evonik Operations GmbH: Procedimiento para la producción de mezclas de ésteres de (met)acrilato, caracterizado por que se hace reaccionar una mezcla de isómeros de glicerinformal […]
(6R,10R)-6,10,14-Trimetilpentadecan-2-ona preparada a partir de 6,10-dimetilundec-5-en-2-ona o 6,10-dimetilundeca-5,9-dien-2-ona, del 24 de Julio de 2019, de DSM IP ASSETS B.V.: Un proceso de fabricación de (6R,10R)-6,10,14-trimetilpentadecan-2-ona en una síntesis de múltiples etapas a partir de 6,10-dimetilundec-5-en-2-ona o 6,10-dimetilundeca-5,9-dien-2-ona […]
Inhibidores de neprilisina, del 28 de Junio de 2019, de Theravance Biopharma R&D IP, LLC: Un compuesto de la fórmula I:**Fórmula** en donde, R1, es H, -alquilo-C1-8, -CH(CH3)OC(O)-O-ciclohexilo, -(CH2)2-morfolinilo, ó -CH2-5-metil-[1,3]dioxol-2-ona; […]
Nuevos acetales de la 1-(3,3-dimetilciclohex-1-enil)etanona, su procedimiento de preparación así como su utilización en perfumería, del 15 de Mayo de 2019, de V.MANE FILS: Compuesto de fórmula general I siguiente: en la que: - m y n representan un número de carbono y son, cada uno de ellos independientemente, 0 ó 1; - R1 representa […]
Síntesis de compuestos de carbomoilpiridona policíclica, del 27 de Febrero de 2019, de GILEAD SCIENCES, INC.: Un proceso para preparar un compuesto de Fórmula ß-1•J-1 de acuerdo con el siguiente esquema:**Fórmula** en el 15 que el proceso comprende hacer […]
Compuesto intermedios y proceso para la preparación de fingolimod, del 25 de Enero de 2019, de Mapi Pharma Limited: Un proceso para la preparación de Fingolimod de fórmula ,**Fórmula** o una sal farmacéuticamente aceptable del mismo, que comprende las etapas de: a) reaccionar […]
Preparación de éster de 3,5-dioxohexanoato en dos etapas, del 21 de Marzo de 2018, de LONZA LTD.: Un método (B) para preparar un compuesto de fórmula (II);**Fórmula** R1 es Cl, Br y CN; el método (B) comprende un paso (C) y un paso (B); el paso (B) se […]