Inhibidores heterocíclicos de MEK y métodos de uso de los mismos.
Composicion farmaceutica que comprende un compuesto que tiene la formula IV:
**Fórmula**
o una sal farmaceuticamente aceptable del mismo, en la que:
R1 es Cl o F;
R3 es H, Me, Et, OH, Me0-, Et0-, HOCH2CH20-, HOCH2C(Me)20-, (S)-MeCH(OH)CH20-, (R)- HOCH2CH(OH)CH20-, ciclopropil-CH20-, HOCH2CH2-,
R7 es metilo o etilo, en el que dicho nnetilo y etilo estan opcionalmente sustituidos con uno o mas F; R8 es Br, I o SMe; y
R9 es H, alquilo C1-C4, Cl o CN, en el que dicho alquilo esta opcionalmente sustituido con uno o mas grupos seleccionados independientemente de F o CN, siempre que cuando
a) R1 es F, R8 es Br, R9 es H y R7 es o bien Me o bien Et, entonces R3 no puede ser HOCH2CH20;
b) R1 es F, R8 es I, R9 es H y R3 es Me0, entonces R7 no puede ser Me; y
c) R1 es F, R8 es Me, R9 es H y R3 es ciclopropil-CH20, entonces R7 no puede ser Me;
en combinación con un agente antitumoral o un inhibidor de la transducción de senates
Tipo: Patente Europea. Resumen de patente/invención. Número de Solicitud: E11003826.
Solicitante: ARRAY BIOPHARMA, INC..
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 3200 WALNUT STREET BOULDER, CO 80301 ESTADOS UNIDOS DE AMERICA.
Inventor/es: STOREY, RICHARD, ANTHONY, LYSSIKATOS, JOSEPH P., PITTAM, JOHN DAVID, BOOTH,REBECCA JANE, LEONARD,JOHN, FIELDING,MARK RICHARD, MARLOW,ALLISON L, SEO,JEONGBEOB, YANG,HONG WOON, WALLACE,Eli , BLAKE,Jim .
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K31/501 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › no condensadas y conteniendo otros heterociclos.
- A61P35/00 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › Agentes antineoplásicos.
- C07D213/80 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07D COMPUESTOS HETEROCICLICOS (Compuestos macromoleculares C08). › C07D 213/00 Compuestos heterocíclicos que contienen ciclos de seis miembros, no condensados con otros ciclos, con un átomo de nitrógeno como el único heteroátomo del ciclo y tres o más enlaces dobles entre miembros cíclicos o entre miembros cíclicos y miembros no cíclicos. › en posición 3.
- C07D213/82 C07D 213/00 […] › en posición 3.
- C07D213/84 C07D 213/00 […] › Nitrilos.
- C07D213/85 C07D 213/00 […] › en posición 3.
- C07D237/24 C07D […] › C07D 237/00 Compuestos heterocíclicos que contienen ciclos de diazina-1,2 o diazina-1,2 hidrogenada. › Atomos de carbono que tienen tres enlaces a heteroátomos con a lo más un enlace a halógeno.
PDF original: ES-2500068_T3.pdf
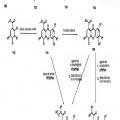
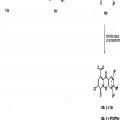
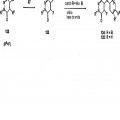
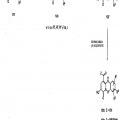
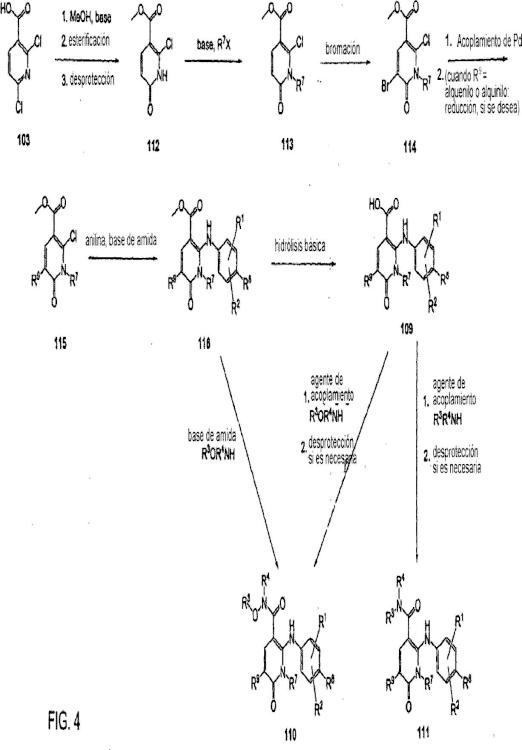
Fragmento de la descripción:
Inhibidores heterocíclicos de MEK y métodos de uso de los mismos Antecedentes de la invención Campo de la invención
Esta invención se refiere a una serie de compuestos heterocíclicos novedosos que son útiles en el tratamiento de enfermedades hiperproliferativas, tales como cáncer e inflamación, en mamíferos. Esta invención también se refiere al uso de tales compuestos en el tratamiento de enfermedades hiperproliferativas en mamíferos, especialmente seres humanos, y a composiciones farmacéuticas que contienen tales compuestos.
Descripción del estado de la técnica
La señalización celular a través de receptores del factor de crecimiento y proteínas cinasas es un regulador importante de la diferenciación, proliferación y crecimiento celular. En el crecimiento celular normal, los factores de crecimiento, a través de la activación del receptor (es decir PDGF o EGF y otros), activan las rutas de la MAP cinasa. Una de las rutas de la MAP cinasa más importante y mejor entendidas implicada en el crecimiento celular normal y no controlado es la ruta de la Ras/Raf cinasa. Ras unida a GTP activo da como resultado la activación y fosforilación indirecta de la Raf cinasa. Entonces Raf fosforila MEK1 y 2 en dos residuos de serina (S218 y S222 para MEK1 y S222 y S226 para MEK2) (Ahn et al., Methods in Enzymology, 2001, 332, 417-431). Entonces la MEK activada fosforila sólo sus sustratos conocidos, las MAP cinasas, ERK1 y 2. La fosforilación de ERK mediante MEK se produce en Y204 y T202 para ERK1 e Y185 y T183 para ERK2 (Ahn et al., Methods in Enzymology, 2001, 332, 417-431). La ERK fosforilada se dimeriza y entonces se traslada al núcleo en el que se acumula (Khokhlatchev ef al., Cell, 1998, 93, 605-615). En el núcleo, ERK está implicada en varias funciones celulares importantes, incluyendo pero sin limitarse al transporte nuclear, transducción de señales, reparación de ADN, ensamblaje de nucleosomas y translocación, y procesamiento de ARNm y traducción (Ahn et al., Molecular Cell, 2000, 6, 1343-1354). En general, el tratamiento de células con los factores de crecimiento conduce a la activación de ERK1 y 2 que da como resultado la proliferación y, en algunos casos, diferenciación (Lewis ef al., Adv. Cáncer Res., 1998, 74, 49-139).
En enfermedades proliferativas, mutaciones genéticas y/o sobreexpresión de los receptores del factor de crecimiento, proteínas de señalización posteriores, o proteínas cinasas implicadas en la ruta de la cinasa ERK conducen a la proliferación celular no controlada y, finalmente, a la formación de tumores. Por ejemplo, algunos cánceres contienen mutaciones que dan como resultado la activación continua de esta ruta debido a la producción continua de factores de crecimiento. Otras mutaciones pueden conducir a defectos en la desactivación del complejo de Ras unida a GTP activado, de nuevo dando como resultado la activación de la ruta de la MAP cinasa. Las formas oncogénicas mutadas de Ras se encuentran en el 50% de cánceres de colon y >90% de pancreático así como muchos otros tipos de cánceres (Kohl et al., Science, 1993, 260, 1834-1837). Recientemente, se han identificado las mutaciones en bRaf en más del 60% de melanomas malignos (Davies, H. et al., Nature, 2002, 417, 949-954). Estas mutaciones en bRaf dan como resultado una cascada de la MAP cinasa constitutivamente activa. Estudios de muestras de tumor primario y líneas celulares también han mostrado la activación constitutiva o sobreactivación de la ruta de la MAP cinasa en cánceres de páncreas, colon, pulmón, ovario y riñón (Hoshino, R. et al., Oncogene, 1999, 18, 813-822). Por tanto, existe una fuerte correlación entre cánceres y una ruta de la MAP cinasa sobreactiva que resulta de mutaciones genéticas.
Puesto que la activación constitutiva o sobreactivación de la cascada de la MAP cinasa desempeña un papel fundamental en la diferenciación y proliferación celular, se cree que la inhibición de esta ruta es beneficiosa en enfermedades hiperproliferativas. MEK es un responsable principal en esta ruta ya que es posterior a Ras y Raf. Adicionalmente, es una diana terapéutica atractiva debido a que los únicos sustratos conocidos para la fosforilación MEK son las MAP cinasas, ERK1 y 2. Se ha mostrado que la inhibición de MEK tiene un posible beneficio terapéutico en varios estudios. Por ejemplo, se ha mostrado que los inhibidores de MEK de molécula pequeña inhiben el crecimiento tumoral humano en xenoinjertos de ratones desnudos, (Sebolt-Leopold et al., Nature- Medlcine, 1999, 5 (7), 810-816; Trachet et al., AACR 6-10 de abril, 2002, Póster n.° 5426; Tecle, H IBC 2a International Conference of Protein Kinases, 9-10 de septiembre, 2002), bloquean alodlnia estática en animales (documento WO 01/05390) e inhiben el crecimiento de células de leucemia mieloide aguda (Mllella et al., J. Clin. Invest., 2001, 108 (6), 851-859).
Se han dado a conocer inhibidores de molécula pequeña de MEK, incluyendo en las publicaciones de patente estadounidense n.os 2003/0232869, 2004/0116710 y 2003/0216460, y las solicitudes de patente estadounidense con números de serle 10/654.580 y 10/929.295. Al menos quince solicitudes de patente adicionales han aparecido en los últimos años. Véanse, por ejemplo: la patente estadounidense n.° 5.525.625; los documentos WO98/43960, WO99/01421; WO99/01426; WO00/41505; WO00/42002; WO00/42003; WOOO/41994; WO00/42022; WO00/42029; WO00/68201; WO01/68619; W002/06213; W003/077914; y WO03/077855. El documento W005/000818 se refiere a derivados de fenilamino-2-piridona 5-sustituldo-4-(sustituido), a composiciones farmacéuticas y a usos de los mismos como inhibidores de MEK.
Sumario de la invención
La invención se describe adicionalmente mediante los siguientes puntos:
1. Una composición farmacéutica que comprende un compuesto que tiene la fórmula IV:
IV
o una sal farmacéuticamente aceptable del mismo, en la que:
R1 es Cl o F;
R3 es H, Me, Et, OH, MeO-, EtO-, H0CH2CH20-, H0CH2C(Me)20-, (S)-MeCH(OH)CH20-, (R)-
H0CH2CH(0H)CH20-, ciclopropil-CH20-, HOCH2CH2-,
hcO<, Hor Y V
*. OH
R7 es metilo o etilo, en el que dicho metilo y etilo están opcionalmente sustituidos con uno o más F;
R8 es Br, I o SMe; y
R9 es H, alquilo C1-C4, Cl o CN, en el que dicho alquilo está opcionalmente sustituido con uno o más grupos seleccionados independientemente de F o CN, siempre que cuando
a) R1 es F, R8 es Br, R9 es H y R7 es o bien Me o bien Et, entonces R3 no puede ser H0CH2CH20;
b) R1 es F, R8 es I, R9 es H y R3 es MeO, entonces R7 no puede ser Me; y
c) R1 es F, R8 es Me, R9 es H y R3 es ciclopropil-CH20, entonces R7 no puede ser Me; en combinación con un agente antitumoral o un inhibidor de la transducción de señales.
2. La composición farmacéutica según el punto 1, en la que R9 de la fórmula IV es H, Me, Et, Cl o CN.
3. Una composición farmacéutica que comprende un compuesto que tiene la fórmula VI:
H
o una sal farmacéuticamente aceptable del mismo, en la que:
R1 es Cl o F;
R3 es H, H0CH2CH20 o (S)-MeCH(OH)CH20; y R9 es H, Me, F o Cl,
en combinación con un agente antitumoral o un inhibidor de la transducción de señales.
4. La composición farmacéutica según el punto 3, en la que dicho compuesto de fórmula VI se selecciona de:
2-(2-cloro-4-yodofen¡lam¡no)-N-(2-h¡droxietoxi)-1-met¡l-6-oxo-1,6-dihidropir¡din-3-carboxamida;
(S)-2-(2-cloro-4-yodofenilamino)-N-(2-hidrox¡propoxi)-1-met¡l-6-oxo-1,6-d¡hidrop¡ridin-3-carboxamida;
2-(2-fluoro-4-yodofenilamino)-1,5-dimet¡l-6-oxo-1,6-dihidropirid¡n-3-carboxamida;
2-(2-fluoro-4-yodofenilamino)-N-(2-hidroxietoxi)-1-met¡l-6-oxo-1,6-dih¡drop¡ridin-3-carboxamida;
(S)-2-(2-fluoro-4-yodofenilam¡no)-N-(2-hidroxipropox¡)-1-met¡l-6-oxo-1l6-dih¡drop¡rid¡n-3-carboxam¡da;
(S)-2-(2-fluoro-4-yodofen¡lam¡no)-N-(2-hidroxipropoxi)-1,5-d¡met¡l-6-oxo-1,6-dih¡dropir¡din-3-carboxam¡da;
2-(2-cloro-4-yodofenilam¡no)-N-(2-hidrox¡etox¡)-1,5-d¡met¡l-6-oxo-1,6-d¡h¡drop¡r¡din-3-carboxam¡da;
5-cloro-2-(2-fluoro-4-yodofenilamino)-N-(2-h¡droxietox¡)-1-metil-6-oxo-1,6-d¡h¡dropiridin-3-carboxamida;
(S)-2-(2-cloro-4-yodofenilamino)-N-(2-hidroxipropox¡)-1,5-d¡met¡l-6-oxo-1,6-d¡h¡drop¡rid¡n-3-carboxamida;
(S)-5-cloro-2-(2-fluoro-4-yodofenilam¡no)-N-(2-h¡drox¡propox¡)-1-met¡l-6-oxo-1,6-d¡h¡drop¡r¡d¡n-3-carboxam¡da;
5-fluoro-2-(2-fluoro-4-yodofen¡lam¡no)-N-(2-hidroxietox¡)-1-met¡l-6-oxo-1,6-d¡h¡drop¡r¡d¡n-3-carboxamida; y
(S)-5-fluoro-2-(2-fluoro-4-yodofenilamino)-N-(2-h¡drox¡propox¡)-1-metil-6-oxo-1,6-dihidrop¡ridin-3-carboxamida.
5. La composición... [Seguir leyendo]
Reivindicaciones:
Composición farmacéutica que comprende un compuesto que tiene la fórmula IV:
O
IV
2.
3.
4.
o una sal farmacéuticamente aceptable del mismo, en la que:
R1 es Cl o F;
R3 es H, Me, Et, OH, MeO-, EtO-, H0CH2CH20-, H0CH2C(Me)20-, (S)-MeCH(OH)CH20-, (R)- H0CH2CH(0H)CH20-, ciclopropil-CH20-, HOCH2CH2-,
R7 es metilo o etilo, en el que dicho metilo y etilo están opcionalmente sustituidos con uno o más F;
R8 es Br, I o SMe; y
R9 es H, alquilo C1-C4, Cl o CN, en el que dicho alquilo está opcionalmente sustituido con uno o más grupos seleccionados independientemente de F o CN, siempre que cuando
a) R1 es F, R8 es Br, R9 es H y R7 es o bien Me o bien Et, entonces R3 no puede ser H0CH2CH20;
b) R1 es F, R8 es I, R9 es H y R3 es MeO, entonces R7 no puede ser Me; y
c) R1 es F, R8 es Me, R9 es H y R3 es ciclopropil-CH20, entonces R7 no puede ser Me; en combinación con un agente antitumoral o un inhibidor de la transducción de señales.
Composición farmacéutica según la reivindicación 1, en la que R9 de la fórmula IV es H, Me, Et, Cl o CN. Composición farmacéutica que comprende un compuesto que tiene la fórmula VI:
o una sal farmacéuticamente aceptable del mismo, en la que:
R1 es Cl o F;
R3 es H, H0CH2CH20 o (S)-MeCH(OH)CH20; y R9 es H, Me, F o Cl,
en combinación con un agente antitumoral o un inhibidor de la transducción de señales.
Composición farmacéutica según la reivindicación 3, en la que dicho compuesto de fórmula VI se selecciona de:
5.
6.
7.
8.
2-(2-cloro-4-yodofenilamino)-N-(2-h¡droxietoxi)-1-met¡l-6-oxo-1,6-d¡h¡drop¡r¡d¡n-3-carboxamida;
(S)-2-(2-doro-4-yodofen¡lamino)-N-(2-hidrox¡propox¡)-1-met¡l-6-oxo-1,6-d¡hidrop¡r¡din-3-carboxamida;
2-(2-fluoro-4-yodofenilam¡no)-1,5-d¡metil-6-oxo-1,6-d¡h¡dropir¡din-3-carboxamida;
2-(2-fluoro-4-yodofenilamino)-N-(2-h¡drox¡etox¡)-1-met¡l-6-oxo-1,6-d¡h¡drop¡r¡din-3-carboxam¡da;
(S)-2-(2-fluoro-4-yodofenilam¡no)-N-(2-h¡droxipropoxi)-1-metil-6-oxo-1,6-dih¡drop¡r¡d¡n-3-carboxam¡da;
(S)-2-(2-fluoro-4-yodofenilam¡no)-N-(2-h¡droxipropoxi)-1,5-dimetil-6-oxo-1,6-dihidropirid¡n-3-carboxam¡da;
2-(2-cloro-4-yodofenilamino)-N-(2-hidrox¡etox¡)-1,5-dimet¡l-6-oxo-1,6-dih¡drop¡r¡d¡n-3-carboxam¡da;
5-cloro-2-(2-fluoro-4-yodofenilamino)-N-(2-hidrox¡etox¡)-1-met¡l-6-oxo-1,6-d¡h¡drop¡r¡d¡n-3-carboxamida;
(S)-2-(2-cloro-4-yodofenilamino)-N-(2-hidroxipropoxi)-1,5-dimet¡l-6-oxo-1,6-d¡h¡dropirid¡n-3-carboxamida;
(S)-5-doro-2-(2-fluoro-4-yodofenilamino)-N-(2-hidroxipropox¡)-1-met¡l-6-oxo-1,6-dih¡dropir¡d¡n-3-
carboxamida;
5-fluoro-2-(2-fluoro-4-yodofenilamino)-N-(2-h¡droxietoxi)-1-met¡l-6-oxo-1,6-d¡h¡dropiridin-3-carboxamida; y
(S)-5-fluoro-2-(2-fluoro-4-yodofen¡lamino)-N-(2-h¡drox¡propox¡)-1-metil-6-oxo-1,6-dihidropiridin-3-
carboxamida.
Composición farmacéutica según la reivindicación 3, en la que el compuesto de fórmula VI es 2-(2-fluoro-4- yodofenilamino)-N-(2-hidroxietox¡)-1,5-dimetil-6-oxo-1,6-dihidropiridin-3-carboxamida.
Composición farmacéutica según la reivindicación 5 que comprende una forma cristalina de un compuesto de fórmula XI
sustancialmente en forma de la forma 2, 2-(2-fluoro-4-yodofenilamino)-N-(2-hidroxietoxi)-1,5-d¡met¡l-6-oxo- 1,6-dihidropiridin-3-carboxam¡da caracterizada por un patrón de difracción de rayos X que tiene picos de caracterización en aproximadamente 9,5 y 12,6 en la escala 20, en combinación con un agente antitumoral o un inhibidor de la transducción de señales.
Composición farmacéutica según la reivindicación 6, en la que la forma cristalina de 2-(2-fluoro-4- yodofenilamino)-N-(2-hidroxietoxi)-1,5-dimetil-6-oxo-1,6-dihidropiridin-3-carboxamida, el compuesto de fórmula XI se caracteriza por un patrón de difracción de rayos X sustancialmente tal como se muestra en la figura 10.
Composición farmacéutica según la reivindicación 5 que comprende una forma cristalina de un compuesto de fórmula XI
sustancialmente en forma de la forma 1, 2-(2-fluoro-4-yodofenilamino)-N-(2-hidroxietoxi)-1,5-dimetil-6-oxo-
1,6-dihidropirid¡n-3-carboxamida caracterizada por un patrón de difracción de rayos X que tiene picos de caracterización en aproximadamente 9,2 y 13,0 en la escala 20, en combinación con un agente antitumoral
11.
12.
13.
14.
o un inhibidor de la transducción de señales.
Composición farmacéutica según la reivindicación 8, en la que la forma cristalina de 2-(2-fluoro-4- yodofenilamino)-N-(2-hidroxietoxi)-1,5-dimetil-6-oxo-1,6-dihidropiridin-3-carboxamida, un compuesto de fórmula XI se caracteriza por un patrón de difracción de rayos X sustancialmente tal como se muestra en la figura 11.
Composición farmacéutica según cualquiera de las reivindicaciones 1-9, para el tratamiento de un trastorno hiperproliferativo en un mamífero.
Composición farmacéutica para su uso según la reivindicación 10, en la que dicho trastorno hiperproliferativo es cáncer o un trastorno no canceroso.
Composición farmacéutica para su uso según la reivindicación 11, en la que dicho cáncer es cáncer de cerebro, de pulmón, de células escamosas, de vejiga, gástrico, pancreático, de mama, de cabeza, de cuello, renal, de riñón, de ovario, de próstata, colorrectal, esofágico, testicular, ginecológico o de tiroides.
Composición farmacéutica para su uso según la reivindicación 11, en la que dicho trastorno no canceroso es hiperplasia benigna de la piel, reestenosis o próstata (por ejemplo, hipertrofia prostética benigna).
Composición farmacéutica para su uso según cualquiera de las reivindicaciones 1-13, en la que el agente antitumoral es un agente quimioterápico.
Composición farmacéutica para su uso según la reivindicación 14, en la que el agente quimioterápico se selecciona de fármacos antiproliferativos, fármacos antineoplásicos, agentes citostáticos, agentes antiinvasión, inhibidores de la función de factores de crecimiento, agentes antiangiogénicos, agentes de daño vascular, terapias antisentido, terapias génicas, ¡nterferón e inmunoterapia.
Patentes similares o relacionadas:
 Composiciones y métodos para el tratamiento de trastornos de células plasmáticas y trastornos prolinfocíticos de células b, del 29 de Julio de 2020, de Knopp Biosciences LLC: Una composición que comprende una cantidad terapéuticamente eficaz de dexpramipexol para su uso en el tratamiento de un trastorno de células B caracterizado por niveles elevados […]
Composiciones y métodos para el tratamiento de trastornos de células plasmáticas y trastornos prolinfocíticos de células b, del 29 de Julio de 2020, de Knopp Biosciences LLC: Una composición que comprende una cantidad terapéuticamente eficaz de dexpramipexol para su uso en el tratamiento de un trastorno de células B caracterizado por niveles elevados […]
Derivados de piperidina 1,4 sustituidos, del 29 de Julio de 2020, de 89Bio Ltd: Un compuesto de acuerdo con la Fórmula I: **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en donde: A se selecciona de […]
Profármacos de gemcitabina, del 29 de Julio de 2020, de NuCana plc: Una formulación farmacéutica que comprende gemcitabina-[fenil-benzoxi-L-alaninil)]-(S)-fosfato 3: **(Ver fórmula)** o una sal o solvato […]
Formas cristalinas de 6-((6,7-dimetoxiquinazolin-4-il)oxi)-N,2-dimetilbenzofuran-3-carboxamida, del 29 de Julio de 2020, de Hutchison Medipharma Limited: Forma I de 6-((6,7-dimetoxiquinazolin-4-il)oxi)-N,2-dimetilbenzofuran-3-carboxamida, en donde el difractograma de rayos X de polvo de la Forma […]
Compuestos y procedimientos de uso, del 29 de Julio de 2020, de Medivation Technologies LLC: Un compuesto de fórmula (Aa-1): **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en la que: A representa H, halógeno, amino, […]
Complejos de agentes terapéuticos de base vírica y poli(beta-amino-ésteres) modificados, del 29 de Julio de 2020, de Sagetis Biotech, SL: Un complejo de un agente terapéutico de base vírica con un polímero de fórmula I: **(Ver fórmula)** donde cada L1 y L2 están seleccionados […]
Compuestos de alquinilbenceno heterocíclicos, y composiciones médicas y usos de los mismos, del 29 de Julio de 2020, de Guangzhou Healthquest Pharma Co., Ltd: Un compuesto de alquinilbenceno heterocíclico que tiene la fórmula (I) y una sal farmacéuticamente aceptable, o estereoisómero del mismo, **(Ver […]
Régimen de terapia y métodos para sensibilizar células de cáncer tratadas con una terapia epigenética frente a inhibidores de PARP en múltiples cánceres, del 22 de Julio de 2020, de THE JOHNS HOPKINS UNIVERSITY: Una combinación que comprende un agente desmetilante del ADN y un inhibidor de poli ADP ribosa polimerasa (PARP) para su uso en el tratamiento del cáncer, en […]